一种后生元及其制备方法与流程
1.本发明涉及生物技术领域,具体涉及一种后生元及其制备方法。
背景技术:
2.后生元是益生菌经加工处理后的益生菌代谢物成分统称,包括菌体与代谢产物。近年来的研究发现,灭活的益生菌(non-viable probiotics)以及益生菌的溶胞产物(lysate)、提取产物或分离部分[被称为后生元(postbiotics)]具有相近于益生菌的功效,并且相较于益生菌具有更高的胃酸耐受性且更易于保存。
[0003]
嗜酸乳杆菌作为乳酸菌的一种,在代谢过程产生很多抗菌物质,主要包括酸性物质、抗菌肽等,可有效抵抗食物变质和食源性病原微生物。抗菌肽具有广谱抗菌活性,对细菌有很强的杀伤作用,尤其是其对某些耐药性病原菌的杀灭作用更引起了人们的重视;提高后生元中的抗菌肽的含量是现有技术急需解决的技术问题,现有技术有通过向乳酸菌中添加沙门氏菌作为竞争关系促进抗菌肽的产生,但竞争过程中会影响乳酸菌的存活率,进而还是会影响抗菌肽的得率,如何在确保嗜酸乳杆菌数量的同时提高抗菌肽的得率是现有技术急需解决的技术问题。
技术实现要素:
[0004]
本发明的目的在于克服上述技术不足,提供一种后生元及其制备方法,解决现有技术中如何在确保嗜酸乳杆菌数量的同时提高抗菌肽的得率的技术问题。
[0005]
为达到上述技术目的,本发明的技术方案提供一种后生元的制备方法,包括以下步骤:
[0006]
s1、将嗜酸乳杆菌接入乳酸菌培养液中培养,在35-38℃下培养得到第一发酵液,之后在第一发酵液中加入柠檬酸和水解蛋白继续在25-30℃下培养得到第二发酵液,之后将第二发酵液在35-38℃下培养得到第三发酵液;
[0007]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;
[0008]
s3、向所述浓缩液中加入明胶,之后在5-10℃下冷藏得到第四发酵液;
[0009]
s4、将所述第四发酵液进行灭活处理。
[0010]
进一步地,在步骤s1中,所述柠檬酸的添加量为所述第一发酵液体积的0.1-0.5%,所述柠檬酸的浓度为0.3mol/l-0.5mol/l。
[0011]
进一步地,在步骤s1中,所述水解蛋白的添加量为所述第一发酵液质量的0.1-0.5%。
[0012]
进一步地,在步骤s4中,所述明胶的加入量为所述浓缩液质量的0.5-1%。
[0013]
进一步地,在步骤s4之后还包括:步骤s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元。
[0014]
进一步地,在步骤s5中,所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的1-3%。
[0015]
进一步地,在步骤s3中,所述浓缩液的体积为所述上清液体积的0.5-0.6倍。
[0016]
进一步地,在步骤s3中,所述冷藏的时间为30-60min。
[0017]
进一步地,在步骤s1中,在35-38℃下培养2-3天得到第一发酵液;在25-30℃下培养3-5h得到第二发酵液,在35-38℃下培养1-2天得到第三发酵液。
[0018]
此外,本发明还提出一种后生元,由上述制备方法制备得到。
[0019]
与现有技术相比,本发明的有益效果包括:将嗜酸乳杆菌接入乳酸菌培养液中培养,在较高温度35-38℃下培养有利于嗜酸乳杆菌的生长,之后在第一发酵液中加入柠檬酸和水解蛋白继续在较低温度25-30℃下培养得到第二发酵液,在第一发酵液中加入柠檬酸和水解蛋白且在较低的温度下,之后继续在较高温度35-38℃下培养得到的第三发酵液中,水解蛋白提供抗菌肽生成所需的氨基酸,柠檬酸提高嗜酸乳杆菌的稳定性,先低温再高温培养有利于再次促进嗜酸乳杆菌的生长且促进抗菌肽的生成,之后过滤、浓缩得到浓缩液,向浓缩液中加入明胶,并在5-10℃下冷藏得到第四发酵液,明胶具有粘结作用,在较低温度下能够稳固嗜酸乳杆菌的所在位置,进一步进行灭活处理能够提高灭活的精准性,进而提高灭活的效率,仅需要在80-85℃下灭活30-60min即可实现嗜酸乳杆菌的全部灭活,从而得到嗜酸乳杆菌数量较多且后生元中抗菌肽的含量高。
具体实施方式
[0020]
本具体实施方式提供了一种后生元的制备方法,包括以下步骤:
[0021]
s1、将嗜酸乳杆菌接入乳酸菌培养液中培养,在35-38℃下培养1-2天得到第一发酵液,之后在第一发酵液中加入柠檬酸和水解蛋白继续在25-30℃下培养3-5h得到第二发酵液,之后将第二发酵液在35-38℃下培养1-2天得到第三发酵液;所述水解蛋白优选为小麦水解蛋白;所述柠檬酸的添加量为所述第一发酵液体积的0.1-0.5%,所述柠檬酸的浓度为0.3mol/l-0.5mol/l;所述水解蛋白的添加量为所述第一发酵液质量的0.1-0.5%;
[0022]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩液的体积为所述上清液体积的0.5-0.6倍;
[0023]
s3、向所述浓缩液中加入明胶,之后在5-10℃下冷藏30-60min得到第四发酵液;所述明胶的加入量为所述第三发酵液质量的0.5-1%;
[0024]
s4、将所述第四发酵液在80-85℃下进行灭活处理30-60min;
[0025]
s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的1-3%。壳聚糖使得后生元形成微胶囊,微胶囊进入肠道会开始释放后生元,且在后生元中明胶的作用下提高与肠道的粘附力,进而延长后生元的作用时间,有利于提高对肠道炎症的治疗效果。
[0026]
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0027]
下述实施例中,乳酸菌培养基由水1000ml、牛肉膏10g、蛋白胨20g、酵母膏10g、番茄汁200g、葡萄糖10g、吐温0.5ml、碳酸钙17g、溴甲酚绿0.1g、琼脂15g构成。下述实施例中的嗜酸乳杆菌为自己采集的现有技术中的已知菌种。
[0028]
实施例1
[0029]
本实施例提出一种后生元,由以下步骤制得:
[0030]
s1、将104个嗜酸乳杆菌接入乳酸菌培养液中培养,在35℃下培养2天得到第一发酵液,之后在第一发酵液中加入柠檬酸和水解蛋白继续在25℃下培养3h得到第二发酵液,之后将第二发酵液在35℃下培养1天得到第三发酵液;检测第三发酵液,嗜酸乳杆菌的数量为3.5
×
10
10
cfu/ml;所述柠檬酸的添加量为所述第一发酵液体积的0.3%,所述柠檬酸的浓度为0.3mol/l;所述水解蛋白的添加量为所述第一发酵液质量的0.4%;
[0031]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩液的体积为所述上清液体积的0.5倍;
[0032]
s3、向所述浓缩液中加入明胶,之后在5℃下冷藏30min得到第四发酵液;所述明胶的加入量为所述第三发酵液质量的0.8%;
[0033]
s4、将所述第四发酵液在80℃下进行灭活处理60min;
[0034]
s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元162g,采用现有技术的透析浓缩法重复本实施例的方法制得的抗菌肽的质量为0.923g;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的1%。
[0035]
计算抗菌肽的得率为0.923g/(162g+0.923g)*100%=0.567%。
[0036]
实施例2
[0037]
本实施例提出一种后生元,由以下步骤制得:
[0038]
s1、将104个嗜酸乳杆菌接入乳酸菌培养液中培养,在37℃下培养1天得到第一发酵液,之后在第一发酵液中加入柠檬酸和水解蛋白继续在30℃下培养5h得到第二发酵液,之后将第二发酵液在37℃下培养2天得到第三发酵液;检测第三发酵液,嗜酸乳杆菌的数量为3.2
×
10
10
cfu/ml;所述柠檬酸的添加量为所述第一发酵液体积的0.1%,所述柠檬酸的浓度为0.5mol/l;所述水解蛋白的添加量为所述第一发酵液质量的0.2%;
[0039]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩液的体积为所述上清液体积的0.6倍;
[0040]
s3、向所述浓缩液中加入明胶,之后在10℃下冷藏60min得到第四发酵液;所述明胶的加入量为所述第三发酵液质量的0.5%;
[0041]
s4、将所述第四发酵液在85℃下进行灭活处理45min;
[0042]
s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元158g;采用现有技术的透析浓缩法重复本实施例的方法制得的得到抗菌肽的质量为0.884g;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的2%。
[0043]
计算抗菌肽的得率为0.884g/(158g+0.884g)*100%=0.556%。
[0044]
实施例3
[0045]
本实施例提出一种后生元,由以下步骤制得:
[0046]
s1、将104个嗜酸乳杆菌接入乳酸菌培养液中培养,在38℃下培养1.5天得到第一发酵液,之后在第一发酵液中加入柠檬酸和水解蛋白继续在28℃下培养4h得到第二发酵液,之后将第二发酵液在38℃下培养1天得到第三发酵液;检测第三发酵液,嗜酸乳杆菌的数量为2.9
×
10
10
cfu/ml;所述柠檬酸的添加量为所述第一发酵液体积的0.5%,所述柠檬酸的浓度为0.4mol/l;所述水解蛋白的添加量为所述第一发酵液质量的0.1%;
[0047]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩
液的体积为所述上清液体积的0.6倍;
[0048]
s3、向所述浓缩液中加入明胶,之后在8℃下冷藏50min得到第四发酵液;所述明胶的加入量为所述第三发酵液质量的1%;
[0049]
s4、将所述第四发酵液在85℃下进行灭活处理40min;
[0050]
s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元162g;采用现有技术的透析浓缩法重复本实施例的方法制得的抗菌肽的质量为0.824g;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的3%。
[0051]
计算抗菌肽的得率为0.828g/(162g+0.824g)*100%=0.506%。
[0052]
实施例4
[0053]
本实施例提出一种后生元,由以下步骤制得:
[0054]
s1、将104个嗜酸乳杆菌接入乳酸菌培养液中培养,在36℃下培养1天得到第一发酵液,之后在第一发酵液中加入柠檬酸和水解蛋白继续在27℃下培养5h得到第二发酵液,之后将第二发酵液在36℃下培养2天得到第三发酵液;检测第三发酵液,嗜酸乳杆菌的数量为3.1
×
10
10
cfu/ml;所述柠檬酸的添加量为所述第一发酵液体积的0.4%,所述柠檬酸的浓度为0.4mol/l;所述水解蛋白的添加量为所述第一发酵液质量的0.3%;
[0055]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩液的体积为所述上清液体积的0.5倍;
[0056]
s3、向所述浓缩液中加入明胶,之后在7℃下冷藏40min得到第四发酵液;所述明胶的加入量为所述第三发酵液质量的0.8%;
[0057]
s4、将所述第四发酵液在80℃下进行灭活处理30min;
[0058]
s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元159g;采用现有技术的透析浓缩法重复本实施例的方法制得的抗菌肽的质量为0.817g;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的3%。
[0059]
计算抗菌肽的得率为0.817g/(159g+0.817g)*100%=0.511%。
[0060]
实施例5
[0061]
本实施例提出一种后生元,由以下步骤制得:
[0062]
s1、将104个嗜酸乳杆菌接入乳酸菌培养液中培养,在37℃下培养1天得到第一发酵液,之后在第一发酵液中加入柠檬酸和水解蛋白继续在25℃下培养4h得到第二发酵液,之后将第二发酵液在37℃下培养2天得到第三发酵液;检测第三发酵液,嗜酸乳杆菌的数量为3.2
×
10
10
cfu/ml;所述柠檬酸的添加量为所述第一发酵液体积的0.5%,所述柠檬酸的浓度为0.3mol/l;所述水解蛋白的添加量为所述第一发酵液质量的0.1%;
[0063]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩液的体积为所述上清液体积的0.5倍;
[0064]
s3、向所述浓缩液中加入明胶,之后在5℃下冷藏30min得到第四发酵液;所述明胶的加入量为所述第三发酵液质量的0.6%;
[0065]
s4、将所述第四发酵液在80℃下进行灭活处理50min;
[0066]
s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元155g,采用现有技术的透析浓缩法重复本实施例的方法制得的抗菌肽的质量为0.851g;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的2%。
[0067]
计算抗菌肽的得率为0.851g/(155g+0.851g)*100%=0.546%。
[0068]
对比例1
[0069]
本对比例与实施例1的区别仅在于:嗜酸乳杆菌一直在35℃下培养,具体如下:
[0070]
本实施例提出一种后生元,由以下步骤制得:
[0071]
s1、将104个嗜酸乳杆菌接入乳酸菌培养液中培养,在35℃下培养2天得到第三发酵液;检测第三发酵液,嗜酸乳杆菌的数量为3.5
×
107cfu/ml;所述柠檬酸的添加量为所述第一发酵液体积的0.3%,所述柠檬酸的浓度为0.3mol/l;所述水解蛋白的添加量为所述第一发酵液质量的0.4%;
[0072]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩液的体积为所述上清液体积的0.5倍;
[0073]
s3、向所述浓缩液中加入明胶,之后在5℃下冷藏30min得到第四发酵液;所述明胶的加入量为所述第三发酵液质量的0.8%;
[0074]
s4、将所述第四发酵液在80℃下进行灭活处理60min;
[0075]
s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元112g,采用现有技术的透析浓缩法重复本实施例的方法制得的抗菌肽的质量为0.512g;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的1%。
[0076]
计算抗菌肽的得率为0.512g/(112g+0.512g)*100%=0.457%。
[0077]
对比例2
[0078]
本对比例与实施例1的区别仅在于:发酵过程中没有添加柠檬酸和水解蛋白,具体如下:
[0079]
本实施例提出一种后生元,由以下步骤制得:
[0080]
s1、将104个嗜酸乳杆菌接入乳酸菌培养液中培养,在35℃下培养2天得到第一发酵液,将第一发酵液继续在25℃下培养3h得到第二发酵液,之后将第二发酵液在35℃下培养1天得到第三发酵液;检测第三发酵液,嗜酸乳杆菌的数量为3.2
×
109cfu/ml;
[0081]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩液的体积为所述上清液体积的0.5倍;
[0082]
s3、向所述浓缩液中加入明胶,之后在5℃下冷藏30min得到第四发酵液;所述明胶的加入量为所述第三发酵液质量的0.8%;
[0083]
s4、将所述第四发酵液在80℃下进行灭活处理60min;
[0084]
s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元145g,采用现有技术的透析浓缩法重复本实施例的方法制得的抗菌肽的质量为0.312g;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的1%。
[0085]
计算抗菌肽的得率为0.312g/(145g+0.312g)*100%=0.215%。
[0086]
从对比例1可以看出,没有经过高低温处理的制备方法得到的发酵液中嗜酸乳杆菌的数量较少,而且抗菌肽的得率较低;另外从对比例2可以看出,没有加入柠檬酸和水解蛋白发酵对于嗜酸乳杆菌的数量影响较小,但对抗菌肽的得率影响较大。
[0087]
对比例3
[0088]
本对比例与实施例1的区别在于,没有添加明胶,具体如下:
[0089]
本对比例提出一种后生元,由以下步骤制得:
[0090]
s1、将104个嗜酸乳杆菌接入乳酸菌培养液中培养,在35℃下培养2天得到第一发酵液,之后在第一发酵液中加入柠檬酸和水解蛋白继续在25℃下培养3h得到第二发酵液,之后将第二发酵液在35℃下培养1天得到第三发酵液;检测第三发酵液,嗜酸乳杆菌的数量为3.5
×
10
10
cfu/ml;所述柠檬酸的添加量为所述第一发酵液体积的0.3%,所述柠檬酸的浓度为0.3mol/l;所述水解蛋白的添加量为所述第一发酵液质量的0.4%;
[0091]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩液的体积为所述上清液体积的0.5倍;
[0092]
s3、将所述浓缩液在5℃下冷藏30min得到第四发酵液;
[0093]
s4、将所述浓缩液在80℃下进行灭活处理60min;
[0094]
s5、向灭活后的所述浓缩液中加入壳聚糖,之后喷雾干燥得到后生元163g,采用现有技术的透析浓缩法重复本实施例的方法制得的抗菌肽的质量为0.911g;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的1%。
[0095]
计算抗菌肽的得率为0.921g/(163g+0.921g)*100%=0.562%。
[0096]
对比例4
[0097]
本对比例与实施例1的区别在于没有进行冷藏,具体如下:
[0098]
本对比例提出一种后生元,由以下步骤制得:
[0099]
s1、将104个嗜酸乳杆菌接入乳酸菌培养液中培养,在35℃下培养2天得到第一发酵液,之后在第一发酵液中加入柠檬酸和水解蛋白继续在25℃下培养3h得到第二发酵液,之后将第二发酵液在35℃下培养1天得到第三发酵液;检测第三发酵液,嗜酸乳杆菌的数量为3.5
×
10
10
cfu/ml;所述柠檬酸的添加量为所述第一发酵液体积的0.3%,所述柠檬酸的浓度为0.3mol/l;所述水解蛋白的添加量为所述第一发酵液质量的0.4%;
[0100]
s2、将所述第三发酵液过滤得到上清液,将所述上清液浓缩得到浓缩液;所述浓缩液的体积为所述上清液体积的0.5倍;
[0101]
s3、向所述浓缩液中加入明胶得到第四发酵液;所述明胶的加入量为所述第三发酵液质量的0.8%;
[0102]
s4、将所述第四发酵液在80℃下进行灭活处理60min;
[0103]
s5、向灭活后的所述第四发酵液中加入壳聚糖,之后喷雾干燥得到后生元163g,采用现有技术的透析浓缩法重复本实施例的方法制得的抗菌肽的质量为0.923g;所述壳聚糖的加入量为所述灭活后的所述第四发酵液质量的1%。
[0104]
计算抗菌肽的得率为0.923g/(163g+0.923g)*100%=0.563%。
[0105]
检测实施例1-5及对比例3和对比例4灭火后的第四发酵液或者浓缩液中嗜酸乳杆菌的存活情况,结果如表1所示。
[0106]
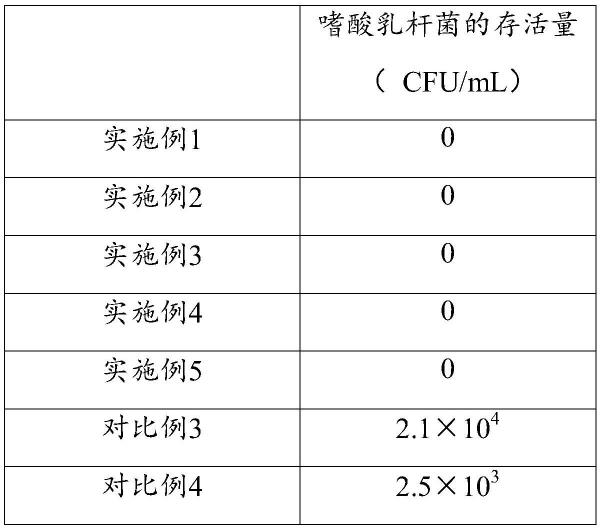
表1实施例1-5及对比例3灭火后的第四发酵液或者浓缩液中嗜酸乳杆菌的存活情况
[0107][0108]
从表1可以看出,没有添加明胶的对比例3灭活后还有部分嗜酸乳杆菌没有完全灭活,没有冷藏的对比例4灭活后还还存在部分嗜酸乳杆菌没有完全灭活,实施例1-5的嗜酸乳杆菌全部灭活。
[0109]
以上所述本发明的具体实施方式,并不构成对本发明保护范围的限定。任何根据本发明的技术构思所做出的各种其他相应的改变与变形,均应包含在本发明权利要求的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1