衢枳壳挥发油在制备预防、缓解和治疗急性肝损伤的产品中的应用的制作方法
1.本发明涉及急性肝损伤治疗领域,具体涉及衢枳壳挥发油在制备预防、缓解和治疗急性肝损伤的产品中的应用,一种活性组合物,一种药物组合物以及所述活性组合物或所述药物组合物在制备预防、缓解和治疗急性肝损伤的药物中的应用。
背景技术:
2.急性肝损伤(alf)是短期内突发的肝细胞损害,最常见于药物中毒、病毒感染、免疫反应、缺血-再灌注。因其高死亡率和不良预后,迄今为止,alf仍是难以解决的临床疾病。目前肝移植是临床上针对alf的主要治疗方法。然而,肝脏来源短缺、术后并发症复杂及价格昂贵限制其临床应用。因此,迫切需要新的有效疗法,寻找安全、有效、经济的药物,显得尤为迫切和需要。
技术实现要素:
3.本发明的目的是为了克服现有技术存在的上述问题,提供衢枳壳挥发油或活性组合物在制备预防、缓解和治疗急性肝损伤的产品中的应用。本发明以衢枳壳挥发油为活性成分,能够用于预防、缓解和治疗急性肝损伤。
4.为了实现上述目的,本发明一方面提供衢枳壳挥发油在制备预防、缓解和治疗急性肝损伤的产品中的应用。
5.本发明第二方面提供一种活性组合物,所述组合物包含d-棕檬烯、α-揽香烯、月桂烯、γ-萜品烯、木根香叶烯、α-松油醇、4-松油醇和β-丁香烯;
6.其中,相比于1重量份的β-丁香烯,d-棕檬烯的含量为10-15重量份,α-揽香烯的含量为1-5重量份,月桂烯的含量为1-5重量份,γ-萜品烯的含量为1-5重量份,木根香叶烯的含量为1-5重量份,α-松油醇的含量为1-5重量份,4-松油醇的含量为0.5-1.5重量份。
7.本发明第三方面提供一种药物组合物,所述药物组合物包含如上所述的活性组合物以及药学上可接受的载体。
8.本发明第四方面提供所述的活性组合物或如上所述的药物组合物在制备预防、缓解和治疗急性肝损伤的药物中的应用。
9.本发明创造性地对衢枳壳挥发油发掘了新的医疗用途,开拓了一个新的应用领域。所述衢枳壳挥发油具有抗炎、改善肝功能的作用,能够用于预防、缓解和治疗急性肝损伤,且药理作用强、安全无毒。
10.衢枳壳挥发油的来源丰富、价廉、安全无毒副作用,制备工艺路线简单、生产成本低廉,可制成药物或食品等,使用方便,是一种非常有前景和开发价值的治疗急性肝损伤的药物。
附图说明
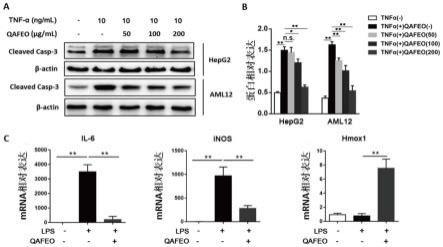
11.图1示出了衢枳壳挥发油在体外具有保护肝细胞和抗炎的作用;其中,a和b表示tnf-α处理4h后,不同浓度挥发油混合物对hepg2和aml12细胞凋亡的影响;c表示挥发油混合物作用下raw264.7细胞炎症相关因子的mrna水平。
12.图2示出了衢枳壳挥发油对正常小鼠肝组织的影响;a和b表示各组he染色结果;c为血清ast和alt水平;d为不同浓度衢枳壳挥发油对细胞ldh释放的影响。
13.图3示出了衢枳壳挥发油改善lps/d-galn诱导的急性肝损伤小鼠肝功能;a表示衢枳壳挥发油对小鼠血清alt和ast的影响;b表示衢枳壳挥发油对小鼠肝脏alt和ast的影响;c表示he染色结果;d表示各因子的mrna水平。
14.图4示出了衢枳壳挥发油改善cona诱导的急性肝损伤小鼠肝功能;a表示衢枳壳挥发油对小鼠血清alt和ast的影响;b表示衢枳壳挥发油对小鼠肝脏alt和ast的影响。c表示he染色结果;d表示各因子的mrna水平。
具体实施方式
15.在本文中所披露的范围的端点和任何值都不限于该精确的范围或值,这些范围或值应当理解为包含接近这些范围或值的值。对于数值范围来说,各个范围的端点值之间、各个范围的端点值和单独的点值之间,以及单独的点值之间可以彼此组合而得到一个或多个新的数值范围,这些数值范围应被视为在本文中具体公开。
16.本发明一方面提供衢枳壳挥发油在制备预防、缓解和治疗急性肝损伤的产品中的应用。
17.衢枳壳,即胡柚片,为芸香科植物常山胡柚(citrus changshan-huyou y.b.chang)的干燥未成熟果实,7月果皮尚绿时采收,自中部切断为两半,晒干或低温干燥。味苦、辛、酸,性微寒,归脾、胃经,有理气宽中、行滞消胀功效,可用于胸胁气滞、胀满疼痛、食积不化、痰饮内停、胃下垂、脱肛、子宫脱垂等症。于2016年8月被纳入2015年版《浙江省中药炮制规范》。其中,所述常山胡柚的未成熟果实与成熟果实以及果皮的成分组成以及含量有着较大区别,如此也就导致了他们在效果上的不同。
18.所述衢枳壳挥发油可以采用本领域常规的方法制备,优选地,所述衢枳壳挥发油的制备方法包括:对衢枳壳进行粉碎并与水混合后,经水蒸气蒸馏提取得到衢枳壳挥发油。
19.可以采用本领域常规的方法对衢枳壳进行粉碎处理,在此不再赘述。所述衢枳壳可以以衢枳壳饮片的形式存在。
20.水的用量可以在较宽的范围内选择,优选地,相比于1重量份的衢枳壳,水的用量为1-10重量份,更优选为1.5-5重量份。
21.应当理解的是,在水蒸气蒸馏提取前,可以使用先浸泡一段时间(比如可以为1-4h),以提高提取效率。
22.优选地,所述水蒸气蒸馏提取的条件包括:温度为140-180℃,更优选为150-170℃。
23.所述水蒸气蒸馏提取的时间可以在较宽的范围内选择,优选地,所述提取的时间为4-12h。
24.为了进一步加强提取效率,所述提取可以分为多次进行,例如,可以分为2次、3次、
4次、5次等,然后将每次提取的提取液合并作为最终的提取液。本领域技术人员可以根据实际的提取效果进行选择,只要将回流提取的总时间控制在如上的范围内即可,每次提取可以等时间进行。
25.所述提取可以在挥发油提取器中进行。
26.优选地,所述衢枳壳挥发油包含活性组合物,所述活性组合物包含d-棕檬烯、α-揽香烯、月桂烯、γ-萜品烯、木根香叶烯、α-松油醇、4-松油醇和β-丁香烯。
27.活性组合物中,优选地,相比于1重量份的β-丁香烯,d-棕檬烯的含量为10-15重量份,α-揽香烯的含量为1-5重量份,月桂烯的含量为1-5重量份,γ-萜品烯的含量为1-5重量份,木根香叶烯的含量为1-5重量份,α-松油醇的含量为1-5重量份,4-松油醇的含量为0.5-1.5重量份。
28.更优选地,相比于1重量份的β-丁香烯,d-棕檬烯的含量为12-14重量份,α-揽香烯的含量为2-4重量份,月桂烯的含量为2-4重量份,γ-萜品烯的含量为1-3重量份,木根香叶烯的含量为1-3重量份,α-松油醇的含量为1-3重量份,4-松油醇的含量为0.8-1.2重量份。
29.优选地,所述衢枳壳挥发油还包含水,更优选地,所述衢枳壳挥发油中水的含量为60-99重量%,优选为70-90重量%。
30.所述产品可以为药物或食品。当所述产品为药品的时候,所述衢枳壳挥发油还可以与其他用于预防、缓解或治疗急性肝损伤的药物配合使用。
31.当所述产品为药品的时候,所述药物还可含有药学上可接受的载体。
32.所述药学上可接受的载体可以为医药领域中制备各种剂型时常用的载体,例如,药学上可接受的佐剂、防腐剂或稳定剂。其中,佐剂、防腐剂或稳定剂的种类和含量为本领域技术人员所公知,在此不再赘述。
33.根据本发明,所述药物可以制备为各种剂型,例如,可以制备为但不限于片剂、胶囊(包括软胶囊和硬胶囊)、散剂、缓释制剂、栓剂、口服液、颗粒剂、丸剂或注射液。所述药物可以安全地口服给药或肠胃外给药(例如,局部、直肠、静脉内给药等)。所述注射剂能够用于静脉内、肌内、皮下或器官内给药,或能够直接施用于病灶。
34.应当理解的是,当所述产品为食品(比如可以为起保健和辅助治疗作用的食品)时,也可含有食品领域允许的辅料,在此不在赘述。
35.本发明第二方面提供一种活性组合物,所述组合物包含d-棕檬烯、α-揽香烯、月桂烯、γ-萜品烯、木根香叶烯、α-松油醇、4-松油醇和β-丁香烯;
36.其中,相比于1重量份的β-丁香烯,d-棕檬烯的含量为10-15重量份,α-揽香烯的含量为1-5重量份,月桂烯的含量为1-5重量份,γ-萜品烯的含量为1-5重量份,木根香叶烯的含量为1-5重量份,α-松油醇的含量为1-5重量份,4-松油醇的含量为0.5-1.5重量份。
37.优选地,相比于1重量份的β-丁香烯,d-棕檬烯的含量为12-14重量份,α-揽香烯的含量为2-4重量份,月桂烯的含量为2-4重量份,γ-萜品烯的含量为1-3重量份,木根香叶烯的含量为1-3重量份,α-松油醇的含量为1-3重量份,4-松油醇的含量为0.8-1.2重量份。
38.所述活性组合物中的各组分的来源没有特别的限制,可以来自于生物提取或化学合成等,比如可以分离自衢枳壳挥发油,所述分离的方法可以为本领域常规的分离方法,比如柱层析。
39.本发明第三方面提供一种药物组合物,所述药物组合物包含如上所述的活性组合
物以及药学上可接受的载体。
40.所述药学上可接受的载体可以如第一方面所述的载体,本领域技术人员可以根据实际情况选择合适的载体,并调整载体的用量。
41.所述药物组合物的剂型可以参见第一方面,在此不再赘述。
42.本发明第四方面提供所述的活性组合物或如上所述的药物组合物在制备预防、缓解和治疗急性肝损伤的药物中的应用。
43.以下将通过实施例对本发明进行详细描述。以下实施例中,
44.谷丙转氨酶(alt)、谷草转氨酶(ast)检测试剂盒,购自南京建成生物工程研究所;trizol试剂购自天根生化科技有限公司;cdna逆转录试剂盒购自美国thermofisher公司;sybr green试剂盒购自生工生物工程有限公司;β-actin抗体、cleaved caspase-3抗体均购自美国cell signaling technology公司。
45.实验动物:雄性balb/c小鼠(体重25g左右),由浙江中医药大学动物实验中心提供,生产许可证号scxk(沪)2008-0016。饲养于浙江中医药大学实验动物中心,自由摄食及饮水。动物实验条件合格证号syxk(浙)2013-0184。动物实验得到伦理委员会批准。
46.alt、ast测定:按照试剂盒说明测定各组小鼠血清、肝脏alt、ast水平。
47.肝组织病理学观察:取肝脏组织,用10%福尔马林固定,常规石蜡包埋切片,he染色,400倍显微镜下观察。
48.所有数据均用spss 17.0统计软件进行处理,数据以均值
±
标准差(x
±
sd)表示,组间差异按方差分析进行检验,并用最小显著差法检验作两两比较,以p《0.05时有统计学意义。
49.制备例1
50.本制备例用于说明衢枳壳挥发油的制备方法。
51.取1kg衢枳壳药材粉碎后装入圆底烧瓶中,与2l纯水混合后,用挥发油提取器提取挥发油。将电热套温度调至160℃,加热2h后有挥发油流出,提取6h,重复10次,得黄色挥发油80ml。
52.经测定,挥发油中,d-棕檬烯:α-揽香烯:月桂烯:γ-萜品烯:木根香叶烯:α-松油醇:4-松油醇:β-丁香烯的重量比为13:3:3:2:2:2:1:1;β-丁香烯的含量为6.81mg/g。
53.实施例1
54.本实施例用于说明衢枳壳挥发油在体外对细胞有抗炎作用。
55.(1)细胞培养
56.hepg2和aml12细胞用含10%胎牛血清的dmem培养基于37℃、5%co2培养箱中培养。tnf-α和衢枳壳挥发油处理细胞4h后用胰酶消化收集细胞。raw264.7细胞用含10%胎牛血清的rpmi 1640培养基于37℃、5%co2培养箱中培养。lps和衢枳壳挥发油处理细胞4h后加trizol提取rna。
57.(2)rt-pcr法检测
58.按照trizol试剂盒,提取各组小鼠肝脏rna,并逆转录为cdna。按照sybr green荧光染料法进行定量pcr测定,引物由金唯智公司合成,引物序列见表1。pcr反应条件:95℃30s;95℃5s,60℃31s,40个循环。采用2-δδct法进行半定量分析。
59.表1
[0060][0061]
如图1a和1b所示,衢枳壳挥发油能显著改善tnf-α诱导的细胞凋亡。图1c说明衢枳壳挥发油对lps诱导的细胞炎症反应具有强大的抗炎作用,促炎因子il-6和inos的mrna水平显著降低,抗炎因子hmox1的mrna水平显著升高,p<0.01。
[0062]
实施例2
[0063]
本实施例用于说明衢枳壳挥发油对正常小鼠肝组织的影响。
[0064]
将小鼠随机分为对照组(3只)、衢枳壳挥发油低剂量口服组(6只)和衢枳壳挥发油高剂量口服组(6只)、衢枳壳挥发油低剂量腹腔注射组(6只)和衢枳壳挥发油高剂量腹腔注射组(6只)。低剂量按50mg/kg给衢枳壳挥发油,高剂量按100mg/kg给衢枳壳挥发油,衢枳壳挥发油共给药3天,每天记录小鼠体重情况。末次给药6h后,称重并处死小鼠,分离血清,-80℃冻存;取肝脏称重,左肝脏固定,右肝脏冻存。固定肝脏,石蜡包埋,切片,肝组织he染色。
[0065]
如图2a和b肝组织he染色结果显示,各衢枳壳挥发油组与对照组小鼠肝小叶完整,未见明显肝实质细胞病变以及炎症细胞浸润;图2c表明衢枳壳挥发油对正常小鼠血清ast和alt无影响;图2d说明衢枳壳挥发油对细胞生存无影响。以上皆表明衢枳壳挥发油对正常小鼠无不良影响。
[0066]
实施例3
[0067]
本实施例用于说明衢枳壳挥发油在预防、缓解和治疗急性肝损伤中的应用。
[0068]
(1)lps/d-galn诱导的急性肝损伤
[0069]
将小鼠随机分为对照组(3只)、模型组(6只)、衢枳壳挥发油低剂量口服组(6只)和衢枳壳挥发油高剂量口服组(6只)、衢枳壳挥发油低剂量腹腔注射组(6只)和衢枳壳挥发油高剂量腹腔注射组(6只)。低剂量按50mg/kg给衢枳壳挥发油,高剂量按100mg/kg给衢枳壳挥发油,衢枳壳挥发油共给药3天,每天记录小鼠体重情况。末次给药后2h,模型组和各给药组分别腹腔注射lps/d-galn(lps 6μg/kg,d-galn 800mg/kg),对照组注射等量生理盐水,注射后6h,称重并处死小鼠,分离血清,-80℃冻存;取肝脏称重,左肝脏固定,右肝脏冻存。固定肝脏,石蜡包埋,切片,肝组织he染色。
[0070]
如图3a和3b结果所示,衢枳壳挥发油能显著降低小鼠血清和肝脏中的alt和ast,且具有统计学差异(p<0.01);图3c的he染色表明衢枳壳挥发油能显著缓解lps/d-galn造成的小鼠肝脏病理改变和中性粒细胞浸润(图3c,p<0.01);图3d表示,衢枳壳挥发油能显著降低促炎因子il-1β、tnf-α、il-6、il-18的mrna水平(p<0.01)。
[0071]
(2)cona诱导的急性肝损伤
[0072]
将小鼠随机分为对照组(3只)、模型组(6只)、衢枳壳挥发油低剂量口服组(6只)和衢枳壳挥发油高剂量口服组(6只)、衢枳壳挥发油低剂量腹腔注射组(6只)和衢枳壳挥发油高剂量腹腔注射组(6只)。低剂量按50mg/kg给衢枳壳挥发油,高剂量按100mg/kg给衢枳壳挥发油,衢枳壳挥发油共给药3天,每天记录小鼠体重情况。末次给药后2h,模型组和各给药组分别尾静脉注射cona(刀豆蛋白a,用生理盐水配成2.5mg/ml,每只小鼠20mg/kg剂量注射),对照组注射等量生理盐水,注射后6h,称重并处死小鼠,分离血清,-80℃冻存;取肝脏称重,左肝脏固定,右肝脏冻存。固定肝脏,石蜡包埋,切片,肝组织he染色。
[0073]
如图4a和4b结果所示,衢枳壳挥发油能显著降低小鼠血清和肝脏中的alt和ast,且具有统计学差异(p<0.01);图4c的he染色表明衢枳壳挥发油能显著缓解cona造成的小鼠肝脏病理改变和中性粒细胞浸润(p<0.01);图4d表示,衢枳壳挥发油能显著降低促炎因子il-1β、il-6、il-18的mrna水平(p<0.01),显著升高抗炎因子il-10的mrna水平(p<0.01)。
[0074]
以上试验结果表明,此衢枳壳挥发油有强大的抗炎作用,对lps/d-galn和cona诱导的急性肝损伤有保护作用。
[0075]
以上详细描述了本发明的优选实施方式,但是,本发明并不限于此。在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,包括各个技术特征以任何其它的合适方式进行组合,这些简单变型和组合同样应当视为本发明所公开的内容,均属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1