一种基于细胞聚集体的微脉管肝脏芯片及其制备和使用方法与流程
本发明涉及一种基于细胞聚集体的微脉管肝脏芯片及其制备和使用方法,属于微流体芯片加工设计和生物医药技术领域。
背景技术:
研发安全有效的药物是一个长期、艰难和昂贵的进程。细胞培养和动物实验是现代医学和药学研究中广泛使用并极为依赖的两种实验平台。药物进入临床前都要通过离体实验和动物过渡实验来检测药物对体外培养细胞和动物机体的效应,并反复进行药效学、药代动力学、毒理学的定性和定量预测。然而药物研发失败的一个重要原因便是当前用于药物评估的模型与人的疾病模型存在无法回避的差异。通常情况下,细胞培养模式很难模拟人体微环境,同时,使用动物模型对正常和疾病的生理过程进行分析,它不但昂贵、耗时,而且存在伦理上的争论。通过这两类实验平台验证的实验性药物在进入临床试验后被淘汰,或药效低或毒副作用强,导致药物研发中人力和物力的巨大浪费。器官芯片可以突破细胞培养和模式动物实验的局限。它是一个基于多通道流体芯片的三维细胞培养系统,由多个模拟人体组织和器官环境的细胞培养分区集合而成。在各分区通过仿生循环系统进行连接。微通道的尺寸可以与细胞尺寸相当,可以精确地控制微环境的成分、温度等因素,尽可能模拟细胞外基质的情况,增强实验的可靠性和可操作性。同时可以设计不同的二维或三维结构和精密加工成微电极等器件实现细胞的培养、定位、有序、图案化以及检测等多种功能。在芯片上模拟生物体的环境进行细胞、组织和器官的培养,研究并控制细胞在体外培养过程中的生物学行为,并在药物开发、疾病诊断和治疗方面具有广泛的应用前景。人体器官芯片的研究在国际上尚处于起步阶段,但是欧美日等国家已开发出不同种类的脑芯片、肺芯片、心脏芯片、肾芯片、肝脏芯片、脾芯片、肠芯片等多种器官的芯片,以期用于器官功能模拟和替代动物模型进行药物筛选等研究。肝脏是人体最重要的解毒器官,也是药物实现转化和代谢的主要器官,构建模拟肝脏器官功能和结构的肝脏芯片将给药物筛选提供良好的平台。然而,目前的肝脏芯片类型非常的少,仅有个别的可以模拟类血管内皮屏障和部分微环境,还是很难实现肝脏微环境的系统模拟并广泛用于药物筛选的研究中。肝脏本身就是一个极佳的肝细胞反应器,肝脏的基本结构和功能单位为肝小叶,其内肝细胞不仅达到数量和密度的要求,还呈现极性有序排列;肝脏细胞处于一种三维环境中,肝细胞与其周围的肝血窦内皮细胞,肝星状细胞,库普弗细胞,及细胞外基质等相互作用,细胞间相互作用也有助于调节细胞的生长和功能分化。肝脏内血管和胆管系统为肝脏细胞提供氧气和营养物质,药物也在肝脏内实现代谢和转化,同时带走肝细胞的代谢废物。
技术实现要素:
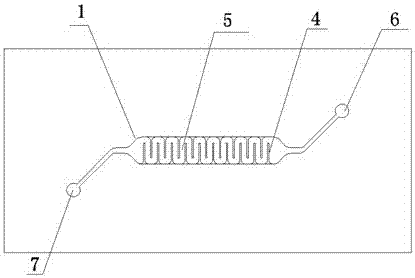
针对上述现有技术的不足,本发明的目的是提供一种基于细胞聚集体的微脉管肝脏芯片及其制备和使用方法,该器官芯片模拟了肝脏复杂的多种微环境要素,解决了传统的药物筛选中使用细胞和动物模型的固有缺陷,解决了现有肝脏细胞培养体系存在的结构单一,和模拟功能少的缺点,能够有效进行多细胞的依次定位植入和培养,并进行药物的安全性和有效性评价。为实现上述目的,本发明采用以下技术方案:一种基于细胞聚集体的微脉管肝脏芯片,包括位于上层的微脉管系统,中间的类血管内皮屏障系统和下层的肝脏器官多细胞共培养系统,微脉管系统和肝脏器官多细胞共培养系统分别设置于各自的片基上;其中,所述微脉管系统包括由若干阻流栅栏交错布置构成的弯曲脉管,所述弯曲脉管两端分别设有微脉管进口和微脉管出口;所述类血管内皮屏障系统由多孔膜组成;所述肝脏器官多细胞共培养系统包括细胞聚集体富集区和多种细胞共培养区,并在两端分别设置有培养系统进口和培养系统出口,肝脏器官多细胞共培养系统位于培养系统进口的内部区域设置有两个分流栅栏,其中,细胞聚集体富集区由多个月牙槽状结构组成,每个月牙槽状结构上均设置有若干缝隙,多个月牙槽状结构纵向排列成若干列,且该若干列交错布置,所有月牙槽状结构的开口均朝着培养系统进口。所述片基为聚二甲基硅氧烷(PDMS)、聚甲基丙烯酸甲酯(PMMA)、玻璃、聚碳酸酯(PC)、聚四氟乙烯、硝酸纤维素、生物膜、硅片的一种或几种。所述肝脏器官多细胞共培养系统所用的细胞粘附和培养基质为胶原蛋白、纤维蛋白胶、细胞外基质蛋白、BSA蛋白、丝素蛋白、明胶、壳聚糖、精氨酸-甘氨酸-天冬氨酸(RGD)、基质胶(Matrigel)、海藻酸钠、异甲基丙烯酰胺(NIPAM)、聚乙二醇(PEG)或聚乙二醇丙烯酸酯(PEGDA)的一种或几种,优先选择为胶原蛋白。所述微脉管系统的微脉管入口和微脉管出口通道深度,阻流栅栏高度和弯曲脉管深度均为100μm;阻流栅栏的宽度为20μm,形状为半圆形倒角,且与肝脏器官多细胞共培养系统中月牙槽状结构的位置相对应;弯曲脉管是圆滑的通道,通道宽度为600μm,弯曲数为20。所述多孔膜的材料为聚二甲基硅氧烷(PDMS)、Transwell用的PET或PC膜的一种,厚度为10μm,孔径为0.4,1,3,5,8μm,优先选择孔径为1μm的PDMS柔性膜。所述肝脏器官多细胞共培养系统的培养系统入口和培养系统出口通道深度,分流栅栏和月牙槽状结构的高度均为100μm;分流栅栏为圆滑弧形,与进口通道对齐,并等距对称布置;月牙槽状结构的个数为80个,其外圆环半径为350μm,内圆环半径为150μm,月牙槽状结构上的缝隙为四个,并均匀发散排列,其宽度为20μm,深度100μm,内圆环开口直线距离为100μm,月牙槽状结构相互之间的间隔距离为100μm。一种基于细胞聚集体的微脉管肝脏芯片的制备方法,包括以下步骤:(1)用计算机辅助设计软件设计和绘制器官芯片的掩膜板,精确绘制各层芯片的微结构和微通道图形;(2)通过微加工技术,特别是光刻蚀的方法,制备出上下两层的掩膜,制备出含有微结构和微通道的芯片;(3)将上层的微脉管系统芯片,中间的多孔膜和下层的肝脏器官多细胞共培养系统进行对齐,加压,并进行等离子体键合,形成三维立体的微结构和微通道网络;(4)通过微脉管进口和培养系统进口通道依次种植不同细胞种类,并进行贴壁和三维聚集体培养,并进行肝脏实质细胞形貌和功能性(白蛋白分泌,尿素合成,P450酶活性等)评价;(5)通过上层和下层通道依次通入药物进行药物肝脏毒性和药物活性评价(药物的长期和短期肝脏毒性,以及药物的IC50值)。在微脉管系统和类血管内皮屏障系统形成的密闭区域中种植血管内皮细胞,细胞密度为1x106个/mL,贴壁培养2~4小时,形成血管内皮细胞层。在肝脏器官多细胞共培养系统依次种植多种细胞,肝脏细胞聚集体首先通过培养系统进口通道进入细胞聚集体富集区的月牙槽状结构,并富集生长为三维聚集体生长;多种细胞共培养区通过培养系统进口通道种植共培养细胞种类,共培养细胞种类包括肝星形细胞,库普弗细胞,角质细胞,以及成纤维细胞,细胞密度为1x106个/mL,贴壁培养2~4小时。一种基于细胞聚集体的微脉管肝脏芯片的使用方法,:在进行药物评价时,药物通过微脉管系统进入芯片,然后穿透类血管内皮屏障系统,进入到下层的肝脏器官多细胞共培养系统,从而评价其肝脏的毒性作用以及进行药物的代谢和转化;或者,药物也通过培养系统进口直接进入肝脏器官多细胞共培养系统,与肝实质细胞聚集体和共培养细胞直接进行接触并实现代谢和转化,并验证药物的肝脏毒性和药物活力。本发明的有益效果是:(1)肝脏芯片构建了微脉管系统,并以多孔膜和内皮细胞为基础制备了类血管内皮屏障系统,有效模拟了肝血窦内部的微脉管和内皮屏障功能,可以供给营养和氧气。(2)肝脏芯片通过多缝隙月牙槽设计富集肝实质细胞聚集体,并进行三维聚集体的长期培养,有效实现肝脏内部细胞的高密度、定位和三维培养,有助于实现细胞的信息交流和相互促进作用。(3)肝脏芯片通过多缝隙月牙槽设计肝细胞聚集体富集区域周围种植其他肝脏种类的细胞,实现多种细胞的共培养,有效模拟了实际肝脏器官内部多样的细胞类型和细胞间的相互作用。(4)肝脏芯片可以实现肝实质细胞的长期培养,并进行有效的药物评价应用,透明材质可以在线监测细胞、组织和器官的生物学行为,从而为细胞-药物相互作用和药物筛选提供了一个全新的技术平台。附图说明图1是本发明的结构示意图;图2是微脉管系统的结构示意图;图3是类血管内皮屏障系统的结构示意图;图4是肝脏器官多细胞共培养系统的结构示意图;图5是图4中A部位的放大图;图6是基于细胞聚集体的微脉管肝脏芯片的细胞定位分布情况,(a)为贴壁生长在多孔膜上的血管内皮细胞层,并进行了绿色荧光Calcein-AM染...
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1