一种眼科疾病相关SNP位点引物组合物及应用
一种眼科疾病相关snp位点引物组合物及应用
技术领域
1.本发明涉及分子生物学技术领域,具体涉及一种眼科疾病相关snp位点引物组合物及应用。
背景技术:
2.眼科疾病是指发生在眼部区域的疾病,常见眼科疾病有近视、散光、白内障、青光眼、中心浆液性视网膜病变、干眼症、交感性眼炎、夜盲症、弱视、沙眼、糖尿病视网膜病变、结膜炎、老花眼、色盲、视网膜色素变性、视网膜中央动脉阻塞、视网膜脱落、远视、针眼、雪盲症、霰粒肿、飞蚊症等。其中,白内障是老年人常见的眼科疾病,在全世界范围内白内障是致盲的最常见病因,50岁以上老年人白内障发病率60%,70岁以上攀升至80%以上。
3.除环境作用外,遗传因素是一些眼科疾病的重要致病因素,评估眼科疾病的遗传风险,对于眼科疾病的早筛和预防具有重要意义。如已有研究表明,年龄相关性黄斑变性(amd)与cfh、arms2、htra1等基因有关。而角膜曲率相关基因mtor、cmpk1、pdgfra、rbp3与高度近视有关。
4.单核苷酸多态性(single nucleotide polymorphism,snp)是由单个核苷酸的变异(包括转换、颠换、缺失和插入四种形式)所引起的dna序列的多态性,一般情况下只会发生转换和颠换这两种形式,二者之比约为1:2。snp在人类基因组中广泛存在,大约每五百到一千个碱基中就会出现一个,占全部已知基因多态性的90%以上,可以说是人类最常见的可遗传变异。单核苷酸多态性最常出现在cg序列中,c等位基因型转换为t等位基因型的情况最为常见,这可能与胞嘧啶容易通过甲基化形成胸腺嘧啶有关。单核苷酸多态性作为被发掘的第三代dna遗传标志物,相比前两代标志物而言,具有数量多、密度大、分布广、稳定性强、易于检测等优点,有利于单核苷酸多态性在医学方面的应用和推广。
5.专利cn103201393b公开了一种用于鉴定具有更大风险进展为晚期老年性黄斑变性(amd)的患有中期amd个体的方法,通过使用基于全基因组基因关联研究的结果计算多基因计分,需使用数千种snp。《7个单核苷酸多态性位点与中国汉族人群高度近视的相关性分析》(李芳.四川:电子科技大学,2017.)一文则研究了高度近视与rs1656404、rs7829127、rs7084402、rs17648524、rs1254319、rs12205363和rs3138144七个snp位点的关系。但以上现有技术中仅提供了针对某一种眼科疾病评估方法或相关snp位点,并未给出针对多种眼科疾病的检测方法或系统。
6.因此,亟需构建一种能够同时针对多种眼科疾病的相关snp位点及其引物组合物,用于眼科疾病的预防或治疗,便于更好地维持人机体的健康。
技术实现要素:
7.针对上述不足,本发明提供了一种眼科疾病相关snp位点及其引物组合物。本发明通过ngs的方法,设计开发了一组snp位点扩增引物,通过生物信息学分析方法,检测个体体内与眼科疾病相关的基因结构变化,预测个体患病风险,提高眼科疾病的预防和/或治疗效
果。本技术所述的引物组合物及检测方法检测成本低,操作简便,灵敏度好,且准确率高,重复性好,具有极大的临床应用价值。
8.为了实现上述发明目的,本发明的技术方案如下:
9.一方面,本发明提供了一种眼科疾病相关snp位点引物组合物,所述的snp位点包括:rs10034228、rs13382811、rs2730260、rs4395927、rs4455882、rs6469937、rs7839488、rs9318086、rs11911275、rs7615568、rs10483727、rs1063192、rs2487032、rs3213787、rs523096、rs7865618。
10.具体地,所述的引物组合物如下表1所示。
11.表1引物组合物
12.[0013][0014]
具体地,所述的眼科疾病包括近视、年龄相关性白内障和青光眼等。
[0015]
另一方面,本发明提供了上述snp位点引物组合物在制备检测和/或评估眼科疾病产品中的应用。
[0016]
又一方面,本发明提供了一种用于检测和/或评估眼科疾病的产品,所述产品包括上述snp位点引物组合物。
[0017]
具体地,所述的产品为独立试剂或试剂盒。
[0018]
又一方面,本发明提供了上述snp位点引物组合物或产品在检测眼科疾病相关snp位点中的应用。
[0019]
又一方面,本发明提供了一种眼科疾病相关snp位点的检测方法,所述方法为非疾病诊断和治疗方法,所述方法包括利用上述引物组合物或产品对待测样品基因组中的snp位点进行检测。
[0020]
具体地,所述的方法包括以下步骤:
[0021]
(1)基因组dna提取;
[0022]
(2)第1轮多重pcr反应;
[0023]
(3)第1轮磁珠纯化;
[0024]
(4)第2轮多重pcr反应;
[0025]
(5)第2轮磁珠纯化;
[0026]
(6)文库定量;
[0027]
(7)文库质量检测;
[0028]
(8)将文库上机测序,得到fastaq序列文件,经过质量评估、比对、snp calling步
骤得到待测样本捕获区域的snp的基因型信息;
[0029]
(9)将得到的每一个snp的基因型赋予其在人群研究中的疾病的or值;
[0030]
(10)将个体某一疾病所涉及的snp的所有or值进行相乘,即该个体针对该疾病的绝对遗传风险;
[0031]
(11)将绝对遗传风险在千人基因组/中国人基因组队列中排名,即该个体针对该疾病的相对遗传风险,排名在5%以内为低风险,在95%以上为高风险,5
‑
95%之间为正常范围。
[0032]
进一步具体地,步骤(8)中所述质量评估软件为fastqc软件,所述比对软件为bwa软件,所述snp calling软件为gatk软件。
[0033]
与现有技术相比,本发明的积极和有益效果在于:
[0034]
1、本发明提供了一种用于检测眼科疾病snp位点引物组合物,能够同时对近视、年龄相关性白内障和青光眼等眼科疾病进行检测及患病风险评估,进一步提高眼科疾病的预防和/或治疗效果。
[0035]
2.本发明提供的snp位点引物组合物及检测方法,可从微量外周血中获取到足够多的遗传信息,进行遗传风险评估,灵敏度好,同时高效特异的扩增引物,精准地获取snp位点信息,杜绝非特异扩增,大大的提高了精准度,并降低实验成本,操作简便。从获取的snp组合,经过特异的分析方法,计算预测个体未来有可能的患病风险,具有极大的临床应用价值。
[0036]
3.本发明包含的snp位点信息覆盖多种眼科疾病,对于每一种疾病,获得了n个该疾病易感位点基因型,每一个易感位点的基因型等位基因有自己的or值,根据测序结果得到的位点的基因型信息,获得某种疾病所覆盖的位点基因型对应的or值,进一步计算该疾病整体的遗传风险值。对于个体某种疾病的风险评估,要将个体的绝对遗传风险放到足够大的人群中去比较,才能更准确的代表该个体的患病风险。因此,本发明利用已建立的中国自然人群以及千人基因组人群为参照,确定所检测个体的疾病遗传风险。以95%为cut
‑
off,个体某种疾病or值超过所在人群95%的人,则认为该个体该种疾病遗传风险偏高。
附图说明
[0037]
图1为下机测序数据示例图。
[0038]
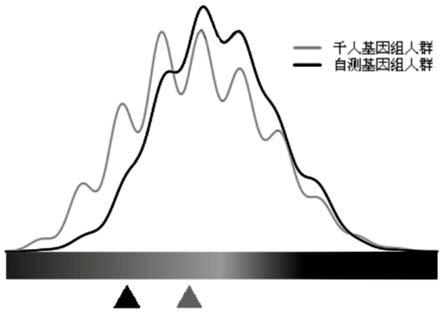
图2为近视遗传风险评估图。
[0039]
图3为青光眼遗传风险评估图。
[0040]
图4为年龄相关性白内障遗传风险评估图。
具体实施方式
[0041]
下面结合具体实施例,对本发明作进一步详细的阐述,下述实施例不用于限制本发明,仅用于说明本发明。以下实施例中所使用的实验方法如无特殊说明,实施例中未注明具体条件的实验方法,通常按照常规条件,下述实施例中所使用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0042]
除非另外定义,否则本文中所用的全部技术与科学用语均具有本领域技术人员通常理解的含义。
[0043]
在某些实施例中,所用试剂或仪器详细信息如下:
[0044]
无水乙醇:北京化工分析纯;
[0045]
agencourtampure xp kit:beckman(a63881);
[0046]
qubitdsdna hs assay kit:life technologies(q32851);
[0047]
nuclease
‑
free water:ambion(am9930);
[0048]
high sensitivity dna kit:agilent(p/n 5067
‑
4626);
[0049]
custom panel:艾吉泰康生物科技(北京)有限公司(igmu062),包括box 1(
‑
20℃保存):igt
‑
i7(5μm)、igt
‑
em101 polymerase mixture、enhancer nb(1n)和box 2(
‑
20℃保存):yf buffer b(4℃保存)、igt
‑
i5(5μm);
[0050]
pcr仪器:life公司abi 9700;
[0051]
dynamag
‑
96 side:life technologies(cat.no.12331d);
[0052]
fluorometer:thermo(q33216);
[0053]
agilent 2100bioanalyzer system:agilent(g2939aa)。
[0054]
实施例1引物组合物
[0055]
本技术所述引物组合物具体如下表2所示。
[0056]
表2引物组合物
[0057][0058]
实施例2文库构建及检测
[0059]
1.基因组dna提取
[0060]
按照商业化基因组dna提取试剂盒操作步骤进行唾液或血液基因组dna(gdna)的提取,使用qubit(life technologies)进行定量。
[0061]
2.第1轮多重pcr反应
[0062]
1.1.反应体系如下表3所示。
[0063]
表3反应体系
[0064]
reagentvolume(μl)
ddh2o4
‑
xenhancer nb(1n)5primer(表2)2.4gdnax(30ng)igt
‑
em101polymerase mixture3.6
[0065]
其中,primer引物混合物中每条引物的终浓度为0.5pmol。
[0066]
1.2.反应程序为:95℃3min30s;98℃20s,60℃8min,18cycle;72℃5min。
[0067]
3.第1轮磁珠纯化
[0068]
3.1.向15μl pcr产物加入15μl室温平衡后的ampure xp磁珠,用移液器吸打混匀数次;
[0069]
3.2.室温孵育5min后,将pcr管置于dynamag
‑
96 side磁力架上3min;
[0070]
3.3.彻底移除上清,将pcr管从磁力架取下,向管内加入40μlyf buffer b,用移液器吸打混匀数次;
[0071]
3.4.室温孵育5min后,将pcr管置于dynamag
‑
96 side磁力架上3min;
[0072]
3.5.移除上清,pcr管继续放置在磁力架上,向管内加入180μl 80%乙醇溶液,静置30s;
[0073]
3.6.移除上清,pcr管继续放置在磁力架上,向管内加入180μl 80%乙醇溶液,静置30s后彻底移除上清;
[0074]
3.7.室温静置10min,使残留乙醇彻底挥发;
[0075]
3.8.将pcr管从磁力架取下,加入22μl nuclease
‑
free water,移液器轻轻吸打重悬磁珠,避免产生气泡,室温静置2min;
[0076]
3.9.将pcr管重新置于磁力架上,静置3min;
[0077]
3.10.用移液器吸取9.4μl上清液,转移到新的200μl pcr管内,管内上清液为多重pcr产物。
[0078]
4.第2轮多重pcr反应
[0079]
4.1.反应体系如下表4所示。
[0080]
表4反应体系
[0081]
reagentvolume(μl)步骤3.10多重pcr反应产物混合物9.4igt
‑
i5(5μm)1igt
‑
i7(5μm)1igt
‑
em101polymerase mixture3.6
[0082]
4.2.反应程序为:95℃3min30s;98℃20s,58℃1min,72℃30s,8cycle;72℃5min。
[0083]
5.第2轮磁珠纯化
[0084]
5.1.向15μl pcr产物加入13.5μl室温平衡后的ampure xp磁珠,用移液器吸打混匀数次;
[0085]
5.2.室温孵育5min后,将pcr管置于dynamag
‑
96 side磁力架上3min;
[0086]
5.3.彻底移除上清,将pcr管从磁力架取下,向管内加入40μl yf buffer b,用移液器吸打混匀数次;
[0087]
5.4.室温孵育5min后,将pcr管置于dynamag
‑
96 side磁力架上3min;
[0088]
5.5.移除上清,pcr管继续放置在磁力架上,向管内加入180μl 80%乙醇溶液,静置30s;
[0089]
5.6.移除上清,pcr管继续放置在磁力架上,向管内加入180μl 80%乙醇溶液,静置30s后彻底移除上清;
[0090]
5.7.室温静置10min,使残留乙醇彻底挥发;
[0091]
5.8.将pcr管从磁力架取下,加入24μl nuclease
‑
free water或者1
×
te buffer(ph 8.0),移液器轻轻吸打重悬磁珠,避免产生气泡,室温静置2min;
[0092]
5.9.将pcr管重新置于磁力架上,静置3min;
[0093]
5.10.用移液器吸取20μl上清液,转移到新的pcr管内,管内上清液为制备的多重pcr文库。
[0094]
6.文库定量
[0095]
取2μl文库样本使用fluorometer(qubitdsdna hs assay kit)进行文库浓度测定,记录文库浓度。
[0096]
7.文库质量检测
[0097]
取1μl文库样本使用agilent 2100bioanalyzer system(high sensitivity dna kit)进行文库片段长度和纯度测量,正常文库的靶片段分布区间在300
‑
400bp之间,主峰在360bp左右。
[0098]
8.将文库上机测序,得到fastaq序列文件。经过质量评估、比对、snp calling等步骤得到待测样本捕获区域的snp的基因型信息,其中质量评估使用fastqc软件,比对使用bwa软件,snp calling使用gatk软件。
[0099]
9.将得到的每一个snp的基因型赋予其在人群研究中的疾病的or值。
[0100]
10.将个体某一疾病所涉及的snp的所有or值进行相乘,即该个体针对该疾病的绝对遗传风险。
[0101]
11.将绝对遗传风险在千人基因组/中国人基因组队列中排名,即该个体针对该疾病的相对遗传风险,排名在5%以内为低风险,在95%以上为高风险,5
‑
95%之间为正常范围。
[0102]
实施例3
[0103]
眼科疾病与基因和检测位点的对应关系如下表5所示。
[0104]
表5
[0105][0106]
实验例1准确性检测
[0107]
使用本技术所述的检测方法对上述16个位点进行检测,同时用sanger测序进行验证,结果如下表6所示。
[0108]
表6准确性检测结果
[0109]
样本位点本技术基因型sanger测序基因型1rs10034228tctc2rs13382811cccc3rs2730260gtgt4rs4395927ctct5rs4455882aaaa6rs6469937gggg7rs7839488gggg8rs9318086gggg9rs11911275agag10rs7615568tttt11rs10483727tttt12rs1063192gggg13rs2487032aaaa14rs3213787agag15rs523096aaaa16rs7865618gggg
[0110]
由表6可知,本技术所述引物组合物及检测方法准确性为100%。
[0111]
实验例2重复性检测
[0112]
选取1例外周血样本a和1例唾液样本b,每个样本重复3次进行一个批次的检测,检测结果如下表7所示。
[0113]
表7重复性检测结果
[0114][0115][0116]
备注:样本a
‑
1为样本a第1次检测。
[0117]
由表7检测结果可知,本技术所述的引物组合物及检测方法重复性为100%。
[0118]
实验例3精密度检测
[0119]
选取1例外周血样本a和1例唾液样本b,每个样本分别使用三个批次的引物组合物进行检测,检测结果如下表8所示。
[0120]
表8精密度检测结果
[0121][0122]
由表8检测结果可知,本技术所述的引物组合物及检测方法精密度为100%。
[0123]
实验例4
[0124]
选取1例外周血样本a按照本技术实施例1和实施例2的方法进行检测,并进行眼科疾病遗传风险的评估,以近视、青光眼、年龄相关性白内障为例,该样本在千人基因组人群和现阶段参照自测基因组人群中的遗传风险如图2
‑
4所示。其中,横坐标为标准化后相对风险or值的自然对数,纵坐标为所对应or值上的人群概率密度。该样本近视or=0.5877,rank
千人基因组
=46.2%,rank
自测
=35.2%;青光眼or=0.6241,rank
千人基因组
=99.7%,rank
自测
=98.6%;年龄相关性白内障or=1,rank
千人基因组
=0.5%,rank
自测
=0.4%。
[0125]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1