一种抗高原反应配方奶粉及其制备方法与流程
1.本发明涉及配方奶粉技术领域,尤其涉及一种抗高原反应配方奶粉及其制备方法。
背景技术:
2.当人从平原进入高原时,会发生呼吸系统、消化系统、神经系统和血液循环系统等一系列应激反应,可能引起心悸、气短、厌食、头晕、视力模糊及焦虑等高原病症状,长期缺氧可诱发心、脑、肺等多器官的不可逆损伤,进而可能发展成为高原肺水肿或高原脑水肿等致命性高原病。高原病的病理生理过程主要是由于高原环境低压性缺氧,使人体血氧饱和度下降,组织缺氧,物质和能量代谢障碍和生理代偿机能衰竭。在这个过程中,营养物质参与体内物质和能量代谢全过程,对改善缺氧环境,减少高原病的发生起重要作用。
3.我国是世界上高原地域最辽阔、居住人口最多的国家,每年都有大批游客、施工人员进入高原。他们都面临着急性高原反应的威胁,同时,急性高原反应也对进驻高原部队官兵的身体健康和生命安全造成了威胁,从一定程度上降低了部队的战斗力。
4.流行病学调查表明,急性高原病在3000m以上高海拔地区的发病率约75%,严重制约着高原人群健康水平的提升以及经济社会与国防军事的发展。
5.现有针对急性高原反应的实施方案,一般是采用药物治疗,或者是采用药食同源的成分进行干预。目前,用于防治高原病的化学药物主要有乙酰唑胺、地塞米松、硝苯地平、布洛芬、扑热息痛等,但均因不同程度的毒副作用,在临床使用上备受限制。
技术实现要素:
6.解决的技术问题:针对现有技术存在的缺点,本发明提供一种抗高原反应配方奶粉及其制备方法,通过营养干预的手段,从清除体内自由基,减缓氧化应激反应;改善胃肠道菌群,预防胃肠道功能紊乱;增加人体细胞的携氧能力,减缓缺氧症状等角度出发,得到了一种能够有效预防或减轻高原反应、增强机体的高原适应力和提高劳动能力的配方奶粉。
7.技术方案:一种抗高原反应配方奶粉,以质量份计含有以下成分:葡萄糖10-30份、乳糖5-10份、糊精5-10份、可溶性膳食纤维5-10份、浓缩乳清蛋白粉15-25份、玉米肽5-10份、全脂牦牛乳粉15-25份、沙棘粉5-10份、l-抗坏血酸0.4-0.8份、醋酸视黄酯0.008-0.01份、硫酸亚铁0.2-0.25份、牛磺酸0.3-0.4份、左旋肉碱酒石酸盐0.4-0.6份、复合益生菌1-1.5份。
8.上述所述的一种抗高原反应配方奶粉,以质量份计含有以下成分:葡萄糖12份、乳糖10份、糊精10份、可溶性膳食纤维10份、浓缩乳清蛋白粉20份、玉米肽10份、全脂牦牛乳粉20份、沙棘粉5份、l-抗坏血酸0.5份、醋酸视黄酯0.01份、硫酸亚铁0.2份、牛磺酸0.4份、左旋肉碱酒石酸盐0.4份、复合益生菌1.5份。
9.上述所述的复合乳酸菌由重量比为1:1:1的乳双歧杆菌、鼠李糖乳杆菌和长双歧
杆菌组成,乳双歧杆菌、鼠李糖乳杆菌和长双歧杆菌的活性均为300亿cfu/g。
10.上述所述的一种抗高原反应配方奶粉的制备方法,该方法的制备步骤如下:
11.步骤一,湿法工艺部分:
12.1)在配料罐中加入温度为40-50℃的纯水,再向配料罐中依次投入葡萄糖、乳糖、糊精、可溶性膳食纤维、浓缩乳清蛋白粉、玉米肽、全脂乳粉、l-抗坏血酸、醋酸视黄酯、硫酸亚铁、牛磺酸、左旋肉碱酒石酸盐这些配料,持续搅拌15-20min,得到料液,其中配料总重量与纯水的重量比为1∶(3-4),
13.2)将料液进行均质,均质压力为20-25mpa,均质温度为50-60℃,得到物料,
14.3)采用三效蒸发器对物料进行浓缩,使得出料浓度为40-45%,得到浓缩液,
15.4)采用压力式喷雾干燥对浓缩液进行干燥,进风温度为140-200℃,出风温度为70-80℃,得到半成品;
16.步骤二,干法工艺部分:
17.将半成品与复合益生菌进行气动混合,混合压力为0.4-0.6mpa,混合时间300s,混合均匀后,进行定量包装,即得抗高原反应配方奶粉。
18.本发明配方中的葡萄糖、乳糖、糊精和可溶性膳食纤维提供了奶粉中的碳水化合物。在高原地区,保证碳水化合物摄取量对维持体力非常重要,配方添加了单糖、二糖、多糖和可溶性膳食纤维,可迅速补充体力,并实现梯度吸收。
19.浓缩乳清蛋白粉和玉米肽提供了奶粉中的蛋白质。当缺氧时,蛋白质和氨基酸分解代谢加强,氮摄入量减少,排出量增加,机体呈负氮平衡;在缺氧适应过程中并不需要增加食物蛋白质的供给量,但重要的是应该选用优质蛋白质食品并注意维持氨基酸平衡。
20.全脂乳粉提供了奶粉中的脂肪。
21.l-抗坏血酸钠、醋酸视黄酯、硫酸亚铁、牛磺酸、左旋肉碱酒石酸盐和益生菌提供了奶粉中的营养素。其中l-抗坏血酸提供了维生素c,有效含量为40-80mg/100g;醋酸视黄酯提供了维生素e,添加量为400-500μg视黄醇当量μg re/100g;硫酸亚铁提供了铁,有效含量为8-10mg/100g;牛磺酸有效含量为30-40mg/100g;左旋肉碱酒石酸盐提供了左旋肉碱,有效含量为30-40mg/100g;乳双歧杆菌、鼠李糖乳杆菌和长双歧杆菌提供了益生菌,活菌含量在配方中不小于1亿cfu/100g。
22.上述所述中的维生素c可以改善缺氧状态下氧化还原过程,提高氧的利用率,改善过氧化损伤。维生素e能减少组织氧的消耗,提高氧的利用率,同时能促进红细胞的生成合含铁细胞酶的合成,并且能改善因缺氧导致的过氧化损伤。硫酸亚铁,按每日300克的剂量补充硫酸亚铁,有利于血红蛋白、肌红蛋白、含铁蛋白质和酶的合成;牛磺酸能够能改善急性缺氧对大鼠肌线粒体功能的损害,减轻急性缺氧所致的视觉损伤,预防急性缺氧时大鼠线粒体中某些酶活性的降低。左旋肉碱能改变呼吸链酶的活性,急性缺氧条件下,适当补充肉碱,可改善缺氧症状,降低高原适应症状。益生菌可以维持胃肠道的平衡,预防因高原缺氧、低气压、氧化应激反应造成的胃肠道功能紊乱。
23.有益效果:本发明提供的一种抗高原反应配方奶粉及其制备方法,具有以下有益效果:
24.1.本发明的配方奶粉以食品为原料,添加营养强化剂和复合益生菌,通过营养干预的手段,迅速补充能量,能够清除因高原强紫外线辐射造成的自由基,增加血红蛋白携氧
能力,调节胃肠道功能,减缓高原急性高原反应症状;
25.2.本发明的配方奶粉,采用营养干预的手段,与药物治疗以及中药材提取物相比,无副作用,更安全。
具体实施方式
26.实施例1
27.该实施例提供一种抗高原反应配方奶粉,以质量份计含有以下成分:葡萄糖12份、乳糖10份、糊精10份、可溶性膳食纤维10份、浓缩乳清蛋白粉20份、玉米肽10份、全脂牦牛乳粉20份、沙棘粉5份、l-抗坏血酸0.5份、醋酸视黄酯0.01份、硫酸亚铁0.2份、牛磺酸0.4份、左旋肉碱酒石酸盐0.4份、乳双歧杆菌0.5份、鼠李糖乳杆菌0.5份和长双歧杆菌0.5份。
28.一种抗高原反应配方奶粉的制备方法,制备步骤如下:
29.步骤一,湿法工艺部分:
30.1)在配料罐中加入温度为40-50℃的纯水,再向配料罐中依次投入葡萄糖、乳糖、糊精、可溶性膳食纤维、浓缩乳清蛋白粉、玉米肽、全脂乳粉、l-抗坏血酸、醋酸视黄酯、硫酸亚铁、牛磺酸、左旋肉碱酒石酸盐这些配料,持续搅拌15-20min,得到料液,其中配料总重量与纯水的重量比为1∶(3-4),
31.2)将料液进行均质,均质压力为20-25mpa,均质温度为50-60℃,得到物料,
32.3)采用三效蒸发器对物料进行浓缩,使得出料浓度为40-45%,得到浓缩液,
33.4)采用压力式喷雾干燥对浓缩液进行干燥,进风温度为140-200℃,出风温度为70-80℃,得到半成品;
34.步骤二,干法工艺部分:
35.将半成品与乳双歧杆菌、鼠李糖乳杆菌、长双歧杆菌进行气动混合,混合压力为0.4-0.6mpa,混合时间300s,混合均匀后,进行定量包装,即得抗高原反应配方奶粉。
36.对本实施例制备得到的抗高原反应配方奶粉进行缓解体力疲劳功能检验和耐缺氧功能试验研究,过程如下。
37.1缓解体力疲劳功能检验
38.1.1材料和方法
39.1.1.1样品
40.由实施例1制备得到的抗高原反应配方奶粉,样品性状乳黄色粉末;规格:1kg/袋;保存条件:常温;保质期:18个月。人体推荐剂量:每日20g/60kgbw。用无菌水配制成不同剂量的受试物,供实验用。
41.1.1.2实验动物
42.选用北京华阜康生物科技股份有限公司[许可证号:scxk-(京)2019-0008]繁殖的18g~20gkm种spf级雄性小鼠204只,经过动物适应饲养观察后,共分为四批进行实验,每批随机分为4组,实验一批每组15只,其余三批每组12只。实验一批进行负重游泳试验,实验二批进行血清尿素的测定,实验三批进行肝糖原的测定,实验四批进行血乳酸的测定。实验动物质量合格证:no.110322210102202737。实验动物饲养于北京联合大学应用文理学院保健食品功能检测中心spf级动物室[许可证号:syxk(京)2017-0038]。维持饲料由北京华阜康生物科技股份有限公司[许可证号:scxk(京)2019-0008]生产。
[0043]
1.1.3剂量
[0044]
实施例1制备得到的抗高原反应配方奶粉的推荐剂量为人体每日20g/60kgbw。实验设人体推荐量的5倍、10倍、30倍,即每日1.67g/kgbw、3.33g/kgbw、10.00g/kgbw为低、中、高剂量组。高剂量受试物:称取样品25.00g,加无菌水至50.0ml;中剂量受试物:称取样品8.32g,加无菌水至50.0ml;低剂量受试物:称取样品4.18g,加无菌水至50.0ml。每日一次经口给予,连续灌胃34d测各项指标。小鼠灌胃体积为20ml/kgbw。同时设一空白对照组(0g/kgbw)。每日灌胃体积与各受试物组相同。各剂量组均给予维持饲料。
[0045]
2.1.4仪器与试剂
[0046]
1.1.4.1仪器
[0047]
uv2600紫外可见分光光度计(2015003)、全自动生化分析仪au480(2015011)、乳酸仪biosenc-line(2017001)、t1000电子天平(2012003)、bs2202s电子天平(2014007)、bs2202s电子天平(2014008)、bs223s电子天平(2008007)、离心机、振荡器、游泳箱、铅丝、加样器、匀浆器、试管。
[0048]
1.1.4.2试剂
[0049]
尿素试剂盒(中生北控生物科技股份有限公司,批号:2011081)。三氯乙酸(天津市光复精细化工研究所,批号:2018.5.6)、葡萄糖.h2o(amresco,批号:2734b53)、硫酸(北京化工厂,批号:20171107)、蒽酮(中国医药集团上海化学试剂公司,批号:20031203)、硫脲(国药集团化学试剂有限公司,批号:20140424)、乙醇:(北京化工厂,批号:20210201)。
[0050]
1.1.5实验方法
[0051]
1.1.5.1负重游泳实验
[0052]
末次给小鼠受试物30min后,将尾根部负荷5%体重铅丝的小鼠置于游泳箱中游泳。水深30cm,水温25.0℃
±
1.0℃,记录小鼠自游泳开始至死亡的时间,作为小鼠负重游泳时间。
[0053]
游泳时间为计量资料,若受试物组游泳时间明显长于空白对照组游泳时间,且差异有显著性(p《0.05),可判定该受试物有延长小鼠负重游泳时间的作用。
[0054]
1.1.5.2血清尿素测定
[0055]
末次给小鼠受试物30min后,在温度为30℃的水中游泳90min,休息60min后立即采血0.5ml。置4℃冰箱约3h,血凝固后3000r/min离心15min,取血清。于生化分析仪上测定。
[0056]
所得数据为计量资料,若受试物组血清尿素含量明显低于空白对照组,且差异有显著性(p《0.05),可判定该受试物有减少疲劳小鼠尿素含量的作用。
[0057]
1.1.5.3肝糖原测定:蒽酮法
[0058]
末次给小鼠受试物30min后,立即处死,取肝脏经生理盐水漂洗后用滤纸吸干,精确称取肝脏100mg,加入4.0mltca,匀浆1min,将匀浆液倒入离心管,以3000r/min离心15min,取上清液0.5ml,加95%乙醇2ml,充分混匀至两种液体间不留有界面,用干净塞子塞上,室温下竖立放置过夜。次日以3000r/min离心15min。小心倒掉上清液并使试管倒立放置10min。用2.00ml蒸馏水溶解糖原待测。取0.25ml待测液和0.25ml蒸馏水放入试管中,混匀。试剂空白管:吸0.5ml蒸馏水到干净试管。标准管:吸0.125ml葡萄糖标准液(50mg/dl)和0.375ml蒸馏水放入试管中,混匀。
[0059]
将2.5ml蒽酮试剂用力加入各管,煮沸15min,然后移到冰水浴,冷却后在620nm波
长下,用试剂空白管调零后测定吸光度。按下式计算肝糖原含量:
[0060][0061]
du:样品管吸光度。v:提取液体积(ml);16:为稀释倍数。
[0062]
ds:标准管吸光度。0.0625:0.125ml葡萄糖标准液中的葡萄糖含量。
[0063]
g:肝组织重量(g)。0.9:将葡萄糖换算成糖原的系数。
[0064]
所得数据为计量资料,若受试物组肝糖原含量明显高于空白对照组,且差异有显著性(p《0.05),可判定该受试物有促进小鼠肝糖原储备的作用。
[0065]
1.1.5.4血乳酸测定
[0066]
游泳前采静息血:由小鼠眼内眦静脉丛取血10μl加入反应管中,充分振摇。
[0067]
高血乳酸模型的制作及血标本制备:末次给予受试物30min后,不负重在30℃的水中游泳10min后停止,立即采血10μl加入反应管中,充分振摇;休息20min后立即采血10μl加入反应管中,充分振摇。用乳酸测定仪测定浓度。
[0068]
按下列计算公式计算血乳酸含量及血乳酸曲线下面积:
[0069]
血乳酸曲线下面积=5
×
(游泳前血乳酸值+3
×
游泳后0min的血乳酸值+2
×
游泳后休息20min的血乳酸值)
[0070]
所得数据为计量资料,若受试物组血乳酸曲线下面积明显低于空白对照组,且差异有显著性(p《0.05),可判定该受试物有减少小鼠游泳后血乳酸曲线下面积的作用。
[0071]
1.1.6试验数据统计
[0072]
用spss软件进行数据处理。采用方差分析,但需按方差分析的程序先进行方差齐性检验,方差齐,计算f值,f值《f0.05,结论:各组均数间差异无显著性;f值≥f0.05,p≤0.05,用多个实验组和一个对照组间均数的两两比较方法进行统计;对非正态或方差不齐的数据进行适当的变量转换,待满足正态或方差齐要求后,用转换后的数据进行统计;若变量转换后仍未达到正态或方差齐的目的,改用秩和检验进行统计。
[0073]
1.1.7结果判定
[0074]
若负重游泳实验结果阳性,且血乳酸、血清尿素、肝糖原三项生化指标中任二项指标阳性,即可判定该受试物具有缓解体力疲劳的功能。
[0075]
经口给予小鼠不同剂量的牦牛乳多肽益生菌沙棘奶粉34d后,与0g/kgbw组比较,受试物在3.33g/kgbw组能延长小鼠的负重游泳时间(p《0.05);在10.00g/kgbw组能延长小鼠的负重游泳时间(p《0.05)、能降低疲劳小鼠血清尿素(p《0.05)、能减少游泳后小鼠血乳酸曲线下面积(p《0.05)。
[0076]
1.2结果
[0077]
1.2.1受试小鼠体重的影响如下表1和表2
[0078]
表1各组小鼠的初始体重(x
±
sd)
[0079][0080]
由表1可见,小鼠的初始体重在四批实验动物各剂量组与0g/kgbw组间比较,均无显著性差异。
[0081]
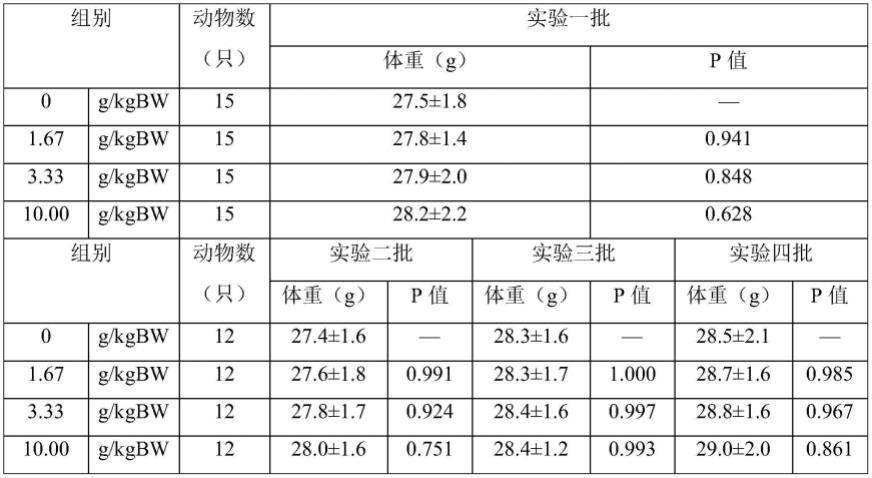
表2给予不同剂量受试物对体重的影响(x
±
sd)
[0082][0083]
由表2可见,经口给予小鼠不同剂量的受试物34d后,小鼠体重在四批实验动物各剂量组与0g/kgbw组间比较,均无显著性差异。
[0084]
1.2.2受试物对小鼠负重游泳时间的影响如下表3
[0085]
表3给予不同剂量受试物对负重游泳时间的影响(x
±
sd)
[0086][0087]
*:与0g/kgbw组间比较有显著性差异
[0088]
由表3可见,经口给予小鼠不同剂量的受试物34d后,与0g/kgbw组间比较,3.33g/kgbw组和10.00g/kgbw组小鼠负重游泳时间延长,有显著性差异。
[0089]
1.2.3受试物对小鼠游泳后血清尿素水平的影响如下表4
[0090]
表4给予不同剂量受试物对游泳后血清尿素的影响(x
±
sd)
[0091][0092]
*:与0g/kgbw组比较有显著性差异。
[0093]
由表4可见,经口给予小鼠不同剂量的受试物34d天后,与0g/kgbw组比较,10.00g/kgbw组小鼠游泳后血清尿素降低,有显著性差异。
[0094]
1.2.4受试物对小鼠肝糖原的影响如下表5
[0095]
表5给予不同剂量受试物对肝糖原含量的影响(x
±
sd)
[0096][0097]
由表5可见,经口给予小鼠不同剂量的受试物34d天后,各剂量组小鼠肝糖原含量与0g/kgbw组比较,均无显著性差异。
[0098]
1.2.5受试物对小鼠游泳后血乳酸值的影响如下表6
[0099]
表6给予不同剂量受试物对游泳后血乳酸值的影响(x
±
sd)
[0100][0101]
*:与0g/kgbw组比较有显著性差异。
[0102]
由表6可见,经口给予小鼠不同剂量的受试物34d天后,与0g/kgbw组比较,10.00g/kgbw组小鼠游泳后血乳酸曲线下面积减少,有显著性差异。
[0103]
1.3结论
[0104]
经口给予小鼠不同剂量的受试物34d后,结果显示:受试物对小鼠体重增长无不良影响。与0g/kgbw组比较,受试物在3.33g/kgbw组能延长小鼠的负重游泳时间(p《0.05);在10.00g/kgbw组能延长小鼠的负重游泳时间(p《0.05)、能降低疲劳小鼠血清尿素(p《0.05)、能减少游泳后小鼠血乳酸曲线下面积(p《0.05)。
[0105]
2耐缺氧功能试验研究
[0106]
2.1材料和方法
[0107]
2.1.1样品
[0108]
由实施例1制备得到的抗高原反应配方奶粉,样品性状为乳黄色粉末;规格:1kg/袋;保存条件:常温;保质期:18个月。人体推荐剂量:每日20g/60kgbw。用无菌水配制成不同剂量的受试物,供实验用。
[0109]
2.1.2实验动物
[0110]
选用北京华阜康生物科技股份有限公司[许可证号:scxk(京)[2019-0008]繁殖的16g~20g昆明种健康清洁级雌性小鼠156只,经过动物适应饲养观察后,共分为三批进行实验,第一批48只,第二批48只,第三批60只,每批按体重随机分为4组。其中实验一批进行常压耐缺氧实验;实验二批进行亚硝酸钠中毒存活实验;实验三批进行急性脑缺血性缺氧实验。实验动物质量合格证:no.110322210102340351。实验动物饲养于北京联合大学应用文理学院保健食品功能检测中心spf级动物室。实验动物使用许可证号:syxk(京)2017-0038。维持饲料由北京华阜康生物科技股份有限公司[许可证号:scxk(京)[2019-0008]生产。
[0111]
2.1.3剂量
[0112]
实施例1制备得到的抗高原反应配方奶粉的推荐剂量为每日20g/60kgbw。实验设人体推荐量的5倍、10倍、20倍,即每日1.67g/kgbw、3.33g/kgbw、6.67g/kgbw为低、中、高剂量组。高剂量受试物:称取样品13.34g,加无菌水至20.0ml;中剂量受试物:称取样品6.66g,加无菌水至20.0ml;低剂量受试物:称取样品3.34g,加无菌水至20.0ml。受试物每日一次经口给予,连续灌胃30d后,测各项指标。小鼠灌胃体积为10g/kgbw。同时设一空白对照组(0g/kgbw),用无菌水代替受试物,每日灌胃体积与各受试物组相同。各剂量组均给予维持饲料。
[0113]
2.1.4仪器与试剂
[0114]
250ml磨口广口瓶、1ml注射器、电子秒表、t1000电子天平、bs2202s电子天平、凡士林、钠石灰、亚硝酸钠
[0115]
2.1.5实验方法
[0116]
2.1.5.1常压耐缺氧试验
[0117]
末次给予实验用受试物后1h,将小鼠分别放入盛有5.0g钠石灰的250ml磨口广口瓶中(每瓶一只小鼠)。用凡士林涂抹瓶口,盖严,使之不漏气。立即记录时间,以呼吸停止为标准,记录小鼠因缺氧而死亡的时间。受试样品组小鼠的常压耐缺氧存活时间显著长于对照组,并具有统计学意义,即可判定受试物的该项指标实验结果阳性。
[0118]
2.1.5.2亚硝酸钠中毒存活试验
[0119]
末次给予实验用受试物后1h,各组小鼠均腹腔注射亚硝酸钠溶液240mg/kgbw(注射量为0.1ml/10gbw),立即计时,记录小鼠存活时间。受试样品组小鼠的亚硝酸钠中毒缺氧存活时间显著长于对照组,并具有统计学意义,即可判定该项指标结果阳性。
[0120]
2.1.5.3急性脑缺血缺氧试验
[0121]
末次给予实验用受试物后1h,将小鼠自颈部逐只断头,立即记录小鼠断头后至张口喘气停止时间。受试样品组小鼠的张口喘气时间显著长于对照组,并具有统计学意义,即可判定该项指标结果阳性。
[0122]
2.1.5.4数据处理
[0123]
用spss软件进行数据处理。采用方差分析,但需按方差分析的程序先进行方差齐性检验,方差齐,计算f值,f值《f0.05,结论:各组均数间差异无显著性;f值≥f0.05,p≤0.05,用多个实验组和一个对照组间均数的两两比较方法进行统计;对非正态或方差不齐的数据进行适当的变量转换,待满足正态或方差齐要求后,用转换后的数据进行统计;若变量转换后仍未达到正态或方差齐的目的,改用秩和检验进行统计。
[0124]
2.1.5.5结果判定依据:
[0125]
常压耐缺氧实验、亚硝酸钠中毒实验、急性脑缺血性缺氧实验三项实验中任二项实验结果阳性,可判定该受试样品具有缺氧耐的作用。
[0126]
2.2结果
[0127]
2.2.1受试物对小鼠体重的影响如下表7和表8
[0128]
表7各组小鼠的初始体重(
±
sd)
[0129][0130]
由表7可见,小鼠的初始体重在三批实验动物各剂量组与0g/kgbw组间比较,差异
均无显著性。
[0131]
表8给予不同剂量受试物对小鼠体重的影响(
±
sd)
[0132][0133]
由表8可见,经口给予小鼠不同剂量的受试物30d后,小鼠的体重在三批各剂量组与0g/kgbw组间比较,差异均无显著性。
[0134]
2.2.2受试物对小鼠常压耐缺氧存活时间的影响如下表9
[0135]
表9给予不同剂量受试物对小鼠常压耐缺氧存活时间的影响(
±
sd)
[0136]
组别动物数(只)存活时间(min)p值0g/kgbw1238.4
±
5.5——1.67g/kgbw1237.5
±
6.10.9843.33g/kgbw1244.2
±
6.80.1126.67g/kgbw1245.3
±
8.7*0.045
[0137]
*:与0g/kgbw组比较有显著差异
[0138]
由表9可见,经口给予小鼠不同剂量的受试物30d后,与0g/kgbw组比较,6.67g/kgbw组小鼠常压耐缺氧存活时间延长,有显著差异。
[0139]
2.2.3受试物对小鼠亚硝酸钠中毒存活时间的影响如下表10
[0140]
表10给予不同剂量受试物对小鼠亚硝酸钠中毒存活时间的影响(
±
sd)
[0141]
组别动物数(只)存活时间(min)p值0g/kgbw1220.1
±
4.7——1.67g/kgbw1223.8
±
4.20.1783.33g/kgbw1224.0
±
6.50.1536.67g/kgbw1226.3
±
4.3*0.012
[0142]
*:与0g/kgbw组比较有显著差异
[0143]
由表10可见,经口给予小鼠不同剂量的受试物30d后,与0g/kgbw组比较,6.67g/kgbw组小鼠亚硝酸钠中毒存活时间延长,有显著差异。
[0144]
2.2.4受试物对小鼠急性脑缺血性缺氧实验的影响如下表11
[0145]
表11给予不同剂量受试物对小鼠急性脑缺血性缺氧实验的影响(
±
sd)
[0146]
组别动物数(只)张口喘气时间(s)p值0g/kgbw1519.8
±
3.1——
1.67g/kgbw1519.9
±
3.40.9993.33g/kgbw1522.3
±
4.80.1656.67g/kgbw1522.5
±
2.90.110
[0147]
由表11可见,经口给予小鼠不同剂量的受试物30d后,各剂量组小鼠急性脑缺血性缺氧实验张口喘气时间与0g/kgbw组比较,差异均无显著性。
[0148]
2.3结论
[0149]
经口给予小鼠不同剂量的受试物30d后,结果显示:受试物对小鼠体重增长无不良影响。与0g/kgbw组比较,6.67g/kgbw组能延长小鼠常压耐缺氧存活时间(p《0.05)、能延长小鼠亚硝酸钠中毒存活时间(p《0.05)。
[0150]
3总结论
[0151]
经给予小鼠不同剂量的受试物34d后,受试物对小鼠体重增长无不良影响。与0g/kgbw组比较,受试物在3.33g/kgbw组能延长小鼠的负重游泳时间(p《0.05);在10.00g/kgbw组能延长小鼠的负重游泳时间(p《0.05)、能降低疲劳小鼠血清尿素(p《0.05)、能减少游泳后小鼠血乳酸曲线下面积(p《0.05)。
[0152]
因此,经过抗缺氧试验以及抗疲劳试验,可以证明实施例1制备得到的抗高原反应配方奶粉,可显著提高小鼠常压缺氧存活时间;能够延长亚硝酸钠中毒存活时间;能够延长小鼠负重游泳时间;能够减少游泳后血液中的乳酸指标;降低疲劳小鼠血清尿素指标,具备耐缺氧和抗疲劳功能功能。
[0153]
以上对本发明实施例进行了详细介绍,对于本领域的一般技术人员,依据本发明实施例的思想,在具体实施方式及应用范围上均会有改变之处,综上所述,本说明书内容不应理解为对本发明的限制。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1