使用IL-2受体激动剂和免疫检查点抑制剂的组合疗法的制作方法
使用il-2受体激动剂和免疫检查点抑制剂的组合疗法
相关申请的交叉引用
1.本技术要求2019年12月24日提交的美国临时专利申请序列号62/953,362和2020年6月22日提交的美国临时专利申请序列号63/042,361的优先权,将其各自通过引用以其整体并入本文。对光盘上提交的“序列表”、表格或计算机程序列表附录的引用
2.本技术含有序列表,所述序列表已经以ascii格式电子提交,并且通过引用以其整体特此并入。在2020年11月6日创建的所述ascii拷贝命名为057318_504001wo_sequence_listing_st25.txt并且大小为28千字节。
背景技术:
3.检查点抑制剂的单一疗法在一些患者中显示出显著的临床功效,但是在其他患者中显示出较差的临床功效。需要开发另外的治疗方法来提高检查点抑制剂的有效性。本发明满足这种和其他需要。
技术实现要素:
4.本公开文本尤其涉及用于使用il-2受体激动剂与免疫检查点抑制剂组合来调节有需要的受试者的免疫应答的方法。
附图说明
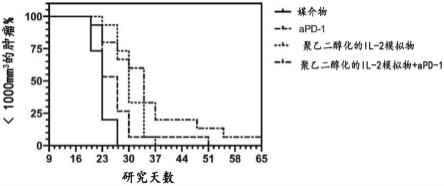
5.图1展现了il-2受体激动剂(聚乙二醇化的il-2模拟物)与pd-1抑制剂组合在ct26结肠癌模型中的抗肿瘤活性。
6.图2展现了il-2受体激动剂(聚乙二醇化的il-2模拟物)与pd-l1抑制剂组合在ct26结肠癌模型中的抗肿瘤活性。
7.图3展现了il-2受体激动剂(聚乙二醇化的il-2模拟物)与pd-1抑制剂组合在mc38结肠癌模型中的抗肿瘤活性。
8.图4展现了il-2受体激动剂(聚乙二醇化的il-2模拟物)与pd-l1抑制剂组合在mc38结肠癌模型中的抗肿瘤活性。
9.图5展现了il-2受体激动剂(聚乙二醇化的il-2模拟物)与pd-1抑制剂和ctla-4抑制剂(cpi)组合在b16f10小鼠黑色素瘤模型中的抗肿瘤活性。
10.图6展现了il-2受体激动剂(聚乙二醇化的il-2模拟物)对cd8+t细胞的pd-1表达的影响。
具体实施方式
i.实施方案的详细描述
11.本公开文本尤其涉及用于使用il-2受体激动剂与免疫检查点抑制剂组合(i)调节
有需要的受试者的免疫应答、(ii)治疗有需要的受试者的癌症或(iii)抑制有需要的受试者的肿瘤的增殖的方法。a.il-2受体激动剂
12.如本文所用的术语il-2受体激动剂是指能够激活il-2受体介导的信号传导的多肽。在示例性实施方案中,il-2受体激动剂是长效il-2受体激动剂。长效意指il-2受体激动剂具有3小时或更长,优选4小时或更长的血浆或血清半衰期。在一些方面,il-2受体激动剂将具有10小时或更长或12小时或更长的血清或血浆半衰期。多肽的半衰期是指多肽的浓度降低50%所需的时间,如通过适当的测定测量的。减少可以由多肽的体内降解、清除或螯合引起。鉴于本公开文本,可以通过本领域已知的任何方式(如通过测量血液中多肽的浓度)确定多肽的半衰期。例如,为了测量多肽在体内的半衰期,将合适剂量的多肽施用至温血动物(即,人或另一种合适的哺乳动物,如小鼠、兔、大鼠、猪、狗或灵长类动物);收集来自所述动物的血液样品或其他样品;确定样品中多肽的水平或浓度;并且根据测量的数据计算直到多肽的水平或浓度降低50%的时间。参见例如,kenneth,a等人,chemical half-life of pharmaceuticals:a handbook for pharmacists和peters等人,pharmacokinetic analysis:a practical approach(1996)。如本文所用,“半衰期增加”或“更长的半衰期”是指与对照相比,用于描述半衰期的任一个或多个参数(如t1/2-α、t1/2-β和曲线下面积(auc))的增加。il-2受体激动剂的长效性质可能是由于与il-2多肽缀合或融合的部分所致。如本文所用,术语“多肽”、“蛋白质”或“肽”是指任何氨基酸残基链,无论其长度或翻译后修饰(例如,糖基化或磷酸化)如何。
13.本发明的示例性il-2受体激动剂是il-2模拟物。il-2模拟物描述于silva等人,nature 2019年1月;565(7738):186-191和美国专利号10,703,791中。用于本发明方法的示例性il-2模拟物诱导il-2rβγc的异二聚化,导致stat5的磷酸化。本发明的il-2模拟物与il-2受体βγc异二聚体(il-2rβγc)结合,并且通常包含四个螺旋肽,任选地由氨基酸接头分开。
14.neo-2/15(silva等人,nature 2019年1月;565(7738):186-191和美国专利号10,703,79)包含4个螺旋结构域x1、x2、x3和x4。螺旋结构域x1包含seq id no:27所示的氨基酸序列(pkkkiqlhaehalydalmilni);螺旋结构域x2包含seq id no:28所示的氨基酸序列(kdeaekakrmkewmkrikt);螺旋结构域x3包含seq id no:29所示的氨基酸序列(ledyafnfelileeiarlfesg);并且螺旋结构域x4包含seq id no:30所示的氨基酸序列(edeqeemanaiitilqswifs)。在neo-2/15中,这些螺旋结构域的顺序为x1-x3-x2-x4并且通过氨基酸接头连接在一起。由于neo-2/15是从头合成的蛋白质,在本发明中用作il-2受体激动剂的neo-2/15的变体在螺旋结构域和氨基酸接头中可能具有很大的可变性同时仍保留与il-2受体βγc异二聚体结合的能力。用于确定与il-2受体βγc异二聚体(il-2rβγc)结合的方法是本领域已知的,用于确定il-2受体激动剂活性的方法(例如,经由stat5磷酸化测定)也是如此。参见例如,silva等人,nature 2019年1月;565(7738):186-191。
15.要用于本发明方法的il-2受体激动剂包括这样的il-2模拟物,所述模拟物包含与seq id no:1所示的氨基酸序列(即,neo-2/15多肽)至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列。在其他方面,要用于本发明方法的il-2受体激动剂包括这样的il-2模拟物,所述模拟物包含与seq id no:2所示
的氨基酸序列至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列。seq id no:2是与seq id no:1相同的序列,但是接头氨基酸是任选的并且接头的每个氨基酸残基,当存在时,可以包含任何天然或非天然氨基酸。在seq id no:2中,带下划线的残基(用x标记)是接头并且接头的每个残基,当存在时,可以是任何氨基酸(优选地,天然氨基酸)。在示例性实施方案中,所述氨基酸是天然氨基酸。氨基酸接头,当存在时,连接结构域。氨基酸接头可以是被认为适合预期用途的任何长度。包含具有与seq id no:1或seq id no:2的氨基酸序列的同一性(例如,与seq id no:1或seq id no:2的80%-99%同一性)的氨基酸序列的il-2模拟物在本文中也称为neo-2/15变体。术语天然氨基酸是指蛋白质中天然存在的20种氨基酸。如本文所用,术语“非天然氨基酸”是指除蛋白质中天然存在的20种氨基酸之外的氨基酸。非天然氨基酸是本领域中已知的。
16.如本文所用的关于多肽序列的术语“同一性”是指两个分子之间的氨基酸序列同一性。当两个分子中的一个氨基酸位置被相同的氨基酸占据时,则所述分子在该位置上是相同的。两个多肽之间的同一性是相同位置数的直接函数。通常,将序列进行比对,以便获得最高级别的匹配(必要时包括空位)。可以使用已公布的技术和广泛可用的计算机程序来计算同一性,所述计算机程序如gcg程序包(devereux等人,nucleic acids res.12:387,1984)、blastp、fasta(atschul等人,j.molecular biol.215:403,1990)等。序列同一性可以例如使用序列分析软件以其默认参数来测量,如university of wisconsin biotechnology center(1710university avenue,麦迪逊,威斯康星州53705)的genetics computer group的序列分析软件包。如果添加或缺失氨基酸,则应以不会严重干扰蛋白质向其结合配偶体的呈递和二级结构的方式进行。通常,但不是必须地,相对于参考肽结构域的氨基酸取代优选为保守氨基酸取代。
17.如本文所用,“保守氨基酸取代”意指给定的氨基酸可以被具有相似理化特征的残基替代,例如,用一个脂肪族残基取代另一个(如用ile、val、leu或ala相互取代),或者用一个极性残基取代另一个(如在lys和arg之间;glu和asp之间;或gln和asn之间)。其他此类保守取代,例如具有相似疏水性特征的整个区域的取代,是已知的。可以使用本领域已知的方法测试包含氨基酸取代的多肽以确认所需的活性,例如受体结合活性被保留。氨基酸可根据其侧链特性的相似性进行分组(a.l.lehninger,biochemistry,第二版,第73-75页,worth publishers,纽约(1975)):(1)非极性:ala(a)、val(v)、leu(l)、ile(i)、pro(p)、phe(f)、trp(w)、met(m);(2)不带电荷的极性:gly(g)、ser(s)、thr(t)、cys(c)、tyr(y)、asn(n)、gln(q);(3)酸性:asp(d)、glu(e);(4)碱性:lys(k)、arg(r)、his(h)。可替代地,天然存在的残基可以基于共同的侧链特性分成多组:(1)疏水性的:正亮氨酸、met、ala、val、leu、ile;(2)中性亲水性的:cys、ser、thr、asn、gln;(3)酸性:asp、glu;(4)碱性:his、lys、arg;(5)影响链取向的残基:gly、pro;(6)芳香族:trp、tyr、phe。非保守取代将需要将这些类别之一的成员交换为另一类别。特定的保守取代包括,例如:ala变成gly或变成ser;arg变成lys;asn变成gln或变成his;asp变成glu;cys变成ser;gln变成asn;glu变成asp;gly变成ala或变成pro;his变成asn或变成gln;ile变成leu或变成val;leu变成ile或变成val;lys
变成arg、变成gln或变成glu;met变成leu、变成tyr或变成ile;phe变成met、变成leu或变成tyr;ser变成thr;thr变成ser;trp变成tyr;tyr变成trp;和/或phe变成val、变成ile或变成leu。在一些方面,结合或活性不需要的氨基酸被半胱氨酸替代以允许附接稳定性部分。
18.如本文所用,天然氨基酸残基缩写如下:丙氨酸(ala;a)、天冬酰胺(asn;n)、天冬氨酸(asp;d)、精氨酸(arg;r)、半胱氨酸(cys;c)、谷氨酸(glu;e)、谷氨酰胺(gln;q)、甘氨酸(gly;g)、组氨酸(his;h)、异亮氨酸(ile;i)、亮氨酸(leu;l)、赖氨酸(lys;k)、甲硫氨酸(met;m)、苯丙氨酸(phe;f)、脯氨酸(pro;p)、丝氨酸(ser;s)、苏氨酸(thr;t)、色氨酸(trp;w)、酪氨酸(tyr;y),和缬氨酸(val;v)。
19.本发明的il-2受体激动剂包括在x1、x2、x3、x4和/或氨基酸接头结构域中具有一个或多个氨基酸取代的neo-2/15的变体,条件是所述变体保留neo-2/15活性(例如,与il-2受体βγc异二聚体(il-2rβγc)结合而导致stat5磷酸化的能力)。
20.本发明包括包含neo-2/15的x1结构域的neo-2/15变体,条件是:位置1处的氨基酸是p或如果被取代是a、f、i、l、m、q、r、s或w;位置2处的氨基酸是k或如果被取代是a、d、e、g或v;位置3处的氨基酸是k或如果被取代是d、e、f或w;位置4处的氨基酸是k或如果被取代是d、e、n、p、r或w;位置5处的氨基酸是i或如果被取代是d、e、h、k、l、m或s;位置6处的氨基酸是q或如果被取代是a、d、e、g、l、p、s或w;位置7处的氨基酸是l或如果被取代是d、e、q、y或i;位置8处的氨基酸是h或如果被取代是a、f、w、y、m或t;位置9处的氨基酸是a或如果被取代是c、f或p;位置10处的氨基酸是e或如果被取代是c、d、f、k或p;位置11处的氨基酸是h或如果被取代是d、f或e;位置12处的氨基酸是a或如果被取代是d、e、p、s、t或v;位置13处的氨基酸是l或如果被取代是h、i、m、p、r、v或w;位置14处的氨基酸是y或如果被取代是f、r、w或k;位置15处的氨基酸是d或如果被取代是e、n或y;位置16处的氨基酸是a或如果被取代是c、l、m或s;位置17处的氨基酸是l或如果被取代是f、i、m、p或r;位置18处的氨基酸是m或如果被取代是g、q、y或s;位置19处的氨基酸是i或如果被取代是l、m、p、q或v;位置20处的氨基酸是l或如果被取代是a、k、m、q、r或s;位置21处的氨基酸是n或如果被取代是g、k、p、r、s或w;位置22处的氨基酸是i或如果被取代是d、e、k、m、n、w或y;并且氨基酸位置参考seq id no:27。
21.在一些此类实施方案中,以下中的1个、2个、3个、4个或5个不是真的:位置7是i、位置8是m或t、位置11是e、位置14是k、以及位置18是s。氨基酸位置参考seq id no:27。
22.本发明包括包含neo-2/15的x2结构域的neo-2/15变体,条件是:位置1处的氨基酸是k或如果被取代是a、h、l、m、r、s或v;
位置2处的氨基酸是d或如果被取代是a、e、q、r、s、t、v、w或y;位置3处的氨基酸是e或如果被取代是c、g、k、l、n、q、r或w;位置4处的氨基酸是a或如果被取代是f、g、n、s、t、v或y;位置5处的氨基酸是e或如果被取代是a、g、i、m、r、v或c;位置6处的氨基酸是k或如果被取代是c、e、l、n、r或v;位置7处的氨基酸是a或如果被取代是c、e、i、l、s、t、v或w;位置8处的氨基酸是k或如果被取代是h、l、m、s、t、w或y;位置9处的氨基酸是r或如果被取代是a、i、l、m、q、或s;位置10处的氨基酸是m或如果被取代是a、i、s、w或y;位置11处的氨基酸是k或如果被取代是c、i、l、s或v;位置12处的氨基酸是e或如果被取代是c、k、l、p、q、r或t;位置13处的氨基酸是w或如果被取代是a、d、h或n;位置14处的氨基酸是m或如果被取代是a、c、g、i、l、s、t或v;位置15处的氨基酸是k或如果被取代是a、e、g、i、l、m、r或v;位置16处的氨基酸是r或如果被取代是g、h、l、s、t、v或c;位置17处的氨基酸是i或如果被取代是a、l或v;位置18处的氨基酸是k或如果被取代是a、c、d、e、g、h、i、m或s;并且位置19处的氨基酸是t或如果被取代是d、e、g、l、n或v;并且氨基酸位置参考seq id no:28。
23.本发明包括包含neo-2/15的x3结构域的neo-2/15变体,条件是;位置1处的氨基酸是l或如果被取代是a;位置2处的氨基酸是e或如果被取代是d、g、k、m或t;位置3处的氨基酸是d或如果被取代是e、n、y或r;位置4处的氨基酸是y或如果被取代是c、d、g、t或f;位置5处的氨基酸是a或如果被取代是f、h、s、v、w或y;位置6处的氨基酸是f或如果被取代是a、i、m、t、v、y或k;位置7处的氨基酸是n或如果被取代是d、k、s、t或r;位置8处的氨基酸是f或如果被取代是a、c、g、l、m、s或v;位置9处的氨基酸是e或如果被取代是c、h、k、l、r、s、t或v;位置10处的氨基酸是l或如果被取代是f、i、m、y或r;位置11处的氨基酸是i或如果被取代是l、n、t或y;位置12处的氨基酸是l或如果被取代是f、k、m、s或v;位置13处的氨基酸是e或如果被取代是a、d、f、g、i、n、p、q、s、t或w;位置14处的氨基酸是e或如果被取代是a、f、g、h、s或v;位置15处的氨基酸是i或如果被取代是c、l、m、v或w;位置16处的氨基酸是a或如果被取代是d、g、s、t或v;位置17处的氨基酸是r或如果被取代是h、k、l或n;位置18处的氨基酸是l或如果被取代是c、d、g、i、q、r、t或w;位置19处的氨基酸是f或如果被取代是d、m、n或w;
位置20处的氨基酸是e或如果被取代是a、c、f、g、m、s或y;位置21处的氨基酸是s或如果被取代是d、e、g、h、l、m、r、t、v或w;位置22处的氨基酸是g或如果被取代是a、d、k、n、s或y;并且氨基酸位置参考seq id no:29。
24.在一些此类实施方案中,以下中的1个、2个、3个、4个、5个、6个、7个或所有8个不是真的:位置3是r、位置4是f、位置6是k、位置7是r、位置10位是r、位置11是n、位置13是w、以及位置14是g。氨基酸位置参考seq id no:29。
25.本发明包括包含neo-2/15的x4结构域的neo-2/15变体,条件是:位置1处的氨基酸是e或如果被取代是d、g、k或v;位置2处的氨基酸是d或如果被取代是i、m或s;位置3处的氨基酸是e或如果被取代是g、h或k;位置4处的氨基酸是q或如果被取代是e、g、i、k、r或s;位置5处的氨基酸是e或如果被取代是a、d、g、h、s或v;位置6处的氨基酸是e或如果被取代是c、d、g、i、m、q、r、t或v;位置7处的氨基酸是m或如果被取代是c、e、l、p、r或t;位置8处的氨基酸是a或如果被取代是f、l、m或w;位置9处的氨基酸是n或如果被取代是a、g、l、q、r或t;位置10处的氨基酸是a或如果被取代是c、d、e、f、h、i或w;位置11处的氨基酸是i或如果被取代是m、n、s、v或w;位置12处的氨基酸是i或如果被取代是k、l、s或v;位置13处的氨基酸是t或如果被取代是c、l、m、r或s;位置14处的氨基酸是i或如果被取代是l、p、t或y;位置15处的氨基酸是l或如果被取代是f、g、i、m、n或v;位置16处的氨基酸是q或如果被取代是h、k或r;位置17处的氨基酸是s或如果被取代是c、f、k、w或y;位置18处的氨基酸是w或如果被取代是k、q或t;位置19处的氨基酸是i或如果被取代是c、g或n;位置20处的氨基酸是f或如果被取代是c、g、l或y;并且位置21处的氨基酸是s或如果被取代是a、f、g、h或y;并且氨基酸位置参考seq id no:30。
26.在一些此类实施方案中,位置19不是i。在一些此类方面,位置19是c、g或n。氨基酸位置参考seq id no:30。
27.这些实施方案中的任一个中包括neo-2/15变体,其中以下中的1个、2个、3个、4个、5个、6个、7个、8个、9个、10个、11个、12个、13个或所有14个不是真的:位置7是i、位置8是t或m、位置11是e、位置14是k、位置18是s、位置33是q、位置36是r、位置37是f、位置39是k、位置40是r、位置43是r、位置44是n、位置46是w、以及位置47是g,其中所述位置参考seq id no:1。在另一实施方案中,以下中的一个或两个不是真的:位置68是i以及位置98是f,其中所述位置参考seq id no:1。当接头的长度为不同长度时,残基的编号将相应地改变。
28.用于本发明方法的示例性il-2模拟物(包括neo-2/15变体)与稳定部分(例如像水
稳定部分,如含peg部分)缀合或融合。在一些方面,il-2模拟物中的半胱氨酸残基用于附接peg部分。因此,本发明包括作为il-2模拟物的il-2受体激动剂,所述模拟物包含与seq id no:1或seq id no:2所示的氨基酸序列至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列,除了对结合不是必需的氨基酸突变为半胱氨酸残基用于将稳定部分附接至其上。在一些方面,所述il-2模拟物包含seq id no:1或2所示的氨基酸序列,除了相对于seq id no:1的位置50、53、62、69、73、82、56、58、59、66、77或85中的一处或多处的氨基酸被突变为半胱氨酸残基用于将部分(例如,含peg部分)附接至其上。如上所述,本领域技术人员将理解,在其中氨基酸接头具有不同长度的实施方案中,残基的编号将相应地改变。如上所述,本领域技术人员将理解,在其中氨基酸接头具有不同长度的实施方案中,残基的编号将相应地改变。例如,提及相对于seq id no:1的“位置50”意指seq id no:2中对应于seq id no:1中位置50的位置。
29.本发明包括这样的il-2模拟物,所述模拟物包含与seq id no:1或2所示的氨基酸序列至少25%、27%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、98%或100%相同,但是存在以下突变中的一个、二个、三个、四个、五个、六个、七个、八个、九个、十个、十一个或所有十二个的氨基酸序列:d56c;k58c;d59c;r66c;t77c;e85c;r50c;e53c;e62c;e69c;r73c;和/或e82c。
30.本发明包括这样的il-2模拟物,所述模拟物包含与seq id no:1或2所示的氨基酸序列至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同,但是存在以下突变中的一个、二个、三个、四个、五个、六个、七个、八个、九个、十个、十一个或所有十二个的氨基酸序列:d56c;k58c;d59c;r66c;t77c;e85c;r50c;e53c;
e62c;e69c;r73c;和/或e82c。
31.本领域技术人员将理解,关于seq id no:2,上文提及的位置56、58、59、66、77、85、50、53、62、69、73和82是指分别对应于seq id no:1中的位置56、58、59、66、77、85、50、53、62、69、73、82的seq id no:2中的位置,而不一定是seq id no:2中的实际位置,这可能会因接头的长度而变化。
32.用于本发明的示例性il-2模拟物包括包含seq id no:3-26所示的氨基酸序列的那些。在一些此类实施方案中,il-2模拟物包含与选自seq id no:3-26中的任一个的氨基酸序列至少80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%相同的氨基酸序列。带下划线的残基是接头并且接头的每个残基(“x”),当存在时,可以是任何天然或非天然氨基酸(优选天然氨基酸)。对于以下的每个il-2模拟物,提供了两个seq id no:列出了如下所示的序列的第一seq id no:;和包括接头位置作为变量的第二seq id no:。应当理解,相当于r50c(或所列突变)的位置将根据接头的长度并入指定位置。在说明性实施方案中,存在所指示的半胱氨酸。包含具有与seq id no:3-26的氨基酸序列的同一性(例如与seq id no:3-26的80%-99%同一性)的氨基酸序列的il-2模拟物在本文中也称为neo-2/15变体。
33.因此,本文提供了用于本发明的il-2受体激动剂,所述激动剂是包含与选自seq id no.3-26的氨基酸序列至少80%相同的氨基酸序列的il-2模拟物。本文提供了用于本发明的il-2受体激动剂,所述激动剂是包含与选自seq id no.3-26的氨基酸序列至少85%相同的氨基酸序列的il-2模拟物。本文提供了用于本发明的il-2受体激动剂,所述激动剂是包含与选自seq id no.3-26的氨基酸序列至少90%相同的氨基酸序列的il-2模拟物。本文提供了用于本发明的il-2受体激动剂,所述激动剂是包含与选自seq id no.3-26的氨基酸序列至少95%相同的氨基酸序列的il-2模拟物。本文提供了用于本发明的il-2受体激动剂,所述激动剂是包含选自seq id no.3-26的氨基酸序列的il-2模拟物。在这些实施方案中的任一个中,所述多肽可以是如本文所述的il-2模拟物,其中以下中的1个、2个、3个、4
个、5个、6个、7个、8个、9个、10个、11个、12个、13个或所有14个不是真的:位置7是i、位置8是t或m、位置11是e、位置14是k、位置18是s、位置33是q、位置36是r、位置37是f、位置39是k、位置40是r、位置43是r、位置44是n、位置46是w、以及位置47是g。在另一实施方案中,以下中的一个或两个不是真的:位置68是i以及位置98是f。所述位置参考seq id no:1。在说明性实施方案中,存在所指示的半胱氨酸。
34.本发明的示例性il-2模拟物与其他化合物连接,以促进体内半衰期的增加,例如peg化合物。“peg”是聚(乙二醇)分子,其是乙二醇的水溶性聚合物。peg可以以不同的大小获得,并且也可以在商业上以化学激活的形式获得,这些形式用化学反应性基团衍生,以使得能够与蛋白质共价缀合。产生各种分子量的直链peg,如重量平均分子量为5,000道尔顿、10,000道尔顿、20,000道尔顿、30,000道尔顿和40,000道尔顿的peg聚合物。还开发了支化的peg聚合物。用于将多肽与peg缀合的方法是本领域已知的并且可以在本文中使用。通常使用的激活的peg聚合物是用马来酰亚胺或碘乙酰胺基团(用于与硫醇(如半胱氨酸残基)偶联)衍生的。例如,在一些实施方案中,含有聚乙二醇(“peg”)的部分的添加可能包括使与马来酰亚胺基团连接的peg基团(例如,“peg-mal”)与多肽的半胱氨酸残基附接。与马来酰亚胺基团连接的peg基团(“peg-mal”)的合适的例子包括但不限于甲氧基peg-mal 5kd;甲氧基peg-mal20kd;甲氧基(peg)2-mal 40kd;甲氧基peg(mal)2 5kd;甲氧基peg(mal)2 20kd;甲氧基peg(mal)2 40kd;或其任何组合。还参见美国专利号8,148,109。熟练技术人员将能够使用本文所述的方法或替代方法来设计用于本发明的长效il-2受体激动剂,所述方法包括通过将peg基团与本发明的il-2模拟物附接,无论是经由马来酰亚胺或另一种附接策略。
35.在一些实施方案中,要用于本发明方法的il-2受体激动剂包含seq id no:13(neo 2-15e62c)所示的氨基酸序列,其中位置62处的半胱氨酸是聚乙二醇化的。聚乙烯基团可以经由任何合适的附接化学来附接,包括例如用马来酰亚胺(例如,马来酰亚胺修饰的peg、peg-mal 5kd;peg-mal 20kd;或peg-mal 40kd)。在一些实施方案中,聚乙二醇化是用peg-mal 30kd进行的。在一些实施方案中,聚乙二醇化是用peg-mal 40kd进行的。在一些实施方案中,聚乙二醇化的肽中重复peg单元的范围是约800-1000。在一些实施方案中,聚乙二醇化的肽中重复peg单元的平均数量是约850-950。本领域技术人员将理解peg部分可以是直链的或支化的。
36.在一些实施方案中,要用于本发明方法的il-2受体激动剂包含seq id no:23(neo 2-15e82c)所示的氨基酸序列,其中位置82处的半胱氨酸是聚乙二醇化的。聚乙烯基团可以经由任何合适的附接化学来附接,包括例如用马来酰亚胺(例如,马来酰亚胺修饰的peg、peg-mal 5kd;peg-mal 20kd;或peg-mal 40kd)。在一些实施方案中,聚乙二醇化是用peg-mal 30kd进行的。在一些实施方案中,聚乙二醇化是用peg-mal 40kd进行的。在一些实施方案中,聚乙二醇化的肽中重复peg单元的范围是约800-1000。在一些实施方案中,聚乙二醇化的肽中重复peg单元的平均数量是约850-950。本领域技术人员将理解peg部分可以是直链的或支化的。
37.在一些实施方案中,要用于本发明方法的il-2受体激动剂包含seq id no:17(neo 2-15e69c)所示的氨基酸序列,其中位置69处的半胱氨酸是聚乙二醇化的。聚乙烯基团可以经由任何合适的附接化学来附接,包括例如用马来酰亚胺(例如,马来酰亚胺修饰的peg、
peg-mal 5kd;peg-mal 20kd;或peg-mal 40kd)。在一些实施方案中,聚乙二醇化是用peg-mal 30kd进行的。在一些实施方案中,聚乙二醇化是用peg-mal 40kd进行的。在一些实施方案中,聚乙二醇化的肽中重复peg单元的范围是约800-1000。在一些实施方案中,聚乙二醇化的肽中重复peg单元的平均数量是约850-950。本领域技术人员将理解peg部分可以是直链的或支化的。
38.在一些实施方案中,要用于本发明方法的il-2受体激动剂包含seq id no:19(neo 2-15r73c)所示的氨基酸序列,其中位置73处的半胱氨酸是聚乙二醇化的。聚乙烯基团可以经由任何合适的附接化学来附接,包括例如用马来酰亚胺(例如,马来酰亚胺修饰的peg、peg-mal 5kd;peg-mal 20kd;或peg-mal 40kd)。在一些实施方案中,聚乙二醇化是用peg-mal 30kd进行的。在一些实施方案中,聚乙二醇化是用peg-mal 30kd进行的。在一些实施方案中,聚乙二醇化是用peg-mal 40kd进行的。在一些实施方案中,聚乙二醇化的肽中重复peg单元的范围是约800-1000。在一些实施方案中,聚乙二醇化的肽中重复peg单元的平均数量是约850-950。本领域技术人员将理解peg部分可以是直链的或支化的。
39.本文公开的多肽和肽结构域可以在n末端、c末端或二者处包括另外的残基;在确定本公开文本的多肽或肽结构域相对于参考多肽的同一性百分比时,不包括这些另外的残基。此类残基可以是适用于预期用途的任何残基,所述预期用途包括但不限于检测标签(即:荧光蛋白、抗体表位标签等)、衔接子、适用于纯化目的的配体(his标签等)、为多肽添加功能性的其他肽结构域等。适用于此类基团的附接的残基可以包括例如半胱氨酸、赖氨酸或对乙酰苯丙氨酸残基,或者可以是标签,如适用于与转谷氨酰胺酶反应的氨基酸标签,如在美国专利号9,676,871和9,777,070中所披露。b.免疫检查点抑制剂
40.免疫检查点是刺激或抑制免疫应答的信号传导蛋白。靶向免疫检查点的组合物调节这些蛋白质以改变个体的天然免疫应答。本文所述的免疫检查点抑制剂是抑制或阻断有助于阻止免疫应答的免疫检查点分子(例如,它们阻止细胞(如t细胞)杀伤癌细胞)的那些。当这些免疫检查点分子被阻断或抑制时,免疫系统的“刹车(brake)”被松开,并且细胞(如t细胞)能够更好地定位并杀伤癌细胞。因此,如本文所用,免疫检查点抑制剂是抑制免疫检查点分子压制免疫系统的能力的分子。在一些方面,所述抑制剂可以直接结合免疫检查点分子、控制免疫检查点分子表达的分子、或介导免疫检查点分子活性的免疫检查点分子的配体。所述抑制剂或拮抗剂可以是抗体(包括人源化抗体或人抗体)、小分子、肽或核酸(例如,反义分子或单链或双链rnai分子)。
41.在一些方面,检查点抑制剂是生物治疗剂或小分子。在一些实施方案中,检查点抑制剂是单克隆抗体(例如,嵌合抗体、人源化抗体或完全人抗体)或融合蛋白。在一些实施方案中,检查点抑制剂抑制选自clta-4、pd-1或pd-l1的检查点抑制剂的配体。在一些实施方案中,检查点抑制剂是pd-l1、pd-1或ctla-4抑制剂。
42.在一些实施方案中,免疫检查点抑制剂是ctla-4拮抗剂,如拮抗性ctla-4抗体。在一些实施方案中,clta-4拮抗剂选自yervoy(伊匹单抗)、曲美木单抗、agen1884和agen2041。
43.在一些实施方案中,免疫检查点抑制剂是pd-1拮抗剂,如拮抗性pd-1抗体。合适的pd-1抗体包括例如opdivo(纳武单抗)、keytruda(派姆单抗)或medi-0680(amp-514)。免疫
肿瘤学药剂还可以包括匹地利珠单抗(ct-011),尽管其对pd-1结合的特异性受到质疑。另一种靶向pd-1受体的方法是由pd-l2(b7-dc)的胞外结构域与iggl的fc部分融合构成的重组蛋白,称为amp-224。
44.在一些实施方案中,免疫检查点抑制剂是pd-ll拮抗剂,如拮抗性pd-ll抗体。合适的pd-ll抗体包括例如,阿特利珠单抗、阿维鲁单抗、度伐鲁单抗、bms-936559、mpdl3280a(rg7446;w02010/077634)和msb0010718c。
45.在一些实施方案中,两种免疫检查点抑制剂与il-2受体激动剂组合使用,例如pd-l1拮抗剂或pd-1拮抗剂与ctla-4拮抗剂组合。
46.本公开文本的抗体免疫检查点抑制剂可以使用本领域已知的方法制备。例如,本公开文本的人单克隆抗体可以使用scid小鼠来制备,已经将人免疫细胞重构到所述小鼠体内,使得可以在免疫时产生人抗体应答。此类小鼠描述于,例如,wilson等人的美国专利号5,476,996和5,698,767中。本公开文本的免疫检查点抑制剂也可以被配制以延缓药剂的降解或使抗体的免疫原性最小化。已知本领域中多种技术可以实现此目的。c.治疗方法
47.本公开尤其提供了用于调节受试者的免疫应答的方法,所述方法通过向所述受试者施用本公开文本的il-2受体激动剂与免疫检查点抑制剂组合。如本文所用,术语“受试者”是指动物,优选哺乳动物,更优选人。
48.如本文所用,被调节的“免疫应答”是指免疫系统的细胞(如b细胞、t细胞(cd4或cd8)、调节t细胞、抗原呈递细胞、树突细胞、单核细胞、巨噬细胞、nkt细胞、nk细胞、嗜碱性粒细胞、嗜酸性粒细胞或嗜中性粒细胞)对刺激的应答。在一些实施方案中,所述应答对特定抗原具有特异性(“抗原特异性应答”),并且是指cd4 t细胞、cd8 t细胞或b细胞通过其抗原特异性受体进行的应答。在一些实施方案中,免疫应答是t细胞应答,如cd4+应答或cd8+应答。这些细胞的此类应答可以包括例如细胞毒性、增殖、细胞因子或趋化因子产生、运输或吞噬作用,并且可能依赖于正在经历应答的免疫细胞的性质。在本文所述的组合物和方法的一些实施方案中,被调节的免疫应答是t细胞介导的。测量免疫应答的方法是本领域已知的并且包括例如测量促炎性细胞因子(如il-6、il-12和tnf-α)以及共刺激分子(如cd80、cd86和趋化因子受体)。
49.在另一方面,本公开文本提供了用于治疗癌症的方法,所述方法包括向有需要的受试者施用如本文所述的组合治疗方案。如本文所用,“治疗(treat)”或“治疗(treating)”是指完成以下中的一项或多项:(a)减小受试者中肿瘤和/或转移瘤的大小或体积;(b)限制受试者中肿瘤和/或转移的大小或体积的任何增加;(c)增加存活;(d)减轻与癌症相关的症状的严重程度;(e)限制或预防与癌症相关的症状的发展;以及(f)抑制与癌症相关的症状的恶化。
50.所述方法可以用于治疗癌症,包括但不限于,结肠癌、黑色素瘤、肾细胞癌、头颈部鳞状细胞癌、胃癌、尿路上皮癌、霍奇金淋巴瘤、非小细胞肺癌、小细胞肺癌、肝细胞癌、胰腺癌、默克尔细胞癌、结直肠癌、急性髓性白血病、急性成淋巴细胞性白血病、慢性淋巴细胞白血病、非霍奇金淋巴瘤、多发性骨髓瘤、卵巢癌、宫颈癌、乳腺癌、肝癌、肾细胞癌、黑色素瘤、和通过诊断测试(如微卫星不稳定性、肿瘤突变负荷、pd-l1表达水平或免疫得分测定(如由癌症免疫治疗协会开发的))的任何肿瘤类型。在一些方面,所述癌症是实体瘤或液体瘤。在
一些方面,所述癌症是对用检查点抑制剂的单一疗法具有抗性的癌症。在一些方面,所述癌症是对用检查点抑制剂的单一疗法敏感的癌症。
51.在另一方面,本公开文本提供了用于抑制受试者的肿瘤增殖的方法,所述方法包括向有需要的受试者施用如本文所述的组合治疗方案。所述肿瘤可能与实体癌或液体癌相关。在一些方面,所述肿瘤与以下相关:结肠癌、黑色素瘤、肾细胞癌、头颈部鳞状细胞癌、胃癌、尿路上皮癌、霍奇金淋巴瘤、非小细胞肺癌、小细胞肺癌、肝细胞癌、胰腺癌、默克尔细胞癌、结直肠癌、急性髓性白血病、急性成淋巴细胞性白血病、慢性淋巴细胞白血病、非霍奇金淋巴瘤、多发性骨髓瘤、卵巢癌、宫颈癌、乳腺癌、肝癌、肾细胞癌或黑色素瘤。
52.在一些实施方案中,本文所述的方法除上述il-2受体激动剂和免疫检查点抑制剂外还包括一种或多种另外的药剂。例如,在某些癌症如黑色素瘤中,可以使用另一种药剂,如抗tyrp1抗体。在一些实施方案中,所述抗typr1抗体是ta99。
53.术语“治疗有效量”意指主题肽、抗体或其他活性剂将引起研究人员、兽医、医生或其他治疗提供者所寻求的细胞、组织、系统或动物(如人)的生物或医学反应的量。
54.术语“抑制”或
“……
的抑制”意指减少可测量的量或完全防止。如本文所用的术语抑制可以是指至少10%、至少15%、至少20%、至少25%、至少30%、至少40%、至少50%、至少60%、至少70%或至少80%的抑制或减少。
55.如本文所用的术语协同作用或协同效应当与药剂组合的功效的描述结合使用时,意指所述组合的任何测量的作用大于从单独药剂的作用总和预测的作用(即,大于累加效应)。在一些实施方案中,使用肿瘤生长速率或肿瘤大小(例如,肿瘤的大小(例如,体积、质量)的变化速率)来确定药物组合是否是协同的(例如,当肿瘤生长速率比在药物组合产生累加效应的情况下所预期的更慢时,所述药物组合是协同的)。在一些实施方案中,使用存活时间来确定药物组合是否是协同的(例如,当受试者或受试者群体的存活时间比在药物组合产生累加效应的情况下所预期的更长时,药物组合是协同的)。d.组合疗法的施用方法
56.本文所述的方法包括向受试者(例如人受试者)施用治疗有效量的il-2受体激动剂和治疗有效量的一种或多种免疫检查点抑制剂。在一些实施方案中,所述一种或多种免疫检查点抑制剂是pd-1抑制剂。在一些实施方案中,所述一种或多种免疫检查点抑制剂是pd-l1抑制剂。在一些实施方案中,所述一种或多种免疫检查点抑制剂是ctla-4抑制剂。在一些实施方案中,所述一种或多种免疫检查点抑制剂是pd-1抑制剂和ctla-4抑制剂。在一些方面,治疗剂的组合协同作用以影响癌症的治疗或预防或免疫反应的调节或肿瘤细胞增殖的抑制。
57.取决于疾病状态和受试者的状况,本公开文本的肽、抗体和配制品可以通过任何合适的方式施用。通常,肠胃外施用(例如,肌内、腹膜内、静脉内、icv、脑池内注射或输注、皮下注射或植入)肽和抗体疗法。其他施用方式也可适用于本发明方法,例如口服施用。此外,肽和抗体可以单独或一起配制在合适的剂量单位配制品中,所述配制品含有适合于每种施用途径的常规的无毒的药学上可接受的载体、佐剂和媒介物。
58.应当理解,用于任何特定患者的具体剂量水平和剂量频率可以变化并且将取决于多种因素,包括所采用的活性剂的活性、这些药剂的代谢稳定性和作用长度、年龄、体重、遗传特征、一般健康状况、性别、饮食、施用方式和时间、排泄速率、药物组合、特定病症的严重
程度以及正在经历疗法的宿主。il-2受体激动剂的合适的剂量范围可以是例如,0.1ug/kg-100mg/kg体重;可替代地,它可以是0.5ug/kg至50mg/kg;1ug/kg至25mg/kg或5ug/kg至10mg/kg体重。在其他实施方案中,推荐的剂量可以基于体重/m2(即体表面积),和/或其可以以固定剂量(例如,.05-100mg)施用。在一些方面,il-2模拟物的合适的剂量范围是从0.5ug/kg至30ug/kg或从1ug/kg至10ug/kg或8ug/mg。
59.通常,在本文提供的方法(例如癌症的治疗)中有效的il-2受体激动剂和检查点抑制剂的最佳量可以通过标准临床技术确定。此外,可以任选地采用体外测定来帮助鉴定最佳剂量范围。待用于配制品中的确切剂量还将取决于施用途径以及恶性肿瘤的阶段,并且应当根据从业者的判断和每名患者的情况决定。可以从源自体外或动物模型测试系统的剂量-反应曲线外推有效剂量。
60.在一些实施方案中,il-2受体激动剂和检查点抑制剂将以最大耐受剂量(mtd)或最佳生物剂量(obd)施用至受试者。本领域技术包括确定mtd或obd。在一些方面,il-2受体激动剂将以其mtd或obd提供,并且检查点抑制剂将以mtd或obd的50%-100%,优选50%至90%给药。可替代地,检查点抑制剂将以其mtd或obd给药,并且il-2受体激动剂将以mtd或obd的50%-100%,优选50%至90%给药。在一些方面,il-2受体激动剂和检查点抑制剂二者均将以mtd或obd的60%至90%给药。
61.如在本发明中使用的,组合方案可以同时给予或可以以交错方案给予,其中检查点抑制剂在治疗进程期间以与il-2受体激动剂不同的时间给予。在两种药剂的施用之间,此时间差异的范围可以是几分钟、几小时、几天、几周或更长。因此,术语组合不一定意指同时施用或作为单一剂量施用,而是在所需治疗阶段期间施用每种组分以提供所需效果。也可以通过不同的途径施用所述药剂。e.试剂盒
62.在一些方面,本文提供了含有il-2受体激动剂和一种或多种免疫检查点抑制剂的试剂盒。试剂盒可以包含含有il-2受体激动剂的药物组合物和一种或多种含有免疫检查点抑制剂(例如,抗pd-1抑制剂、抗pd-l1和/或抗ctla-4抑制剂)的药物组合物。在一些情况下,所述试剂盒包括书面材料,例如肽、抗体或其药物组合物的使用说明书。不受束缚,所述试剂盒可以包括缓冲液、稀释剂、过滤器、针、注射器以及具有进行本文公开的任何方法的说明书的药品说明书。
63.尽管出于清楚理解的目的,前述发明已通过说明和举例的方式被稍微详细地描述,但本领域技术人员应理解,可以在所附权利要求的范围内实践某些改变和修改。另外,将本文提供的每篇参考文献通过引用以其整体并入,其程度就如同每篇参考文献均单独地通过引用并入一样。在本技术与本文提供的参考文献存在冲突的情况下,应以本技术为准。ii.实施例实施例1:示例性聚乙二醇化的il-2模拟物的制备:
64.将具有单一e62c突变的neo-2/15储液(seq id no:19)透析到磷酸盐缓冲液(ph7.0)中,并且调整为1.0-2.0mg/ml。以与蛋白质的10:1的摩尔比添加tcep,并且在rt下孵育10分钟以还原二硫化物。将马来酰亚胺修饰的peg40k(peg40k-ma)或peg30k(peg30k-ma)粉末以10:1peg:半胱氨酸的摩尔比直接添加到还原的蛋白质溶液中并且在搅拌的情况下孵育2小时。直接从反应混合物中取得用于sds-page的等分试样。这些数据证实了以预期
的化学计量在peg40k-ma或peg30k-ma与neo-2/15半胱氨酸突变体之间的共价连接的快速、自发和接近定量的形成。将此聚乙二醇化的il-2模拟物用于下文实施例中。实施例2:在ct26小鼠结肠癌模型中聚乙二醇化的il-2模拟物与检查点抑制的组合研究
65.进行这项研究以在ct26小鼠结肠癌模型中评价il-2r激动剂与pd-1(apd-1;克隆rmp1-14)和pd-l1(apd-l1;克隆10f.9g2)免疫检查点的抗体抑制剂的组合抗肿瘤活性。将ct26肿瘤细胞维持在培养基中。在指数生长期收获细胞。将每只balb/c小鼠右后侧腹皮下接种在0.1ml pbs中的ct26肿瘤细胞(5e5)。当平均肿瘤大小达到80-120mm^3时,随机化为处理组。分组后立即开始处理。媒介物是一种非特异性抗体,每两周以10mg/kg ip给药,持续6剂。将il-2r激动剂(聚乙二醇化的il-2模拟物)qw以60ug/kg iv给药,持续2剂。将抗pd-1或抗pd-l1每两周以10mg/kg ip给药,持续6剂。使用卡尺在两个维度上每周两次测量肿瘤体积。使用公式v=((lxw)xw)/2以mm^3表示肿瘤体积。对于(i)对照组、抗pd-1单一疗法组、聚乙二醇化的il-2模拟物单一疗法组和抗pd-1/聚乙二醇化的il-2模拟物组合疗法组(参见图1和表1),以及对于(i)对照组、抗pd-l1单一疗法组、聚乙二醇化的il-2模拟物单一疗法组和抗pd-l1/聚乙二醇化的il-2模拟物组合疗法组(参见图2和表2),示出了在第16天、第23天、第30天、第37天、第44天、第51天和第58天小于1000mm3的肿瘤的百分比。表1表1表2
66.用媒介物处理的小鼠的该中值存活期(ms)是23天。用apd-l1处理使ms增加4天,用低剂量聚乙二醇化的il-2模拟物处理使ms增加7天,并且聚乙二醇化的il-2模拟物处理与apd-l1组合使ms增加18天。当与单独的每种处理相比时,聚乙二醇化的il-2模拟物处理与apd-l1组合的ms增加是协同的。
67.关于聚乙二醇化的il-2模拟物与apd-1处理的组合研究,在不同时间点,ms示出了累加效应,而肿瘤生长的抑制示出了协同作用。在第30天,apd-1组显示6.7%的肿瘤小于1000mm3,聚乙二醇化的il-2模拟物组显示33.3%的肿瘤小于1000mm3,但组合组显示61.5%的肿瘤小于1000mm3。实施例3:在mc38小鼠结肠癌模型中聚乙二醇化的il-2模拟物与检查点抑制的组合研究
68.进行这项研究以评价在mc38小鼠结肠癌模型中il-2r激动剂与pd-1(apd-1;克隆rmp1-14)和pd-l1(apd-l1;克隆10f.9g2)免疫检查点的抗体抑制剂的组合抗肿瘤活性。将mc38肿瘤细胞维持在培养基中。在指数生长期收获细胞。将每只c57bl6小鼠右后侧腹皮下接种在0.1ml pbs中的mc38肿瘤细胞(1e6)。当平均肿瘤大小达到80-120mm^3时,随机化为处理组。分组后立即开始处理。媒介物是一种非特异性抗体,每两周以10mg/kg ip给药,持续6剂。将il-2r激动剂qw以60ug/kg iv给药,持续2剂。将抗pd-1或抗pd-l1每两周以10mg/kg ip给药,持续6剂。使用卡尺在两个维度上每周两次测量肿瘤体积。使用公式v=((lxw)xw)/2以mm^3表示肿瘤体积。示出了对于(i)对照组、抗pd-1单一疗法组、聚乙二醇化的il-2模拟物单一疗法组和抗pd-1/聚乙二醇化的il-2模拟物组合疗法组(参见图3和表3),以及对于(i)对照组、抗pd-l1单一疗法组、聚乙二醇化的il-2模拟物单一疗法组和抗pd-l1/聚乙二醇化的il-2模拟物组合疗法组(参见图4和表4),在第15天、第22天、第29天、第36天、第43天和第50天小于1000mm3的肿瘤的百分比。表3
表4
69.用媒介物处理的小鼠的该中值存活期(ms)是22天。用apd-1处理没有使ms增加,但是用apd-l1处理使ms增加3天。用低剂量聚乙二醇化的il-2模拟物处理使ms增加7天,而聚乙二醇化的il-2模拟物处理+apd-1以及聚乙二醇化的il-2模拟物处理+apd-l1的组合使ms增加17天和21天,相比于单独的聚乙二醇化的il-2模拟物处理有10天和14天的改善。当与单独的每种处理相比时,聚乙二醇化的il-2模拟物处理与apd-1或apd-l1的组合的ms增加是协同的。实施例4:在b16f10小鼠黑色素瘤模型中聚乙二醇化的il-2模拟物与检查点抑制的组合研究
70.进行这项研究以评价在b16f10小鼠黑色素瘤模型中,聚乙二醇化的il-2模拟物和pd-1(apd-1;克隆rmp1-14)免疫检查点的抗体抑制剂与ctla-4抑制剂(actla-4;克隆9d9)组合的组合抗肿瘤活性。将b16f10肿瘤细胞维持在培养基中。在指数生长期收获细胞。将每只c57bl6小鼠右后侧腹皮下接种在0.1ml pbs中的b16f10肿瘤细胞(2e5)。当平均肿瘤大小达到约80mm^3时,随机化为处理组,其中每组12只动物。分组后立即开始处理。媒介物是一种非特异性抗体,每两周以10mg/kg ip给药,持续6剂。将聚乙二醇化的il-2模拟物qw以275ug/kg iv给药,持续2剂。将抗pd-1与抗ctla-4(下表5和图5中表示为cpi)组合每两周以10mg/kg ip给药,持续6剂。每周测量肿瘤体积三次。使用公式v=((lxw)xw)/2以mm^3表示肿瘤体积。参见图5表5
71.用媒介物处理的小鼠的该中值存活期(ms)是10.5天。用抗pd-1与抗ctla-41处理组合使ms增加1.5天,并且用聚乙二醇化的1l-2模拟物使ms增加1.5天,并且用组合疗法(抗pd1、抗ctla-4和聚乙二醇化的il-2模拟物)使ms增加5.5天。当与单独的每种处理相比时,组合的ms增加是协同的。实施例5:聚乙二醇化的il-2模拟物对cd8+细胞的pd-1表达的影响
72.为了评价聚乙二醇化的il-2模拟物刺激对淋巴细胞的免疫检查点受体pd-1表达的影响,从10名人供体分离pbmc,并且用聚乙二醇化的il-2模拟物(0-30ng/ml)处理,然后洗涤,染色,并且通过流式细胞术进行分析。聚乙二醇化的il-2模拟物刺激导致cd8+t细胞的pd-1表达的浓度依赖性增加,与诱导的增殖一致,这表明将聚乙二醇化的il-2模拟物与pd-1抑制剂组合可以克服免疫检查点介导的cd8+t细胞抑制。参见图6
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1