一种用于神经阻滞可显影的高黏附药物缓释体的制备方法
1.本发明涉及生物技术领域,具体涉及一种用于神经阻滞可显影的高黏附药物缓释体及其制备方法。
背景技术:
2.神经阻滞术是一种有效治疗各种急慢性疼痛的主要手段。超声引导下的神经阻滞是利用实时超声清晰显示绝大部分外周神经及其周围的解剖结构,用以精确定位注射麻醉药物至治疗部位,在疼痛治疗方面已取得良好效果。
3.但在这个过程中,超声虽然同时还能够通过显示穿刺针的位置来提高穿刺的准确性,但注射过程中以及注射后药物扩散的位置并不能有效的呈现,并且局部大剂量麻醉药物的注射一方面会带来不可控的神经损伤,另一方面过快的药物代谢速度也会降低药物的作用时间。
4.因此,开发一种在超声引导下可显影的高黏附药物缓释体(其显影作用可精确定位药物的作用位置;其黏附作用和缓释作用可以延长药物的作用时间)是非常有必要的。
技术实现要素:
5.本公开旨在至少解决现有技术或相关技术中存在的技术问题之一。
6.为此,在本公开的第一方面,提供了一种用于神经阻滞可显影的高黏附药物缓释体的制备方法,包括:
7.制备微米级球形材料;
8.对所述微米级球形材料的表面进行黏附分子修饰,与药物分子结合,干燥后得到超声显影高黏附药物缓释体。
9.进一步地,所述制备微米级球形材料包括:
10.通过医用材料制备微米级球体结构;
11.所述球体的直径为1
‑
50μm;所述球体结构包括均一球体结构、多孔球体结构和空心球体结构。
12.进一步地,
13.通过医用材料和表面修饰黏附分子实现在所述球形材料内的黏附。
14.进一步地,所述黏附分子包括:
15.聚多巴胺、氨基酸二羟基苯丙氨酸或去甲肾上腺素聚合物。
16.进一步地,
17.所述空心球体结构的壳层厚度为球体直径的10%到50%。
18.进一步地,其特征在于,所述空心球体结构的壳层包括均一或多孔结构。
19.进一步地,所述多孔球体结构中孔的尺寸为2
‑
500nm。
20.进一步地,所述空心球体结构的壳内气体包括空气、氟碳类气体、氮气或氩气。
21.进一步地,所述与药物分子结合包括物理吸附和/或分子印迹技术。
22.在本公开的第二方面,提出了一种用于神经阻滞可显影的高黏附药物缓释体,所述用于神经阻滞可显影的高黏附药物缓释体根据上述所述的制备方法制得。
23.本发明所述的主料组分作用与功效:
24.聚多巴胺:聚多巴胺是黑色素的主要成分,可通过多巴胺的氧化自聚合反应得到,具有良好的生物相容性和光热转换性能,可在近红外激光照射下升温。其化学结构中具有丰富的易于修饰的基团,易实现表面改性。聚多巴胺具有粘附性,可包覆在多种材料表面。聚多巴胺还具有ph敏感性,可在肿瘤的微酸性环境中解聚;
25.去甲肾上腺素聚合物:一种儿茶酚胺,由于其化学结构的特殊性,可以在几乎任何物质的表面上形成一层粘附性较强的薄膜。与其他儿茶酚胺类物质(如多巴胺等)不同的是,去甲肾上腺素聚合形成的薄膜在纳米级的尺度上表现出更加光滑的性质。
26.本发明的原理是:药物缓释体在超声下可显影是根据声波散射原理由微球的结构和直径决定。不同微球的结构及直径在超声波下产生的散射效果也不同。黏附分子天然的黏附性可使微球进入体内后黏附在生物体组织内部。
27.超声波遇见球型散射体会发生散射,其散射的强弱与散射体的大小、形状及其与周边组织的声阻抗差别相关。聚乳酸
‑
羟基乙酸共聚物、丝素蛋白及壳聚糖都是内部疏松的分子结构,内部存留较小的尺寸不均的孔隙。因此均一材质的球体、多孔结构及空心球体内部都存在与周边组织声阻相差比较大的空气。超声波遇到这些微球体后散射则会增强,出现球形状的显影。另外,儿茶酚胺聚合物具有类似于贻贝蛋白天然的黏附性,即使在液体相中也可实现高的黏附作用,因此修饰在药物缓释体表面可实现药物的原位固定。
28.有益效果:本发明的超声显影的药物缓释体可精确定位药物的作用位置,其缓释作用又可以延长药物的作用时间,提升了神经阻滞治疗的精准性和药物的生物利用度。
附图说明
29.结合附图并参考以下详细说明,本公开各实施例的上述和其他特征、优点及方面将变得更加明显。在附图中,相同或相似的附图标记表示相同或相似的元素,其中:
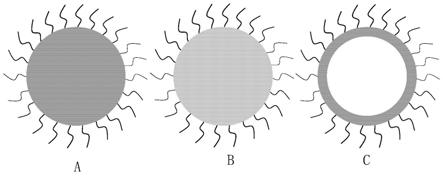
30.图1是本技术的一个实施例的高黏附球形药物缓释体的结构图。
具体实施方式
31.以下结合实施例对本发明的原理和特征进行描述,所举实例只用于解释本发明,并非用于限定本发明的范围。
32.另外,本文中术语“和/或”,仅仅是一种描述关联对象的关联关系,表示可以存在三种关系,例如,a和/或b,可以表示:单独存在a,同时存在a和b,单独存在b这三种情况。另外,本文中字符“/”,一般表示前后关联对象是一种“或”的关系。
33.如图1所示,球形药物缓释体的结构可为均一材质球体结构a、多孔球体结构b或者空心球体结构c。
34.所述黏附分子为聚多巴胺、氨基酸二羟基苯丙氨酸或去甲肾上腺素聚合物的一种;
35.空心球体结构的壳层厚度为球体直径的10%到50%;
36.球体结构中球体材质为聚乳酸
‑
羟基乙酸共聚物、丝素蛋白或壳聚糖的一种;
37.空心球体结构的壳层为均一或多孔结构的一种;
38.多孔球体结构中孔的尺寸为2
‑
500nm;
39.空心球体结构的壳内气体为空气、氟碳类气体、氮气或氩气的一种;
40.球体材料负载药物的方式为物理吸附或分子印迹技术。
41.在本公开中,均一材质的聚乳酸
‑
羟基乙酸共聚物、丝素蛋白和壳聚糖微球的制备可采用乳化法或微流控技术;
42.多孔的聚乳酸
‑
羟基乙酸共聚物、丝素蛋白和壳聚糖微球的制备可采用表面活性剂模板法或纳米粒子模板法。为了高效地使微球负载药物,其负载过程可采用多次重复的手段,即将微球多次浸泡于药物溶液并干燥。制备好的药物微载体保存于干燥气体环境中。
43.下面结合具体实施例具体介绍上述超声显影药物缓释体的制备:
44.实施例1
45.聚多巴胺修饰的均一球体结构的丝素蛋白超声显影药物缓释体的制备
46.1)丝素蛋白前聚体溶液的制备:丝素蛋白是由从家蚕的茧提取得到。将冷冻干燥后的丝素蛋白溶解于六氟异丙醇溶剂中,制备了蚕丝/六氟异丙醇溶液。之后将所需体积的去离子水缓慢滴入3ml 15%w/v蚕丝/六氟异丙醇溶液,然后通过轻轻旋转进行彻底混合,即得到丝素蛋白前聚体溶液。
47.2)单分散聚多巴胺修饰的丝素蛋白微球的制备:单分散丝素蛋白微球的制备采用的是微流控技术。即将上述得到的丝素蛋白前聚体溶液作为微流控的水相,外相采用含有表面活性剂的正十六烷,收集产生的液滴,并将其转移到一个玻璃瓶中,密封并静置4天,使其形成丝素蛋白水凝胶。最后,在100℃下用去离子水冲洗成型水凝胶,并重复多次(约2小时),通过溶剂交换和溶剂蒸发彻底去除残留的六氟异丙醇溶剂。之后在微球的水溶液中加入0.1g的盐酸多巴胺和三羟甲基氨基甲烷,调节溶液ph为8.5,25℃下混悬24小时即可得到聚多巴胺修饰的丝素蛋白微球。
48.3)利多卡因负载的丝素蛋白药物缓释体的制备:将0.05g聚多巴胺修饰的丝素蛋白微球浸泡于1ml质量分数为0.04g/ml的利多卡因溶液中,8小时后进行真空干燥,重复3次后即得到利多卡因负载的丝素蛋白药物缓释体。
49.实施例2
50.去加肾上腺素聚合物修饰的基于丝素蛋白材质的多孔结构的超声显影高黏附药物缓释体的制备
51.1)二氧化硅粒子的制备:
52.①
单分散二氧化硅纳米粒子的制备:将水、正硅酸乙酯、精氨酸、环己烷均匀混合,制备出具有单分散性、尺寸在10
‑
20nm的二氧化硅纳米粒子;将上述粒子溶液分散于乙醇、氨水构建的种子生长反应体系中,在均匀搅拌下,缓慢滴入二氧化硅前聚体溶液,得到所需尺寸的单分散的二氧化硅粒子。
53.②
制备二氧化硅微球模板的制备:将单分散的200nm的二氧化硅纳米粒子进行离心纯化,调节纳米粒子溶液中的胶体纳米粒子溶液中的配比制胶体纳米粒子的质量百分数为20%的胶体纳米粒子溶液,超声分散后作为微流控中的水相。为防止粒子有序组装,我们在水相中另外加入20%的乙醇溶剂。外相采用含有表面活性剂的正十六烷,收集产生的液滴,将其加热固化后,放入马弗炉内进行800℃煅烧,以提高微球的稳定性。
54.2)大孔结构的丝素蛋白微球的制备:将上述得到的二氧化硅微球浸泡于10%的丝素蛋白水溶液中,过夜后干燥,该过程重复三次。之后将干燥的丝素蛋白
‑
二氧化硅微球浸泡于4%的氢氟酸溶液中,过夜后冷冻干燥微球得到孔径在200nm的大孔结构的丝素蛋白微球。之后在微球的水溶液中加入与微球质量1:1的去甲肾上腺素和三羟甲基氨基甲烷,调节溶液ph为8.5,常温下混悬过夜即可得到去甲肾上腺素聚合物修饰的丝素蛋白微球。
55.3)布比卡因负载的大孔结构的丝素蛋白药物缓释体的制备:将0.01g大孔结构的丝素蛋白微球浸泡于1ml质量分数为0.04g/ml的布比卡因溶液中,8小时后进行真空干燥,重复3次后即得到布比卡因负载的丝素蛋白药物缓释体。
56.实施例3
57.聚多巴胺修饰的基于聚乳酸
‑
羟基乙酸材质的空心结构的超声显影的高黏附药物缓释体的制备
58.1)空心结构的聚乳酸
‑
羟基乙酸微球的制备:将0.3g聚乳酸
‑
羟基乙酸加入到6ml二氯甲烷溶剂中,混合均匀后加入4ml水,300rpm转速下搅拌1小时,之后加入50ml 1%的聚乙烯醇溶液,50rmp转速下搅拌24小时,得到空心结构的聚乳酸
‑
羟基乙酸微球。获得的聚乳酸
‑
羟基乙酸空心微球通过离心(3000rpm,5min),用去离子水冲洗三次后,在冻干机中冷冻干燥。所得粉末进一步分散在水中,进一步在该微球水溶液中加入0.1g的多巴胺和三羟甲基氨基甲烷,调节溶液ph为8.5,常温下混悬过夜即可得聚多巴胺修饰的丝素蛋白微球。
59.2)布比卡因负载的空心结构的聚乳酸
‑
羟基乙酸药物缓释体的制备:将0.01g空心结构的聚乳酸
‑
羟基乙酸微球浸泡于1ml质量分数为0.04g/ml的布比卡因溶液中,8小时后进行真空干燥,重复3次后即得到布比卡因负载的聚乳酸
‑
羟基乙酸药物缓释体。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1