全反式维甲酸在制备治疗放射性脑损伤的药物中的用途
本发明涉及药物用途领域,具体地指一种全反式维甲酸在制备治疗放射性脑损伤的药物中的用途。
背景技术:
1、放射性脑损伤(radiation-induced brain injury,rbi)是头颈部肿瘤放疗后产生的常见神经系统损伤,近年来,头部放疗已成为原发性和转移性脑部恶性肿瘤的主要治疗方式之一,且通过放疗能明显延长患者生存,甚至可通过预防性颅脑照射预防小细胞肺癌脑转移,然而,随着脑部放疗普及以及患者生存时间延长,各种放疗相关神经毒性开始显现,尤其是脑部放疗后导致的放射性脑损伤,严重影响患者生活质量。rbi根据放疗后发生时间可分为:急性、早迟发反应型及晚迟发反应型。
2、急性放射性脑损伤是指在辐射暴露后数小时至数周内的急性脑损伤事件,其可导致头部不适、精神神经症状、记忆力下降等,为可逆性反应,贝伐单抗、甘露醇、糖皮质激素等可通过减轻脑水肿进而改善急性脑损伤。早迟发反应型(亚急性)放射性脑损伤一般出现在放疗后1-6个月,表现为嗜睡、易怒等神经精神反应,还包括恶心、呕吐等消化系统反应,甚至记忆力减退等。晚迟发型(慢性)放射性脑损伤即不可逆脑白质病,为放疗6个月后出现的脑损伤,最终导致认知障碍和性格改变,特别是全脑放疗,可导致弥漫性脑萎缩。
3、目前据统计50-90%接受头部照射后存活的肿瘤患者表现出不同程度的认知功能障碍,包括学习、记忆、逻辑、注意力等,严重者可出现阿尔兹海默样痴呆,目前就放射性脑损伤发病机制尚不明确,放疗可直接损伤神经元或神经胶质细胞,或通过间接改变周围微环境,如上调神经炎症因子白介素(interleukin,il)-6、肿瘤坏死因子α(tumour necrosisfactor-alpha,tnf-α)、白介素(interleukin,il)-1β等导致rbi,另外,神经发生减少也是导致rbi认知功能障碍的主要原因,因此,避免海马神经发生减少和抑制神经炎症的增加或许可以保护全脑放疗导致的认知功能损伤,但目前由于辐射导致的认知功能障碍相关机制及相关细胞分子基础尚未完全阐明,因此对于头部放疗导致的认知功能损伤的预防和治疗仍需要进一步关注和研究。
4、全反式维甲酸(all-trans retinoic acid,atra)又称视黄酸或维a酸,是一类维生素a衍生物,对胚胎发育、精子发生、视觉和细胞分化都有十分重要的作用。早期研究表明维生素a缺乏的动物易发生肿瘤。维甲酸类化合物最引人注目的作用是预防及治疗一些恶性肿瘤,包括白血病、乳腺癌、皮肤癌、宫颈癌、中枢神经系统肿瘤等,其抗肿瘤作用主要通过经典的核受体信号通路。
5、一直以来,atra一直被当作第一个靶向治疗癌症的例子,最近发现,atra诱导的脯氨酰顺反异构酶pin1(protein interaction with nma1,pin1)消除会降解融合癌基因pml-rara编码的蛋白,且在急性早幼粒细胞白血病(apl)细胞、动物模型和病人中都得到了验证。atra诱导的pin1消除也强烈抑制了三阴性乳腺癌细胞的生长,这种作用是通过影响pin1底物中的癌基因和肿瘤抑制因子表达实现的。
6、在中枢神经系统疾病中,atra可加速损伤信号清除,减轻神经炎症,挽救缺血后的神经元损伤,从而改善缺血性脑损伤,同时atra可改善阿尔兹海默病(alzheimer'sdisease,ad)中神经干细胞的受损及抑制海马区的小胶质细胞激活,减轻ad转基因小鼠淀粉蛋白沉积,改善记忆缺陷。
7、综上所述,rbi是脑部肿瘤患者放疗后常见并发症,但因其认知功能障碍相关机制及相关细胞分子基础尚不十分明确,缺乏有效的预防和治疗手段及药物,因此,迫切希望能为临床提供有效治疗rbi的药物。
技术实现思路
1、针对上述现有技术存在的不足,本发明的目的在于提供一种全反式维甲酸在制备治疗放射性脑损伤的药物中的用途。本发明克服现有了治疗方式及药物存在的不足,提供atra作为治疗rbi药物的用途,扩大atra药物适应症。
2、为达到上述目的,本发明通过下述技术方案实现:
3、本发明提供一种全反式维甲酸在制备治疗放射性脑损伤的药物中的用途。
4、优选的是,所述全反式维甲酸用于改善放射性脑损伤、减轻放射性脑衰老、以及抑制胶质瘤细胞生长、增殖、侵袭及迁移。
5、进一步优选的是,所述全反式维甲酸用于改善放射性脑损伤的具体表现为:减轻神经炎症、修复血脑屏障损伤、改善神经脱髓鞘损伤及有助于髓鞘再生、以及改善放射后认知功能及运动功能。
6、优选的是,所述药物包括有效量的活性成分全反式维甲酸、以及药学上可接受的载体。
7、进一步优选的是,所述药物为药学上可接受的任意剂型,包括片剂、胶囊剂、注射剂、颗粒剂、混悬剂和溶液剂中的至少一种。
8、更进一步优选的是,所述药物的给药方式采用口服给药、静脉注射给药和皮下包埋给药中的至少一种。
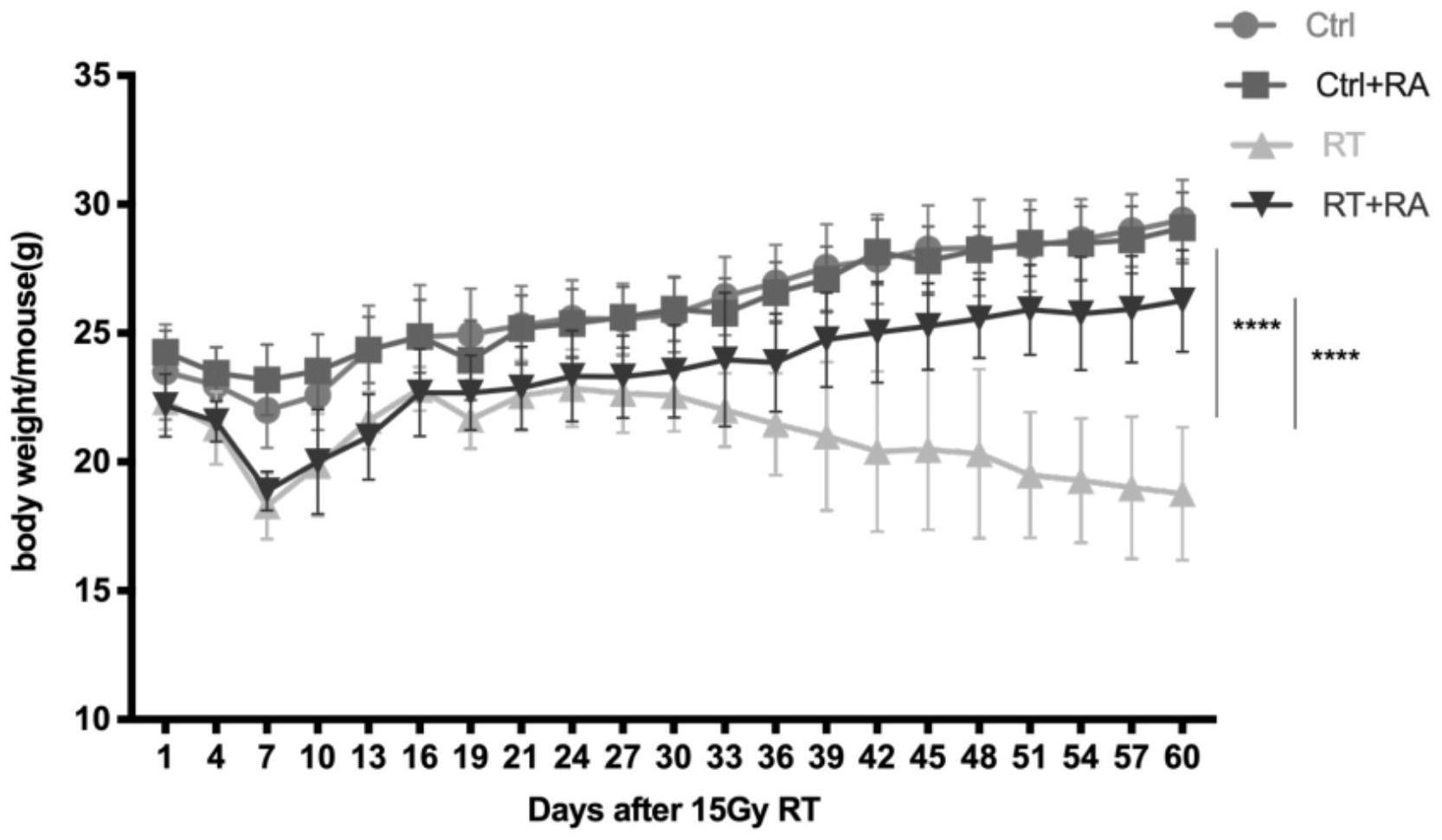
9、本发明通过构建小鼠rbi模型,atra采用腹腔注射给药方式,研究atra对rbi的作用并探讨其可能机制。实验数据显示,atra干预后,小鼠脑组织rt-pcr、wb结果显示,相比于rbi组,其炎症因子表达、星形胶质细胞活化指标神经元纤维酸性蛋白(glial fibrillaryacidic protein,gfap)及衰老指标明显降低,血脑屏障紧密连接蛋白明显增加,髓鞘再生相关因子表达量均升高,行为学实验中atra干预后小鼠体重、探索次数、活动度明显优于rbi组。在体外实验中,atra处理后使辐射后bv2小胶质细胞炎症因子分泌和原代星形胶质细胞活化减少,且在胶质瘤细胞系相关实验中,通过cck8、划痕、克隆形成等方法检测发现atra可明显抑制u87、u251、u118、gl261等胶质瘤细胞系增殖及迁移。这些实验结果证明,atra在改善放射性脑损伤同时可抑制胶质瘤细胞增殖和迁移。
10、本发明与现有技术相比,具有如下优点及有益效果:
11、通过对atra进行动物试验和细胞实验,探索atra在rbi中的作用,发现一定剂量的atra在改善放射性脑损伤同时可抑制胶质瘤细胞生长,且有效减轻放射性脑衰老及其相关炎症反应。因此,拟扩大atra药物新适应症:atra可尝试用于放射性脑损伤及放射性衰老等疾病中,特别是胶质瘤放疗患者中。
技术特征:
1.全反式维甲酸在制备治疗放射性脑损伤的药物中的用途。
2.根据权利要求1所述的用途,其特征在于:所述全反式维甲酸用于改善放射性脑损伤、减轻放射性脑衰老、以及抑制胶质瘤细胞生长、增殖、侵袭及迁移。
3.根据权利要求2所述的用途,其特征在于:所述全反式维甲酸用于改善放射性脑损伤的具体表现为:减轻神经炎症、修复血脑屏障损伤、改善神经脱髓鞘损伤及有助于髓鞘再生、以及改善放射后认知功能及运动功能。
4.根据权利要求1所述的用途,其特征在于:所述药物包括有效量的权利要求1所述的活性成分全反式维甲酸、以及药学上可接受的载体。
5.根据权利要求1或4所述的用途,其特征在于:所述药物为药学上可接受的任意剂型,包括片剂、胶囊剂、注射剂、颗粒剂、混悬剂和溶液剂中的至少一种。
6.根据权利要求5所述的用途,其特征在于:所述药物的给药方式采用口服给药、静脉注射给药和皮下包埋给药中的至少一种。
技术总结
本发明公开了一种全反式维甲酸在制备治疗放射性脑损伤的药物中的用途。所述全反式维甲酸用于改善放射性脑损伤、减轻放射性脑衰老、以及抑制胶质瘤细胞生长、增殖、侵袭及迁移。所述药物包括有效量的活性成分全反式维甲酸、以及药学上可接受的载体。本发明克服现有了治疗方式及药物存在的不足,通过对ATRA进行动物试验和细胞实验,探索ATRA在RBI中的作用,发现一定剂量的ATRA在改善放射性脑损伤同时可抑制胶质瘤细胞生长,且有效减轻放射性脑衰老及其相关炎症反应。因此,拟扩大ATRA药物新适应症:ATRA可尝试用于放射性脑损伤及放射性衰老等疾病中,特别是胶质瘤放疗患者中。
技术研发人员:胡广原,伏敏,李小钰,罗娜,李倩侠,彭小红,朱文君,杨峰,陈子琦,张圆圆
受保护的技术使用者:华中科技大学同济医学院附属同济医院
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!