植入医疗器械及其制备方法与流程
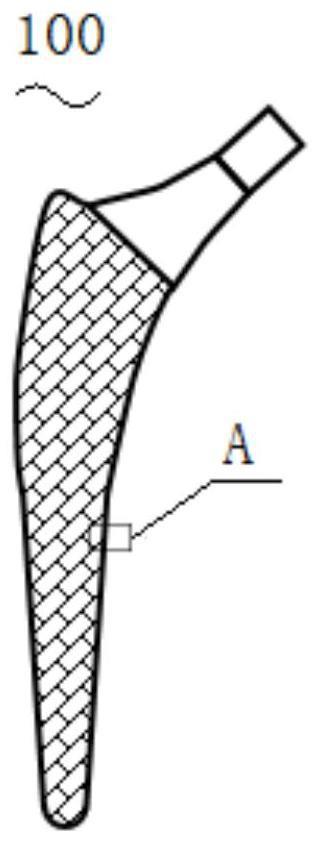
本发明涉及医疗器械,特别是涉及一种植入医疗器械及其制备方法。
背景技术:
1、植入医疗器械是指任何借助外科手术、器械全部或者部分进入人体或自然腔道中,或者是指在手术过程结束后长期留在体内,或者这些器械部分留在体内至少30天以上的器械。其中,用于替代人体某个肢体、器官或组织的医疗器械,也被称为假体。假体周围感染(periprosthetic joint infect,pji)常会引起植入物周围炎症反应,导致周围骨组织溶解和假体松动失效,被认为是植入医疗器械置换术后灾难性的并发症。
2、故而,如何提高植入医疗器械的抗感染能力,以降低假体周围感染(pji)的发生率,变得极为重要。
技术实现思路
1、基于此,有必要提供一种能够提高抗感染能力的植入医疗器械及其制备方法。
2、本发明是通过如下技术方案实现的。
3、本发明的一个方面,提供了一种植入医疗器械,包括:
4、器械基体;及
5、抗菌涂层,设于所述器械基体上,所述抗菌涂层中含有抗菌剂;自所述器械基体向所述抗菌涂层的远离所述器械基体的表面的方向上,所述抗菌涂层中所述抗菌剂的浓度先增大后减小。
6、在其中一个实施例中,所述抗菌涂层中还包括生物相容性材料和基体材料中的至少一种。
7、在其中一个实施例中,所述抗菌涂层中的抗菌剂与所述基体材料和/或所述生物相容性材料的结合形式为物理混合或形成化学键合。
8、在其中一个实施例中,所述抗菌涂层包括依次设于所述器械基体表面的第一子抗菌层及第二子抗菌层;
9、自所述器械基体向所述抗菌涂层的远离所述器械基体的表面的方向上,所述第一子抗菌层中所述抗菌剂的浓度逐渐增大,所述第二子抗菌层中所述抗菌剂的浓度逐渐减小。
10、在其中一个实施例中,所述第一子抗菌层中还包含有基体材料;
11、和/或,所述第二子抗菌层还包含有生物相容性材料。
12、在其中一个实施例中,所述第一子抗菌层为抗菌剂向器械基体的表面扩散形成的扩散涂层;
13、和/或,所述第二子抗菌层为抗菌剂向远离所述器械基体的方向扩散形成的扩散涂层。
14、在其中一个实施例中,所述抗菌涂层还包括第三子抗菌层,所述第三子抗菌层由未扩散的抗菌剂形成。
15、在其中一个实施例中,所述植入医疗器械还包括设于所述第二子抗菌层的远离所述器械基体的表面的生物相容性涂层。
16、在其中一个实施例中,所述抗菌涂层通过在器械基体上依次进行多次涂布形成。
17、在其中一个实施例中,所述抗菌涂层内的最大抗菌剂浓度p1为5wt%~100wt%;
18、和/或,所述第一子抗菌层内的最小抗菌剂浓度p2≤40wt%;
19、和/或,所述第二子抗菌层内的最小抗菌剂浓度p3≤40wt%。
20、在其中一个实施例中,所述生物相容性材料和生物相容性涂层的材料各自独立地选自金属、金属氧化物及医用非金属材料中的一种。
21、在其中一个实施例中,所述器械基体的材质为金属材料;
22、和/或,所述抗菌剂为金属抗菌剂、含有金属的抗菌剂以及有机抗菌剂中的至少一种。
23、在其中一个实施例中,所述抗菌涂层的厚度为0.01~500μm。
24、本发明的另一个方面,提供了一种植入医疗器械的制备方法,包括如下步骤:
25、在器械基体上形成含有抗菌剂的抗菌涂层;自所述器械基体向所述抗菌涂层的远离所述器械基体的表面的方向上,所述抗菌涂层中所述抗菌剂的浓度先增大后减小。
26、在其中一个实施例中,所述在器械基体上形成含有抗菌剂的抗菌涂层的步骤,包括如下步骤:
27、在所述器械基体的表面依次形成抗菌剂材料层及生物相容性材料层,再进行退火扩散处理,以使所述抗菌剂材料层分别与所述器械基体的表面和所述生物相容性材料层相互扩散。
28、在其中一个实施例中,所述退火扩散处理的温度为200~1000℃,时间为0.5h~80h。
29、上述植入医疗器械的抗菌涂层中抗菌剂的浓度,自器械基体向抗菌涂层的远离器械基体的表面的方向上,先增大后减小;即:抗菌涂层中的抗菌剂向器械基体和向抗菌涂层的远离器械基体的表面形成双向浓度梯度,即抗菌涂层中的抗菌剂向内和向外的浓度均逐渐减少。如此上述植入医疗器械,一方面可避免植入医疗器械表面存在较高浓度的抗菌剂,避免抗菌剂爆释,另一方面具有双向浓度梯度的抗菌涂层形成了一个缓释的抗菌剂储池,因此相比于直接在器械表面形成纯抗菌剂涂层,大大改善了抗菌剂爆释导致的生物相容性问题,还延长了抗菌剂的有效作用时长和有利于提高抗菌剂的利用率,进而可提高植入医疗器械的抗感染能力,降低pji的发生率。
技术特征:
1.一种植入医疗器械,其特征在于,包括:
2.如权利要求1所述的植入医疗器械,其特征在于,所述抗菌涂层中还包括生物相容性材料和基体材料中的至少一种。
3.如权利要求2所述的植入医疗器械,其特征在于,所述抗菌涂层中的抗菌剂与所述基体材料和/或所述生物相容性材料的结合形式为物理混合或形成化学键合。
4.如权利要求1所述的植入医疗器械,其特征在于,所述抗菌涂层包括依次设于所述器械基体表面的第一子抗菌层及第二子抗菌层;
5.如权利要求4所述的植入医疗器械,其特征在于,所述第一子抗菌层中还包含有基体材料;
6.如权利要求4所述的植入医疗器械,其特征在于,所述第一子抗菌层为抗菌剂向器械基体的表面扩散形成的扩散涂层;
7.如权利要求6所述的植入医疗器械,其特征在于,所述抗菌涂层还包括第三子抗菌层,所述第三子抗菌层由未扩散的抗菌剂形成。
8.如权利要求4所述的植入医疗器械,其特征在于,所述植入医疗器械还包括设于所述第二子抗菌层的远离所述器械基体的表面的生物相容性涂层。
9.如权利要求1所述的植入医疗器械,其特征在于,所述抗菌涂层通过在器械基体上依次进行多次涂布形成。
10.如权利要求4至9任一项所述的植入医疗器械,其特征在于,所述抗菌涂层内的最大抗菌剂浓度p1为5wt%~100wt%;
11.如权利要求5至9任一项所述的植入医疗器械,其特征在于,所述生物相容性材料和生物相容性涂层的材料各自独立地选自金属、金属氧化物及医用非金属材料中的一种。
12.如权利要求1至9任一项所述的植入医疗器械,其特征在于,所述器械基体的材质为金属材料;
13.如权利要求1至9任一项所述的植入医疗器械,其特征在于,所述抗菌涂层的厚度为0.01~500μm。
14.一种植入医疗器械的制备方法,其特征在于,包括如下步骤:
15.如权利要求14所述的制备方法,其特征在于,所述在器械基体上形成含有抗菌剂的抗菌涂层的步骤,包括如下步骤:
16.如权利要求15所述的制备方法,其特征在于,所述退火扩散处理的温度为200~1000℃,时间为0.5h~80h。
技术总结
本发明涉及一种植入医疗器械及其制备方法,包括器械基体及抗菌涂层。抗菌涂层设于器械基体上。抗菌涂层中含有抗菌剂。自器械基体向抗菌涂层的远离器械基体的表面的方向上,抗菌涂层中抗菌剂的浓度先增大后减小。抗菌涂层中的抗菌剂向内外两侧形成双向浓度梯度。如此上述植入医疗器械,一方面可避免植入医疗器械表面存在较高浓度的抗菌剂,避免抗菌剂爆释,另一方面具有双向浓度梯度的抗菌涂层形成了一个缓释的抗菌剂储池,因此相比于直接在器械表面形成纯抗菌剂涂层,大大改善了抗菌剂爆释导致的生物相容性问题,还延长了抗菌剂的有效作用时长和有利于提高抗菌剂的利用率,进而可提高植入医疗器械的抗感染能力,降低PJI的发生率。
技术研发人员:刘诗伟,贺达,徐寒冬,陈夕辉
受保护的技术使用者:上海联影智融医疗科技有限公司
技术研发日:
技术公布日:2024/1/16
- 还没有人留言评论。精彩留言会获得点赞!