一种抑制PCSK9的仿生纳米脂质体制剂及其制备方法、应用
一种抑制pcsk9的仿生纳米脂质体制剂及其制备方法、应用
技术领域
1.本发明属于生物医药技术领域,具体涉及一种抑制pcsk9的仿生纳米脂质体制剂及其制备方法和应用。
背景技术:
2.目前动脉粥样硬化性心血管疾病(arteriosclerotic cardiovascular disease,ascvd)已超过传染病成为世界头号杀手。血脂代谢异常是冠心病发生发展过程中的一个重要危险因素,其中低密度脂蛋白胆固醇(ldl-c)水平升高占据核心位置。《中国心血管健康与疾病报告2019》指出,目前我国血脂异常患病人群大幅上升,而知晓率、治疗率以及控制率总体仍处于较低水平。在10年动脉粥样硬化性心血管疾病(ascvd)高危人群中,ldl-c治疗率为5.5%,达标率为25.5%;而极高危人群中,ldl-c治疗率仅为14.5%,达标率更低仅为6.8%。2020年《超高危动脉粥样硬化性心血管疾病患者血脂管理中国专家共识》指出,对于超高危ascvd患者,强化降脂治疗使ldl-c目标值达到更低水平甚至需控制于1.0mmol/l以下,可带来显著心血管获益。
3.依洛尤单抗(evolocumab)是一种新型的生物单抗制剂,其商品名为瑞百安,是一种人单克隆免疫球蛋白g2(igg2),针对人前蛋白转化酶枯草溶菌素kexin9型(pcsk9),与pcsk9结合,抑制循环中的pcsk9与低密度脂蛋白受体(ldlr)的结合,从而阻止pcsk9介导的ldlr降解,使得ldlr可重新循环至肝细胞表面,导致能够清除血液中低密度脂蛋白的ldlr的数量增加,从而降低ldl-c水平。依洛尤单抗于2018年获国家药品监督管理局批准上市,成为首个且唯一一个在中国获批用于治疗成人或12岁以上青少年纯合子型家族性高胆固醇血症的pcsk9抑制剂;于2019年获批用于动脉粥样硬化性心血管疾病(ascvd)成人患者;同年再次获批更广泛适应症,成为中国首个获批用于成人原发性高胆固醇血症(包括杂合子型家族性高胆固醇血症)和混合型血脂异常患者的pcsk9抑制剂。
4.在依洛尤单抗显示良好治疗前景的同时,其不良反应也日益受到关注。在临床研究报告中,该药常见的副作用是上呼吸道感染、流感、胃肠炎、鼻咽炎,其次是局部注射部位反应、过敏反应,而导致停用瑞百安且发生率高于安慰剂组的最常见的不良反应为肌痛。
5.鉴于依洛尤单抗全身用药的用药剂量较高导致的不良反应及其给药方式的局限性,如何在不影响疗效的前提下降低使用剂量,并且减少副作用,是目前应用该药治疗动脉粥样硬化的关键。
6.纳米技术的发展为这一医学难题的解决带来了希望。纳米脂质体是一种利用具有磷脂双分子层生物膜结构的脂质体,通过对活性物质进行包埋,以此来提高生物利用度,保持其原有的性能;此外,因尺寸小、表面效应等特点也能增强物质与细胞之间的接触,提高靶向性。但是,脂质体进入体内后,由于血中的白蛋白、调理素、抗体等各种因素作用,脂质体发生破裂,包封药物快速渗漏,很快被网状内皮系统识别、吸收,限制了它的“导弹”功能。为此,需要用聚乙二醇(peg)修饰躲避网状内皮吞噬系统监视,增加脂质体在血液中的稳定性,延长药物的半衰期。另一方面,通过巨噬细胞膜的包裹,可以借助细胞膜上的特征蛋白
协助脂质体逃避机体免疫系统的清除,同时达到利用炎症趋化性来治疗动脉粥样硬化的作用。
技术实现要素:
7.有鉴于此,本发明提供一种抑制pcsk9的仿生纳米脂质体制剂及其制备方法、应用,该抑制pcsk9的仿生纳米脂质体制剂能够将脂质体包载的依洛尤单抗靶向缓释递送,延长血液驻留时间,降低用药剂量,并且有效降低pcsk9表达水平,缓解动脉粥样硬化的进展。
8.本发明提供的一种抑制pcsk9的仿生纳米脂质体制剂,包括抗体、脂质膜材和仿生细胞膜。
9.作为优选,所述抗体为依洛尤单抗;所述脂质膜材包括大豆卵磷脂、胆固醇、dspe-peg2000-nh2;所述仿生细胞膜为巨噬细胞膜。
10.本发明还提供一种抑制pcsk9的仿生纳米脂质体制剂的制备方法,包括以下步骤:
11.s1、制备仿生细胞膜;
12.s2、采用逆向蒸发法制备抑制pcsk9的纳米脂质体:定量称取大豆卵磷脂、胆固醇、dspe-peg2000-nh2混合溶于氯仿、乙醚和超纯水混合液中;将依洛尤单抗加到类脂溶液中,水浴超声,形成w/o型乳液;将所得乳液置于旋转蒸发仪中减压蒸发除去有机溶剂,达胶态后,加入水合介质,继续减压蒸馏除去剩余的有机溶剂;旋转水合至瓶壁凝胶脱落,过0.22μm微孔滤膜,得到抑制pcsk9的纳米脂质体;采用透析法分离未包载的游离抗体;
13.s3、将抑制pcsk9的纳米脂质体溶液与仿生细胞膜的pbs溶液混合后搅拌得到所述抑制pcsk9的仿生纳米脂质体制剂。
14.作为优选,s1中,所述仿生细胞膜的具体制备过程为:当细胞培养皿中的raw264.7细胞长满后,用细胞刮刀将细胞刮下后离心;收集的细胞在4℃下用pbs(ph7.4)洗涤2遍,然后悬浮在含有pmsf(1mm)的膜蛋白提取剂a中;混合物在冰浴中裂解30-60min,4℃水浴超声10-15min;37℃和-80℃反复冻融4次,每次20-30min;然后离心取上清液,继续离心得到巨噬细胞膜。
15.作为优选,所述卵磷脂与所述抗体的质量比为1-5:1;所述卵磷脂与所述dspe-peg2000-nh2的质量比为10-20:6。
16.作为优选,所述水合介质为含2%吐温-80的磷酸缓冲液。
17.作为优选,所述透析是使用截留分子量为200-300kda的透析袋透析24-72h。
18.作为优选,所述卵磷脂和巨噬细胞膜的质量比为10:1;所述搅拌转速为800-1000rpm,时间为1-2小时。
19.作为优选,s2中,所述的抑制pcsk9的纳米脂质体的平均粒径为160-180nm;抑制pcsk9的纳米脂质体对抗体活性成分的包封率为:90%。
20.本发明还提供一种抑制pcsk9的仿生纳米脂质体制剂的应用,用于制备预防和/或治疗动脉粥样硬化的药物。
21.本发明的有益效果为:
22.1、因纳米脂质体本身结构与细胞膜结构类似,都是由磷脂和胆固醇等物质组成,无毒性,安全性较高,故本发明将其选作包载药物的载体,不会对人体产生毒/副作用。
23.2、本发明构建的仿生纳米脂质体制剂,负载依洛尤单抗,利用依洛尤单抗抑制
pcsk9与低密度脂蛋白受体(ldlr)的结合,从而使ldlr可重新循环至肝细胞表面,降低ldl-c水平来治疗动脉粥样硬化。
24.3、本发明将peg和巨噬细胞膜共同修饰于脂质体表面,达到躲避网状内皮吞噬系统监视,增加血液中稳定性,延长药物循环半衰期的目的,实现动脉粥样硬化防治效果的最大化。
25.4、本发明解决了药物临床应用剂量大、体内半衰期短和药物毒副作用的问题,为开发新型防治动脉粥样硬化的药剂及相关临床预防和治疗提供新理论支持,具有重要的科学意义、使用价值和经济价值。
附图说明
26.为了使本发明的内容更容易被清楚地理解,下面根据具体实施例并结合附图,对本发明作进一步详细的说明,其中
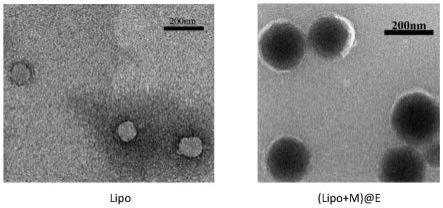
27.图1为纳米脂质体及仿生膜包裹下的纳米脂质体载药电镜图;
28.图2为仿生细胞膜的蛋白质免疫印迹图;
29.图3为lipo、lipo@e和(lipo+m)@e的粒径和电位图;
30.图4为lipo、lipo@e和(lipo+m)@e的药物摄取及溶酶体逃逸能力;
31.图5为evol从lipo@e和(lipo+m)@e上累计释放量;
32.图6为(lipo+m)@e降低pcsk9表达的western blot情况;
33.图7为(lipo+m)@e降低pcsk9表达的if情况;
34.图8为(lipo+m)@e在小鼠体内的血液半衰期;
35.图9为(lipo+m)@e在小鼠体内动脉粥样硬化斑块部位靶向性;
36.图10为不同处理组治疗动脉粥样硬化的血管大体油红o染色情况;
37.图11为不同组处理下小鼠主动脉根部、弓部及腹主动脉油红o染色情况;
38.图12为不同处理组治疗动脉粥样硬化小鼠后血清中pcsk9的表达情况。
39.图13为不同处理组治疗动脉粥样硬化小鼠心、肝、脾、肺和肾h&e染色图。
具体实施方式
40.以下结合说明书附图和具体优选的实施例对本发明作进一步描述,但并不因此而限制本发明的保护范围。
41.以下实施例中,若无特别说明,所采用的原料和仪器均为市售,所用方法均为本领域常规方法。
42.一种抑制pcsk9的仿生纳米脂质体制剂,包括抗体、脂质膜材和仿生细胞膜。所述抗体为依洛尤单抗;所述脂质膜材包括大豆卵磷脂、胆固醇、dspe-peg2000-nh2;所述仿生细胞膜为巨噬细胞膜。
43.一种抑制pcsk9的仿生纳米脂质体制剂的制备方法,包括以下步骤:
44.s1、制备仿生细胞膜,具体过程为:当细胞培养皿中的raw264.7细胞长满后,用细胞刮刀将细胞刮下后离心;收集的细胞在4℃下用pbs(ph7.4)洗涤2遍,然后悬浮在含有pmsf(1mm)的膜蛋白提取剂a中;混合物在冰浴中裂解30-60min,4℃水浴超声10-15min。37℃和-80℃反复冻融4次,每次20-30min;然后离心取上清液,继续离心得到巨噬细胞膜。
45.s2、采用逆向蒸发法制备抑制pcsk9的纳米脂质体:定量称取大豆卵磷脂、胆固醇、dspe-peg2000-nh2混合溶于氯仿、乙醚和超纯水混合液中;将依洛尤单抗加到类脂溶液中,水浴超声,形成w/o型乳液;将所得乳液置于旋转蒸发仪中减压蒸发除去有机溶剂,达胶态后,加入水合介质,继续减压蒸馏除去剩余的有机溶剂;旋转水合至瓶壁凝胶脱落,过0.22μm微孔滤膜,得到抑制pcsk9的纳米脂质体;采用透析法分离未包载的游离抗体;所述的抑制pcsk9的纳米脂质体的平均粒径为160-180nm;抑制pcsk9的纳米脂质体对抗体活性成分的包封率为:90%。
46.s3、将抑制pcsk9的纳米脂质体溶液与仿生细胞膜的pbs溶液混合后搅拌得到所述抑制pcsk9的仿生纳米脂质体制剂。
47.所述卵磷脂与所述抗体的质量比为1-5:1;所述卵磷脂与所述dspe-peg2000-nh2的质量比为10-20:6。所述水合介质为含2%吐温-80的磷酸缓冲液。所述透析是使用截留分子量为200-300kda的透析袋透析24-72h。所述卵磷脂和巨噬细胞膜的质量比为10:1;所述搅拌转速为800-1000rpm,时间为1-2小时。
48.所述仿生纳米脂质体制剂用于制备预防和/或治疗动脉粥样硬化的药物。
49.实施例1
50.(1)(lipo+m)@e仿生纳米制剂的制备
51.a.制备仿生细胞膜(m)
52.巨噬细胞(raw264.7细胞)膜的制备按照膜蛋白提取制剂盒的说明进行。当细胞培养皿中的raw264.7细胞长满后,pbs洗涤细胞三次,用细胞刮刀将细胞刮下,800rpm离心5min。收集的细胞在4℃下用pbs(ph7.4)洗涤2遍,然后悬浮在含有pmsf(1mm)的膜蛋白提取剂a中。混合物在冰浴中裂解30min,4℃探头超声10min(80w,开0.3s,关0.5s)。然后在37℃和-80℃反复冻融5次,每次20-30min。然后以4℃,800rpm离心10min。取上清液,继续在4℃,13000rpm下离心30min得到巨噬细胞膜。
53.b.制备lipo@e,本技术中lipo指现有技术中已有的单独的脂质体,作为对照例使用;
54.称取大豆卵磷脂20mg,胆固醇9mg,dspe-peg2000-nh2 6mg混合溶于13ml溶剂中,溶剂包括4ml氯仿、6ml乙醚和3ml超纯水;将依洛尤单抗稀释成10mg/ml溶液,用注射器缓慢滴加到类脂溶液中,水浴超声5分钟,形成w/o型乳液,要求所得乳液在半小时内不分层。将所得乳液置于旋转蒸发仪中37℃减压蒸发除去有机溶剂,达胶态后,加入30ml水合介质,继续减压蒸馏除去剩余的有机溶剂。旋转水合至瓶壁凝胶脱落,过0.22μm微孔滤膜,得到抑制pcsk9的纳米脂质体。采用透析法分离未包载的游离抗体。
55.c.制备(lipo+m)@e仿生纳米制剂;
56.将上述所得巨噬细胞膜溶解成1mg/ml,将lipo@e溶液与水浴超声处理后的仿生细胞膜(m)按质量比10:1混合,37℃下,800rpm水浴搅拌1小时得到(lipo+m)@e仿生纳米制剂;
57.(2)(lipo+m)@e仿生纳米制剂的表征
58.如图1所示,对本实施例中制得的lipo、lipo@e和(lipo+m)@e仿生纳米制剂进行dls粒径大小分析。结果表明均匀分散的球形lipo材料和(lipo+m)@e仿生纳米被成功制备,粒径分别在100nm和200nm左右。
59.如图2所示,对本实施例制得的仿生细胞膜进行膜特征性蛋白分析,其结果表明仿
生膜成功制备。
60.如图3所示,通过dls分别对lipo、lipo@e和(lipo+m)@e进行粒径电位分析,结果显示(lipo+m)@e粒径均值在180nm,电位情况良好。
61.如图5所示,与lipo@e相比,仿生细胞膜包裹以后evol累积释放量减少。说明制得的仿生纳米制剂实现了缓释。
62.实施例2
63.一种抑制pcsk9的仿生纳米脂质体制剂,与实施例1不同之处在于制备包载依洛尤单抗的纳米脂质体时,磷脂与抗体的质量比为1:1。
64.实施例3
65.一种抑制pcsk9的仿生纳米脂质体制剂,与实施例1不同之处在于制备包载依洛尤单抗的纳米脂质体时,磷脂与抗体的质量比为5:1。
66.实施例4
67.一种抑制pcsk9的仿生纳米脂质体制剂,与实施例1不同之处在于,卵磷脂与dspe-peg2000-nh2的质量比为10:6。
68.实施例5
69.一种抑制pcsk9的仿生纳米脂质体制剂,与实施例1不同之处在于,透析使用截留分子量为200-300kda的透析袋透析36h。
70.实施例6
71.一种抑制pcsk9的仿生纳米脂质体制剂,与实施例1不同之处在于,制备仿生巨噬细胞膜包裹的纳米脂质体包载药物时,磷脂与巨噬细胞膜的质量比为5:1。
72.实施例7
73.本发明提供的一种抑制pcsk9的仿生纳米脂质体制剂在动脉粥样硬化预防和治疗中的应用,以实施例1制备的(lipo+m)@e仿生纳米制剂为例对此效果进行阐明。
74.如图4所示,将空白脂质体和仿生巨噬细胞膜包裹的纳米脂质体分别用dil标记,加入平滑肌细胞中,并用溶酶体探针标记溶酶体,采用共聚焦显微镜观察仿生纳米脂质体的摄取及溶酶体逃逸能力。结果显示平滑肌细胞对(lipo+m)@e的摄取呈浓度依赖性,且有效避免溶酶体的摄取,保护依洛尤单抗免受微酸环境的破坏。
75.综上结果说明,实施例1制备的(lipo+m)@e仿生纳米脂质体制剂可在循环中逃避免疫系统的清除并且进入细胞后可逃避溶酶体的摄取。
76.实施例8
77.如图6所示,将实施例1中制备的各组纳米药物加入lps干预的平滑肌细胞中,通过蛋白免疫印迹观察(lipo+m)@e对pcsk9表达的影响,结果显示,(lipo+m)@e显著降低pcsk9的表达。
78.如图7所示,将实施例1中制备的各组纳米药物加入lps干预的平滑肌细胞中,通过免疫荧光观察(lipo+m)@e对pcsk9表达的影响,结果显示,(lipo+m)@e显著降低pcsk9的表达。
79.实施例9
80.采用实施例1制得的(lipo+m)@e仿生纳米脂质体制剂,通过小动物活体成像检测荧光强度对(lipo+m)@e仿生纳米脂质体制剂在小鼠体内的血液半衰期和体内靶向进行测
定。
81.试验一:取250ul lipo(4mg/ml)、40ul二氢卟吩(ce6)(1mg/ml)加入1710ul双蒸水,将混合液置于4℃800-1000rpm搅拌过夜,制得lipo@ce6。取250ul lipo(4mg/ml)、40ul二氢卟吩(ce6)(1mg/ml)、50ul巨噬细胞膜加入1660ul双蒸水,将混合液置于4℃800-1000rpm搅拌过夜,制得(lipo+m)@ce6。另制备1mg/ml ce6设置对照实验。
82.将试验一制得的ce6、lipo@ce6、(lipo+m)@ce6通过尾静脉注射c57bl/6小鼠,每只注射200μl,于不同时间点眼眶采集血样进行荧光强度测定。
83.结果如图8所示,(lipo+m)@ce6组相比ce6组、lipo@ce6组荧光显著延长,说明仿生纳米脂质体显著延长体内半衰期。
84.试验二:apoe-/-小鼠高脂饮食饲养一个月后,尾静脉注射200μl剂量浓度为10mg/kg的icg、lipo@icg和(lipo+m)@icg。12h后取小鼠主动脉进行荧光成像。
85.其中,lipo@icg是按照以下方法制备得到:
86.称取大豆卵磷脂20mg,胆固醇9mg,dspe-peg2000-nh2 6mg混合溶于13ml溶剂中,溶剂包括4ml氯仿、6ml乙醚和3ml超纯水;室温搅拌15分钟,使其充分溶解,随后加入圆底烧瓶中通过旋转蒸发仪中37℃减压蒸发除去有机溶剂,将icg溶液加到上述圆底烧瓶中,55℃水域搅拌4h,探头冰浴超声10分钟得到lipo@icg。
87.(lipo+m)@icg是按照以下方法制备得到:
88.将lipo@icg溶液与含巨噬细胞膜的pbs溶液混合,将混合液置于4℃结果如图9所示,与icg和lipo@icg组相比,(lipo+m)@icg组在主动脉弓和腹主动脉处显著聚集,说明实施例1制得的(lipo+m)@e仿生纳米制剂可有效靶向到动脉粥样硬化斑块部位。
89.实施例10
90.沿用实施例1制得的(lipo+m)@e仿生纳米制剂用于动脉粥样硬化早期预防治疗。
91.apoe-/-小鼠高脂饮食一个月后,给药剂量5mg/kg,每周两次,连续给药2个月,期间维持高脂饮食;均为尾静脉注射给药,给药组分为单独evol组、lipo@e组和(lipo+m)@e组。在治疗结束后3天,剥离小鼠主动脉进行大体油红o染色以考察不同治疗组的治疗效果。
92.结果如图10所示,(lipo+m)@e治疗组在治疗方案中,显著减少动脉粥样硬化斑块的形成,说明本发明所构建的仿生纳米制剂能够有效的预防早期动脉粥样硬化进展。
93.实施例11
94.运用实施例10所采取的治疗方案,在apoe-/-小鼠治疗结束后,将各组小鼠主动脉根部、弓部及腹主动脉冰冻切片进行油红o染色,倒置显微镜下观察脂质染色情况。
95.如图11所示,(lipo+m)@e组相比evol组、lipo@e组主动脉根部、弓部腹主动脉油红o着色明显减少,说明(lipo+m)@e有效清除各部位脂质。
96.实施例12
97.运用实施例10所采取的治疗方案,在apoe-/-小鼠治疗结束后,采集不同治疗方案下不同治疗组分的小鼠的血清,以考察不同治疗组之间血清中pcsk9的表达情况。
98.结果如图12所示,(lipo+m)@e组相比evol组、lipo@e组血清中pcsk9表达量明显降低,说明(lipo+m)@e有效降低血液中pcsk9的表达。
99.实施例12
100.运用实施例10所采取的治疗方案,在apoe-/-小鼠治疗结束后,采集不同治疗方案
下不同治疗组分的小鼠的主要脏器(心、肝、脾、肺和肾)做h&e染色,以考察不同治疗组的生物安全性。
101.结果如图13所示,不同治疗组小鼠脏器均未见明显的器质性病变,说明本发明所构建的仿生纳米制剂有良好的生物安全性。
102.以上所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本发明的具体实施例而已,并不用于限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1