含有谷胱甘肽盐的水性溶液的制作方法
本公开涉及化学和药物制剂的一般领域。在一些方面,本公开涉及药物制剂(例如含有谷胱甘肽的药物制剂,适用于肺部给药)及其使用方法。在一些方面,本公开提供了与arina-1相关的药物制剂和产品,用于治疗以粘液过多和炎症为特征的慢性炎症性肺病患者,如肺移植、囊性纤维化(cf)、非cf支气管扩张症、慢性阻塞性肺病(copd)和其他炎症性肺病患者。
背景技术:
粘液过多和炎症是慢性炎症性肺病的标志。离子失调导致粘液产生过多和慢性失调性炎症,这两种情况都会导致肺损伤和瘢痕,进而导致肺衰竭。ramsey等人,《美国呼吸与危重监护医学杂志》(american journal of respiratory and critical care medicine)201(6):661–670(2020);borok等人,《柳叶刀》(lancet)338:215–216(1991);behr等人,《移植》(transplantation)69:1856-1860(2000)。谷胱甘肽是一种重要的抗氧化离子,有助于粘液结构的完整(meldrum等人,《科学报告》(scientific reports)8(1):文章编号5802(2018)https://doi.org/10.1038/s41598-018-24223-3)和调节炎症反应。elferink,《免疫生物学》(immunobiology)184(1):25-36(1991)。慢性炎症还导致气道酸度增加,造成肺损伤。谷胱甘肽失调和气道酸度增加直接导致粘液粘稠,伴有粘液纤毛清除延迟或缺失,进而导致中小气道阻塞。这导致了有利于细菌定植、慢性感染和炎症的反馈回路的环境。目前治疗慢性炎症性肺病的疗法包括阿法链道酶和高渗盐水。阿法链道酶(pulmozyme;美国基因泰克公司)是一种吸入性重组人脱氧核糖核酸酶,其裂解积聚在cf粘液中的细胞外dna,yang等人,cochrane database syst rev.4:cd001127(2016)。高渗盐水被认为是通过渗透压驱动的流体转移来水合粘液层。donaldson等人,n engl j med.354:241-250(2006)。然而,这些试剂在肺功能、病情加重和生活质量的改善方面效果有限且多变。yang等人,cochrane database syst rev.4:cd001127(2016);henke等人,paediatrrespir rev.8:24-29(2007)。arina-1是一种用于治疗cf和其他慢性炎症性肺病的复配药物制剂。arina-1是通过将碳酸氢盐、l-谷胱甘肽和抗坏血酸溶解在水中制备的。先对由此获得的水性溶液进行雾化,再施用于患者肺部。参见,例如,adewale等人,am j respir cell mol biol.63:362-373(2020);美国专利号9,308,234和11,058,743;以及美国专利申请号2019/0351005和2020/0397849。本领域需要用于肺病治疗的稳定的药物制剂和产品。
背景技术
0、背景
技术实现思路
1、本公开提供了与arina-1相关的药物制剂和产品,用于治疗以粘液过多和炎症为特征的慢性炎症性肺病患者,如肺移植、囊性纤维化(cf)、非cf支气管扩张症、慢性阻塞性肺病(copd)和其他炎症性肺病患者。
2、arina-1和相关药物制剂的复配包括将碳酸氢盐(如碳酸氢钠)、l-谷胱甘肽和抗坏血酸溶解在水中。申请人发现,当在二氧化碳气氛下制备、包装和储存时,这种水性组合物具有令人惊讶的稳定性。
3、在一个方面,本公开提供了一种制剂,该制剂包含在具有顶部空间的封闭容器中的水性溶液,其中:
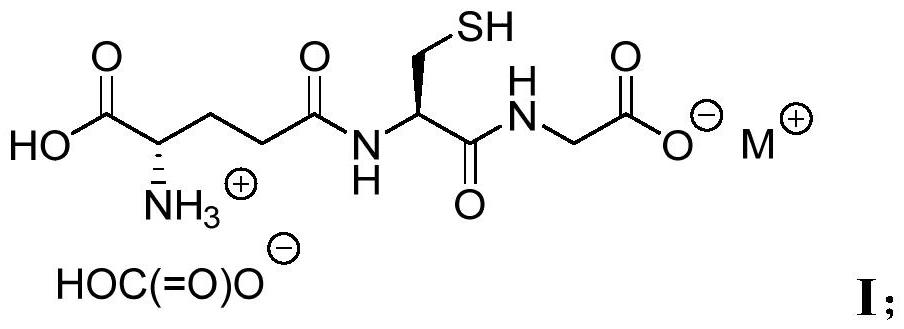
4、(i)所述水性溶液包含具有式i的盐:
5、
6、(ii)所述顶部空间的气氛包含90体积%或更多的二氧化碳;并且
7、(iii)m+是na+、li+、k+或cs+。
8、在另一方面,本公开提供了一种制备包含水性溶液且该水性溶液含有式i盐的方法,该方法包括:
9、(i)在二氧化碳气氛下将l-谷胱甘肽、抗坏血酸和m+hco3-溶解在注射用水中以得到水性溶液,其中,m+为na+、li+、k+或cs+;
10、(ii)将一部分水性溶液转移到容器中;
11、(iii)用二氧化碳覆盖水性溶液;和
12、(iv)用塞子密封容器。
13、在另一方面,本公开提供了一种包含式i盐的水性溶液,其通过在二氧化碳气氛下将l-谷胱甘肽、抗坏血酸和m+hco3-溶解在注射用水中而制备,其中,m+为na+、li+、k+或cs+。
技术特征:
1.一种制剂,其包含在具有顶部空间的封闭容器中的水性溶液,其中:
2.如权利要求1所述的制剂,其中,在约5℃下的24小时或更长时间内,所述水性溶液具有6.0±0.4的ph。
3.如权利要求2所述的制剂,其中,在约5℃下的24小时或更长时间内,所述水性溶液具有6.0±0.1的ph。
4.如权利要求1-3中任一项所述的制剂,其中,所述水性溶液还包含具有式ii的盐:
5.如权利要求1-4中任一项所述的制剂,其中,所述水性溶液还包含具有式iii的盐:
6.如权利要求1-5中任一项所述的制剂,其中,所述顶部空间的气氛包含95体积%或更多的二氧化碳。
7.如权利要求1-6中任一项所述的制剂,其中,所述水性溶液包含约10重量%至约20重量%的具有式i的盐。
8.如权利要求7所述的制剂,其中,所述水性溶液包含约13重量%至约17重量%的具有式i的盐。
9.如权利要求8中任一项所述的制剂,其中,所述水性溶液包含约14.7重量%的具有式i的盐。
10.如权利要求3-9中任一项所述的制剂,其中,所述水性溶液包含约5重量%至约15重量%的具有式ii的盐。
11.如权利要求10所述的制剂,其中,所述水性溶液包含约7重量%至约11重量%的具有式ii的盐。
12.如权利要求11所述的制剂,其中,所述水性溶液包含约9.1重量%的具有式ii的盐。
13.如权利要求1-12中任一项所述的制剂,其中,所述水性溶液的密度为约1.13g/l。
14.如权利要求1-13中任一项所述的制剂,其中,所述水性溶液是冷冻的。
15.如权利要求1-14中任一项所述的制剂,其中,m+是na+。
16.如权利要求1-15中任一项所述的制剂,其被包装为单个单位剂量。
17.如权利要求1-16中任一项所述的制剂,其中,所述制剂是药物产品。
18.一种制备如权利要求15所述的制剂的方法,所述方法包括:
19.如权利要求18所述的制备制剂的方法,其中,将约11重量%至约15重量%的l-谷胱甘肽、约5重量%至约9重量%的抗坏血酸和约5重量%至约9重量%的碳酸氢钠溶解在约68重量%至约76重量%水中,以得到所述水性溶液。
20.如权利要求19所述的制备制剂的方法,其中,将约13.0重量%的l-谷胱甘肽、约7.6重量%的抗坏血酸和约7.3重量%的碳酸氢钠溶解在约72.0重量%的水中,以得到所述水性溶液。
21.一种水性溶液,其包含具有式i的盐:
22.如权利要求21所述的水性溶液,其中,在约5℃下的24小时或更长时间内,所述水性溶液具有6.0±0.4的ph。
23.如权利要求22所述的水性溶液,其中,在约5℃下的24小时或更长时间内,所述水性溶液具有6.0±0.1的ph。
24.如权利要求21-23中任一项所述的水性溶液,其中,所述水性溶液还包含具有式ii的盐:
25.如权利要求21-24中任一项所述的水性溶液,其中,所述水性溶液还包含具有式iii的盐:
26.如权利要求21-25中任一项所述的水性溶液,其中,将约11重量%至约15重量%的l-谷胱甘肽、约5重量%至约9重量%的抗坏血酸和约5重量%至约9重量%的碳酸氢钠溶解在约68重量%至约76重量%的水中,以得到所述水性溶液。
27.如权利要求26所述的水性溶液,其中,将约13.0重量%的l-谷胱甘肽、约7.6重量%的抗坏血酸和约7.3重量%的碳酸氢钠溶解在约72.0重量%的水中,以得到所述水性溶液。
技术总结
本公开提供了与ARINA‑1相关的药物制剂、产品和方法,用于治疗患有慢性炎症性肺病患者,如患有肺移植、囊性纤维化(CF)、非CF支气管扩张症、慢性阻塞性肺病(COPD)和其他炎症性肺病的患者。
技术研发人员:E·J·德莱尼,C·德尔汉姆,D·W·科普兰德
受保护的技术使用者:莱诺翁股份有限公司
技术研发日:
技术公布日:2024/9/12
- 还没有人留言评论。精彩留言会获得点赞!