κ阿片受体激动剂在制备预防和/或治疗颞叶癫痫药物中的应用
本发明涉及生物,具体地,涉及一种κ阿片受体激动剂在制备预防和/或治疗颞叶癫痫药物中的应用。
背景技术:
1、颞叶癫痫起源灶位于双侧大脑颞叶部,患者数量约占所有癫痫患者的70%。目前临床使用治疗颞叶癫痫的药物主要有两类,一类为以卡马西平为代表的离子通道阻滞剂,另一类为以丙戊酸钠为代表的增强gaba系统活性的增强剂。但是,现有技术中的上述药物具有诸多不足,例如起效较慢、对30%左右的癫痫患者无效、长期使用具有严重的神经及躯体不良反应等缺陷。
2、颞叶癫痫患者的发病与海马硬化密切相关。痫样放电时,海马神经元兴奋性急剧升高,需氧量大幅增加,海马组织缺血缺氧,局部炎症反应加剧,引起神经元坏死并伴发胶质细胞增多,进而引发海马硬化。而海马硬化过程中gaba能中间神经元的丢失使得对于谷氨酸能神经元的抑制减少,脑内兴奋性机制增强,从而加剧痫样放电。因此,海马硬化既是难治性或反复发作癫痫所致的后果,也是引发癫痫发作的原因。减少海马兴奋性机制及后续系列反应是预防海马硬化及癫痫病理进程的有效措施。
3、另一方面,现有技术已知的κ阿片受体(kor)在海马区分布广泛,在颗粒细胞、椎体细胞等各型神经元及胶质细胞中均有表达。强啡肽是κ阿片受体的内源性配体,其在海马谷氨酸能突触传递中以与谷氨酸共释放的形式作用于突触前膜及突触后膜的κ阿片受体。前者通过抑制ca2+通道的开放,减少ca2+内流降低突触前神经元兴奋性,阻止谷氨酸的进一步释放;后者通过增加k+通道介导的外向k+电流稳定突触后膜,避免突触后神经元的过度兴奋。因此κ阿片受体可以作为治疗颞叶癫痫的潜在药物靶点。然而,现有技术中的κ阿片受体激动剂主要分为以强啡肽结构为基础的肽类物质、含氮类小分子化合物及以天然化合物鼠尾草素a分子骨架为基础的非含氮二萜类化合物。前两种激动剂多因不能透过血脑屏障、生物利用度低、副作用严重等不同的原因导致其无法在临床上使用。鼠尾草素a为墨西哥鼠尾草(salviadivinorum)的活性组分,墨西哥鼠尾草是墨西哥本土的唇形(薄荷)科的多年生草本植物。鼠尾草素a为最高度有效的、天然产生的非肽,且为唯一的非含氮κ类阿片受体激动剂;尤其地,鼠尾草素a为非常疏水的分子且不可溶于水,已知可溶于有机溶剂(如乙醇、dmso和丙酮)中,但是这些溶剂不适用于常规临床使用,尤其是不适用于静脉内(iv)递送。另一方面,现有技术中鼠尾草素a在临床上主要适用于神经病症,通常以口服或吸入形式达到有效血药浓度,并通过血脑屏障作用于目标脑区,但是,目前尚未有将非含氮二萜类κ阿片受体激动剂应用于颞叶癫痫预防和/或治疗的药物的报道。
技术实现思路
1、针对现有技术存在的技术问题,本发明公开了一种非含氮二萜类κ阿片受体激动剂在制备预防和/或治疗颞叶癫痫药物中的应用。
2、为实现上述目的,本发明提供了一种κ阿片受体激动剂在制备预防和/或治疗颞叶癫痫的药物中的应用,所述κ阿片受体激动剂为非含氮二萜类物质。
3、优选地,所述非含氮二萜类物质为鼠尾草素a,鼠尾草素a是由鼠尾草中提取出的非含氮二萜类物质,它是一种天然的选择性κ阿片受体激动剂,其化学名称是2h-萘(2,1-c)吡喃-7-羧酸,9-(乙酰氧基)-2-(3-呋喃基)十二烷基-6a,10b-二甲基-4,10-二氧-甲酯-(2s,4ar,6ar,7r,9s,10as,10br)-二维鸟苷a,化学结构式如式(1)所示
4、
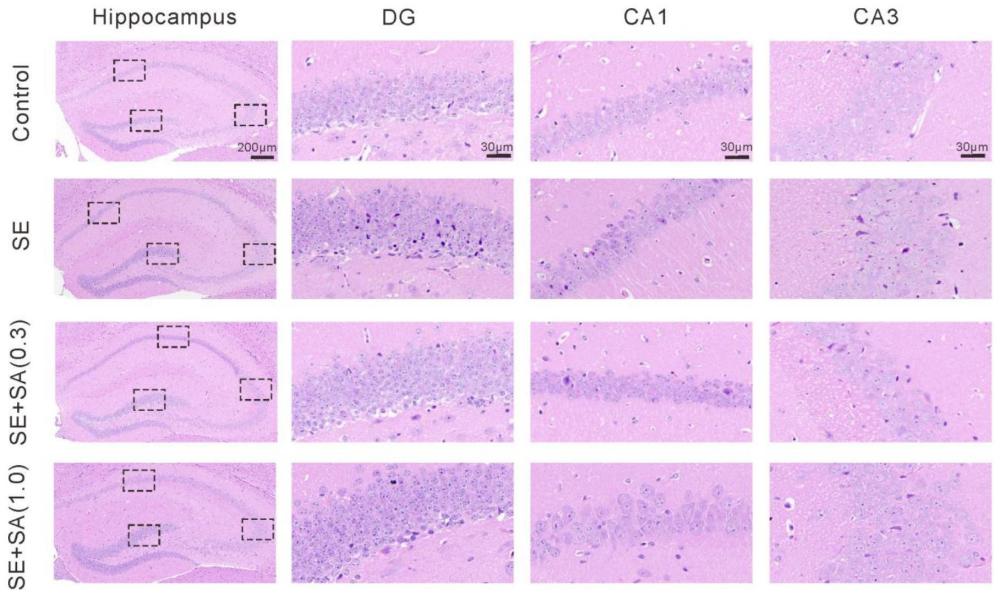
5、优选地,鼠尾草素a在预防和/或治疗颞叶癫痫中,可以延长阵挛发作的潜伏期,减少癫痫发作的时间及发作强度,减少海马区神经元的丢失,降低海马区炎症介质的水平。
6、优选地,所述预防和/或治疗颞叶癫痫的药物以所述κ阿片受体激动剂作为靶点。
7、优选地,所述预防和/或治疗颞叶癫痫的药物包括口服剂、吸入剂及注射针剂中的至少一种。
8、优选地,所述注射针剂包括将鼠尾草素a溶解于含有5%二甲基亚砜的生理盐水中。
9、优选地,小鼠实验中,鼠尾草素a的摄入剂量为0.3~1.0mg/kg,可降低促炎因子il-1β、tnf-a蛋白水平,降低提高inos蛋白水平,提高和arg-1的蛋白水平。
10、优选地,鼠尾草素a的摄入剂量为1.0mg/kg时,可降低3h内癫痫发作的总时长。
11、本发明基于匹鲁卡品腹腔注射诱导的颞叶癫痫模型小鼠,采用脑电记录、免疫组织化学、分子生物学、行为学等多种现代神经科学技术,对非含氮二萜类κ阿片受体激动剂鼠尾草素a的抗癫痫效应及相关机制进行研究,使其能够成为预防和治疗颞叶癫痫的临床药物。
12、本发明的具体实施方式中,以注射方式为例进行了详细说明,将鼠尾草素a溶解于含有5%二甲基亚砜的生理盐水,以腹腔注射方式给与匹鲁卡品所致癫痫模型小鼠,实验发现,鼠尾草素a可以延长阵挛发作的潜伏期,减少癫痫发作的时间及发作强度,减少海马区神经元的丢失,降低海马区炎症介质的水平,对癫痫模型小鼠具有神经保护作用。基于注射方式进行的测试为例,将鼠尾草素a用于预防和/或治疗颞叶癫痫的药物中,具有显著的效果,抗癫痫效果稳定,且不易产生耐药性。
13、本发明产生的技术效果:
14、1.本发明采用鼠尾草素a通过位于不同突触结构的κ阿片受体同时降低突触前细胞和突触后细胞兴奋性,发挥抑制脑内兴奋性机制的作用进而预防及治疗颞叶癫痫;相对于其他现有的抗癫痫药物,鼠尾草素a作用于一个全新的靶点,可以同时调节位于不同位置的多种离子通道,抗癫痫效果稳定,且不易产生耐药性。
15、2.本发明基于匹鲁卡品腹腔注射诱导的颞叶癫痫模型小鼠,采用脑电记录、免疫组织化学、分子生物学、行为学等多种现代化神经科学技术,对非含氮二萜类κ阿片受体激动剂鼠尾草素a的抗癫痫效应及相关机制进行研究,发现其有望成为预防和治疗颞叶癫痫的临床药物。
16、3.本发明采用的鼠尾草素a作为κ阿片受体激动剂在经腹腔注射后,可发挥抗炎抗凋亡作用,有效减少神经元过度兴奋引起的海马神经元丢失,减缓海马硬化过程。
17、4.本发明将鼠尾草素a应用于治疗癫痫的药物中,其摄入的方式可通过口服、吸入、注射等多种方式入血,且易通过血脑屏障,可成药性强;在抗癫痫的有效剂量下,鼠尾草素a的外周副作用小,在中枢中具有抗抑郁作用,可避免现有抗癫痫药物加重抑郁症状的副作用。
技术特征:
1.一种κ阿片受体激动剂在制备预防和/或治疗颞叶癫痫的药物中的应用,其特征在于,所述κ阿片受体激动剂为非含氮二萜类物质。
2.根据权利要求1所述的应用,其特征在于,所述非含氮二萜类物质为鼠尾草素a,化学式如式1所示,
3.根据权利要求2所述的应用,其特征在于,鼠尾草素a在预防和/或治疗颞叶癫痫中,可以延长阵挛发作的潜伏期,减少癫痫发作的时间及发作强度,减少海马区神经元的丢失,降低海马区炎症介质的水平。
4.根据权利要求1所述的应用,其特征在于,所述预防和/或治疗颞叶癫痫的药物以所述κ阿片受体作为靶点。
5.根据权利要求1所述的应用,其特征在于,所述预防和/或治疗颞叶癫痫的药物包括口服剂、吸入剂及注射针剂中的至少一种。
6.根据权利要求5所述的应用,其特征在于,所述注射针剂包括将鼠尾草素a溶解于含有5%二甲基亚砜的生理盐水中。
7.根据权利要求1所述的应用,其特征在于,小鼠实验中,鼠尾草素a的摄入剂量为0.3~1.0mg/kg。
8.根据权利要求7所述的应用,其特征在于,小鼠实验中,鼠尾草素a的摄入剂量为1.0mg/kg时,可降低3h内癫痫发作的总时长。
9.一种预防和/或治疗颞叶癫痫的药物,至少包括鼠尾草素a。
技术总结
本发明提供了一种κ阿片受体激动剂在制备预防和/或治疗颞叶癫痫的药物中的应用,所述κ阿片受体激动剂为非含氮二萜类物质,所述非含氮二萜类物质为鼠尾草素A。本发明采用鼠尾草素A通过κ阿片受体发挥抑制脑内兴奋性机制的作用进而预防及治疗颞叶癫痫;相对于其他现有的抗癫痫药物,鼠尾草素A作用于一个全新的靶点,可以同时调节位于不同位置的多种离子通道,抗癫痫效果稳定,且不易产生耐药性。
技术研发人员:计妙锦,杨银银,刘超,吴同轩
受保护的技术使用者:徐州医科大学
技术研发日:
技术公布日:2024/7/4
- 还没有人留言评论。精彩留言会获得点赞!