一种利用方沸石粉体制备铵型沸石的方法与流程
本发明涉及一种利用方沸石粉体制备铵型沸石的方法,所合成的铵型沸石可作为缓释氮肥或缓释肥料的载体使用。
背景技术:
方沸石属于似长石矿物,为含水的钠铝硅酸盐。化学分子式:naalsi2o6·h2o。与沸石有很多相关的地方,具有良好的吸附性能,离子交换性能和催化性能。根据这一特点,可将传统的化学速溶性氮肥与沸石相复合,制备负载有铵态氮的沸石。若将此类沸石施用于土壤,可实现养分的缓慢释放,即缓释性氮肥。目前市场上应用较广泛的缓释肥料几乎主要采用有机包膜法制备,其生产成本高且制备方法复杂。采用铵型沸石作为肥料的载体,可以延长肥效,提高养分利用率,且其成本低,制备方法简单。
likhacheva等人曾采用硝酸铵亚熔盐在较为苛刻的条件下(盐/水质量比=20,铵/钠摩尔比=40,140℃,7天)制备了铵型沸石。该方法物料消耗大,时间长,且利用危险易爆试剂硝酸铵,显然无工业利用价值。
技术实现要素:
本发明的目的是提供一种利用方沸石粉体制取铵型沸石的方法。铵型沸石可以作为缓释型氮肥或者缓释肥料载体使用。
为实现上述目的,本发明采取以下技术方案:
一种利用方沸石粉体制备铵型沸石的方法,采用下述步骤进行:
(1)将方沸石粉体与nh4+浓度为1.0~5.0mol/l的碳酸铵或碳酸氢铵溶液按照液固比为5~20ml/g的比例相混合;
(2)将上述浆料置于反应釜中,在60~150℃条件下,水热反应1~24h;反应结束后过滤,滤饼在90±5℃下干燥,所得粉料即负载有铵态氮的沸石粉体。
如上所述的利用方沸石粉体制备铵型沸石的方法,优选地,所述方沸石粉体是方沸石含量达到60%以上的天然方沸石矿物或人工合成方沸石制成的粉体。
如上所述的利用方沸石粉体制备铵型沸石的方法,优选地,所述方沸石粉体的粒度为1000~200目。
如上所述的利用方沸石粉体制备铵型沸石的方法,优选地,所述水热反应温度为110~150℃。
如上所述的利用方沸石粉体制备铵型沸石的方法,优选地,所述水热反应时间为1.5~4小时。
如上所述的利用方沸石粉体制备铵型沸石的方法,优选地,所述方沸石粉体与碳酸铵或碳酸氢铵溶液按照液固比为9~15ml/g的比例相混合。
另一方面,本发明提供一种铵型沸石,其是采用如上所述的方法制备的。
本发明中所用碳酸铵或碳酸氢铵优选为工业级,所用水优选为工业用水。
本发明的有益效果在于:
(1)原料成本低廉,方法过程简单,条件温和可控,易于工业化实施;
(2)可实现沸石矿物的高效利用;
(3)所得铵型沸石中nh4+含量达到约10~19%,nh4+以离子交换和吸附两种形式存在,可作为缓释氮肥或缓释肥料的载体使用。
附图说明
图1为利用方沸石粉体合成铵型沸石流程图;
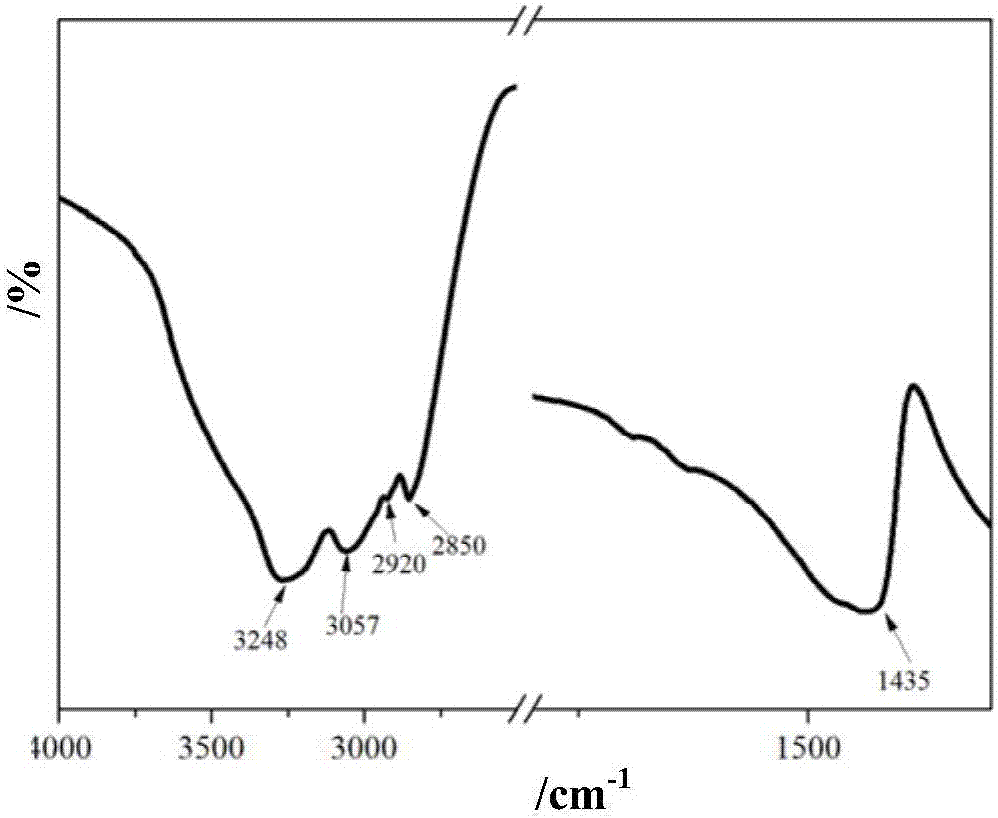
图2为实施例1所制备铵型沸石的红外光谱;
图3为实施例1所制备铵型沸石的粉晶x射线衍射图谱。
具体实施方式
实施例1
表1实施例1所用方沸石粉体的化学成分分析结果(wb%)
(1)方沸石粉体的化学成分分析结果如表1所示。
(2)操作步骤如附图1所示,准确称取3.00g方沸石粉体,与50mlnh4+浓度为5.0mol/l的碳酸铵溶液相混合制得浆料。将浆料转入聚四氟乙烯内衬反应釜中,130℃下水热晶化24h。反应结束后过滤,得到铵型沸石滤饼。滤饼在90±5℃下干燥12h,即制成铵型沸石粉体。产物(记为nan-1)主要成分为sio2、al2o3和nh4+,nh4+含量为19%。若方沸石成分中全部na+被nh4+替代,理论nh4+含量为9.2%,可见产物中除交换型nh4+外,部分以吸附形式存在,用蒸馏水重复清洗5次以上,nh4+含量降为10.31%。产物的红外光谱见附图2,波数为3248、3057、2920、2850、1435cm-1处的吸收峰均属于nh4+中n-h键的振动。产物的x射线粉晶衍射图谱见附图3,其衍射数据与jcpds卡片中铵白榴石(卡片号40-0474)基本一致(表2)。
表2实施例1所得铵型沸石粉体的晶格常数与jcpds卡片标准值对比
注:α=β=γ=90°,a=b.
实施例2
表3实施例2所用方沸石粉体的化学成分分析结果(wb%)
(1)原料方沸石粉体化学成分分析结果见表3。
(2)准确称取将10.00g方沸石粉体,与50mlnh4+浓度为5.0mol/l的碳酸氢铵溶液相混合制得浆料。将浆料转入聚四氟乙烯内衬反应釜中,110℃下水热晶化12h。反应结束后过滤,得到铵型沸石滤饼。滤饼在90±5℃下干燥12h,即制成铵型沸石粉体。产物nh4+含量通过纳氏分光光度法测定为10.82%,折氮含量8.42%。产物(记为nan-2)化学成分分析结果见表4,其中未测定bao含量,nh4+含量10.82%未在表中列出,部分烧失量由nh4+贡献,其余少量烧失量是原方沸石结构中残留部分水造成。
表4实施例2所得铵型沸石的化学成分分析结果(wb%)
技术特征:
技术总结
本发明涉及一种利用方沸石粉体制备铵型沸石的方法。该方法是将方沸石粉体置于碳酸铵或碳酸氢铵溶液中,在60~150℃下进行水热反应,结束后过滤,得到的固体滤饼在90±5℃温下干燥,即获得负载有铵态氮的沸石粉体。该粉体可作为缓释氮肥或缓释肥料的载体使用。
技术研发人员:刘昶江;马鸿文;高原;姚文贵
受保护的技术使用者:昊青薪材(北京)技术有限公司
技术研发日:2017.12.08
技术公布日:2018.05.11
- 还没有人留言评论。精彩留言会获得点赞!
- 一种纳米粉体工业生产系统的制作方法
- 一种高红外辐射粉体及其制备方法
- 一种铈锌共掺NiFe<sub>2</sub>O<sub>4</sub>纳米粉体及其制备方法
- 一种纳米Al<sub>2</sub>O<sub>3</sub>/Er<sub>3</sub>Al<sub>5</sub>O<sub>12</sub>/ZrO<sub>2</sub>复合粉体材料的制备方法
- 一种β?氢氧化镍纳米片的制备方法
- 一种硫化亚铜纳米玫瑰花的制备方法
- 一种球形氧化钇粉体的制备方法
- 一种亚微米级碳化硼粉体及其制备方法和用图
- 一种B<sub>4</sub>C纳米片的制备方法及B<sub>4</sub>C纳米片的制作方法
- 氮化铝粉体的制备方法