用于急性淋巴细胞白血病的预后方法和治疗系统与流程
相关申请的交叉引用
本申请要求2014年7月30日提交的美国临时专利申请号62/030,629的优权益,其内容通过引用整体并入本文中。
本文提供的是用于确定诊断患有急性淋巴细胞白血病(all)的患者的预后的方法,并且特别是确定标准治疗后疾病复发风险的方法。本文进一步提供的是治疗的系统,该系统由健康护理提供者指导,并且其包括所描述的预后方法和为被确定为具有特定复发风险的患者推荐的治疗。
背景技术:
白血病是一种血液或骨髓的癌症,其特征在于血细胞(通常是白细胞)的异常增加。白血病在临床上和病理上被细分为多种大组,包括其急性形式和慢性形式。急性白血病的特征在于未成熟血细胞的快速增加。这种拥挤使得骨髓不能产生健康的血细胞。由于恶性细胞的快速发展和积累在急性白血病中需要立即治疗,所述恶性细胞然后溢出到血流中并扩散到身体的其他器官。白血病的急性形式是儿童中白血病最常见的形式,其中急性淋巴细胞白血病(all)是最普遍的。
目前对all的治疗被患者评估和分类引入特定风险组中。这种分类的实例包括柏林-法兰克福-明斯特(berlin-frankfurt-münster)(bfm)、儿童肿瘤学小组(children’soncologygroup)(cog)(schrappe,annhematol.(2004);83:s121-3;vroomanlm等人,curropinpediatr.(2009);21(1):1-8)、来自英国的ukall、中国儿童白血病组(chinesechildren’sleukemiagroup)(cclg)和dana-farber癌症研究所all联盟(dana-farbercancerinstituteallconsortium)(dfci)。在所述分类中,患者特别是在白细胞计数、染色体重排和在治疗开始后第8天对泼尼松治疗的反应性方面进行分类。分类为特定组将确定如何积极地治疗患者以便提供有效治疗并降低疾病复发的可能性。
虽然目前的诊断和治疗方法已将治愈率提高了高达80-90%,但是某些儿童仍然被过度治疗或不足治疗(schrappem等人,leukemia.(2010);24:253-254;puich和evanswe,n.engl.j.med.(2006);354:166-178;bhojwanid等人,clin.lymphoma.myeloma.(2009);3:s222-230)。此外,目前的预后方法仅确定患者在初始诊断后的几个月的复发风险。因此,存在对可以在更接近治疗开始时对患者分类的更好的all预后方法以及由确定的复发风险规定的治疗系统两者的持续需求。
技术实现要素:
本文提供的是通过以下在受试者中急性淋巴细胞白血病(all)的预后方法:确定在来自所述受试者的样品(诸如骨髓样品)中mir-1290的表达水平;以及将所述受试者中的mir-1290表达水平与mir-1290的对照表达进行比较,其中与所述对照表达相比,所述受试者中mir-1290表达的显著增加表明所述受试者具有增加的all复发的风险;并且其中与对照表达相比,所述受试者中mir-1290表达的显著降低表明所述受试者具有降低的all复发的风险。
还提供的是通过以下在受试者中急性淋巴细胞白血病(all)的预后方法:确定在来自所述受试者的样品(诸如骨髓样品)中mir-1290的表达水平以及mir-151-5p和mir-451中的至少一种的表达水平;以及将确定的mir-1290以及mir-151-5p和/或mir-451的表达与mir-1290以及mir-151-5p和/或mir-451的对照表达进行比较,其中与所述对照mir-1290表达相比在所述受试者中mir-1290表达的显著增加,和与所述mir-151-5p和/或mir-451的对照表达相比mir-151-5p和mir-451中的至少一种的表达的显著降低结合,表明受试者具有增加的all复发的风险;并且其中与所述对照表达相比所述受试者中mir-1290表达的显著降低,和与mir-151-5p和/或mir-451的对照表达相比mir-151-5p和mir-451中的至少一种的表达的显著增加结合,表明所述受试者具有降低的all复发的风险。
本文进一步描述的是all治疗的系统,其包括确定来自所述受试者的样品(诸如骨髓样品)中mir-1290的表达水平;将所述受试者中mir-1290的表达水平与mir-1290的对照表达进行比较,其中与所述对照表达相比在所述受试者中mir-1290表达的显著增加,表明所述受试者具有增加的all复发的风险,并且需要适合于具有增加的all复发风险的受试者的治疗;以及给予所述患者被指定为适合于具有增加的all复发风险的患者的all治疗。
另外描述的all治疗的系统包括确定来自所述受试者的样品(诸如骨髓样品)中mir-1290的表达水平以及mir-151-5p和mir-451中的至少一种的表达水平;以及将确定的mir-1290以及mir-151-5p和/或mir-451的表达与mir-1290以及mir-151-5p和/或mir-451的对照表达进行比较,其中与所述对照mir-1290表达相比在所述受试者中mir-1290表达的显著增加,和与所述mir-151-5p和/或mir-451的对照表达相比mir-151-5p和mir-451中的至少一种的表达的显著降低结合,表明受试者具有增加的all复发的风险,并且需要适合于具有增加的all复发风险的受试者的治疗;以及给予所述患者被指定为适合于具有增加的all复发风险的患者的all治疗。
根据参照附图进行的以下详细描述,上述的和其他目的、特征以及优点将变得更加显而易见。
附图说明
图1是在125名all患者的群组中无复发生存率(rfs)的kaplanmeier估计。在图中,代表mir-1290的高或低表达的线相应地被指示。
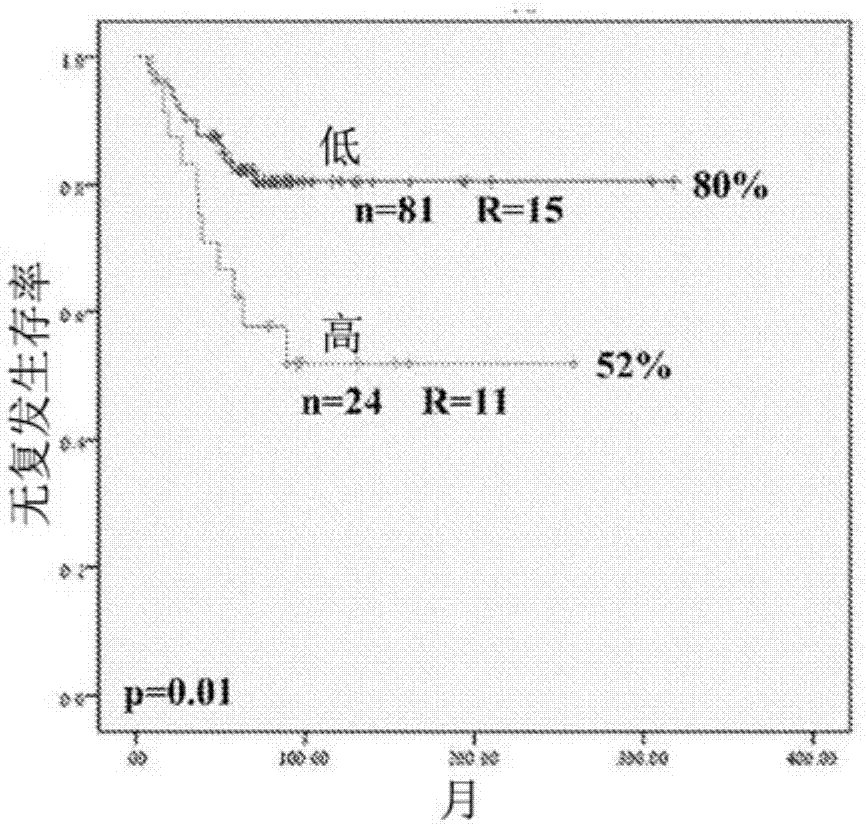
图2是仅用于b谱系all群组(n=105)的无复发生存率的kaplanmeier图。在所述图中,代表mir-1290的高或低表达的线相应地被指示。
图3是通过组合的mir的表达水平的无复发生存率的kaplanmeier分析:all患者的前体b细胞中两种下调的mir与上调的mir-1290一起。下面的线代表下调的mir-451和mir-151-5p以及上调的mir-1290的组合。上面的线代表用于mir-451、mir-151-5p和mir-1290的所有其他表达组合。
图4a-4c示出了hsa-mir-451转染减少了体内all细胞生长。图4a:通过定量实时pcr(qrt-pcr)测量的hsa-mir-451的表达分析。在用mir-451转染后24小时、转染后5天和10天的nalm-6细胞中hsa-mir-451的表达,以及在用混杂(杂乱的,scrambled)mirna转染的细胞中hsa-mir-451的表达作为阴性对照(对照)。图4b:在用由mir-451转染的nalm-6细胞移植的雌性nod/scid小鼠中的肿瘤大小的比较,用由混杂的mirna转染的细胞转染的nalm-6(细胞移植的小鼠中的肿瘤大小)作为阴性对照(对照),皮下注射细胞后持续31天。图4c:在实验结束时,在用由mir-451转染的nalm-6细胞移植的nod/scid小鼠中的平均肿瘤重量,用混杂的mirna转染的nalm-6细胞(移植的nod/scid小鼠中的平均肿瘤重量)作为阴性对照(对照)。误差棒,se.*,p<0.05。
图5a-5b示出了mir-451对nampt表达的影响。图5a:通过facs测量的在表达mir-451模拟物、抑制剂和混杂对照的nalm-6细胞系中的nampt的表达分析。图5b:验证mir-451与nampt的3'utr直接相互作用的荧光素酶报告物测定。误差棒,se.*,p<0.05。
图6a-6b示出了nampt表达对nad水平的影响。图6a:通过定量逆转录-pcr(rt-pcr)测定的在用50ng/ml的tpa处理24小时的nalm-6细胞系中的nampt的表达分析。图6b:在用50nm的tpa处理24小时的细胞中的nad+测定。误差棒,se。
图7a-7b示出了nampt抑制剂fk866诱导nalm-6细胞中的凋亡和nad水平的降低。图7a:在用fk866处理1小时、3小时和6小时的细胞中使用nad测定法来测量nad水平。图7b:使用凋亡试剂盒在用nampt抑制剂fk866处理的细胞中测量凋亡。误差棒,se.*,p<0.05。
图8a-8b示出了all细胞系对nampt抑制剂fk866的敏感性。在用fk866处理3小时的细胞中使用nad测定法来确定nad水平。用mir-451模拟物(图8a)、抑制剂(图8b)或混杂的阴性对照来转染测定的细胞(一个实验的代表性图)。
图9示出了与对照(混杂)相比,mir-1290(模拟物)过表达后的socs4蛋白表达水平。通过蛋白质印迹来确定和定量蛋白质表达。
图10a-10b示出了具有高和低mir-1290水平的allbm样品中的socs4蛋白水平。示出了代表性的蛋白质印迹和(图10a)和定量(图10b)。
图11示出了mir-1290(模拟物)的过表达后磷酸化stat5蛋白水平的定量。
图12是使用茎-环寡核苷酸引物通过rt-qpcr的mirna扩增的示意图。
所描述序列的简要说明
使用如在37c.f.r.1.822中定义的核苷酸碱基的标准字母缩写,示出了本文提供的核酸序列。示出了每个核酸序列的仅一条链,但是互补链被理解为通过对所显示的链的任何参考而被包括。序列表作为名为3044_3_seqlist.txt的,在2015年7月30日创建的约1.48kb的ascii文本文件提交,其通过引用被并入本文。在所附的序列表中:
seqidno:1是mir-151-5p的核苷酸序列。
seqidno:2是mir-451的核苷酸序列。
seqidno:3是mir-1290的核苷酸序列。
seqidno:4是mir-1290模拟物的核苷酸序列。
seqidno:5是mir-1290抑制剂的核苷酸序列。
seqidno:6是用于mir-151-5p的茎环逆转录dna引物的核苷酸序列。
seqidno:7是用于mir-451的茎环逆转录dna引物的核苷酸序列。
seqidno:8是用于mir-1290的茎环逆转录dna引物的核苷酸序列。
具体实施方式
i.缩写
all急性淋巴细胞白血病
mrd最小残留疾病(最小残留病)
ii.术语
除非另有说明,否则技术术语根据常规用法使用,例如其可以在由牛津大学出版社出版的benjaminlewin,genesv,1994(isbn0-19-854287-9);kendrew等人(编辑)中找到。除非上下文另有明确说明,否则单数术语“一个(a)”、“一个(an)”和“该”包括复数指代。类似地,除非上下文另有明确说明,否则词语“或”旨在包括“和”。还应当理解,对于核酸或多肽所给出的所有碱基大小或氨基酸大小以及所有分子量或分子质量值是近似的,并且被提供用于描述。尽管与本文所描述的那些方法和材料类似或等同的方法和材料可用于本公开的实践或测试中,但下文描述了合适的方法和材料。术语“包括(包含,comprise)”意指“包括(include)”。缩写“例如”来源于拉丁语例如,并且在本文中用于表示非限制性实例。因此,缩写“例如(e.g.)”与术语“例如(forexample)”同义。在冲突的情况下,本说明书(包括术语的解释)将处于支配地位。另外,所有所述材料、方法和实施例是说明性的,而不是限制性的。
异常的:与正常特征的偏差(偏离于正常特性)。正常特征(特性)可以在对照、群体的标准等中找到。例如,当所述异常状况是疾病状况诸如all时,少数正常特征的适当来源可能包括没有患有所述疾病的个体或没有经历所述疾病的特定预后结果(诸如all复发)的群体。类似地,异常可以指与疾病或疾病复发相关的病症。术语“与……相关”包括发展所述疾病或其复发的增加的风险。例如,某种异常(诸如mirna表达的异常)可以被描述为与all复发的生物学病症相关。适于与样品比较的对照或标准品(用于确定异常,诸如在表达临界值的确定中)包括被认为是正常的以及实验室确定的值的样品,即使这样的值可能是任意设置的,并记住这样的值可能随实验室与实验室的不同而不同。实验室标准和值可以基于已知的或确定的群体值来设置,并且可以以允许容易地比较测量的、实验确定的值的图表或表格的格式提供。
改变的表达:受试者或来自受试者的生物样品中生物分子(例如,mirna)的表达,其偏离于受试者或来自具有对于与所述分子相关的生物病症而言正常的或未改变的特征的受试者的生物样品中相同的生物分子的表达。正常表达可以在对照、群体的标准品等中找到。生物分子的改变的表达可以与其疾病或病症(诸如all复发)相关。
扩增:当用于提及核酸时,增加样品或样本中核酸分子的拷贝数的任何技术。扩增的实例是聚合酶链反应(以其所有形式),其中从受试者收集的生物样品在允许所述引物与样品中的核酸模板杂交的条件下与一对寡核苷酸引物接触。所述引物在合适的条件下延伸,从所述模板解离,然后重新退火、延伸和解离以扩增所述核酸的拷贝数。体外扩增的产物可以使用标准技术通过电泳、限制性内切核酸酶切割模式、寡核苷酸杂交或连接和/或核酸测序来表征。体外扩增技术的其他实例包括链置换扩增(参见美国专利号5,744,311);无转录等温扩增(参见美国专利号6,033,881);修复链反应扩增(参见wo90/01069);连接酶链反应扩增(参见ep-a-320308);间隙填充连接酶链反应扩增(参见美国专利号5,427,930);偶合连接酶检测和pcr(参见美国专利号6,027,889);以及nasbatmrna无转录扩增(参见美国专利号6,025,134)。
生物样品:可直接或间接从生物体获得的任何样品,包括全血、血浆、血清、眼泪、粘液、唾液、尿液、胸膜液、脊髓液、胃液、汗液、精液、阴道分泌物、痰液、来自溃疡和/或其他表面皮疹、水疱、脓肿、组织、细胞(诸如,成纤维细胞、外周血单核细胞或肌细胞)、器官和/或组织、细胞或器官的提取物(诸如,成纤维细胞、外周血单核细胞或肌肉细胞)。样品是使用本领域技术人员公知的方法收集或获得的。
cdna(互补dna):缺失内部非编码片段(内含子)和转录调节序列的一段dna。cdna也可以含有非翻译区(utr),诸如负责在相应rna分子中的翻译控制的那些。cdna在实验室中通过从提取自细胞的rna逆转录来合成。
化疗剂:在治疗以异常细胞生长或增生为特征的疾病中具有治疗用途的药剂。这样的疾病包括癌症、自身免疫性疾病以及以增生性生长为特征的疾病(诸如牛皮癣)。本领域技术人员可以容易地识别化疗剂(例如,参见slapak和kufe,principlesofcancertherapy,harrison'sprinciplesofinternalmedicine,第14版,第86章;perry等人,chemotherapy(化学疗法),abeloff,clinicaloncology第二版第17章,
对照:参考标准。对照可以是指示诸如mir-1290的诊断分子的基础表达的已知值。在具体实例中,对照样品获自已知不患有疾病或病症的受试者,包括经历或未经历疾病复发的all患者。在其他实例中,对照获自被诊断的受试者,但是在更早的时间点(在疾病发作之前或在疾病治疗的早期时间点之前或在疾病治疗的早期时间点)。测试样品和对照之间的差异可以是增加或相反地减少。所述差异可以是定性差异或定量差异,例如统计学上显著的差异。在一些实例中,差异是相对于对照增加或减少至少约10%,诸如至少约20%、至少约30%、至少约40%、至少约50%、至少约60%、至少约70%、至少约80%、至少约90%、至少约100%、至少约150%、至少约200%、至少约250%、至少约300%、至少约350%、至少约400%、至少约500%或大于500%。在另一具体实例中,感兴趣的mirna的对照表达值被设定为开始疾病治疗之前的一组all患者的上三分位数或中位数。
检测:确定是否存在或不存在试剂(诸如信号或特定核酸探针)。在一些实例中,这可以进一步包括定量。
确定基因产物的表达:以定性或定量方式检测表达(例如核酸)的水平。在一个实例中,如本文所述,其是mirna的检测。
诊断:通过其征兆、症状和各种测试和方法(例如本文公开的方法)的结果来鉴定疾病或发展疾病或病症(例如all或其复发)的倾向性(易感性,predisposition)的过程。通过该过程得到的结论也被称为“诊断”。术语“倾向性”是指使受试者易于或有风险患上病症、疾病或失调(诸如all或其复发)的一种或多种因素的影响。在所公开的方法中,特异性mirna表达确定来鉴定倾向于all复发(或处于all复发的风险增加的)受试者。
增加的风险:如本文所使用的,all复发的“增加的风险”是指在标准疾病治疗后相对于一般群体的all患者复发的统计概率的增加。如本文所描述的,被确定为具有all复发的增加的风险的受试者的风险可能具有高风险或中级风险,与“标准风险”相比,这两者都是增加的风险。
标记物:一种可检测的化合物或组合物,其直接或间接地结合至另一分子以便于该分子的检测。标记物的具体的非限制性实例包括放射性同位素、酶底物、辅助因子、配体、化学发光剂或荧光剂、半抗原和酶。
哺乳动物:该术语包括人类和非人类哺乳动物。类似地,术语受试者包括人类和动物疾病的受试者。
microrna(mirna):18-24个核苷酸长的短的单链rna分子。在细胞中内源性地产生自转录的非编码dna的更长的前体分子的mirna可以抑制翻译,或者可以通过与靶核酸互补的或接近互补的杂交来指导靶mrna的切割(boyd,labinvest.,88:569-578,2008)。如本文所使用的,“microrna序列”包括成熟mirna序列和前体序列两者,诸如pri-mirna、pre-mirna等。
寡核苷酸:多个连接的核苷酸,长度为约6个至约300个核苷酸。寡核苷酸类似物是指包含与寡核苷酸类似地起作用但具有非天然存在部分的部分的寡核苷酸的亚类。例如,寡核苷酸类似物可以含有非天然存在的部分,诸如改变的糖部分或糖间连接(糖间键,inter-sugarlinkage),诸如硫代磷酸酯寡脱氧核苷酸。天然存在的多核苷酸的功能类似物可以结合至rna或dna,并且包括肽核酸(pna)分子。特定的寡核苷酸和寡核苷酸类似物可以包括长度高至约200个核苷酸的线性序列,例如至少6个碱基的序列(诸如dna或rna),例如至少8、10、15、20、25、30、35、40、45、50、100或甚至200个碱基长,或来自约6个至约50个碱基,例如约10-25个碱基,诸如12、15或20个碱基。
预期受益:表明受试者可能将受益于特定治疗。例如,目前对all复发高风险患者的治疗包括蒽环类药物治疗。如本文所使用的,被确定为具有all复发高风险的患者将被预期受益于蒽环类药物治疗。
探针和引物:核酸探针和引物可以基于本发明中提供的核酸分子容易地制备。探针包含连接至可检测的标记物或报告分子的分离的核酸。典型的标记物包括放射性同位素、酶底物、辅助因子、配体、化学发光剂或荧光剂、半抗原和酶。讨论了用于适合于各种目的的标记物的标记的方法和选择的指导方法,例如,在sambrook等人(编),molecularcloning:alaboratorymanual,第2版,1-3卷,coldspringharborlaboratorypress(冷泉港实验室出版社),coldspringharbor(冷泉港),纽约州,1989和ausubel等人shortprotocolsinmolecularbiology,第4版,johnwiley&sons公司,1999中。
引物是短核酸分子,优选长度为10个核苷酸或更多个核苷酸的dna寡核苷酸。更优选地,更长的dna寡核苷酸的长度可以为约15、17、20或23个核苷酸或更多个核苷酸。引物可以通过核酸杂交而被退火至互补的靶dna链,以在所述引物和所述靶dna链之间形成杂交体,然后所述引物通过dna聚合酶沿靶dna链延伸。引物对可以被用于核酸序列的扩增,例如通过pcr或本领域公知的其他核酸扩增方法。
pcr引物对例如通过使用计划用于该目的的计算机程序可以从已知的序列衍生。本领域普通技术人员将理解,特定探针或引物的特异性随其长度而增加。因此,为了获得更高的特异性,可以选择包含被扩增的所述靶序列的至少17、20、23、25、30、35、40、45、50或更多个连续核苷酸的探针和引物。
定量实时pcr:用于检测和测量在pcr的每个循环中产生的产物的方法,所述产物与pcr开始之前存在的模板核酸的量成比例。获得的信息(诸如扩增曲线)可以被用于定量模板核酸序列的初始量。
逆转录:通过酶(逆转录酶)从rna模板生产dna。逆转录反应的dna产物被称为cdna。
序列同一性:两个核酸序列或两个氨基酸序列之间的相似度以所述序列之间的相似度表示,或者称为序列同一性。序列同一性通常以百分比同一性(或相似度或同源性)来测量;该百分比越高,两个序列越相似。用于比较的序列的比对方法在本领域中是公知的。
两个核酸分子紧密相关的可替换指征是两个分子在严格的条件下彼此杂交。严格条件是序列依赖性的,并且在不同的环境参数下是不同的。通常,严格的条件被选择为在限定的离子强度和ph下,比特定序列的热解链温度(热熔点)(tm)低约5℃至20℃。所述tm是50%的靶序列保持与完全匹配的探针或互补链杂交的温度(在限定的离子强度和ph下)。用于核酸杂交的条件和严格性的计算可以在sambrook等人(编),molecularcloning:alaboratorymanual,第2版,1-3卷,coldspringharborlaboratorypress(冷泉港实验室出版社),coldspringharbor(冷泉港),纽约州,1989和tijssen的laboratorytechniquesinbiochemistryandmolecularbiology-hybridizationwithnucleicacidprobes,第一部分第2章,elsevier,纽约,1993中找到。
导致特定程度的严格性的杂交条件将根据所选择的杂交方法的性质和杂交核酸序列的组成和长度而变化。通常,杂交的温度和杂交缓冲液的离子强度(特别是na+浓度)将决定杂交的严格性,尽管浪费时间也影响严格性。关于获得特定严格度所需的杂交条件的计算是标准的。以下是一组示例性的杂交条件:
非常高的严格性(检测共享90%同一性的序列)
杂交:5×ssc,65℃下16小时
洗涤两次:2×ssc,室温(rt)下,每次15分钟
洗涤两次:0.5×ssc,65℃下,每次20分钟
高严格性(检测共享80%同一性或更高同一性的序列)
杂交:5×-6×ssc,65℃-70℃下,16-20小时
洗涤两次:2×ssc,室温下,每次5-20分钟
洗涤两次:1×ssc,55℃-70℃下,每次30分钟
低严格性(检测共享大于50%同一性的序列)
杂交:6×ssc,室温至55℃下,16-20小时
至少洗涤两次:2×-3×ssc,室温至55℃下,每次20-30分钟。
治疗的系统:由单个行为者(诸如公共卫生保健提供者(例如国家卫生服务机构或其提供者)、健康维护组织(hmo)或医院组织)(通过其雇员或合同代理)指导的多步健康护理方法。虽然具有治疗系统的单独步骤可以由多个行为者进行,但是总方法由来自提供医疗保健的单个行为者组织。
iii.几种实施方式的概述
本文提供的是通过以下在受试者中急性淋巴细胞白血病(all)的预后方法:确定来自所述受试者的样品(诸如骨髓样品)中mir-1290的表达水平;并且将所述受试者中的mir-1290表达水平与mir-1290的对照表达进行比较,其中与所述对照表达相比,所述受试者中mir-1290表达的显著增加表明所述受试者具有all复发的增加的风险;并且其中与对照表达相比,所述受试者中mir-1290表达的显著降低表明所述受试者具有降低的all复发的风险。
还提供的是通过以下在受试者中急性淋巴细胞白血病(all)的预后方法:确定来自所述受试者的样品(诸如骨髓样品)中mir-1290的表达水平以及mir-151-5p和mir-451中的至少一种的表达水平;并将确定的mir-1290以及mir-151-5p和/或mir-451的表达与mir-1290以及mir-151-5p和/或mir-451的对照表达进行比较,其中与所述对照mir-1290表达相比在所述受试者中mir-1290表达的显著增加(其和与所述mir-151-5p和/或mir-451的对照表达相比mir-151-5p和mir-451中的至少一种的表达的显著降低结合),表明受试者具有增加的all复发的风险;并且其中与所述对照表达相比所述受试者中mir-1290表达的显著降低(其和与mir-151-5p和/或mir-451的对照表达相比mir-151-5p和mir-451中的至少一种的表达的显著增加结合),表明所述受试者具有降低的all复发的风险。
在具体的实施方式中,mir-1290、mir-151-5p和mir-451的对照水平是单独的(分开的,separate)临界值。
在其他具体实施方式中,所述受试者中all复发的风险进一步与选自由以下组成的组中的all相关的临床标准相关联:b-all和t-all诊断,最小残留疾病(mrd)高和低风险定义,在治疗第8天对泼尼松的反应(反应);bfm高、中、低风险定义,白细胞计数(wbc)高于或低于20,000个细胞/ml;患者年龄超过一岁和在六岁以下或相反,ccg高和低风险定义,以及性别。
在具体的实施方式中,所述受试者已经诊断患有b-all。
在进一步的实施方式中,受试者具有增加的all复发的风险的确定预测所述受试者可以受益于包含至少nampt或jak2抑制剂的治疗。
本文进一步描述的是all治疗的系统,其包括确定来自所述受试者的样品(诸如骨髓样品或血液样品)中mir-1290的表达水平;将所述受试者中mir-1290的表达水平与mir-1290的对照表达进行比较,其中与所述对照表达相比,在所述受试者中mir-1290表达的显著增加表明所述受试者具有增加的all复发的风险,并且需要适合于具有增加的all复发风险的受试者的治疗;以及给予所述患者被指定为适合于具有增加的all复发风险的患者的all治疗。
另外描述的all治疗的系统包括确定来自所述受试者的样品(诸如骨髓样品)中mir-1290的表达水平以及mir-151-5p和mir-451中的至少一种的表达水平;并将确定的mir-1290以及mir-151-5p和/或mir-451的表达与mir-1290和mir-151-5p和/或mir-451的对照表达进行比较,其中与所述对照mir-1290表达相比在所述受试者中mir-1290表达的显著增加(其和与所述mir-151-5p和/或mir-451的对照表达相比mir-151-5p和mir-451中的至少一种的表达的显著降低结合),表明受试者具有增加的all复发的风险,并且需要适合于具有增加的all复发风险的受试者的治疗;并给予所述患者被指定为适合于具有增加的all复发风险的患者的all治疗。
在所述系统的具体实施方式中,mir-1290、mir-151-5p和mir-451的对照表达是单独的临界值。
在该系统的具体实施方式中,所述受试者中all复发的风险进一步与选自由以下组成的组中的all相关的临床标准相关联:b-all和t-all诊断,最小残留疾病(mrd)高和低风险定义,在治疗第8天对泼尼松的反应;bfm高和低风险定义,白细胞计数(wbc)高于或低于20,000个细胞/ml;患者年龄超过一岁和在六岁以下或相反,ccg高和低风险定义,以及性别。
在所述系统的另外的实施方式中,所述受试者已经诊断患有b-all。
在具体实施方式中,所述受试者具有标准的(诱导前治疗非高的)复发风险或高复发风险。
在其他具体实施方式中,所述治疗是针对被确定为具有all复发高风险的患者的方案,诸如包括包含蒽环类化合物的组合物的治疗。
iv.通过检测mir-1290、mir-151-5p和mir-451的all预后
复发的预测已证明是成功治疗小儿all的关键。本文描述的是这样的观察,即使在all诊断当天,mirna表达的差异预示疾病复发,并且指示为患者推荐的治疗的适当形式。特别地,本文描述的是这样的观察,mir-1290的过表达与all复发相关,并且mir-151和mir-451表达(与标准相比,低表达的)的组合确定的预测能力,以及mir-1290表达(与标准相比,过表达的)大于其任何亚组合。all复发的增加的风险因此预示着所述患者将受益于如本文所述的all高风险治疗。
目前用于all治疗的实践包括确定标准治疗后疾病复发的风险。所确定的风险预后对于给予患者的治疗是决定性的。标准预后确定方法包括cog、bfm、mrd、ukall、cclg、dfci系统,从其中患者被确定为高风险(hr)、中级风险(ir)和标准风险(sr)。因此,在目前的实践下,all治疗作为基于风险的治疗被提供,即高风险患者接受更强化的治疗,而标准风险患者接受治疗减少。
根据bfm系统(vroomanlm等人,curropinpediatr.(2009);21:1-8),标准风险包括(1)无不利的细胞遗传,(2)年龄在1至6岁之间,(3)在第8天对泼尼松治疗有良好的反应。高风险包括以下中的至少一者:(1)细胞遗传异常(例如t(9;22)和t(4;11)),(2)在1岁以下或6岁以上,(3)在第8天对泼尼松治疗的反应差和(4)染色体亚二倍性(低二倍性,hypodiploidy)。中度风险包括那些年龄在1至6岁之间,没有显示出不利的细胞遗传,无染色体亚二倍性并且在治疗的第8天对泼尼松的良好反应,以及条件不满足标准风险或高风险标准的那些风险。
复发风险的可替换定义是mrd诊断,其是基于在治疗期间和/或治疗后在患者的骨髓(bm)中剩余的白血病母细胞的量的指示,其可以通过流式细胞术(facs)和聚合酶链反应(pcr)测量。(vandongenjjm等人,lancet.(1998);352:1731-1738)。在治疗开始后第33天和第78天的mrd分析后进行mrd风险分层(风险分级,riskstratification)。mrd标准风险被定义为在第33天和第78天发现的阴性mrd。mrd高风险被定义为在第78天发现10-3个白血病细胞(1000个正常细胞中有1个白血病细胞)。所有其他发现都被定义为中级风险。在本发明中,所述mrd测试是通过免疫球蛋白和t细胞重排位点的pcr扩增(pcr-mrd)进行的,并根据all中mrd检测的欧洲研究组(esg-mrd-all)的指南解释。
患者接受相同的治疗,直至根据从治疗第78天之后的mrd分析获得的结果来定义风险分层。
根据所述cog系统(smith等人,jclinoncol.(1996);14:18-24;hunger,amsocclinoncoleducbook(2012);611-615),nci标准风险包括(1)wbc计数小于50,000/μl和(2)年龄1岁至小于10岁。nci高风险包括(1)wbc计数为50,000/μl或更大和/或(2)年龄10岁或以上。
在根据所述cog方案的典型治疗中,在治疗的前四周给予诱导药物。没有cns3或明显的睾丸疾病的nci标准风险的诱导药物在其他治疗之中包括:(1)地塞米松,(2)长春新碱和(3)天冬酰胺酶。nci高风险药物或具有cns3或明显的睾丸疾病的药物包括(1)地塞米松,(2)长春新碱,(3)天冬酰胺酶和(4)蒽环霉素(诸如柔红霉素)。在治疗的初始阶段之后,在高风险和非高风险复发患者之间提供的治疗中的其他差异包括施用环磷酰胺、持续的长春新碱和天冬酰胺酶。高风险和非高风险cog(以及bfm)治疗之间的其他差异是本领域公知的(borowitz等人,blood(2008);111:5477-5485;并且总结在hunger,amsocclinoncoleducbook.2012,611-615)中。在所述cog方案中,mrd在第8天的血液中和第29天的骨髓中测量,并且与其他预后因素(以在诱导后确定患者的复发风险是否为低/平均/高/非常高)和诱导后治疗的方法一起使用。
因此,所描述的方法不仅允许用于改善all预后和复发风险的确定,而且还允许用于改善all治疗的整体系统,该方法包括提供如通过在显著早于目前用mrd测试可实现的时间点的时间点确定的复发风险所确定的最佳治疗方案。特别是,所描述的方法允许健康护理提供者确定受试者(诸如确定为具有增加机会的all复发(使用所描述的方法)的受试者)是否将受益于本领域公知的“高风险”治疗方案,诸如但不限于hrbfm或hrcog治疗方案。此外,如本文所描述的,nampt和jak2诱导的磷酸化蛋白分别在低表达mir-451和过表达mir-1290的细胞中被上调。因此,所描述的方法还允许健康护理提供者预测患者是否可以受益于涉及提供nampt和/或jak2抑制剂的治疗。
因此,本文提供的是通过以下用于受试者中all预后的方法:单独或与mir-151-5p和/或mir-451的表达组合来确定mir-1290的表达水平以及比较所述确定的表达与对照或标准(诸如预确定的临界值)。在一个具体实施方式中,mir-1290的表达被检测。在另一实施方式中,mir-1290和mir-151-5p的表达被检测。在又一实施方式中,mir-1290和mir-451的表达被检测。
在所描述的方法中,受试者样品中的mir-1290的表达单独或与mir-151-5p和/或mir-451的表达结合与对照样品中特异性mirna的表达进行比较,其中单独mir-1290表达的相对显著的增加或与mir-151-5p和mir-451中至少一种的显著降低结合,表明增加的all复发的风险。如通过本文所述的方法确定的增加的all复发的风险表明所述受试者将受益于目前给予被归类为all复发的“高风险”的受试者的治疗方案。如本文所理解的,对照是由来自一个或多个受试者的样品中的特异性mirna表达的量所定义的标准,所述受试者或者是无all的,或者是具有all但没有复发的。当额外的患者数据被累积时,这种标准可随时间改变。
在一些实施方式中,受试者样品与之比较的预定对照值被描述为临界值,其中偏离所述临界值表示与对照值的显著差异和增加的all复发的风险。在这样的实施方式中,与所述临界值相关的所述mirna的表达决定了所述患者应如何与那些与特定复发率相关的预先建立的all患者群体分组。例如,患者以高于临界值的水平表达mir-1290的确定(其与mir-151-5p和mir-451中的至少一种被表达低于临界值的确定结合),表明了所述患者比不表现出这样的mirna表达水平的患者具有更高的复发的风险。如本文所用的,这种表达(检测到的mir-151-5p和mir-451的下调和检测到的mir-1290的上调)可以被称为“阳性表达值”。
如本文所描述的,“临界值”,有时被称为“临界”,是满足高诊断灵敏度(真阳性率)和高诊断特异性(真阴性率)二者要求的值。确定的临界值是在预先建立的复发或者保持无疾病的群体中的mirna表达值差异的统计分析的结果。
应当强调的是,其他患者数据的累积可以提高当前提供的临界值的精确度,在特定实施例中,其可以基于根据所述患者数据使用例如可商购的分析软件程序所产生的roc(接受者工作特征)曲线。为了预后敏感性和预后特异性(其尽可能接近100%)的最佳组合沿着所述roc曲线选择所述mir-151-5p和/或mir-451表达值,并且将所得值用作(以所述给定的灵敏度和特异性)区分以一定比率复发的患者和不会以一定比率复发的那些患者的临界值。所述roc曲线可以随着越来越多的患者复发的数据和相关的mir-151-5p、mir-451和mir-1290表达值被记录和考虑、修改最佳临界值以及提高灵敏度和特异性而演变。因此,所提供的用于mir-151-5p和mir-451的临界值应当被视为非限制性的,而仅仅是统计分析的说明。
在一个具体实施方式中,用于mir-151-5p和mir-451的临界值分别为0.00015和0.001(相对于内标的表达的单位;其确定描述于国际专利申请号pct/il2011/000754中)。因此,低于0.00015和0.001的各mir-151-5p和mir-451表达水平表明受试者以比对照显著更低的水平表达这些mirna。关于mir-1290,如果受试者被确定为在确定的临界值以上表达mir-1290,则所述受试者被鉴定为以比对照显著更高的水平表达mir-1290。
在具体实施方式中,根据确定的表达水平,mir-1290表达的确定结合mir-151-5p和mir-451中的至少一种的确定是与特定的复发风险相关的。在其他实施方式中,所确定的mirna表达与其他临床特征组合(包括白细胞(wbc)计数、年龄、最小残留病变(mrd)风险指数、细胞遗传畸变、在第8天对泼尼松治疗的反应和染色体亚二倍性)以确定疾病预后和复发风险。
在具体实施方式中,可通过所述的方法检查的all患者群体组根据至少一种临床标准通过所述患者的亚群分组(sub-grouping)而可选地被进一步定义,并且每个患者亚组属于特定的预先建立的与特定复发率相关的all患者群体。根据某些实施方式,所述临床标准包括根据以下的亚群分组(subgrouping):b-all和/或t-all诊断;最小残留疾病(mrd)高、中和低风险定义;在治疗的第8天对泼尼松的反应;bfm高和低风险定义;白细胞计数(wbc)高于或低于20,000个细胞/ml;患者年龄超过一岁和在六岁以下或相反;ccg高和低风险定义;以及性别。
通常,在治疗的第8天对泼尼松的良好反应被定义为发现小于1000个白血病原始细胞(母细胞,blastcell)/ml血液,而差的反应被定义为发现超过1000个白血病原始细胞/ml血液。
在具体实施方式中,本发明的方法特别适用于预测b-all复发。
本文所述的mirna可以通过本领域公知的任何方法检测,包括标准寡核苷酸引物和探针的使用,其中每一种都可以特异性地杂交至mir-151-5p(seqidno:1)、mir-451(seqidno:2)和mir-1290(seqidno:3)中的至少一种和至少一种对照参考mirna的核酸序列。这样的序列包括与seqidno:1-3的反向互补体100%相同的序列。应理解,这样的引物和探针也可以低于与seqidno:1-3的反向互补体例如98%、95%、90%、85%或甚至更低相同,并且这种引物的设计在本领域是公知的。
然而,应当理解,虽然某些技术可以利用标准引物和探针,但所述mirna的18-24个核苷酸长度排除了简单扩增技术的使用。在具体实施方式中,使用dna微阵列检测mirna,其中从样品中提取mirna,对其进行逆转录,标记并暴露于具有匹配寡核苷酸的dna微阵列。通过在洗涤非特异性结合的逆转录序列之后测量的荧光来定量mirna的量。
在另一实施方式中,可以通过向提取的rna中加入聚腺苷酸(poly-a)区段(tract),使用聚腺苷酸(poly-a)引物逆转录(反转录)所述聚腺苷酸化的rna,随后是mirna-序列特异性qpcr,用特异性(mirna特异性)和非特异性(聚-aa)引物来确定mirna。
在又一实施方式中,使用mirna结构特异性茎环引物对所提取的mirna进行逆转录。然后,所述逆转录的mirna序列通过用mirna序列特异性正向引物和对mirna环特异性的反向引物的qpcr被扩增和定量。mirna茎环引物的设计及其在rt-qpcr中的使用被描述在kramer,curr.protinmolec.biol.15:10,2011年7月(可在ncbi.nlm.nih.gov/pmc/articles/pmc3152947/在线获得)中。用于逆转录mir-151-5p、mir-451和mir-1290的茎-环引物的非限制性实例基于kramer(curr.protinmolec.biol.15:10,2011年7月)中描述,并分别如seqidno6-8所阐述的。在图12中说明了rt-qpcr中茎-环引物的使用(也参见chen等人,nar,33:e179,2005)。
标准核酸检测方法的非限制性实例包括pcr(以其所有形式,包括qpcr)、核酸微阵列、northern印迹分析和各种形式的引物延伸。
用于检测所述的mirna的引物和探针可以是rna或dna或其类似物。dna/rna类似物的实例包括但不限于2-′o-烷基糖修饰物、甲基膦酸酯、硫代磷酸酯、二硫代磷酸酯、甲缩醛、3-硫代甲缩醛、砜、氨基磺酸酯和氮氧化物骨架修饰物以及类似物(例如lna类似物),其中碱基部分已被修饰。此外,寡聚物的类似物可以是其中糖部分已被修饰或被另一合适的部分替换的聚合物,从而导致包括但不限于吗啉代类似物和肽核酸(pna)类似物的聚合物。探针也可是任何所述寡核苷酸类似物类型一起或与天然dna或rna组合的混合物。在具体实施方式中,所述寡核苷酸和类似物可以单独使用;在其他实施方式中,它们可以与一种或多种另外的寡核苷酸或类似物组合使用。
在具体实施方式中,所描述的寡核苷酸是一对引物或核苷酸探针中的任一者,用于检测mir-1290以及mir-151-5p和mir-451中至少一种的表达水平,使用核酸扩增测定法(包括但不限于实时pcr、微阵列、pcr、原位杂交和比较基因组杂交)。用于检测核酸应用产物的,使用具有和/或不具有内部对照的自淬灭荧光探针的方法和杂交测定法在本领域中是公知的,例如,美国专利号6,258,569;6,030,787;5,952,202;5,876,930;5,866,336;5,736,333;5,723,591;5,691,146;以及5,538,848。
在具体实施方式中,除了检测感兴趣的mir(mir-1290等)外,所述特定的检测方法还使用引物和/或探针来检测待用作内部归一化对照的核酸的表达。根据该实施方式,被所述方法使用的检测核酸分子包括与mir-1290以及mir-151-5p和mir-451中至少一种的核酸序列特异性杂交的分离的寡核苷酸;以及与至少一种参考rna的核酸序列特异性杂交的分离的寡核苷酸。这种参考rna的非限制性实例包括参考mirna(其表达已知是相同的,不论all病症如何)、5s核糖体rna(rrna)、u6小核rna或mirxplore通用参考(ur)(miltenyibiotech),这代表用于比较多个样品的979合成mirna的库。
所描述的方法涉及基于检测某些mirna(特别是测试样品(特别是从受试者获得的生物样品)中的mir-151-5p、mir-451和mir-1290)的表达的all的预后,处理这样的样品以分离用于所述的方法的核酸的方法在本领域是公知的。在具体实施方式中,所述样品来源于所述受试者的骨髓。在其他具体实施方式中,所述样品是血液样品。
所描述的方法涉及确定mir-151-5p、mir-451和mir-1290的表达水平。如本文所述的,在患者中mir-151-5p和mir-451低表达(相对于对照)并且mir-1290过表达(相对于对照)的观察表明复发的增加的风险。因此,这样的患者可以受益于更强的all治疗。然而,相反的情况也是正确的:在具体实施方式中,如本文所述的样品中mir的检测,以及mir-151-5p和mir-451过表达(相对于对照)和mir-1290低表达(相对于对照)的观察表明了复发的降低的风险,甚至对标准治疗的更大的反应性。这样的观察预示着这样的患者可以受益于all治疗强度的降低(参见例如conter等人,blood115:3206-3214,2010)。
在具体实施方式中,本文所述的方法在受试者(患者)被诊断后的单个时间点使用。在其他实施方式中,本文所述的方法可被用于监测患者的进展以及其复发预后随时间的变化。多个时间点可被用于这样的监测,例如在诊断和治疗开始之后1个、2个、3个、4个、5个或6个月或更长时间(和其间的任何时间点)可以是用来测量来自患者的样品中mir-151-5p、mir-451和mir-1290的表达的合适的时间点。
本文还描述的是mir-451的低表达导致nampt的增加的观察,以及mir-1290的过表达导致jak2的增加的观察。nampt和jak2的过表达都与各种癌症相关。因此,如果适当的话,所描述的确定在受试者中mir-451和/或mir-1290异常表达的方法也允许预测所述受试者将受益于采用nampt和/或jak2抑制剂的治疗。
v.all治疗的系统
本文另外描述的是治疗all患者的系统。所描述的系统涉及首先通过所描述的检测mir-1290的表达以及mir-151-5p和mir-451中的至少一种的表达的方法确定all复发的风险。一旦确定受试者具有增加的all复发的风险,就根据所确定的复发风险调整,给予适当治疗。
如本文所描述的,用于all患者的典型治疗通过高或非高复发风险的预后来确定。标准方案(例如但不限于,bfm高风险和cog高风险,参见borowitz等人,blood(2008);111:5477-5485;并且总结在hunger,amsocclinoncoleducbook.2012,611-615中)已被开发从而比非高风险患者更强烈地治疗高风险患者,并降低标准风险患者中的治疗强度。在具有高复发风险和非高复发风险的患者之间的这种药物方案的差异包括在治疗过程中早期使用诸如柔红霉素的蒽环类药物。
在所描述的系统之前,确定合适的all治疗不仅依赖于完全不同的临床参数(例如wbc计数、泼尼松反应),但是这样的确定在初始诊断后的数天或甚至数周进行。相比之下,所述当前系统可以在对mir-1290的表达以及mir-151-5p和mir-451中的至少一种的表达的测试之后,在初始all诊断时确定适当的治疗。一旦确定患者可能具有增加的复发风险,则可以施用“高风险”治疗方案(诸如采用蒽环类药物(蒽环类抗生素)的那些方案)。
当前的系统基于这样的理解,即现代医疗服务由大实体提供,在其中向患者提供多重医疗服务。这样的实体的具体非限制性实例包括医师小组、医院联盟或网络以及公共或私人健康维护组织。在这些实体内,患者的健康护理可以由单个行为者(诸如医师、护士从业者等)管理,但专门的服务由所述系统内的多个行为者(诸如诊断者和专家)向所述患者提供。应认识到,在具体实施方式中,某些服务可外包给主要服务提供者之外的提供者。因此,诊断者可能不同于主要医师或肿瘤学家。然而,在所有实施方式中,正在指导所描述的治疗系统的是所述主要服务提供者或其代表或雇员。
提供以下实施例以说明某些具体特征和/或实施方式。这些实施例不应被解释为将本公开限制为特定特征或所描述的实施方式。
实施例:
实施例1:一般方法
患者材料收集:在诊断时,从95名儿科all患者获得骨髓(bm)活组织检查样品(biopsy),并且那些样品中白血病母细胞的百分比为至少80%。53例男性和42例女性,中位年龄6.6岁(范围0.3-18岁),28例患者具有t-all,46例患者具有wbc>20000,18例患者为泼尼松弱反应者,32例患者被临床分类为bfm高风险,40例中级风险和23例标准风险,31例患者复发。患者的中位随访期为69个月(范围6-296个月)。所有患者均在以色列施奈德儿童医疗中心被治疗。根据ins-84、ins-89、ins-98和ins-2003方案分别治疗4名、16名、25名和50名患者(所有这些都是一般bfm研究和方案的一部分)[starkb等人,leukemia.(2010);24:419-424;ins-2003]。
rna分离:根据mirneasy迷你试剂盒(qiagen)从来自bm活组织检查样品的107个细胞中分离rna。rna浓度通过测量在260nm处的吸光度以1.8的a260/a280比率来确定。
mirna表达谱:使用miltenyi生物技术公司微阵列平台(miltenyibiotech,德国)对48个all样品进行微阵列分析。rna的质量通过agilent2100bioanalyzer平台(安捷伦技术公司,agilenttechnologies)评估,并通过琼脂糖凝胶电泳显示。根据mirxploretm微阵列平台用户手册(miltenyibiotech,德国)进行样品标记。对于那些显示足够的rna产量的样品,2μg的总rna被用于标记,对于所有其他样品,可用量的总rna被使用。随后,使用a-hybtm杂交站(miltenyibiotech,德国)将荧光标记的样品与mirxploretm微阵列杂交过夜。对照样品用hy3标记,并且实验样品用hy5标记。mirxplore通用参照(ur)用作对照样品,并且其代表用于比较多个样品的979个合成mirna库。使用来自agilent(安捷伦技术公司,agilenttechnologies)的激光扫描仪检测所述杂交的mirxploretm微阵列的荧光信号。通过piqortm分析仪(miltenyibiotech,德国)为每个一式四份计算归一化的hy5/hy3比率。只有具有等于或高于背景信号强度50%百分位的信号的mirna被用于hy5/hy3比率计算。将数据转化为用于数据聚类(使用pearson相关和平均连锁的2d聚类)的log2比率。
qrt-pcr:mirna-微阵列结果通过95个样品上的qrt-pcr来验证。根据制造商说明书(exiqon,丹麦)从100ng制备cdna。对所选择的mirna使用lnatm引物(exiqon)进行qrt-pcr。5srrna用作参照物。用lightcycler480一式两份进行qrt-pcr。
统计分析:使用paswstatistics18(spssinc.,芝加哥,伊利诺伊)分析mirna表达数据。为了与年龄、性别、wbc、d8、类型和风险组相关,使用fisher的精确检验。为了确定最佳临界值,对每个mirna进行roc分析。进行kaplan-meier分析以评价所选择的mirna是否与复发相关,并且cox-回归被用于确定那些mirna是否可以被认为是独立的风险因素。<0.05的p值被认为对于存活分析是显著的。
实施例2:mir-151-5p、mir-451和mir-1290表达与各种all临床参数相关
该实施例表明,通过mir-151-5p和mir-451降低的表达,伴随着mir-1290增加的表达,可以准确地预测all预后。
微阵列分析被用于确定all特异性mirna表达。根据979合成mirna的组(panel),相对于通用参照(ur),仅116个显著更高,以及116个显著更低。用年龄、类型、wbc、d8、风险组和复发聚类显示了10个、33个、20个、14个、19个和33个mirna分别在all中被显著较低表达,而9个、36个、16个、12个、14个和28个分别在all中被显著较高表达。在国际专利申请号pct/il2011/000754(其全部内容通过引用并入本文)中描述了较低表达的mirna的分析。其中,描述了mir-151-5p和mir-451表达的组合减少预示增加的all复发的风险和更差的疾病预后。
在mir-all微阵列的进一步分析中,选择4个被上调并与至少3种不利预后标记物:mir-196b、mir-424、mir-1248和mir-1290相关的mir。为了证实表达和all之间的相关性,通过在一群125位儿科all患者(b谱系和t细胞)中的实时定量pcr进一步分析这4种mir的表达水平。在分析的4种mir中,只有mir-1290与all结果显著相关。
使用四分位数3作为临界值,表达高水平的mir-1290的患者具有48%的无复发生存率(rfs),对比在那些表达低水平mir患者中的77%的rfs(p=0.005,图1)。当使用中值表达水平作为临界值时,维持了与结果的显著相关性。对于表达高水平的那些患者,rfs为59%,相比对于表达低水平的mir的那些患者,rfs为81%(p=0.017,数据未示出)。当仅分析b谱系all患者(n=105)时,也观察到与结果的显著相关性。表达高水平的mir-1290的患者具有52%的rfs,相对表达低水平的那些患者具有80%的rfs(p=0.010;图2)。
当使用变体:mir-1290、年龄、wbc和在b谱系群中泼尼松的反应应用多变量cox回归分析时,mir-1290和wbc都被鉴定为显著的独立的预后标志物。根据该分析,确定了表达高水平mir-1290的患者具有3倍增加的复发风险(表i)。
表a:在b谱系群(n=105)中对复发的多变量cox回归分析
目前,all复发的风险是基于在诊断后第33天和第78天治疗后检测到最小残留疾病。残余白血病细胞的量决定了风险组,并相应地调整治疗。目的是增加高风险组中的治疗,并减少有利组的治疗。再次应用多变量cox回归分析,包括mrd数据,其可用于61名b谱系all患者。所有患者(不包括2例)为mrd非高风险患者。表达高水平的mir-1290的患者具有4.8倍的增加的复发的风险(p=0.027;表ii)。
表b:用于b谱系mrd非高风险群组(n=61)中的复发的多变量cox回归分析
当与下调的和上调的mir有关的数据被组合时,显示出表达低水平的两种mir(mir-151和mir-451)连同高水平的mir-1290的患者具有非常差的结果;33%对所有其他组合的79%的rfs(p=0.008;图3)。
当多变量cox回归分析被应用于下调和上调mir的组合结果中的复发风险时,显示出表达低水平的mir-151和mir-451两者伴随高水平的mir-1290的患者具有16.7的增加的复发风险(p=0.006;表iii)。
表c:用于pcr-mrd非高风险群(n=54)中复发的多变量cox回归分析
基于这些分析,可以得出结论,在非高风险患者群内,将mir-151、mir-451和mir-1290的检测结合在一起,可以精确地检测到非常高风险的患者,使得那些处于高复发风险的患者可以从已经在诊断时更强的治疗中受益。
实施例3:mir-451的上调减少了all细胞生长
如本文所述的,与对照水平相比mir-451降低的表达可以作为all复发风险的预后因素,因为在诊断时mir-451的低表达预测了更差的结果。为了证明mir-451在all中的作用,使用mir-451模拟物(seqidno:2)转染(nalm-6/mir-451)通过电穿孔(amaxanucleufectortechnology;试剂盒t;程序c-005)在all衍生的nalm-6细胞系中上调了mir-451。使用rq-pcr来确认转染的细胞中的mir-451表达。所述rq-pcr结果显示,相比阴性对照细胞(对照),nalm-6/mir-451中mir-451的表达显著增加(图4a)。
为了进一步研究hsa-mir-451在体内推定的肿瘤抑制功能,将用mir-451体外转染的或用混杂的对照核酸转染的107个活nalm-6未转染细胞皮下注射进6周龄雌性nod/scid小鼠的右侧腹部。虽然移植有混杂的mir对照细胞的动物在20天后发展成大肿瘤,但接受nalm-6/mir-451细胞的动物显示出显著减少的肿瘤生长(图4b)。在第26天,混杂对照小鼠和mir-451小鼠中的中值肿瘤体积分别为204.69mm3(se=63.96)和23.32mm3(se=13.12)(p=0.019)。在实验结束时,处死小鼠并称重肿瘤。混杂对照小鼠和mir-451小鼠中的肿瘤重量中位数分别为0.0966g(se=0.040)和0.0159g(se=0.0009)(p=0.046)(图4c)。这些结果表明hsa-mir-451的上调调节了all中的细胞生长,并支持hsa-mir-451作为肿瘤抑制基因的作用。
实施例4:mir-451在all细胞系中通过靶向nampt3'-utr抑制nampt表达
该实施例证明namptmrna是mir-451翻译抑制的特异性靶点。
使用开放获取软件程序(targetscan和miranda),烟酰胺磷酸核糖基转移酶(nampt)被确定为mir-451的预测靶点。
为了确定mir-451对nampt表达的影响,用mir-451模拟物(seqidno:2)和mir-451抑制剂(genecopoeiamiarrestmir-451,抑制剂表达克隆)转染nalm-6细胞,并且nampt的表达通过使用特异性nampt抗体的facs分析来测量。在细胞中mir-451的过表达后,nampt蛋白表达降低了46%的nampt,而mir-451抑制剂引起nalm-6/mir-451细胞中nampt表达增加60%(图5a,p<0.05)。
为了证实nampt是mir-451的直接靶点,产生了含有nampt3'-utr(lightswitchnampt3'utrreportergoclone)的荧光素酶报告载体。然后在mir-451模拟物和抑制剂存在和不存在的情况下进行荧光素酶报告物测定(lightswitch荧光素酶测定;switchgear),以确定nampt是否是mir-451的直接下游靶点。当mir-451模拟物被转染时,含有nampt3'-utr的报告物的相对荧光素酶活性降低了80%。相比之下,mir-451抑制剂显示报告物的相对荧光素酶活性显著增加17%(图5b,p<0.05)。这些结果证实了,mir-451直接结合nampt转录物的3'-utr,并负向调节其蛋白水平。
几个研究者的研究已经表明12-o-四癸(十四烷)酰基佛波醇-13-乙酸酯(tpa)(sigma)是特别有效的肿瘤启动子并刺激蛋白激酶c(pkc)。由于nampt在几种肿瘤中过表达,因此认为通过tpa治疗实现nampt刺激是可能的。为测试这个假设,外周血细胞用50ng/ml的tpa处理24小时,并且通过使用特异性nampt抗体的facs来测量nampt表达。用tpa处理的细胞显示出nampt表达水平超过4倍的增加(图6a)。
nampt是nad+生物合成途径中的限速酶。因此,使用标准nad+确定(biovisionnadh/nad定量试剂盒)测量被刺激的细胞中的nad+水平。发现在所述tpa刺激的细胞中的细胞nad+水平高2倍(图6b)。
实施例5:nampt增加的表达增加了all细胞对nampt抑制剂fk866的敏感性
实施例4显示mir-451调节nampt的表达,并通过扩展调节细胞nad+水平。该实施例证明了其中mir-451表达降低的all细胞对nampt抑制剂fk866具有增加的敏感性。
fk866是一种有效的nampt抑制剂,已知其导致细胞中细胞内nad+水平的消耗,并最终诱导凋亡。因此nalm-6细胞系中fk866处理对细胞凋亡和nad+水平的效应被表征。
用1nm的fk866(sigma)处理nalm-6细胞1小时、3小时和6小时,并且使用如所述的nad测定法来测量nad+形成。结果显示在fk866处理后nad+检测的逐渐减少(图7a)。因此,fk866是nalm-6细胞系中nad+形成的特异性抑制剂。为了测量fk866处理后nad+消耗对nalm-6细胞的影响,测量了凋亡和存活力。用1nm的fk866处理nalm-6细胞48小时,并使用facs测量凋亡。如图7所示的,fk866有效地抑制nad+形成(图7a)并诱导nalm-6细胞的凋亡(图7b)。
在用mir-451模拟物或mir-451抑制剂转染后,在细胞中测量了nalm-6细胞对nampt抑制剂fk866的敏感性(图8)。所述灵敏度是通过nad+水平来测量的。与nalm-6/mir-nc相比,在fk866处理后nalm-6/mir-451细胞显示了nad+产物的更小的变化(图8a)。然而,与nalm-6/mir-nc相比,在fk866处理后nalm-6/mir-抑制剂细胞显示了nad+产物的超过5倍的变化(图8b;p=0.003)。这些结果表明,表达低水平mir-451的all细胞对nampt抑制剂更敏感。因此,mir-451表达可区分可以受益于用nampt抑制剂(诸如fk866)治疗的患者。
实施例6:mir-1290靶向socs4的表达
本实施例描述了作为mir-1290的靶点的socs4的确定,并且其将受到在具有较高复发率的all受试者中观察到的mir-1290过表达的影响。
使用靶点预测软件(mirdb、miranda),socs4被选择作为mir-1290的潜在靶点。socs4基因编码stat诱导的stat抑制剂(ssi)的成员,也称为细胞因子信号转导(信号传导)抑制剂(socs)家族。ssi家族成员是细胞因子诱导的细胞因子信号转导的负向调节剂。socs4负向调节所述stat家族。该基因的表达是由各种细胞因子(包括il6、il10和干扰素(ifn)-γ)诱导的。被该基因编码的蛋白可以结合至jak激酶,并抑制jak激酶的活性。已知所述jak激酶在白血病中被激活。
在mir-1290模拟物(seqidno:4,过表达)、mir-1290抑制剂(seqidno:5,沉默)和mir-混杂(对照)转染进入nalm6细胞系后,socs4的蛋白水平使用蛋白质印迹法被测量(p=0.029;图9)。图中所示的值是来自3个实验的平均值±s.d。
另外,socs4蛋白水平在all患者的31个bm样品中被测量,并与mir-1290的水平进行比较。在具有高mir-1290表达水平的样品中socs4蛋白水平显著降低(p<0.0001;图10)。
在将mir-1290模拟物(过表达)转染进入nalm-6细胞系之后,通过facs分析来测量磷酸化的stat5(磷酸-stat5)水平。在表达高水平的mir-1290的细胞中,pstat5蛋白水平增加50%是明显的(图11)。
jak2是白血病过程中的必需基因。我们已经表明mir-1290的过表达导致socs4的下调。socs4通常抑制jak2的活性,因此其下调导致jak2的增加的活性,而不需要外部信号(作为细胞因子)。
该结果表明mir-1290的表达水平可预测活化的jak/stat途径的存在或不存在,并预测谁可受益于jak2抑制剂。
鉴于所公开的发明的原理可被应用的许多可能的实施方式,应当认识到,所示出的实施方式仅是本发明的优选实施例,并且不应被视为限制本发明的范围。相反,本发明的范围由所附的权利要求书限定。因此,我们要求保护落入这些权利要求的范围和精神内的所有发明作为我们的发明。
序列表
<110>莫尔研究应用有限公司
<120>用于急性淋巴细胞白血病的预后方法和治疗系统
<130>pn1651703pzc
<140>pct/il2015/050790
<141>2015-07-30
<150>us62/030,629
<151>2014-07-30
<160>8
<170>patentinversion3.5
<210>1
<211>21
<212>rna
<213>智人
<400>1
ucgaggagcucacagucuagu21
<210>2
<211>22
<212>rna
<213>智人
<400>2
aaaccguuaccauuacugaguu22
<210>3
<211>17
<212>rna
<213>智人
<400>3
uggauuuuuggaucagg17
<210>4
<211>29
<212>rna
<213>合成寡核苷酸
<400>4
uggauuuuuggaucaccugauccaaaaau29
<210>5
<211>11
<212>rna
<213>合成寡核苷酸
<400>5
ucccugaucca11
<210>6
<211>50
<212>dna
<213>合成寡核苷酸
<400>6
gtcgtatccagtgcagggtccgaggtattcgcactggatacgacactaga50
<210>7
<211>50
<212>dna
<213>合成寡核苷酸
<400>7
gtcgtatccagtgcagggtccgaggtattcgcactggatacgacaactca50
<210>8
<211>50
<212>dna
<213>合成寡核苷酸
<400>8
gtcgtatccagtgcagggtccgaggtattcgcactggatacgactccctg50
- 还没有人留言评论。精彩留言会获得点赞!