大黄鱼IFNc基因大肠杆菌表达产物的制备方法与应用与流程
本发明属于基因工程领域,具体涉及一种大黄鱼ifnc基因大肠杆菌表达产物的制备方法与应用。
背景技术:
干扰素(interferon,ifn)是一类能诱导脊椎动物细胞抗病毒状态,并在抗病毒防御中起重要作用的诱导性多基因家族细胞因子(robertsenb.theinterferonsystemofteleostfish[j].fishshellfishimmunol,2006,20(2):172-191)。硬骨鱼类作为低等脊椎动物也拥有相对完善的干扰素系统。鱼类ifn分为
最近的研究结果表明,除ifnd与ifnh外(groupiifn),鲈形目鱼如大西洋白姑鱼、鳜鱼等,还存在一种groupiiifn,ifnc(milnedj,campoverdec,andreekb,chenx,zouj,secombescj.thediscoveryandcomparativeexpressionanalysisofthreedistincttypeiinterferonsintheperciformfish,meagre(argyrosomusregius)[j].devcompimmunol,2018,84:123-132.laghariza,chensn,lil,huangb,ganz,zhouy,huohj,houj,niep.functional,signallingandtranscriptionaldifferencesofthreedistincttypeiifnsinaperciformfish,themandarinfishsinipercachuatsi.devcompimmunol.2018,84:94-108)。ifnc在各检测组织中呈组成型表达,在病毒或其类似物polyi:c诱导刺激后其表达量显著上调。大西洋白姑鱼ifnc可诱导自身及干扰素调节因子3和7的表达,并表现出明显地降低病毒滴度的作用(milnedj,campoverdec,andreekb,chenx,zouj,secombescj.thediscoveryandcomparativeexpressionanalysisofthreedistincttypeiinterferonsintheperciformfish,meagre(argyrosomusregius)[j].devcompimmunol,2018,84:123-132.)。
技术实现要素:
本发明的目的之一在于提供可高效表达大黄鱼ifnc基因的大肠杆菌工程菌。
本发明的目的之二在于提供一种大黄鱼ifnc基因的大肠杆菌表达产物及其制备方法。
本发明的目的之三在于提供大黄鱼ifnc重组蛋白的应用。
为实现上述目的,本发明采用如下技术方案:
一种大黄鱼ifnc基因的大肠杆菌工程菌,所述工程菌为大肠杆菌(escherichiacoli)bl21/pet-43.1a-ifnc,已于2018年10月22日保藏于中国典型培养物保藏中心,保藏编号为cctccno:m2018697;中国典型培养物保藏中心的地址为中国,武汉,武汉大学。
一种大黄鱼ifnc基因大肠杆菌工程菌,重组表达了核苷酸序列如seqidno.1所示的基因。
大黄鱼ifnc基因大肠杆菌的表达产物,制备方法包括以下步骤:
(1)利用正向引物ifnc-f和反向引物ifnc-r,采用pcr技术扩增出编码第28位至第189位氨基酸的大黄鱼ifnc成熟肽基因片段;
(2)将步骤(1)得到的大黄鱼ifnc成熟肽基因片段克隆到大肠杆菌表达载体pet-43.1a,得到含大黄鱼ifnc基因片段的重组表达载体pet-43.1a-ifnc;
(3)将重组表达载体pet-43.1a-ifnc转化大肠杆菌bl21菌株,经氨苄青霉素筛选及测序鉴定后,获得含有大黄鱼ifnc基因片段的大肠杆菌bl21/pet-43.1a-ifnc工程菌;同时,表达载体pet-43.1a转化大肠杆菌bl21菌株,获得的大肠杆菌bl21/pet-43.1a作为对照菌株;
(4)大肠杆菌pet-43.1a-ifnc工程菌在lb培养基中经终浓度0.1mmiptg诱导、16ºc振荡培养12小时,将培养物离心收集菌体,利用buffera重悬后,超声破碎,分别收集菌体裂解液上清和沉淀,经聚丙烯酰胺凝胶电泳sds-page分析后表明大黄鱼ifnc重组蛋白为可溶性表达;
(5)利用镍离子金属螯合亲和层析介质柱纯化该重组蛋白:离心收集大肠杆菌bl21/pet-43.1a-ifnc工程菌培养物中菌体,用冰预冷的pbs溶液洗涤三次,然后用buffera重悬菌体,置于冰水混合物中超声破碎15分钟,离心收集上清后上柱,4ºc结合30分钟,分别用预冷的bufferb和bufferc(洗柱,最后用bufferd洗脱,获得大黄鱼ifnc重组蛋白,纯化后的大黄鱼ifnc重组蛋白分别经buffer1、buffer2、buffer3进行3步透析,并最终透析至ph7.4的pbs缓冲液中。
所述buffera包括以下终浓度的试剂:20mmtris-hcl、150mmnacl、0.5%v/vtritonx-100和30mm咪唑,ph7.4;所述bufferb包括以下终浓度的试剂:20mmtris-hcl、150mmnacl、0.5%v/vtritonx-100、60mm咪唑,ph7.4;所述bufferc包括以下终浓度的试剂:20mmtris-hcl、150mmnacl、60mm咪唑,ph7.4;所述bufferd包括以下终浓度的试剂:20mmtris-hcl、500mmnacl、500mm咪唑,ph7.4;所述buffer1包括以下终浓度的试剂:20mmtris-hcl、150mmnacl、250mm咪唑,ph7.4;所述buffer2包括以下终浓度的试剂:20mmtris-hcl、150mmnacl、100mm咪唑,ph7.4;所述buffer3包括以下终浓度的试剂:20mmtris-hcl、150mmnacl,ph7.4。
本发明的优点在于:
本发明获得的大黄鱼ifnc基因的大肠杆菌表达产物为分子量约73kda的大黄鱼ifnc重组蛋白,该大黄鱼ifnc重组蛋白在终浓度为10ng/ml时,不仅在大黄鱼外周血细胞及头肾细胞中显著诱导自身及大黄鱼ifnd、ifnh的表达,还显著上调抗病毒基因mx1、pkr及isg15的表达。并且,该大黄鱼ifnc重组蛋白可明显地抑制石斑鱼虹彩病毒sgiv基因复制、抑制sgiv感染后的石斑鱼脾脏细胞的致病变效应,显示出良好的抗病毒效果,对于我国水产动物病毒病的防治具有广阔的应用价值和市场前景。
附图说明
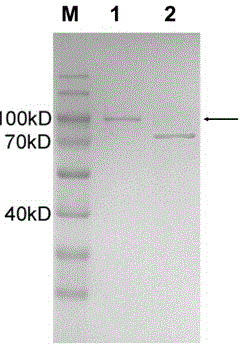
图1为纯化的大黄鱼ifnc重组蛋白的sds-page分析,其中m泳道为蛋白质分子量标准;1泳道为纯化的大黄鱼ifnc重组蛋白;箭头所指的是大黄鱼ifnc重组蛋白;2泳道是纯化的nus重组蛋白;kd(kilodalton)代表千道尔顿。
图2为大黄鱼ifnc重组蛋白对大黄鱼外周血白细胞中抗病毒蛋白基因表达的调节作用;10ng/ml的大黄鱼ifnc重组蛋白处理大黄鱼外周血白细胞2、4和8小时后,收集处理细胞并利用real-timepcr检测其中抗病毒蛋白mx1、pkr和isg15的基因表达水平,对照蛋白为10ng/ml的nus重组蛋白;上述基因的相对表达水平利用大黄鱼β-actin为内参标准化,其倍数变化为大黄鱼ifnc重组蛋白处理组中基因相对表达水平相对于nus重组蛋白处理组中基因相对表达水平的倍数。
图3为大黄鱼ifnc在石斑鱼脾脏细胞中抗石斑鱼虹彩病毒的功能;取10ng/ml的大黄鱼ifnc重组蛋白预处理石斑鱼脾脏细胞2小时后,接种石斑鱼虹彩病毒;感染后24小时,显微镜观察石斑鱼脾脏细胞的形态学变化;同时,于感染后12、24和48小时收集细胞培养物,并利用real-timepcr检测石斑鱼虹彩病毒基因mcp、vp19、vp136和icp18在石斑鱼脾脏细胞中的表达水平;对照蛋白为10ng/ml的nus重组蛋白;上述基因的相对表达水平利用石斑鱼β-actin为内参标准化,其倍数变化为大黄鱼ifnc重组蛋白处理组中基因相对表达水平相对于nus重组蛋白处理组中基因相对表达水平的倍数。每组实验重复三次,星号代表统计分析具有显著差异,*p<0.05,**p<0.01。
具体实施方式
实施例1一种大黄鱼ifnc基因cdna的获得
利用其他鱼类的ifnc序列及大黄鱼基因组(jrpu00000000),经过序列比对后预测得到大黄鱼ifnc基因序列。根据预测的大黄鱼ifnc基因编码序列设计引物,用该引物进行聚合酶链反应得到大黄鱼ifnc基因的编码区序列。该序列全长570个核苷酸,编码一个由189个氨基酸组成的蛋白质。
所述大黄鱼ifnc基因cdna及其推断的氨基酸序列seqidno.1所示;其中,编码的第1-27位氨基酸为预测的大黄鱼ifnc信号肽。
实施例2一种大黄鱼ifnc基因cdna的获得
1.含大黄鱼ifnc基因的重组表达载体bl21/pet-43.1a-ifnc的构建
(1)大黄鱼ifnc成熟肽基因片段的pcr扩增:合成带有限制性核酸内切酶ecori位点的正向引物ifnc-f:ggaattctgtcagctggaaggagatc和带有hindiii位点的反向引物ifnc-r:cccaagcttttagtggacacctctcc;使用takara公司的primestar®hsdnapolymerase按照说明书进行pcr扩增,pcr体系为:
pcr程序如下:
pcr扩增产物进行1.5%琼脂糖凝胶电泳,电泳条件:电压120伏,时间15分钟。使用凝胶成像仪观察,可见一条大小为570个核苷酸的条带,与预期相符,然后用omega公司胶回收试剂盒回收pcr扩增产物。
(2)酶切反应:回收的pcr扩增产物和大肠杆菌原核表达载体pet-43.1a分别进行限制性核酸内切酶ecori和hindiii双酶切,酶切反应体系:
酶切条件:37ºc反应3小时。酶切产物使用omega公司胶回收试剂盒进行回收。
(3)连接反应:使用takara公司t4dna连接酶连接双酶切后的pcr扩增产物和pet-43.1a载体,连接体系如下:
反应条件:16ºc反应4小时。
(4)连接产物转化invitrogen公司大肠杆菌e.colitop10感受态细胞,经菌落pcr筛选阳性克隆,扩大培养后,使用omega公司质粒小量提取试剂盒提取质粒,并测序验证,从而获得了含大黄鱼ifnc基因片段的重组表达载体pet-43.1a-ifnc。
2.大肠杆菌bl21/pet-43.1a-ifnc工程菌的构建
将含有大黄鱼ifnc基因片段的重组表达质粒pet-43.1a-ifnc转化大肠杆菌bl21感受态细胞,将转化后的菌液涂布于含100μg/ml氨苄青霉素的lb平板上,37ºc静置培养16小时,长出单菌落,得到含有大黄鱼ifnc基因的大肠杆菌bl21/pet-43.1a-ifnc工程菌。
培养基配方:
lb液体培养基:10g/l蛋白胨、5g/l酵母抽提物和10g/l氯化钠。
lb平板:10g/l蛋白胨、5g/l酵母抽提物、10g/l氯化钠和15g/l琼脂粉。
实施例3大黄鱼ifnc基因在大肠杆菌中表达及其表达产物纯化
1.大黄鱼ifnc重组蛋白的诱导表达及sds-page分析
将上述构建的大肠杆菌bl21/pet-43.1a-ifnc工程菌,挑取单菌落接种至5ml含100μg/ml氨苄青霉素的lb液体培养基中,37ºc,180转/分钟过夜振荡培养。第二天按体积比1:100比例接种于100ml含终浓度100μg/ml氨苄青霉素的lb液体培养基的中,37ºc,180转/分钟振荡培养。待培养物od600至0.4~0.5时,加入终浓度为0.1mm的iptg诱导蛋白表达,37℃继续振荡培养4小时,将培养物离心,收集菌体。
用10mlbuffera重悬收集的菌体,超声破碎10分钟,再将裂解液在4ºc,12000转/分钟,离心20分钟,收集裂解液上清,并用10mlbuffera重悬裂解液沉淀。菌体裂解液、菌体裂解液上清,菌体裂解液沉淀各取50μl,并加入等体积蛋白电泳上样缓冲液,沸水煮10分钟,然后进行浓度为15%(w/v)的sds-page电泳。结果显示,对照菌株bl21/pet-43.1a的菌体裂解液中出现了一条约73kda左右的蛋白条带,为空载体pet-43.1a所表达的重组蛋白nus。而在大肠杆菌bl21/pet-43.1a-ifnc工程菌的菌体裂解液中则出现了一条约100kda左右的蛋白条带,说明了大黄鱼ifnc重组蛋白在大肠杆菌中得到了表达。同时发现大黄鱼ifnc重组蛋白主要存在于菌体裂解液上清中中,说明大黄鱼ifnc重组蛋白在大肠杆菌bl21/pet-43.1a-ifnc工程菌中主要为可溶性表达。基于此,后续采用可溶性蛋白纯化方法对大黄鱼ifnc重组蛋白进行纯化。
buffera:20mmtris-hcl、150mmnacl、0.5%v/vtritonx-100和30mm咪唑,ph7.4
2.亲和层析法纯化大黄鱼ifnc重组蛋白
参照invitrogen公司镍离子金属螯合亲和层析介质(ni-nta)推荐的方法进行重组蛋白的纯化:首先4ºc,5000转/分钟离心10分钟收集100mliptg诱导后的大肠杆菌bl21/pet-43.1a-ifnc工程菌菌体,用l0mlbuffera重悬菌体,超声破碎15分钟,然后4ºc,12000转/分钟,离心l0分钟收集菌体裂解液上清。
先用lml镍离子金属螯合亲和层析介质装柱,用5倍柱体积双蒸水洗柱,再加入5倍柱体积buffera平衡层析柱,液体流净后,将上述步骤中收集的上清上柱,4ºc孵育30分钟。用10mlbufferb和bufferc洗柱,按照顺序分别洗5次,洗去未结合的杂蛋白。再用1mlbufferc洗脱目的蛋白,重复收集5次。同时,通过相同的方法纯化nus重组蛋白。
bufferb:20mmtris-hcl、150mmnacl、0.5%tritonx-100和60mm咪唑,ph7.4。
bufferc:20mmtris-hcl、150mmnacl和60mm咪唑,ph7.4。
bufferd:20mmtris-hcl、500mmnacl和500mm咪唑,ph7.4。
3.大黄鱼ifnc重组蛋白透析
纯化后的大黄鱼ifnc重组蛋白分别经buffer1、buffer2、buffer3进行3步透析,并最终透析至pbs(ph7.4)中,每步不低于4小时。透析后,4ºc,12000转/分钟离心30分钟去除沉淀,同时通过相同的方法透析nus重组蛋白。取少量进行sds-page电泳分析,结果显示得到了纯度较高的大黄鱼ifnc重组蛋白及nus重组蛋白(图1),剩余的保存于-70ºc备用。
buffer1:20mmtris-hcl、150mmnacl、250mm咪唑,ph7.4。
buffer2:20mmtris-hcl、150mmnacl、100mm咪唑,ph7.4。
buffer3:20mmtris-hcl、150mmnacl,ph7.4。
实施例4大黄鱼ifnc重组蛋白对大黄鱼抗病毒蛋白诱导活性分析
(1)将大黄鱼外周血白细胞以1×106个/ml的细胞密度接种于6孔细胞培养板,每孔2mlleibovitz'sl15培养基(gibico公司),于25ºc生化培养箱过夜培养。
(2)细胞培养基中加入大黄鱼ifnc重组蛋白至终浓度为10ng/ml,分别于处理后2、4和8小时收集细胞培养物,使用微量rna提取试剂盒(svtotalrnaisolationsystem,promega公司)提取细胞总rna,并按照逆转录酶m-mlv(rnaseh−,takara公司)说明书进行反转录pcr。同时,设置nus重组蛋白处理的细胞为阴性对照组。
(3)通过实时荧光定量pcr(real-timepcr)检测抗病毒蛋白基因如mx1、pkr和isg15在大黄鱼外周血白细胞中的表达水平。real-timepcr于mastercyclerepgradientrealplex4荧光定量pcr仪(eppendorf公司)进行反应,条件如下:95ºc预变性30s;95ºc变性5s,58ºc退火15s,72ºc延伸15s并获取荧光,40个循环。以β-actin作为内参基因。各基因引物如表1所示。实验结果采用2-δδct法进行分析。
结果显示,在大黄鱼ifnc重组蛋白处理后,大黄鱼抗病毒蛋白mx1、pkr和isg15的基因表达水平在大黄鱼外周血细胞中被显著上调,并于诱导后4小时达到高峰,分别为对照组的17.3倍,5.4倍和7.5倍(图2)。
表1实时荧光定量pcr各基因引物表
实施例5大黄鱼ifnc重组蛋白的抗病毒活性分析
(1)将石斑鱼脾脏细胞以1×106个/孔的细胞密度接种于6孔细胞培养板,每孔2mlleibovitz'sl15培养基(gibico公司),于28ºc生化培养箱培养18小时。
(2)细胞培养基中加入大黄鱼ifnc重组蛋白至终浓度为10ng/ml,静置孵育。2小时后,以感染复数为2的比例接种石斑鱼虹彩病毒。感染后24小时,显微镜观察石斑鱼脾脏细胞的细胞致病变效应。设置nus重组蛋白处理的细胞为阴性对照组。
(3)同时,于感染后12、24和48小时收集细胞培养物,使用微量rna提取试剂盒(svtotalrnaisolationsystem,promega公司)提取细胞总rna,并按照逆转录酶m-mlv(rnaseh−,takara公司)说明书进行反转录pcr。设置nus重组蛋白处理的细胞为阴性对照组。
(4)通过实时荧光定量pcr(real-timepcr)检测石斑鱼虹彩病毒基因mcp、vp19、vp136、和icp18在石斑鱼脾脏细胞中的表达水平。real-timepcr于mastercyclerepgradientrealplex4荧光定量pcr仪(eppendorf公司)进行反应,条件如下:95ºc预变性30s;95ºc变性5s,58ºc退火15s,72ºc延伸15s并获取荧光,40个循环。以石斑鱼β-actin作为内参基因。其倍数变化为大黄鱼ifnc重组蛋白处理组中基因相对表达水平相对于nus重组蛋白处理组中基因相对表达水平的倍数。每组实验重复三次,星号代表统计分析具有显著差异,*p<0.05,**p<0.01。各基因引物如表2所示。实验结果采用2-δδct法进行分析。
表2实时荧光定量pcr各基因引物表
显微镜观查结果显示,大黄鱼ifnc重组蛋白可保护接种石斑鱼虹彩病毒的石斑鱼脾脏细胞。表现为nus重组蛋白对照组大多数细胞已皱缩变圆,并出现明显地细胞空斑。而大黄鱼ifnc重组蛋白组细胞形态较为完整,无明显空斑(图3a)。real-timepcr结果显示在大黄鱼ifnc重组蛋白处理后,石斑鱼虹彩病毒基因mcp、vp19、vp136、和icp18的基因表达水平在石斑鱼脾脏细胞中被显著抑制(图3b)。表明大黄鱼ifnc重组蛋白具有明显的抗病毒功能。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
sequencelisting
<110>福建农林大学
<120>大黄鱼ifnc基因大肠杆菌表达产物的制备方法与应用
<130>21
<160>21
<170>patentinversion3.3
<210>1
<211>570
<212>dna
<213>人工序列
<400>1
atgacacttcagtcctcttcagtcctccttgtcctcttgcagttctacagcctcaagctg60
atggtggctgccatgccgacctgtcagctggaaggagatctggtccagtcggcccaccac120
ctgctcagagacctgggggcagattttcctgaacactgcctgccgtacaacgccaacatc180
tcctttccaagctctgccttccctgctgccacagccaatcatcctcagtgccacaaatca240
ttatgggtggtgcatgagtccctgcgggaggcggggctagtattccaggacaatgacata300
cctgtcggagagggcggagtcacctggaacgaccagaaactcgaagacttccagaacttg360
cagtaccgactggtggaggaagggagctgtctgtccagtgtcaatggttcaggtgttttg420
tcgtcttacttcagtaacgtgacggcagttcttcaagagcaggacagtgctgcctgtggc480
tggatggctctgaggagagatctgctctgggtcttaaagtctgccctgcagaaacaccgc540
acctgctttacctggagaggtgtccactaa570
<210>2
<211>26
<212>dna
<213>人工序列
<400>2
ggaattctgtcagctggaaggagatc26
<210>3
<211>26
<212>dna
<213>人工序列
<400>3
cccaagcttttagtggacacctctcc26
<210>4
<211>21
<212>dna
<213>人工序列
<400>4
tgttgcactagggcagaagag21
<210>5
<211>21
<212>dna
<213>人工序列
<400>5
gaagcagggagttcagcttct21
<210>6
<211>20
<212>dna
<213>人工序列
<400>6
gcacagaagataggctcggt20
<210>7
<211>20
<212>dna
<213>人工序列
<400>7
tgtctgacgaactggtgtgg20
<210>8
<211>20
<212>dna
<213>人工序列
<400>8
tgctggatggaaagacccac20
<210>9
<211>20
<212>dna
<213>人工序列
<400>9
atcagcagagagacccgaga20
<210>10
<211>21
<212>dna
<213>人工序列
<400>10
gacctgacagactacctcatg21
<210>11
<211>20
<212>dna
<213>人工序列
<400>11
ctccttcctgacctctccgt20
<210>12
<211>20
<212>dna
<213>人工序列
<400>12
gcacgcttctctcaccttca20
<210>13
<211>19
<212>dna
<213>人工序列
<400>13
aacggcaacgggagcacta19
<210>14
<211>20
<212>dna
<213>人工序列
<400>14
cttgatgacggaagcgtggt20
<210>15
<211>23
<212>dna
<213>人工序列
<400>15
tgtcagaggacttggagaaggag23
<210>16
<211>19
<212>dna
<213>人工序列
<400>16
gatgctgccgtgtgaactg19
<210>17
<211>20
<212>dna
<213>人工序列
<400>17
gcacatccttggtggtgttg20
<210>18
<211>19
<212>dna
<213>人工序列
<400>18
atcggatctacgtggttgg19
<210>19
<211>19
<212>dna
<213>人工序列
<400>19
ccgtcgtcggtgtctattc19
<210>20
<211>20
<212>dna
<213>人工序列
<400>20
tacgagctgcctgacggaca20
<210>21
<211>20
<212>dna
<213>人工序列
<400>21
ggctgtgatctccttctgca20
- 还没有人留言评论。精彩留言会获得点赞!