一种用于检测非洲猪瘟病毒野毒株和疫苗株的试剂盒的制作方法
1.本发明属于兽医领域,具体属于动物疾病诊断和病原检测领域,涉及一种用于检测非洲猪瘟病毒野毒株和疫苗株的试剂盒。
背景技术:
2.非洲猪瘟(african swine fever,asf)是由非洲猪瘟病毒(african swine fever virus,asfv)引起的一种猪急性、烈性、高度接触病毒性传染病。临床上典型病例表现为高热、皮肤发绀、心跳加快及内脏各器官广泛出血。该病发病过程短、传染性强、死亡率可达100%,目前无有效疫苗和药物。随着分子生物学技术的发展,不同的技术手段已被开发用于asfv的检测。
3.asf病原学诊断技术包括核酸检测、抗原检测和活病毒检测等。目前,asfv的检测技术主要有针对病毒dna的核酸检测技术和病毒抗原、抗体反应的免疫学技术两大类,通过研究世界卫生组织推荐asfv的检测方法主要有实时荧光定量pcr检测、pcr检测和elisa检测等。通过免疫学的知识进行抗体检测,通过检测我们可以了解到asfv的感染过程以及发生阶段,这样会使我们更好的进行治疗,但是这种方式的检测,抗体只有感染病毒到一定程度才会出现,这样会对治疗造成一定延误,所以elisa等其他抗体检测的方法存在一定的限制性。
4.目前实验室最常用的检测方法即为聚合酶链式反应(polymerase chain reaction,pcr)。根据其基因组高度保守区域设计特异性引物进行常规pcr扩增,因其具有良好的敏感性和特异性而成为最早期的快速诊断病毒感染方法。荧光定量pcr方法较常规pcr方法具有更高的特异性和敏感性。多重pcr可以用于对多种病原进行同时鉴定。
技术实现要素:
5.本发明的目的是提供一种用于检测非洲猪瘟病毒野毒株和疫苗株的试剂盒。
6.第一方面,本发明要求保护用于检测非洲猪瘟病毒野毒株和/或疫苗株的单链dna组。
7.本发明要求保护的用于检测非洲猪瘟病毒野毒株和/或疫苗株的单链dna组,可由如下组成:(a1)用于检测非洲猪瘟病毒的通用型引物对和对应探针,分别记为引物对1和探针1;所述引物对1为由seq id no.1和seq id no.2所示两条单链dna组成;所述探针1为seq id no.3所示单链dna。
8.(a2)用于检测非洲猪瘟病毒cd2v基因的引物对和对应探针,分别记为引物对2和探针2;所述引物对2为由seq id no.4和seq id no.5所示两条单链dna组成;所述探针2为seq id no.6所示单链dna。
9.(a3)用于检测非洲猪瘟病毒mgf360-505r基因的引物对和对应探针,分别记为引物对3和探针3;所述引物对3为由seq id no.7和seq id no.8所示两条单链dna组成;所述
探针3为seq id no.9所示单链dna。
10.其中,所述探针1、所述探针2和所述探针3的两端均分别标记有荧光报告基团和荧光淬灭基团,且所述探针1、所述探针2和所述探针3所标记的荧光报告基团均不同(即三个探针标记三种荧光报告基团)。
11.进一步地,所述探针1、所述探针2和所述探针3的5'端可以标记荧光报告基团,3'端可以标记荧光淬灭基团。
12.所述荧光报告基团可如fam、joe、tet、hex、vic、cy3、quasar 570、rox、txrd、cy5、quasar 670或cy5 .5等。所述荧光淬灭基团可如bhq-1、bhq-2、bhq-3或tamra等。
13.在本发明的具体实施方式中,所述探针1标记的荧光报告基团为fam;所述探针2标记的荧光报告基团为rox;所述探针3标记的荧光报告基团为cy5。所述探针1、所述探针2和所述探针3标记的荧光淬灭基团均为bhq-1。
14.进一步地,在所述单链dna组中,所述引物对1的上游引物、所述引物对1的下游引物、所述探针1、所述引物对2的上游引物、所述引物对2的下游引物、所述探针2、所述引物对3的上游引物、所述引物对3的下游引物、所述探针3的摩尔比为2:2:1:2:2:1:2:2:1。
15.第二方面,本发明要求保护一种用于检测非洲猪瘟病毒野毒株和/或疫苗株的pcr试剂。
16.本发明要求保护的用于检测非洲猪瘟病毒野毒株和/或疫苗株的pcr试剂,含有前文第一方面中所述单链dna组。
17.在所述pcr试剂中,所述引物对1的上游引物、所述引物对1的下游引物、所述引物对2的上游引物、所述引物对2的下游引物、所述引物对3的上游引物、所述引物对3的下游引物的终浓度均为0.4 pmol/μl;所述探针1、所述探针2和所述探针3的终浓度均为0.2 pmol/μl。
18.第三方面,本发明要求保护一种用于检测非洲猪瘟病毒野毒株和/或疫苗株的试剂盒。
19.本发明要求保护的用于检测非洲猪瘟病毒野毒株和/或疫苗株的试剂盒,可含有前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂。
20.根据需要,所述试剂盒还可含有阳性对照;所述阳性对照可选自如下任一:非洲猪瘟病毒或其dna、含有非洲猪瘟病毒p72、mgf360-505r、cd2v基因的质粒、含有非洲猪瘟病毒p72、mgf360-505r、cd2v基因片段的dna等。
21.所述试剂盒还可包括dna聚合酶和/或pcr反应缓冲液(含dntps和mg
2+
)。
22.所述试剂盒还可包括阴性对照,可为去离子水等。
23.在上述第一至第三方面中,所述疫苗株可为mgf360-505r和/或cd2v基因缺失株。
24.第四方面,本发明要求保护如下任一应用:p1、前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂或前文第三方面中所述试剂盒在鉴定或辅助鉴定非洲猪瘟病毒野毒株和/或疫苗株中的应用。
25.p2、前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂在制备用于鉴定或辅助鉴定非洲猪瘟病毒野毒株和/或疫苗株的产品中的应用。
26.p3、前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂或前文第三方面中所述试剂盒在检测或辅助检测待测非洲猪瘟病毒为野毒株还是疫苗株中的应用。
27.p4、前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂在制备用于检测或辅助检测待测非洲猪瘟病毒为野毒株还是疫苗株的产品中的应用。
28.p5、前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂或前文第三方面中所述试剂盒在检测或辅助检测待测病毒是否为非洲猪瘟病毒中的应用。
29.p6、前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂在制备用于检测或辅助检测待测病毒是否为非洲猪瘟病毒的产品中的应用。
30.p7、前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂或前文第三方面中所述试剂盒在检测或辅助检测待测样本中是否含有非洲猪瘟病毒中的应用。
31.p8、前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂在制备用于检测或辅助检测待测样本中是否含有非洲猪瘟病毒的产品中的应用。
32.其中,所述疫苗株可为mgf360-505r和/或cd2v基因缺失株。
33.所述待测样本可选自如下任一:离体全血、血清、血浆、淋巴结、脾脏、肾脏、扁桃体、肌肉、肉骨粉、血粉。
34.第五方面,本发明要求保护一种鉴定或辅助鉴定非洲猪瘟病毒野毒株和/或疫苗株的方法。所述方法为非疾病诊断性方法。
35.本发明要求保护的鉴定或辅助鉴定非洲猪瘟病毒野毒株和/或疫苗株的方法,可包括如下步骤:从待测样本中提取dna作为模板,用前文第一方面中所述单链dna组或前文第二方面中所述的pcr试剂或前文第三方面中所述试剂盒进行三重荧光定量pcr,然后根据各通道的ct值和扩增曲线按照如下进行结果判定:若所述探针1对应通道、所述探针2对应通道、所述探针3对应通道均满足阳性判定条件,则所述待测样品中含有非洲猪瘟病毒,且为或候选为野毒株。
36.若所述探针1对应通道满足阳性判定条件,且所述探针2对应通道和所述探针3对应通道均不满足阳性判定条件,则所述待测样品中含有非洲猪瘟病毒,且为或候选为cd2v与mgf360-505r基因联合缺失株。
37.若所述探针1对应通道和所述探针2对应通道均满足阳性判定条件,且所述探针3对应通道不满足阳性判定条件,则所述待测样品中含有非洲猪瘟病毒,且为或候选为mgf360-505r基因缺失株。
38.若所述探针1对应通道和所述探针3对应通道均满足阳性判定条件,且所述探针2对应通道不满足阳性判定条件,则所述待测样品中含有非洲猪瘟病毒,且为或候选为cd2v基因缺失株。
39.若所述探针1对应通道不满足阳性判定条件,则所述待测样本中不含有或候选不含有非洲猪瘟病毒。
40.所述探针1对应通道、所述探针2对应通道、所述探针3对应通道的所述阳性判定条件均为“ct值≤35”或者“35<ct值≤37且扩增曲线为s型”。
41.进行所述三重荧光定量pcr时,采用多荧光通道检测系统完成,所选择的荧光通过根据各探针所带荧光基团确定,可选择的荧光通道如fam,rox、fitc,hex,cy3,cy5,cy5 .5,cy7,rb200等。
42.在本发明的具体实施方式中,所述探针1选择的荧光通道为fam,所述探针2选择的荧光通道为rox,所述探针3选择的荧光通道为cy5。
1。
58.只要是非洲猪瘟病毒,利用该组引物探针就会有阳性扩增结果。
59.2、用于检测cd2v基因的引物和探针组根据非洲猪瘟病毒cd2v基因设计合成用于检测非洲猪瘟病毒是否缺失cd2v基因的引物和探针组,其引物cd2v-f、引物cd2v-r和探针cd2v-p的序列信息如下:引物cd2v-f:5 '-gagaaccattacttcctaagccttac-3 '(seq id no.4)。
60.引物cd2v-r:5 '-ggtggaggacacggtttaggt-3 '(seq id no.5)。
61.探针cd2v-p:5 '-tggttgtgttgagggacgcatgtag-3 '(seq id no.6)。
62.其中,探针cd2v-p的5'端标记有荧光报告基团rox,3'端标记有荧光淬灭基团bhq-1。
63.利用该组引物探针得到阳性扩增结果,则说明待测非洲猪瘟病毒携带cd2v基因;如果得到阴性扩增结果,则说明待测非洲猪瘟病毒缺失cd2v基因。
64.3、用于检测mgf360-505r基因的引物和探针组根据非洲猪瘟病毒mgf360-505r基因设计合成用于检测非洲猪瘟病毒检测是否缺失mgf360-505r基因的引物和探针组,其引物mgf-f、引物mgf-r和探针mgf-p的序列信息如下:引物mgf-f:5 '-ctgcagaggtcccgggtgtgc-3 '(seq id no.7)。
65.引物mgf-r:5 '-gggaaaacaactacaaccttataa-3 '(seq id no.8)。
66.探针mgf-p:5 '-ccgtagttgatgtccgccccc-3 '(seq id no.9)。
67.其中,探针mgf-p的5'端标记有荧光报告基团cy5,3'端标记有荧光淬灭基团bhq-1。
68.利用该组引物探针得到阳性扩增结果,则说明待测非洲猪瘟病毒携带mgf360-505r基因;如果得到阴性扩增结果,则说明待测非洲猪瘟病毒缺失mgf360-505r基因。
69.二、灵敏性试验1、模板制备阳性重组质粒:为在puc57质粒的ecor
ⅴ
位置插入seq id no.10所示dna片段后得到的重组质粒。seq id no.10中含有非洲猪瘟病毒p72基因、cd2v基因和mgf360-505r基因。
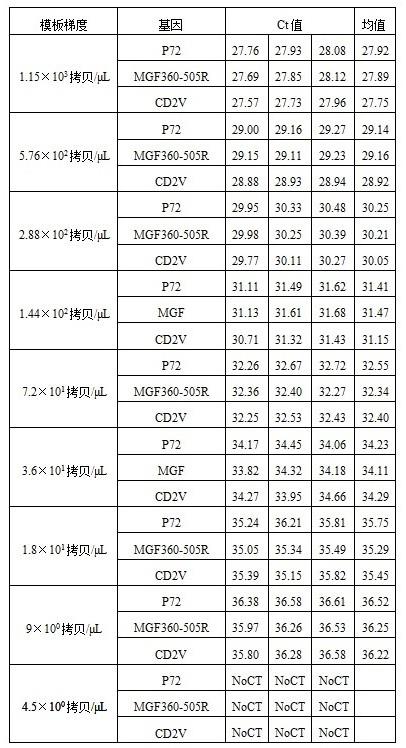
70.将测定浓度和纯度后的阳性重组质粒(阳性dna模板)分别进行2倍的倍比稀释,得到共9个稀释度(如图1)作为标准品模板,每个模板浓度设置3个平行样,对整个pcr体系的灵敏性进行评价。
71.2、三重荧光pcr检测配制反应液50μl,包括:上游引物、下游引物和探针共5μl,缓冲溶液(济凡生物科技(常州)有限公司的“genfq qpcr probe master mix(货号a106)”)35μl,阳性对照或待测样品的dna模板10μl。其中,三个引物对的上游引物和下游引物在反应体系中的终浓度均为0.4 pmol/μl;三个探针在反应体系中的终浓度均为0.2 pmol/μl。
72.使用abi q5 fast real-time pcr system(多荧光通道系统)进行荧光定量pcr检测。
73.反应程序:95℃预变性3min;95℃变性15s,60℃退火15s,45个循环。
74.3、结果
结果如图1。其中前7个稀释度各样品的ct值均≤35,结果均为阳性,而第8个稀释梯度(9个拷贝/μl)的ct值在35~37之间,同是具有典型的s型扩增曲线,第9个稀释梯度(4.5个拷贝/μl)无阳性扩增,因此,其敏感性试验结果为9个拷贝/μl。
75.三、重复性检测1、模板制备分别取7组不同稀释度(如图1前7个稀释度)质粒标准品(即步骤二中的阳性重组质粒),每份模板做8个重复试验,进行重复性试验。
76.2、荧光pcr检测同步骤二2。
77.3、结果如图2所示,可见测试结果重复性良好。
78.四、方法建立1、模板制备提取待测样本的核酸作为模板。
79.2、三重荧光pcr检测配制反应液50μl,包括:上游引物、下游引物和探针共5μl,缓冲溶液(济凡生物科技(常州)有限公司的“genfq qpcr probe master mix(货号a106)”)35μl,阳性对照或待测样品的dna模板10μl。其中,三个引物对的上游引物和下游引物在反应体系中的终浓度均为0.4 pmol/μl;三个探针在反应体系中的终浓度均为0.2 pmol/μl。
80.使用abi q5 fast real-time pcr system(多荧光通道系统)进行荧光定量pcr检测。反应程序:95℃预变性3min;95℃变性15s,60℃退火15s,45个循环。
81.根据各荧光通道的ct值和扩增曲线进行结果判定:若探针p72-p所带荧光报告基团对应通道(即fam通道)、探针cd2v-p所带荧光报告基团对应通道(即rox通道)、探针mgf-p所带荧光报告基团对应通道(即cy5通道)检测均满足阳性判定条件,则所述待测样品中含有非洲猪瘟病毒,且为野毒株。
82.若探针p72-p所带荧光报告基团对应通道(即fam通道)检测满足阳性判定条件,且探针cd2v-p所带荧光报告基团对应通道(即rox通道)和探针mgf-p所带荧光报告基团对应通道(即cy5通道)检测均不满足阳性判定条件,则所述待测样品中含有非洲猪瘟病毒,且为cd2v与mgf360-505r基因联合缺失株。
83.若探针p72-p所带荧光报告基团对应通道(即fam通道)和探针cd2v-p所带荧光报告基团对应通道(即rox通道)检测均满足阳性判定条件,且探针mgf-p所带荧光报告基团对应通道(即cy5通道)检测不满足阳性判定条件,则所述待测样品中含有非洲猪瘟病毒,且为mgf360-505r基因缺失株。
84.若探针p72-p所带荧光报告基团对应通道(即fam通道)和探针mgf-p所带荧光报告基团对应通道(即cy5通道)检测均满足阳性判定条件,且探针cd2v-p所带荧光报告基团对应通道(即rox通道)检测不满足阳性判定条件,则所述待测样品中含有非洲猪瘟病毒,且为cd2v基因缺失株。
85.若探针p72-p所带荧光报告基团对应通道(即fam通道)检测不满足阳性判定条件,则所述待测样本中不含有非洲猪瘟病毒。
86.三个探针对应通道检测的阳性判定条件均为“ct值≤35”或者“35<ct值≤37且扩增曲线为s型”。
87.五、临床样品检测1、样本处理提取核酸:8份临床样品,样品类型包括家猪脏器组织、口腔拭子、唾液、纱布等,经预处理后,用商品化的病毒核酸提取试剂盒,如济凡生物科技(常州)有限公司的“fine quick快速病毒dna/rna离心柱法提取试剂盒(货号fd501t5)”或者“finemag 快速磁珠法病毒dna/rna 提取试剂盒(货号fm502t5-tr系列,需配合自动化核酸提取纯化仪)”,进行核酸提取。
88.2、荧光pcr检测参照步骤四2进行。同时设置阴性对照(ntc),具体为以ddh2o作为模板。
89.针对8份临床样本,同时以现有的同样针对非洲猪瘟病毒的p72基因、cd2v基因和mgf360-505r基因的三重荧光定量商品化试剂盒作为阳性对照。
90.3、结果结果如图3所示,可见本发明试剂盒针对8个临床样本的检测结果与商品化试剂盒一致(所有样本的所有基因的ct值均≤35),同时还可以看出,本发明试剂盒的灵敏度比商品化试剂盒更高(本发明的ct值相对更小)。另外,从图3中还可以看出本发明试剂盒三个基因的重合性更好(本发明同一样本针对3个基因的ct值一致性更高)。
91.由以上实施例可知,本发明提供了一种引物探针组及其试剂盒,该试剂盒可以用于非洲猪瘟病毒野毒株和/或疫苗株的检测,6条引物及3条探针同时加入一个反应体系,不互相干扰。本发明的试剂盒对非洲猪瘟病毒野毒株和/或疫苗株的检测灵敏度高、特异性强、稳定性好,对非洲猪瘟病毒的最低检测限度为9拷贝/μl。
92.以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本技术欲包括任何变更、用途或对本发明的改进,包括脱离了本技术中已公开范围,而用本领域已知的常规技术进行的改变。按以下附带的权利要求的范围,可以进行一些基本特征的应用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1