一种沙格列汀中间体的制备方法与流程
1.本发明属于药物化学合成技术领域,涉及一种抗糖尿病药物中间体的制备方法,具体地说是一种沙格列汀中间体的制备方法。
背景技术:
2.沙格列汀(saxagliplin),又名安立泽,化学名为(1s,3s,5s)-2-[(2s)-2-氨基-2-(3-羟基金刚烷-1-基)乙酰基]-2-氮杂双环「3.1.0]己烷-3-腈,是由 bristol-myers squibb和astrazeneca公司共同开发的新型抗2型糖尿病药物,属二肽基肽酶iv(dpp-iv)抑制剂,2011年在中国上市。
[0003]
沙格列汀具有降糖作用明显、副作用小、患者顺应性好和安全性高等优点,应用开发前景较好,因此其重要中间体的合成工艺研究也引起了市场的广泛关注。化合物i为合成沙格列汀时的重要中间体,经氨基脱保护反应直接合成沙格列汀,其结构式如下所示:
[0004][0005]
合成化合物i时,主要涉及羟基金刚烷甘氨酸化合物的羧基与环丙基吡咯烷-2-甲酰基化合物的仲氨基形成酰胺键,但羧酸和有机胺不能直接生成酰胺,需要对羧酸进行活化或通过加入脱水剂促进反应的进行。目前国内外报道的中间体化合物i的制备方法,普遍存在制备步骤较长、成本高、环境污染严重、原子经济性不理想等缺点。
技术实现要素:
[0006]
本发明要解决的技术问题,是提供一种沙格列汀中间体的制备方法,目的在于降低沙格列汀中间体的制造成本,进一步降低沙格列汀原料药的生产成本,增强市场竞争力,以带来更大的社会效益。
[0007]
为了实现上述目的,本发明采用的技术方案是:
[0008]
一种沙格列汀中间体的制备方法,所述沙格列汀中间体为氨基保护的 (1s,3s,5s)-2-[(2s)-2-氨基-2-(3-羟基金刚烷-1-基)乙酰基]-2-氮杂双环「3.1.0]己烷
ꢀ‑
3-腈,其化学结构为化合物i,
[0009][0010]
其中,pg为氨基的保护基团;
[0011]
该制备方法包括依次进行的以下步骤:
[0012]
s1.羧酸羧基的活化反应
[0013]
将化合物ⅱ溶于非质子溶剂中,加入二碳酸二叔丁酯和4-二甲氨基吡啶 (dmap)进行羧基的活化反应,得到混合物a;
[0014]
s2.酰胺键的形成反应
[0015]
向混合物a中加入化合物ⅲ,进行酰胺键的形成反应,得到混合物b;
[0016]
s3.沙格列汀中间体的纯化
[0017]
将混合物b洗涤,加入干燥剂,抽滤,减压蒸馏,结晶和抽滤,最终得到目标产物化合物ⅰ,即为目标产物沙格列汀中间体;
[0018]
其中所述的化合物ⅱ为氨基保护的(s)-3-羟基金刚烷甘氨酸,其结构式为:
[0019][0020]
所述的化合物ⅲ为(1s,3s,5s)-2-氮杂双环[3.1.0]己烷-3-甲腈或其盐,其结构式为:
[0021][0022]
其中,pg为氨基的保护基团。
[0023]
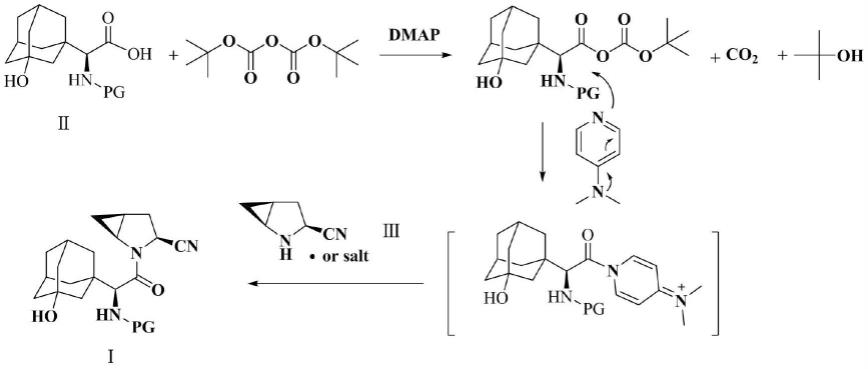
本发明反应过程如下:
[0024][0025]
二碳酸二叔丁酯是一种常用的氨基保护试剂,常用于氨基酸氨基保护中。 1995年第36卷第39期的杂志《tetrahydron letters》在7115-7118页刊登的论文《activation of carboxylic acids by pyrocarbonates.application of di-tert-butylpyrocarbonate as condensing reagent in the synthesis of amides of protected aminoacids and peptides》中,报道了二碳酸二叔丁酯能够将羧酸羧基活化从而将氨基保护的氨基酸或者肽转化为酰胺,但转化得到的酰胺的种类局限于氨基没有取代基的伯酰胺,即经活化的羧酸只能与氨或碳酸氢铵反应。将该论文中二碳酸二叔丁酯的该特性直接应用于沙格列汀酰胺键的形成过程,却并未获得相应的缩合产物。推测原因可能为,沙格列汀酰胺基中的氨基部分为仲胺结构,氮原子上有两个烷基取代基,位阻或电性原因导致反应不能进行。但是,本技术经过其他试剂的优化,将4-二甲氨基吡啶作为间接反应促进剂,获得了理想的结果,反应按照预期得到了氨基保护的沙格列汀中间体。
[0026]
作为对发明的第一种限定,所述制备方法中化合物ⅱ、二碳酸二叔丁酯、二甲氨基吡啶和化合物ⅲ的物质的量比为1:1~2:1~2:1~2。
[0027]
作为对发明的第二种限定,所述的氨基的保护基团为包括但不限于烷氧甲酰基保护基团、酰基保护基团或烷基保护基团。
[0028]
作为对发明的第二种限定的进一步限定,所述烷氧甲酰基保护基团包括叔丁氧甲酰基(boc)、苄氧甲酰基(cbz)或芴甲氧甲酰基(fmoc);
[0029]
所述酰基保护基团包括邻苯二甲酰基(pht)、对甲苯磺酰基(p-ts)或三氟乙酰基(tfa);
[0030]
所述烷基保护基团包括苄基(bn)或三苯甲基(trt)。
[0031]
作为对发明的第三种限定,所述步骤s1中,非质子溶剂为酯类、烃类、腈类或酮类中的至少一种。
[0032]
作为对发明的第三种限定的进一步限定,所述酯类包括乙酸甲酯、乙酸乙酯、乙酸丁酯;所述烃类包括二氯甲烷、1,2-二氯乙烷;所述腈类包括乙腈、丙腈;所述酮类包括丙酮。
[0033]
作为对发明的第四种限定,所述步骤s1和步骤s2在20~30℃下进行反应。
[0034]
作为对发明的第五种限定,所述步骤s3中干燥剂包括无水硫酸镁、无水硫酸钠、无水氯化钙中的至少一种。
[0035]
作为对发明的第五种限定的进一步限定,所述步骤s3中洗涤为依次用酸溶液、水、碱溶液、水和饱和食盐水洗涤;
[0036]
其中,酸溶液包括盐酸、硝酸、硫酸、磷酸中的至少一种,碱溶液包括氢氧化钠溶液、氢氧化钾溶液、碳酸钠、碳酸钾溶液中的至少一种;酸浓度为0.1~ 1mol/l,碱浓度为0.1~1mol/l。
[0037]
作为对发明的第五种限定的另一种限定,所述步骤s3中,所述减压蒸馏,压力为-0.94~-0.99mpa,温度为30~50℃。
[0038]
由于采用了上述技术方案,本发明与现有技术相比,所取得的技术进步在于:
[0039]
①
本发明提供的沙格列汀中间体的制备方法具有反应条件温和、原材料价廉易得、工艺简便、环境污染小、生产成本低、合成效率高等显著优点;
[0040]
②
本发明中二碳酸二叔丁酯和4-二甲氨基吡啶作为羧酸活化剂,活化化合物ⅱ的羧基,活化反应过程中生成的伴生产物为叔丁醇和二氧化碳等环境友好且易于处理的物质,符合绿色化学的理念;
[0041]
③
本发明提供的沙格列汀中间体的制备过程,涉及一种沙格列汀中间体酰胺键形成的新方法,化合物ⅱ经过羧酸羧基活化后可以直接和化合物ⅲ发生反应生成化合物ⅰ,可有效简化制备工艺,提高生产效率;另外该反应在室温条件下进行,不需加热或降温,能耗小。
[0042]
综上所述,本发明提供的沙格列汀中间体的制备方法,具有反应条件温和、原材料易得、工艺简便、环境污染小、生产成本低、生产效率高等显著优点,符合绿色化学理念。
[0043]
本发明提供的制备方法可用于制备沙格列汀中间体,制备的沙格列汀中间体也可进一步应用于生产沙格列汀。
1.65(m,12h),1.88-1.93(m,1h),2.11(m,3h),2.20(dd, 1h),2.51-2.53(m,1h),3.87(s,1h),4.34(d,1h),4.42(s,1h),5.14(d,1h),6.86(d, 1h).
[0063]
沙格列汀中间体化合物ⅰ(pg=boc)的核磁共振
13
c nmr谱图见图2,核磁谱图特征为:
13
c-nmr(125mhz,d6-dmso)13.97,17.82,28.67,30.19, 30.22,30.60,35.71,37.15,37.80,38.14,44.88,45.01,45.67,46.62,59.54,67.08, 78.77,120.61,156.21,169.95。
[0064]
实施例2-8沙格列汀中间体的制备方法
[0065]
实施例2-8分别为一种沙格列汀中间体的制备方法,它们的步骤与实施例 1基本相同,不同之处仅在于原料用量及工艺参数的不同,不同实施例原料种类及用量具体详见表2,不同制备步骤中各项工艺参数见表3。
[0066]
表2实施例2~8中原料用量表
[0067]
[0068][0069]
表3实施例2~8中不同制备步骤中工艺参数表
[0070][0071]
实施例2-8制得目标产物沙格列汀中间体化合物i相对于化合物ⅱ的收率汇总表见表4。
[0072]
表4目标产物收率汇总表
[0073][0074]
从实验结果可以看出,采用本方法可以方便地获得较高且稳定收率的目标产物沙格列汀中间体化合物i,同时该方法具有反应条件温和、原材料易得、工艺简便、环境污染小、生产成本低、生产效率高等显著优点,符合绿色化学理念。
[0075]
显然,本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无法对所有的实施方式予以穷举。凡是属于本发明的技术方案所引伸出的显而易见的变化或变动仍处于本发明的保护范围之列。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1