一种靶向HIF-1α的DNA纳米材料及其制备方法和应用
本发明属于生物医学,具体涉及一种靶向hif-1α的dna纳米材料及其制备方法和应用。
背景技术:
1、大多数生物体需要通过利用氧气进行细胞呼吸,以产生能量维持正常的生命活动。乏氧代表组织细胞的缺氧状况。高等动物主要依赖血管中的红细胞携带氧气,将氧气运输至组织细胞。肿瘤组织由于起内细胞生长快,细胞致密,消耗氧气快;远离血管的肿瘤细胞容往往处于乏氧的状态下。肿瘤细胞乏氧与肿瘤的恶性进展密切相关。乏氧能够促进肿瘤发生代谢重编程,血管新生和肿瘤远端转移。因此,靶向肿瘤细胞的乏氧状态长期以来被作为潜在的肿瘤治疗方案,受到研究者的重视。
2、乏氧情况能够激活乏氧信号通路。乏氧诱导因子(hypoxia induced factors,hifs)是乏氧信号通路的关键因子。hifs家族包括o2感受敏感的α亚基(hif-1α,、hif-2α和hif-3α)和o2感受不敏感的β亚基(hif-1β)。当细胞处于正常状态下时,α亚基被vhl介导的泛素-蛋白酶体途径所降解而处于失活状态;当细胞处于乏氧状态下时,α亚基将不再被降解而转运至细胞核内与β亚基结合形成异源复合体。此时,乏氧诱导因子能够作为转录因子结合dna调控下游靶基因的转录,调控血红蛋白生成、铁转运、糖代谢、血管生成和细胞生长分化等一系列生理过程。相较于肿瘤组织,正常组织往往处于正常的氧气供给状态,所以hifs的活性较低。而乏氧信号通路的活化与肿瘤的恶行进展密切相关,因此靶向hifs设计药物以抑制乏氧信号通路,能够在不影响正常组织的情况下抑制肿瘤的恶行进展,具有重要的意义。
3、目前,靶向乏氧现象以治疗肿瘤的研究已经取得了一系列进展。包括直接以hifs位靶点设计药物;针对hifs进行基因治疗;或是靶向乏氧信号调控的重要下游因子,例如mtor或者upr信号通路。一系列靶向hifs的小分子抑制剂被发现,能够以不同的机制抑制肿瘤乏氧信号的激活。benzopyranyl 1,2,3-triazole、bix01294、idf-11774等可以通过促进vhl对hif-1α的降解,以达到抑制乏氧信号通路活化的作用[6]。而cardenolides则可以通过抑制hifs的转录因子活性,以抑制乏氧信号通路活化。但是这些药物目前都存在特异性不强的问题,除hifs外仍可作用于其他靶点,例如hdacs。因此,开发更加特异靶向于hifs的药物仍然任重而道远。
4、近年来,随着纳米技术的兴起。靶向hifs的纳米药物的研发亦引起了相关研究者的关注[8]。不同形式的纳米材料与肿瘤乏氧现象相结合,被证明可应用于抑制肿瘤生长、增强放化疗敏感性和肿瘤免疫治疗。有研究者研发了一系列纳米材料通过与血红蛋白结合,携带氧气到达乏氧靶细胞,以抑制hifs的活化。亦有研究者将不同形式的纳米材料作为hifs抑制的载体,将二者结合,应用于抗肿瘤治疗。例如,脂质纳米胶囊被作为hifs抑制剂acridine的载体,应用于抗肿瘤治疗。脂质纳米胶囊可以保护acridine不被快速降解,延长药物起效时间[14]。纳米材料亦可作为hifs的sirna载体,将靶向hifs的sirna运送至乏氧肿瘤细胞,抑制hifs的表达。但是目前利用纳米材料设计直接靶向hifs的纳米药物的研究尚不足。
5、dna纳米材料作为一种具有良好自组装特性的天然材料,因具有编码性强、方便合成、易于修饰、高稳定性和结构多样性等优点,在生物传感、生物成像、药物传递及细胞调控等领域发挥着不可或缺的作用。dna纳米材料可通过改变dna碱基序列进行个性化设计,精确控制纳米材料大小、形状与功能,其合成成本相对低廉,并且生物相容性良好。dna纳米材料已经被证明可作为抗肿瘤药物的生物载体应用于抗肿瘤药物在细胞内发挥作用。由于dna纳米材料具有良好的生物相容性,但是dna纳米材料是否可直接作为纳米药物靶向相应的抗肿瘤靶点,目前尚无相关报道。且将dna纳米材料应用到靶向hifs以实现抗肿瘤作用的研究中,亦尚未有相应报道。
技术实现思路
1、本发明目的在于克服现有技术缺陷,提供一种靶向hif-1α的dna纳米材料。
2、本发明的另一目的在于提供上述dna纳米材料的制备方法。
3、本发明的再一目的在于提供上述dna纳米材料的应用。
4、本发明的技术方案如下:
5、一种靶向hif-1α的dna纳米材料,其由正四面体dna纳米材料和一互补单链dna组成,
6、该正四面体dna纳米材料由ta、tb、tc和td四条单链dna等摩尔自组装而成,其核苷酸序列依次如seq id no.01至04所示,且该正四面体dna纳米材料的四个端点均具有一悬臂单链dna,每一悬臂单链dna上均具有多重的特异结合hif-1α的核苷酸序列;
7、该互补单链dna与上述悬臂单链dna互补配对。
8、在本发明的一个优选实施方案中,所述互补单链dna的核苷酸序列如seq idno.05所示。
9、进一步优选的,所述特异结合hif-1α的核苷酸序列如seq id no.06所示。
10、上述dna纳米材料的制备方法,包括如下步骤:将等摩尔浓度的ta、tb、tc和td以及所述互补单链dna在ph为8.0的1×te-mg缓冲液中进行充分混合,再置于95℃下孵育5min,最后快速冷却至室温即可一步自组装合成所述正四面体dna纳米材料。
11、在本发明的一个优选实施方案中,所述ta、tb、tc和td在所述1×te-mg缓冲液中的浓度均为10um。
12、进一步优选的,所述互补单链dna在1×te-mg缓冲液中的浓度为40um。
13、在本发明的一个优选实施方案中,所述1×te-mg缓冲液的配方为:终浓度10mm的tris.hcl,1mm的edta和10mm的mgcl2。
14、上述dna纳米材料在制备抗肿瘤药物中的应用。
15、一种抗肿瘤药物组合物,其有效成分包括上述dna纳米材料。
16、在本发明的一个优选实施方案中,其有效成分为上述的dna纳米材料。
17、本发明的有益效果是:
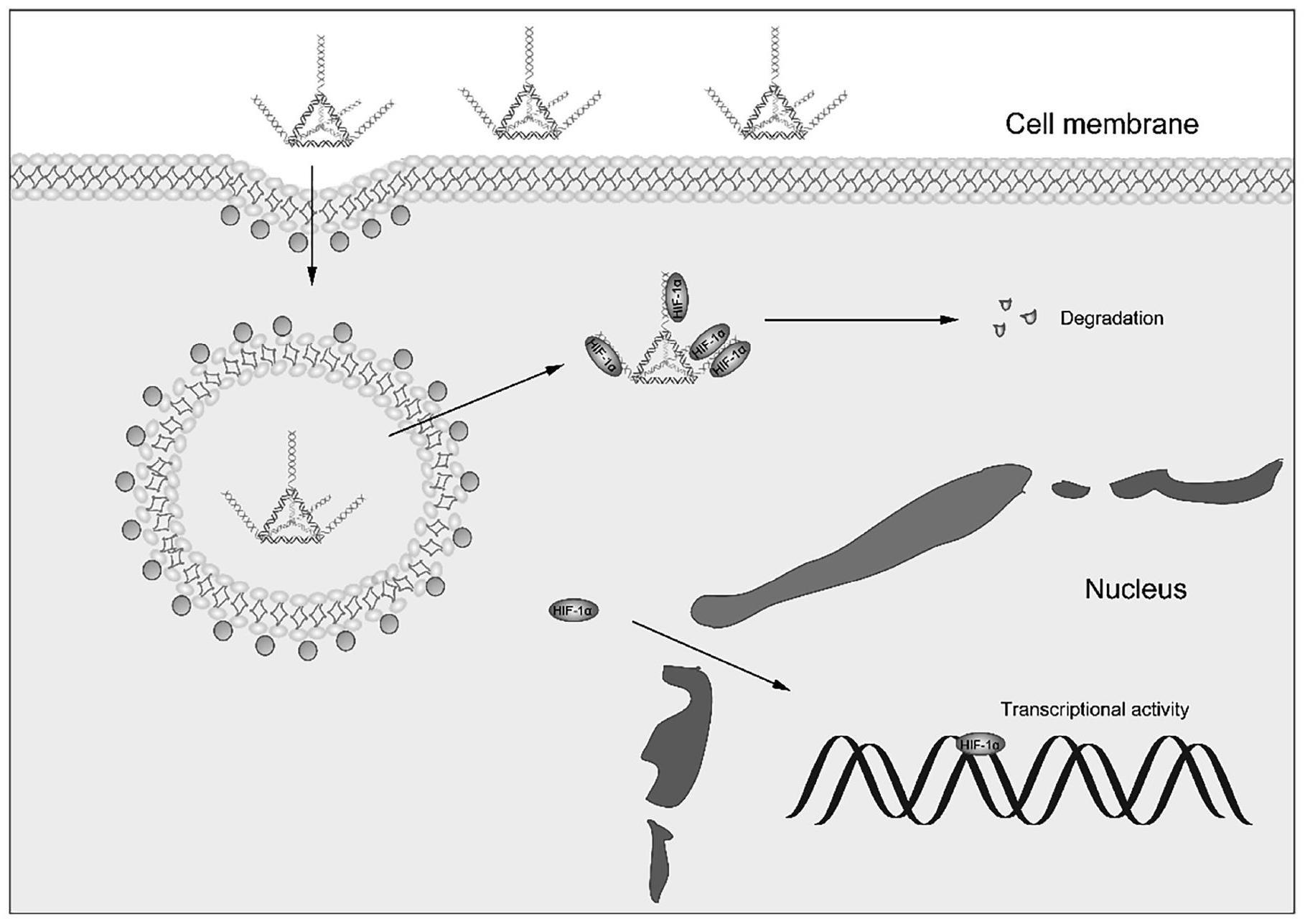
18、本发明基于转录因子hif-1α可以和特定的dna序列ncgtgn特异性结合,设计一种新型的、合成简便且通用的dna纳米材料以靶向hif-1α,实现抗肿瘤治疗的作用。其具体作用原理如图1所示,本发明的dna纳米材料可通过细胞内吞的方式进入肿瘤细胞,其向外延申的四条悬臂单链dna,包含多重的hif-1α的特异性结合dna序列,hif-1α可通过结合dna纳米材料的任意一条悬臂单链dna而被劫持而被困于细胞质中,进而导致其无法转运至细胞核中发挥转录因子活性以调控下游靶基因的表达,并最终被降解;由于hif-1α在乏氧状态的肿瘤细胞中调控了重要靶基因的表达,以维持肿瘤细胞的生长和转移,所以该dna纳米材料可通过劫持hif-1α实现抑制肿瘤细胞生长和转移的抗肿瘤效应。
技术特征:
1.一种靶向hif-1α的dna纳米材料,其特征在于:其由正四面体dna纳米材料和一互补单链dna组成,
2.如权利要求1所述的dna纳米材料,其特征在于:所述互补单链dna的核苷酸序列如seq id no.05所示。
3.如权利要求2所述的dna纳米材料,其特征在于:所述特异结合hif-1α的核苷酸序列如seq id no.06所示。
4.权利要求1至3中任一权利要求所述的dna纳米材料的制备方法,其特征在于:包括如下步骤:将等摩尔浓度的ta、tb、tc和td以及所述互补单链dna在ph为8.0的1×te-mg缓冲液中进行充分混合,再置于95℃下孵育5min,最后快速冷却至室温即可一步自组装合成所述正四面体dna纳米材料。
5.如权利要求4所述的制备方法,其特征在于:所述ta、tb、tc和td在所述1×te-mg缓冲液中的浓度均为10um。
6.如权利要求5所述的制备方法,其特征在于:所述互补单链dna在1×te-mg缓冲液中的浓度为40um。
7.如权利要求4至6中任一权利要求所述的制备方法,其特征在于:所述1×te-mg缓冲液的配方为:终浓度10mm的tris.hcl,1mm的edta和10mm的mgcl2。
8.权利要求1至3中任一权利要求所述的dna纳米材料在制备抗肿瘤药物中的应用。
9.一种抗肿瘤药物组合物,其特征在于:其有效成分包括:权利要求1至3中任一权利要求所述的dna纳米材料。
10.如权利要求9所述的一种抗肿瘤药物组合物,其特征在于:其有效成分为权利要求1至3中任一权利要求所述的dna纳米材料。
技术总结
本发明公开了一种靶向HIF‑1α的DNA纳米材料及其制备方法和应用,其由正四面体DNA纳米材料和一互补单链DNA组成;该正四面体DNA纳米材料由TA、TB、TC和TD四条单链DNA等摩尔自组装而成,其核苷酸序列依次如SEQ ID NO.01至04所示,且该正四面体DNA纳米材料的四个端点均具有一悬臂单链DNA,每一悬臂单链DNA上均具有多重的特异结合HIF‑1α的核苷酸序列;该互补单链DNA与上述悬臂单链DNA互补配对。本发明可通过劫持HIF‑1α实现抑制肿瘤细胞生长和转移的抗肿瘤效应。
技术研发人员:黄菲,张莹
受保护的技术使用者:福建医科大学附属第一医院
技术研发日:
技术公布日:2024/1/13
- 还没有人留言评论。精彩留言会获得点赞!