取代的稠合双环类化合物作为PARP抑制剂及其应用的制作方法
本发明属于药物化学领域。本发明涉及取代的稠合双环类化合物及其作为治疗上有效的parp抑制剂和抗癌药物的应用。
背景技术:
1、poly(adp-ribose)polymerase(parp)是指一组蛋白,它们的功能是以nad+为底物催化向受体蛋白添加adp-ribose的修饰反应。这是蛋白质转译后修饰的多种方式中的一种。因此它们也可被称为是adp-ribose转移酶。
2、根据蛋白的催化区域的氨基酸序列的相似性,在人类细胞中已发现有17种不同的parp酶(vyas et al.,2013nature communication,doi:10.1038)。这些parp酶或者催化对受体蛋白的单一adp-ribose修饰,或者催化对受体蛋白进行多个adp-ribose转移形成多聚adp-ribose,也称poly(adp-ribose)修饰。parp的家族成员可以根据催化转移的adp-ribose是单一还是多个而分为两大亚型。parp酶对受体蛋白进行的adp-ribose修饰所导致的生物学功能涵盖非常广泛,许多功能也还不清楚。
3、parp1是parp大家族中细胞内含量最高、被研究的最多的一个。parp1是一个有1014个氨基酸组成的蛋白(ncbi accession p09874),分子量大约为116kda,其结构包括dna结合和催化等区域。目前所知parp1参与细胞多项功能,在基因扩展、转录、细胞分裂、细胞分化、细胞凋亡以及dna损伤应答及修复等机制中都起着重要作用。当dna损伤发生时,parp1被激活。碱基切除(ber,base excision repair)机制是dna单链损伤修复的一个主要机制,parp1是ber机制的一个重要组成部分。当损伤发生时,parp1结合到dna单链损伤(ssb,single strand break)部位,通过参与ber对dna进行修复。其活性主要体现在对组蛋白、核蛋白的adp-ribose修饰及对自身的adp-ribose修饰。细胞应对dna损伤除了单链损伤ber修复机制外还有修复双链损伤的同源重组(hr,homologous recombination)和非同源重组末端连接(nhej,non-homologous recombination end joining)两个重要的修复机制。结果显示具有同源重组修复机制缺陷的癌细胞对parp1抑制剂敏感,即同源重组缺陷和parp1抑制形成合成致死(synthetic lethality)的一对。这个发现在临床上得到验证,多个parp抑制剂得以获得批准上市用于治疗具有brca1/2突变的卵巢癌、乳腺癌、前列腺癌和胰腺癌等。
4、parp2是一个有559个氨基酸组成的蛋白,分子量大约为62kda,其结构包括dna结合和催化等区域(ame et al.,1999j biol chem 274:17860)。parp2的催化区域和parp1的有极高的相似性。研究显示parp2有和parp1相似的功能,参与ber机制对dna损伤的修复(schreiber et al.,2002j biol chem 277:23028)。目前已上市的parp抑制剂,包括olaparib、niraparib、talazoparib和rucaparib等,除了抑制parp1外都对parp2有相似的抑制活性。从临床试验结果看,这些已上市的parp抑制剂有着类似的药效,然而它们的毒性却有着较大的区别。比如,这些parp抑制剂的血液学毒性相似,但是talazoparib却有着和化疗药类似的脱发的副作用。最近一项比较多个parp抑制剂选择性的研究显示talazoparib除了抑制parp1和parp2外,还对parp家族的另外两个成员tnks1(tankyrase1)和tnks2(tankyrase 2)有相当高的亲和力(ryan et al.,2021,j biol chem 296:100251)。tnks1和tnks2氨基酸序列有很高的相似性,二者的整体序列中氨基酸序列83%相同,而催化区域的相同性达89%。tnks除了也在dna修复中有一定的作用外,它们还在维持端粒结构以及wnt/β-catenin信号通路中有一定的作用。打中除parp1之外的这些靶点有可能是引起机制外毒性,比如脱发和腹泻等的原因。另外,抑制parp2活性也可能导致血液毒性(farrés et al.,2013,blood122:44;farrés et al.,2015,cell death anddifferentiation 22:1144)。这些毒性有可能限制了parp抑制剂的应用,以及和其他靶向药物的联合使用。
5、因此,开发具有高度选择性的parp1抑制剂可能降低与机制相关和机制不相关的毒性,改善、增强和扩大parp1抑制剂的临床应用。
6、已有多种选择性parp1抑制剂被公开。如wo2011006803;wo2013014038;wo2021013735和wo2021260092。
技术实现思路
1、本发明提供结构如式i(包括式ii、iii和iv)所示的化合物,这类化合物可作为parp抑制剂。特别的,相对于parp2,本发明的化合物是选择性parp1抑制剂。
2、本发明还提供了包含有效量的式i(包括式ii、iii和iv)化合物的药用组合物,用来治疗癌症。
3、在一具体实施例中,所述药用组合物还可含有一种或多种可药用载体或稀释剂,用来治疗癌症。
4、在一具体实施例中,所述药用组合物还可含有至少一种已知的抗癌药物或所述抗癌药物的可药用盐,用来治疗癌症。
5、本发明也涉及到结构式i(包括式ii、iii和iv)的新颖化合物的制备方法。
技术特征:
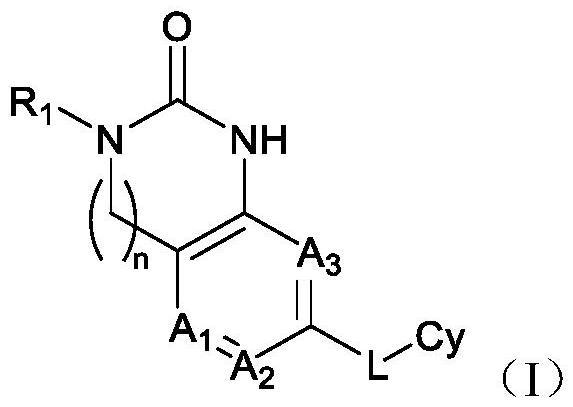
1.下式i所示的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物:
2.如权利要求1所述的式i的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药;其中,r1为任选被1–5个选自卤素、羟基和-nr'r”的取代基取代的c1-3烷基或c3-6环烷基,其中,r′和r″优选各自独立为h、任选被1–5个选自羟基和卤素的取代基取代的c1-4烷基或c3-6环烷基;优选地,r1为c1-3烷基、卤代c1-3烷基或c3-4环烷基。
3.如权利要求1所述的式i的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药,其中,r3和r4优选各自独立为卤素或c1-3烷基;l为键或未被取代的亚烷基,优选为未被取代的c1-3亚烷基,更优选为亚甲基。
4.如权利要求1所述的式i的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药,其中,r2为氢、卤素、任选被1-5个选自卤素和羟基的取代基取代的c1-3烷基或c1-3烷氧基,优选的r2为氢、c1-3烷基或卤素。
5.如权利要求1所述的式i的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药;其中,
6.如权利要求1所述的式i的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药,其中,cy可能被1-5个取代基取代,选自:卤素、c1-4烷基、c1-4烷氧基、卤代c1-4烷基、卤代c1-4烷氧基、任选取代的6-14元芳基、任选取代的5-10元杂芳基、任选取代的4-10元杂环基、任选取代的c3-8环烷基和-(ch2)m-c(o)-nrarb的取代基;
7.如权利要求1所述的式i的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药;其中,cy被r5取代,r5优选为如下基团:
8.如权利要求1所述的式i的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药,其特征在于,所述式i化合物具有下式iia和iib所示结构:
9.如权利要求8所述的式i的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药,其中,
10.如权利要求1所述的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药,其特征在于,所述式i化合物具有下式iiia或iiib所示的结构:
11.如权利要求1所述的化合物,或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物,或其前药,其特征在于,所述式i化合物具有下式iva或ivb所示的结构:
12.如权利要求1的化合物,其特征在于,所述化合物选自:
13.权利要求1~12中任一项所述的化合物、或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物在制备治疗或预防因parp活性异常而引起的疾病或病症的药物中的用途;优选地,所述疾病或病症是癌症;其特征在于,所述癌症是肝癌、黑素瘤、霍奇金病、非霍奇金淋巴瘤、急性淋巴白血病、慢性淋巴白血病、多发性骨髓瘤、成神经细胞瘤、乳腺癌、卵巢癌、维尔姆斯瘤、子宫颈癌、睾丸癌、软组织肉瘤、原发性巨球蛋白血症、膀胱癌、慢性粒细胞白血病、原发性脑癌、恶性黑素瘤、非小细胞肺癌、小细胞肺癌、胃癌、结肠癌、恶性胰腺胰岛瘤、恶性类癌性癌症、绒毛膜癌、蕈樣肉芽腫、头颈癌、骨原性肉瘤、胰腺癌、急性粒细胞白血病、毛细胞白血病、横纹肌肉瘤、卡波西肉瘤、泌尿生殖系统肿瘤病、甲状腺癌、食管癌、恶性高钙血症、子宫颈增生症、肾细胞癌、子宫内膜癌、真性红细胞增多症、特发性血小板增多症、肾上腺皮质癌、皮肤癌和前列腺癌;
14.一种药用组合物,包括权利要求1~12中任一项所述的化合物、或其立体异构体、互变异构体、n-氧化物、水合物、溶剂化物、同位素标记化合物或可药用盐,或其混合物与可药用载体。
15.如权利要求14所述的药用组合物,其特征在于,所述药用组合物还含有至少一种已知的抗癌药物,或所述抗癌药物的可药用盐;优选地,所述至少一种已知的抗癌药物选自下组:伏立诺他、罗咪地辛、帕比司他、贝利司他、帕博西尼、白消安、马法兰、苯丁酸氮芥、环磷酰胺、异环磷酰胺、替莫唑胺、苯达莫司汀、顺铂、丝裂霉素c、博莱霉素、卡铂、喜树碱、伊立替康、托泊替康、阿霉素、表阿霉素、阿克拉霉素、米托蒽醌、甲基羟基玫瑰树碱、铭托泊普、5-氮杂胞苷、吉西他滨、5-氟尿嘧啶、甲氨蝶呤、5-氟-2'-去氧尿苷、氟达拉滨、奈拉滨、阿糖胞苷、普拉曲沙、培美曲塞、羟基脲、硫代鸟嘌呤、秋水仙碱、长春碱、长春新碱、长春瑞滨、紫杉醇、伊沙匹隆、卡巴他赛、多西他赛、单抗、帕尼单抗、耐措妥珠单抗、纳武单抗、派姆单抗、雷莫芦单抗、贝伐珠单抗、帕妥珠单抗、曲妥珠单抗、西妥昔单抗、奥滨尤妥珠单抗、奥法木单抗、利妥昔单抗、阿仑单抗、替伊莫单抗、托西莫单抗、本妥昔单抗、达雷木单抗、埃罗妥珠单抗、t-dm1、ofatumumab、dinutuximab、blinatumomab、易普利姆玛、阿瓦斯丁、赫赛汀、美罗华、伊马替尼、吉非替尼、厄洛替尼、奥斯替尼、阿法替尼、赛立替尼、艾乐替尼、克唑替尼、埃罗替尼、拉帕替尼、索拉非尼、瑞格非尼、维罗非尼、达拉非尼、阿柏西普、舒尼替尼、尼罗替尼、达沙替尼、博舒替尼、普拉替尼、依鲁替尼、卡博替尼、乐伐替尼、凡德他尼、曲美替尼、卡比替尼、阿昔替尼、替西罗莫司、idelalisib、帕唑帕尼、特癌适、依维莫司、伏立诺他、罗咪地辛、帕比司他、贝利司他、他莫昔芬、来曲唑、氟维司群、米托胍腙、奥曲肽、视黄酸、砒霜、唑来膦酸、硼替佐米、卡非佐米、ixazomib、维莫德吉、索尼德吉、狄诺塞麦、萨力多胺、来那度胺、venetoclax、aldesleukin(重组人白介素-2)和sipueucel-t(前列腺癌治疗疫苗)。
技术总结
本发明提供取代的稠合双环类化合物作为PARP抑制剂及其应用。本发明的取代的稠合双环类化合物具有下式I所示的结构,其中,A1、A2、A3、R1、L、Cy和n为本文所定义。本发明式I的化合物是PARP抑制剂,因而可用于治疗因PARP活性异常而引起的疾病、障碍和病症,如癌症。本发明也涉及含有式I化合物的药物组合物以及该式I化合物在制备治疗或预防因PARP活性异常而引起的疾病或病症的药物中的用途。
技术研发人员:蔡遂雄,田野,王晓珠
受保护的技术使用者:上海瑛派药业有限公司
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!