嵌合抗原受体的CD28/CD40共刺激结构域
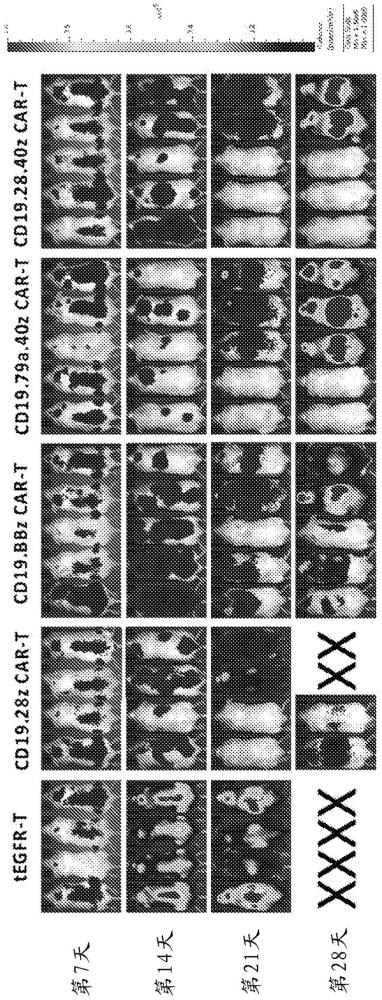
本发明涉及用于治疗白血病和淋巴瘤的嵌合抗原受体的创新共刺激结构域。干预的背景嵌合抗原受体t-细胞(car-t)是一种与施用基因修饰宿主免疫细胞以根除癌症有关的过继细胞治疗(act)。当前,基因修饰以表达抗-cd19(一种泛-b-细胞(pan-b-cell)抗原)的car-t细胞在b-细胞恶性肿瘤中表现出有希望的结果,尤其在复发的/难治性急性b-细胞成淋巴细胞性白血病/淋巴瘤(b-all)患者中,报道了70-93%的完全缓解率(completeresponse rate)。另一方面,car-t细胞在b-细胞非霍奇金淋巴瘤(b-nhl)中的功效不太大,完全缓解率为约20-70%。car的结构主要由单链抗体可变区片段(scfv)细胞外结构域、铰链、跨膜结构域(tm)和共刺激结构域组成。第一代car仅由cd3ζ细胞内结构域组成,其在有限的car-t细胞持久性的情况下在临床试验中显示出令人失望的结果。因此,第二代和第三代cars被开发出来,以通过并入一种或多种共刺激分子来改善car-t细胞功能。最近,并入了cd28或4-1bb共刺激结构域的car-t细胞被广泛用于治疗复发的/难治性b-all和b-nhl患者。尽管初始缓解率(initial response rates)高,但由于差的car-t细胞增殖以及car-t细胞在体内的长期持续存在,仍在显著数目的患者中出现复发。因此,需要创新的car的共刺激分子以使t-细胞持久性和强烈的杀肿瘤作用两者达到最大,以增强抗肿瘤功能和存活结果。公开内容概述本公开内容是嵌合抗原受体的cd28/cd40共刺激结构域。合成方法包括,在所述方法中通过重叠聚合酶链反应(重叠pcr)的dna合成,获得了3个dna片段:hindiii-cd19scfv-28tm-cd28-cd40、cd28-cd40-cd3z和cd40-cd3z-tegfr-noti。dna装配cd19.28.40z组合每个构建的第一、第二和第三dna片段以获得纯cd19.28.40z car基因。cd19.28.40z car基因连接到质粒或载体dna中,然后cd19.28.40z car质粒基因转化至大肠杆菌(escherichiacoli)感受态细胞中。进行dna测序检查。所述步骤获得了cd19.28.40zcar基因级的质粒。
背景技术:
技术实现思路
技术特征:
1.嵌合抗原受体的cd28/cd40共刺激结构域,其包含:
2.根据权利要求1所述的嵌合抗原受体的cd28/cd40共刺激结构域,其中合成方法包括:
3.根据权利要求1或2所述的嵌合抗原受体的cd28/cd40共刺激结构域,其包含t-细胞和b-细胞信号传导受体。
技术总结
本公开内容是嵌合抗原受体的CD28/CD40共刺激结构域。合成方法包括,在所述方法中通过重叠聚合酶链反应(重叠PCR)的DNA合成,获得了3个DNA片段:HindIII‑CD19scFV‑28TM‑CD28‑CD40、CD28‑CD40‑CD3z和CD40‑CD3z‑tEGFR‑NotI。DNA装配CD19.28.40z组合每个构建的第一、第二和第三DNA片段以获得纯CD19.28.40z CAR基因。CD19.28.40z CAR基因连接到质粒或载体DNA中,然后CD19.28.40z CAR质粒基因转化至大肠杆菌(Escherichia coli)感受态细胞中。进行DNA测序检查。所述步骤获得了CD19.28.40z CAR基因级的质粒。
技术研发人员:J·尤拉马尼,S·特拉库拉,P·威邦俊特拉,N·蒋帕塔那暖特,W·科潘勒特
受保护的技术使用者:宋卡王子大学
技术研发日:
技术公布日:2024/2/19
- 还没有人留言评论。精彩留言会获得点赞!