含哌啶修饰的多肽的合成方法与流程
本发明涉及多肽化学合成,具体而言,涉及一种含哌啶修饰的多肽的合成方法。
背景技术:
1、固相合成多肽中,常涉及到多肽的氨基酸残基修饰哌啶,如glu(γ-pip)、asp(γ-pip)。此修饰氨基酸需要单独合成或另外修饰,耗时长、步骤繁琐。比如多肽suc-iie-glu(γ-pip)-gly-arg-pna·hcl的合成,该多肽是一种人工合成可以被活性x因子催化水解的多肽化合物,其简称为s-2732,常作为发色底物。该底物可用于凝血因子xa和肝素抗xa活性的定量检测,因此其在科研和临床上都有着广泛的用途。
2、除了中国专利申请(申请公布号cn107474108a,申请公布日2017.12.15)报道了s-2732的合成方法,目前较少发现该多肽合成方法的报道。根据现有的报道可以发现该多肽的合成有两个关键点:第一点,发色基团对硝基苯胺连接到氨基酸上是s-2732合成的关键点之一。这是因为对硝基苯胺上的硝基具有强吸电子作用,导致对硝基苯胺的亲和性非常差,通过一般的酰胺缩合方法,产物收率低。为了解决这一难题,有研究采用液相的方法,采用三氯氧磷作为缩合试剂,将对硝基苯胺高效率连接到氨基酸上。但是方法有着自身的缺陷,如对硝基苯胺、三氯氧膦对人体或环境具有重大的安全隐患;也有研究者采用高浓度的双氧水及三氟乙酸酐进行加热氧化,但该方法危险系数高。第二点,glu(γ-pip)采用液相合成。如fmoc-glu-otbu与哌啶(pip)反应,形成fmoc-glu(pip)-otbu后,再进行脱fmoc与otbu,并进行纯化,操作过程繁琐复杂。
3、修饰pip的常规方法是使用fmoc-glu(oall)-oh原料合成该多肽,即先合成suc-iie-glu(γ-oall)-gly-arg(pbf)-ppda-树脂,再使用钯碳脱除oall,再与pip形成suc-iie-glu(γ-pip)-gly-arg(pbf)-ppda-树脂。此方法使用的钯碳是一种重金属且价格贵,使用过程中污染环境。或使用fmoc-glu(odmab)-oh原料合成该多肽,即先合成suc-iie-glu(γ-odmab)-gly-arg(pbf)-ppda-树脂,使用水合肼脱除odmab,再与pip形成suc-iie-glu(γ-pip)-gly-arg(pbf)-ppda-树脂。fmoc-glu(odmab)-oh的原料,价格非常昂贵,且此方法使用水合肼脱除odmab困难,且odmab会有残留,而水合肼本身具有毒性,会污染环境。
4、有鉴于此,特提出本发明。
技术实现思路
1、本发明的第一目的在于提供一种含哌啶修饰的多肽的合成方法,包括:
2、步骤1:获取需要哌啶修饰的前体多肽,所述前体多肽在需要哌啶修饰的氨基酸残基上包含至少一个酯基;
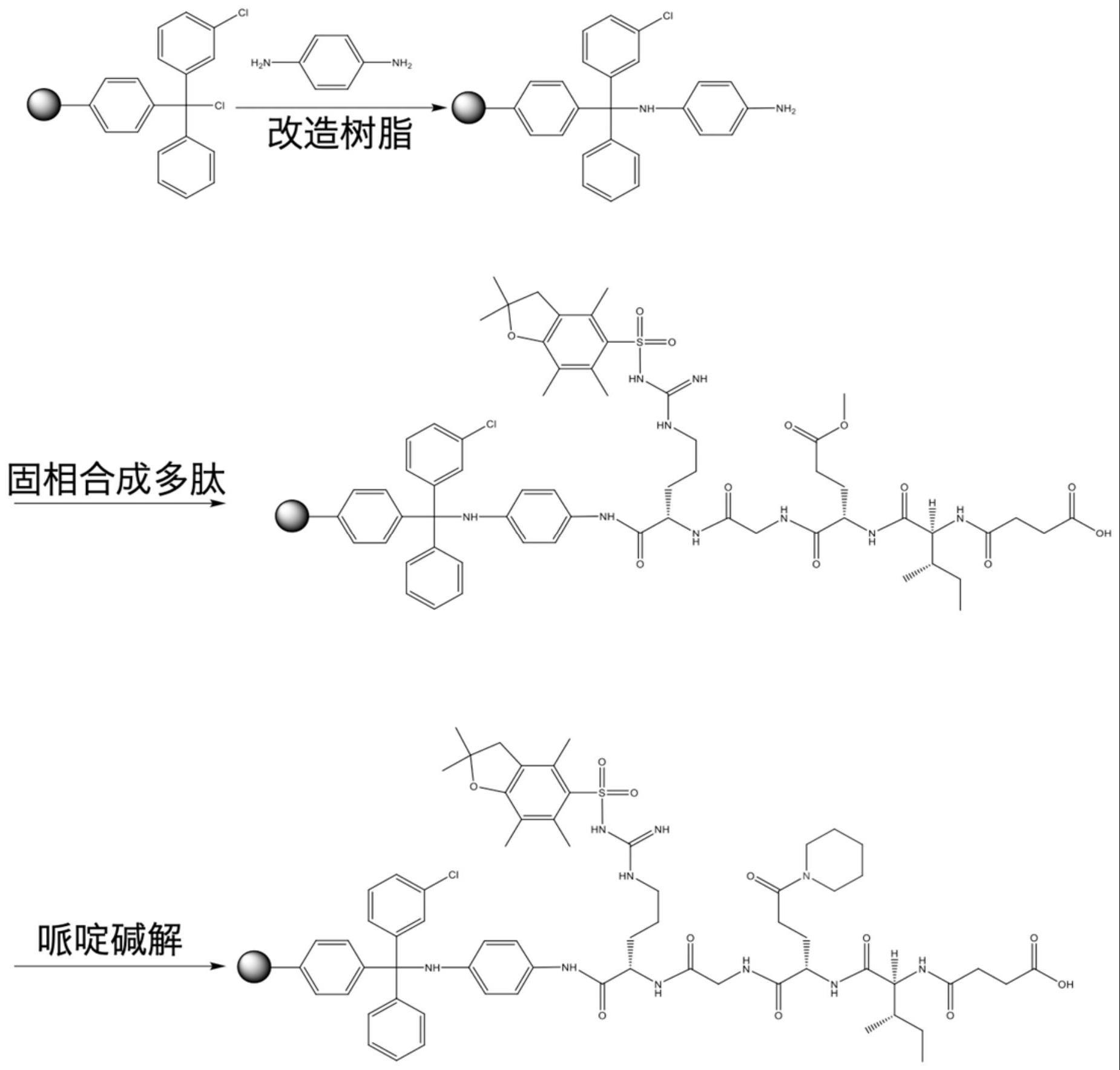
3、步骤2:加入哌啶碱解所述前体多肽中的酯基,得到所述含哌啶修饰的多肽。
4、该方法用哌啶直接将多肽中氨基酸残基上的酯基进行碱解,与相应氨基酸形成酰胺键,操作简便、效率高、成本低,且避免了环境污染与可能产生的毒性,适合工业化生产。
5、本发明的第二目的在于提供一种suc-iie-glu(γ-pip)-gly-arg-pna·hcl的制备方法,包括:
6、a)使用如上所述的方法在表面修饰有对苯二胺的固相载体上合成多肽suc-iie-glu(γ-pip)-gly-arg-ppda,得到所述多肽的固相复合物,其中,所述需要哌啶修饰的谷氨酸残基固相合成原料以衍生物的形式加入,所述衍生物为包含酯基的glu;
7、b)将步骤a)所得多肽从固相载体上裂解下来并把其中的对苯二胺基团氧化为对硝基苯胺;
8、c)步骤b)所得粗品多肽进行分离纯化得到suc-iie-glu(γ-pip)-gly-arg-pna·hcl。
9、通过上述方法合成suc-iie-glu(γ-pip)-gly-arg-pna·hcl(s-2732),极大简化工艺、操作简单、解决了s-2732生产过程中工艺复杂的问题。
技术特征:
1.含哌啶修饰的多肽的合成方法,包括:
2.根据权利要求1所述的方法,所述前体多肽在适合固相合成反应的条件下在固相载体上合成,所述需要哌啶修饰的氨基酸残基的固相合成原料以衍生物的形式加入,所述衍生物包含至少一个酯基。
3.根据权利要求2所述的方法,所述衍生物所对应的氨基酸包含glu和/或asp。
4.根据权利要求1或2所述的方法,所述酯基选自甲酯、乙酯、丙酯、丁酯、戊酯和己酯中的一种或多种。
5.根据权利要求2所述的方法,步骤2中加入的哌啶与所述衍生物的比为(1ml~15ml):1mmol。
6.根据权利要求2所述的方法,步骤2中加入的哌啶与所述固相载体的比为(5ml~50ml):1g。
7.根据权利要求1~6中任一项所述的方法,步骤2中所述碱解反应的温度为20℃~80℃,优选为40℃~60℃。
8.根据权利要求7所述的方法,步骤2中所述碱解反应的时间为8h~48h,优选为16h~40h。
9.根据权利要求1~6、8中任一项所述的方法,步骤2中所述碱解反应在溶液体系中进行,所用溶剂选自哌啶、n,n-二甲基甲酰胺、n-甲基吡咯烷酮、甲苯和苯中的一种或多种。
10.根据权利要求2~6中任一项所述的方法,在固相合成时,所述氨基酸衍生物中氨基酸的氨基保护基为fmoc。
11.根据权利要求10所述的方法,固相合成反应中所述fmoc采用fmoc脱保护剂脱去,所述fmoc脱保护剂为体积比1:(1~4)的哌啶与二甲基酰胺的混合物;优选地,所述fmoc脱保护反应温度为10℃~80℃,反应5min~30min。
12.根据权利要求2~6、11中任一项所述的方法,所述固相载体为树脂,优选为氯树脂、br-acm树脂或mobhb树脂。
13.根据权利要求2~6、11中任一项所述的方法,所述固相合成反应中所用多肽缩合试剂为缩合试剂1,缩合试剂2和缩合试剂3的一种或多种的混合;
14.根据权利要求13所述的方法,所述固相合成反应中各试剂的投料的摩尔比为:氨基酸原料:缩合试剂1:缩合试剂2=(1~3):(1~3):(1~3);或氨基酸原料:缩合试剂1:缩合试剂3=(1~3):(1~3):(1~3);优选地,氨基酸原料:缩合试剂1:缩合试剂2=(1~2):(1~2):(1~2);或氨基酸原料:缩合试剂1:缩合试剂3=(1~2):(1~2):(1~2);更优选地,所述氨基酸原料:缩合试剂1:缩合试剂2=1:1:1或1:1:2;或所述氨基酸原料:缩合试剂1:缩合试剂3=1:1:1或1:1:2。
15.suc-iie-glu(γ-pip)-gly-arg-pna·hcl的制备方法,包括:
16.根据权利要求15所述的制备方法,所述表面修饰有对苯二胺的固相载体为对苯二胺在有机碱的作用下修饰到固相载体上得到。
17.根据权利要求16所述的制备方法,所述有机碱为n,n-二异丙基乙基胺和/或1,8-二氮杂二环[5.4.0]十一碳-7-烯。
18.根据权利要求16所述的制备方法,在对所述固相载体进行修饰时,所述对苯二胺与有机碱的摩尔比为(1:1)~(1:5),优选为1:2。
19.根据权利要求18所述的制备方法,在对所述固相载体进行修饰时,反应的温度为20℃~80℃,反应的时间为1h~24h;优选地,所述反应的温度为30℃~60℃,反应的时间为5h~12h。
20.根据权利要求15所述的制备方法,固相合成时加入的精氨酸衍生物包含胍基保护基,所述胍基保护基选自2,2,4,6,7-五甲基二氢苯并呋喃-5-磺酰基、4-甲氧基-2,3,6-三甲基苯磺酰基或2,2,5,7,8-五甲基苯并二氢吡喃-6-磺酰基。
21.根据权利要求15所述的制备方法,所述裂解所用切割试剂为三氟乙酸混合液,所述混合液中三氟乙酸的体积≥80%。
22.根据权利要求21所述的制备方法,所述混合液中还包括水、三乙基硅烷、三异丙基硅烷、苯酚、1,2二硫苏糖醇和苯甲硫醚中的一种或多种。
23.根据权利要求15~22中任一项所述的制备方法,步骤b)中所述氧化所用氧化剂为双氧水、过氧乙酸、间氯过氧苯甲酸、过硼酸钠和过硫酸氢钾中的一种或多种;优选为过硫酸氢钾。
24.根据权利要求23所述的制备方法,步骤b)中所述氧化剂和从固相载体上裂解得到的多肽的摩尔比为(1~20):1;优选地,所述氧化剂和从固相载体上裂解得到的多肽的摩尔比为(2~10):1。
25.根据权利要求24所述制备方法,所述氧化的时间为1h~48h,氧化的温度为10℃~60℃;优选地,所述氧化的时间为10h~25h,氧化温度为20℃~40℃。
技术总结
本发明涉及多肽化学合成技术领域,具体而言,涉及一种含哌啶修饰的多肽的合成方法,包括:步骤1:获取需要哌啶修饰的前体多肽,所述前体多肽在需要哌啶修饰的氨基酸残基上包含至少一个酯基;步骤2:加入哌啶碱解所述前体多肽中的酯基,得到所述含哌啶修饰的多肽。该方法可用于Suc‑IIe‑Glu(γ‑pip)‑Gly‑Arg‑pNA·HCl的制备。
技术研发人员:王卫国,王克全
受保护的技术使用者:江苏金斯瑞生物科技有限公司
技术研发日:
技术公布日:2024/1/13
- 还没有人留言评论。精彩留言会获得点赞!