一种合成含α-手性三氟甲基的β-二羰基化合物的方法
本发明属于化学合成,具体是一种合成含α-手性三氟甲基的β-二羰基化合物的方法。
背景技术:
1、在药物化学领域中,三氟甲基是一类重要的化学基团,因其具有提高有机分子的脂溶性、良好的代谢稳定性、高电负性和生物利用度使得它在生物活性分子中有着广泛的应用。但是天然的三氟甲基化合物种类较少且自然界中含量也较低,因此科学家们往往通过人工合成的方式开发合成三氟甲基化合物。
2、1,5-二羰基化合物是一类重要的合成子,而手性三氟甲基-1,5-二羰基化合物是构建含手性三氟甲基复杂结构分子的重要合成砌块。目前,手性三氟甲基-1,5-二羰基化合物合成方法报道较为有限,主要围绕着β-cf3-α,β-不饱和酮的michael加成反应实现。例如,赵刚课题组(j.org.chem.2016,81,9973-9982)和张俊良课题组(org.lett.2017,19,5102-5105)分别使用二肽衍生的磷盐催化剂和二胺-膦催化剂通过丙二酸酯与β-cf3-α,β-不饱和酮的不对称michael反应成功构建手性三氟甲基的1,5-二羰基化合物。但是,他们选用的手性催化剂都需要自行合成,步骤较长,合成的成本和难度相对较高。此外他们的方法在构建手性三氟甲基的1,5-二羰基化合物的类型上较为有限,同时为确保高对映选择性,需要较低的反应温度(0-20℃)。因此,我们发展一种三氟甲磺酸镍和手性双噁唑啉催化三氟亚乙基丙二酸酯的不对称mukaiyama-michael反应,为含α-手性三氟甲基的β-二羰基化合物的合成提供一种新的方法。
技术实现思路
1、为了解决现有技术中手性三氟甲基化合物的合成反应类型单一,催化剂制备成本较高,反应条件苛刻等问题,本发明的目的是提供一种利用三氟甲磺酸镍和手性双噁唑啉催化的不对称mukaiyam-micheal反应合成含α-手性三氟甲基的β-二羰基化合物的新方法。
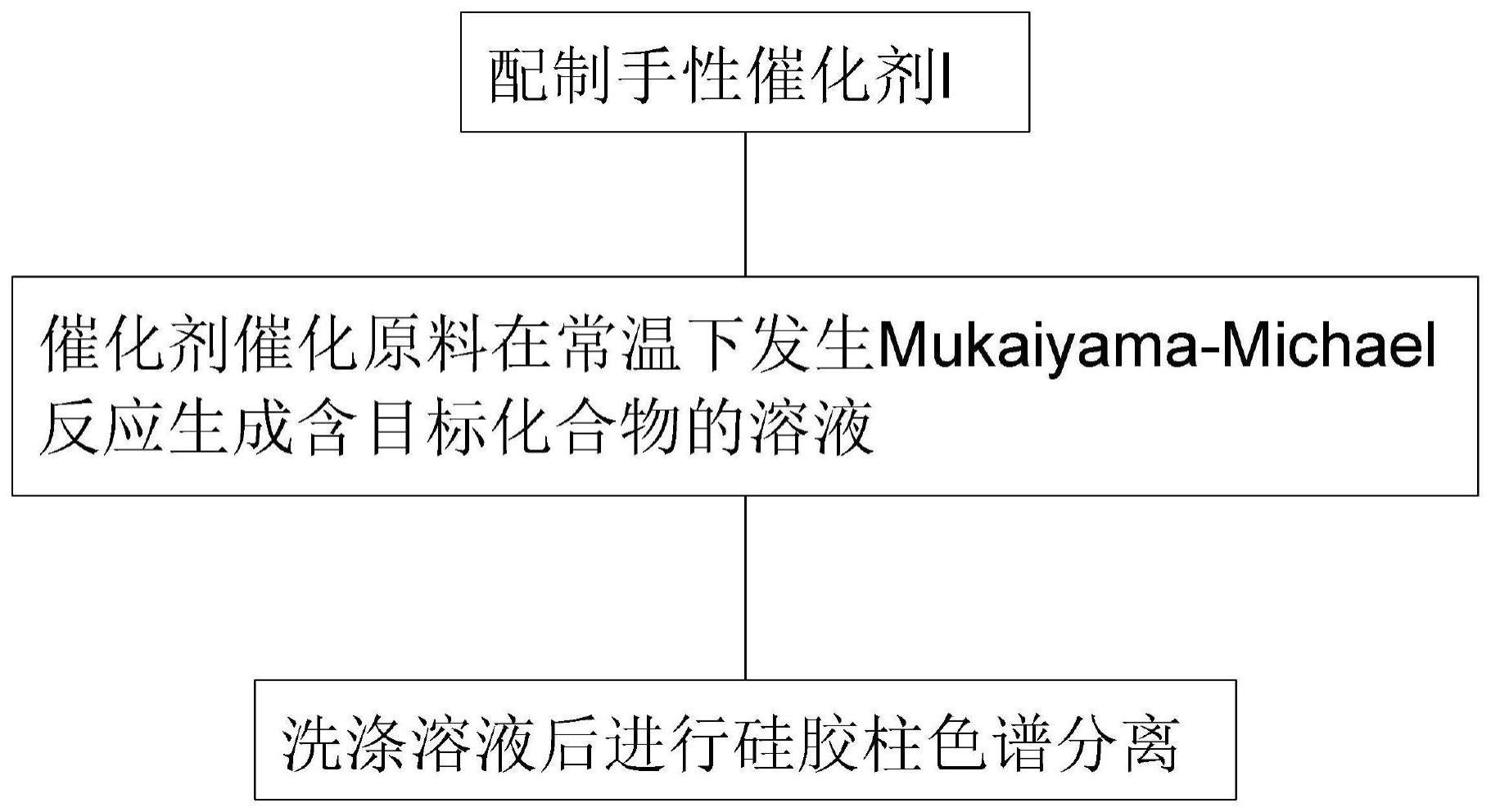
2、为了实现上述目的,本发明的技术方案如下:一种合成含α-手性三氟甲基的β-二羰基化合物的方法,包括如下步骤:
3、s1、配制手性催化剂ⅰ,在干燥的schlenk管中加入三氟甲磺酸镍、手性双噁唑啉配体和甲苯搅拌制得手性催化剂ⅰ;
4、
5、s2、在惰性气体保护下,将三氟乙亚基丙二酸酯、烯醇硅醚和六氟异丙醇依次装有手性催化剂ⅰ的schlenk管中,在常温下发生不对称mukaiyama-michael反应生成含α-手性三氟甲基的β-二羰基化合物,其反应式为:
6、
7、其中,r选自苯基、2-甲苯基、3-甲苯基、4-氯苯基、4-溴苯基、2-萘基,tms为三甲基硅基,cf3为三氟甲基,co2et为酯基,hfip为六氟异丙醇;
8、s3、反应结束后以洗脱剂对其进行硅胶柱层析分离,洗脱后经减压蒸馏浓缩制得含α-手性三氟甲基的β-二羰基化合物。
9、进一步,所述s1中三氟甲磺酸镍用量为8-12mol%。
10、进一步,所述s1中手性双噁唑啉配体用量为10-14mol%。
11、进一步,所述s1中甲苯用量为1-2ml。
12、进一步,所述s1中手性双噁唑啉配体为c4位带苯基、苄基、异丙基或者叔丁基的丙二酸脂类双噁唑啉配体。
13、进一步,所述s2中烯醇硅醚、三氟乙亚基丙二酸酯、六氟异丙醇的摩尔比为1.0-1.5:1.0:1.0-2.0。
14、进一步,所述s2中常温温度保持在20-30℃,反应时长为4-12h。
15、进一步,所述s3中洗脱剂由石油醚与乙酸乙酯按10-20:1的体积比混合所制。
16、采用上述方案后实现了以下有益效果:
17、1.相较于现有技术,本方案通过三氟甲磺酸镍和手性双噁唑啉络合形成手性催化剂i,以六氟异丙醇为添加剂,结合烯醇硅醚和三氟乙亚基丙二酸酯发生不对称mukaiyama-michael反应制得含α-手性三氟甲基的β-二羰基化合物,本方案为含α-手性三氟甲基的β-二羰基化合物的合成提供了新的方法,且本方法中催化剂性能优良,可使反应在室温下取得高收率和对映选择性;
18、2.本方案适用面较广,可替换原料合成多种手性三氟甲基化合物,且三氟甲磺酸镍和手性双噁唑啉配体易获取,无需额外合成。
技术特征:
1.一种合成含α-手性三氟甲基的β-二羰基化合物的方法,其特征在于:包括如下步骤:
2.根据权利要求1所述的合成含α-手性三氟甲基的β-二羰基化合物的方法,其特征在于:所述s1中三氟甲磺酸镍用量为8-12mol%。
3.根据权利要求1所述的合成含α-手性三氟甲基的β-二羰基化合物的方法,其特征在于:所述s1中手性双噁唑啉配体用量为10-14mol%。
4.根据权利要求1所述的合成含α-手性三氟甲基的β-二羰基化合物的方法,其特征在于:所述s1中甲苯用量为1-2ml。
5.根据权利要求1所述的合成含α-手性三氟甲基的β-二羰基化合物的方法,其特征在于:所述s1中手性双噁唑啉配体为c4位带苯基、苄基、异丙基或者叔丁基的丙二酸脂类双噁唑啉配体。
6.根据权利要求1所述的合成含α-手性三氟甲基的β-二羰基化合物的方法,其特征在于:所述s2中烯醇硅醚、三氟乙亚基丙二酸酯、六氟异丙醇的摩尔比为1.0-1.5:1.0:1.0-2.0。
7.根据权利要求1所述的合成含α-手性三氟甲基的β-二羰基化合物的方法,其特征在于:所述s2中常温温度保持在20-30℃,反应时长为4-12h。
8.根据权利要求1所述的合成含α-手性三氟甲基的β-二羰基化合物的方法,其特征在于:所述s3中洗脱剂由石油醚与乙酸乙酯按10-20:1的体积比混合所制。
技术总结
本发明公开了化学合成技术领域的一种合成含α‑手性三氟甲基的β‑二羰基化合物的方法,包括如下步骤:将三氟甲磺酸镍、手性双噁唑啉配体在甲苯溶剂中制备手性催化剂Ⅰ;在惰性气体保护下,将三氟乙亚基丙二酸酯、烯醇硅醚和六氟异丙醇(HFIP)依次加入装有手性催化剂Ⅰ的schlenk管中在室温下反应;反应结束后通过硅胶柱层析分离,减压蒸馏浓缩制得含α‑手性三氟甲基的β‑二羰基化合物。本方案通过手性镍‑双噁唑啉络合物催化体系实现了乙亚基丙二酸酯的不对称Mukaiyama‑Michael反应,生成系列含α‑手性三氟甲基的β‑二羰基化合物,本方案的反应条件较为温和,在常温下反应即可获得高收率和高对映选择性。
技术研发人员:吴昊,肖勋文,方烨汶,冯偲
受保护的技术使用者:宁波工程学院
技术研发日:
技术公布日:2024/1/11
- 还没有人留言评论。精彩留言会获得点赞!