CHRDL1基因敲入小鼠模型及其构建方法
本发明涉及生物工程,特别涉及一种chrdl1基因敲入小鼠模型及其构建方法。
背景技术:
1、鸡脊索生成素样蛋白1(chordin-like 1,chrdl1)是一种具有重复半胱氨酸丰富结构域的分泌糖蛋白,可与骨形态发生蛋白(bone morphogenetic proteins,bmps)家族配体竞争性结合,抑制其与受体结合发挥功能。chrdl1在人体内多个器官广泛分布,主要存在于中枢神经系统、视网膜、甲状腺、心脏、肺部、结直肠、生殖器等的多种细胞类型中。chrdl1蛋白是一种多功能蛋白质,具有促进神经元发育,调节体内免疫反应、促进血管生成、调控骨软骨生成、调控癌症发生等作用。因此chrdl1在运动系统疾病、免疫系统疾病、癌症治疗等多个方面有着广阔的应用前景。
2、chrdl1在国内外的研究还比较有限,暂时还没有人研究过生产chrdl1蛋白的方法。先前人们常用哺乳动物细胞、昆虫细胞培养或微生物发酵等传统方法来表达某种蛋白,但这类方法一般存在蛋白表达量较低、生产成本较高或纯化过程复杂等缺点,很难实现大规模的工业化生产。
3、因此,为了日后能够实现大规模生产,有必要开发一种利用crispr/cas9制备高表达人chrdl1蛋白转基因鼠及其方法。
技术实现思路
1、本发明目的是提供一种chrdl1基因敲入小鼠模型及其构建方法,该方法基因编辑效率高、该转基因鼠可高表达人chrdl1蛋白。
2、在本发明的第一方面,提供了chrdl1基因敲入小鼠的打靶载体,所述打靶载体的核苷酸序列如seq id no.1所示。
3、进一步地,所述打靶载体包含核苷酸序列如seq id no.2所示的dna片段结构cagpr-loxp-stop-loxp-ege-zk-037cds-wpre-pa,其中,所述cag为启动子,所述pr-loxp-stop-loxp为调控元件;ege-zk-037cds-wpre-pa为表达元件,且包含zk-037cds的5’端和3’端的同源臂。
4、在本发明的第二方面,提供了一种chrdl1基因敲入小鼠模型的构建方法,所述方法包括:
5、将sgrna12体外转录成mrna,获得活性的sgrna12,所述sgrna12的核苷酸序列如seq id no.3所示;
6、获得有活性的cas9 mrna,所述cas9核苷酸序列如seq id no.4所示;
7、将所述有活性的sgrna12、cas9 mrna和核苷酸序列如seq id no.1所示的打靶载体混合后显微注射到小鼠受精卵中,获得f0代小鼠;
8、选择f0代小鼠基因型鉴定结果中的f0代阳性小鼠,使其与野生型小鼠进行交配,从而获得具有稳定基因型的f1代小鼠;后筛选出发生正确重组的基因打靶小鼠,即获得chrdl1基因敲入模式小鼠。
9、在本发明的第三方面,提供了一种用于构建人源性chrdl1转基因小鼠模型的成套核酸分子,所述成套核酸分子包括:
10、(a)编码grna的核苷酸序列,如seq id no.3所示;
11、(b)编码cas9的核苷酸序列,如seq id no.4所示;
12、(c)核苷酸序列如seq id no.1所示的打靶载体。
13、在本发明的第四方面,提供了采用所述的方法获得的chrdl1基因敲入小鼠模型。
14、在本发明的第五方面,提供了所述的chrdl1基因敲入小鼠模型在制备过表达人源性chrdl1蛋白或者筛选药物中的应用。
15、本发明实施例中的一个或多个技术方案,至少具有如下技术效果或优点:
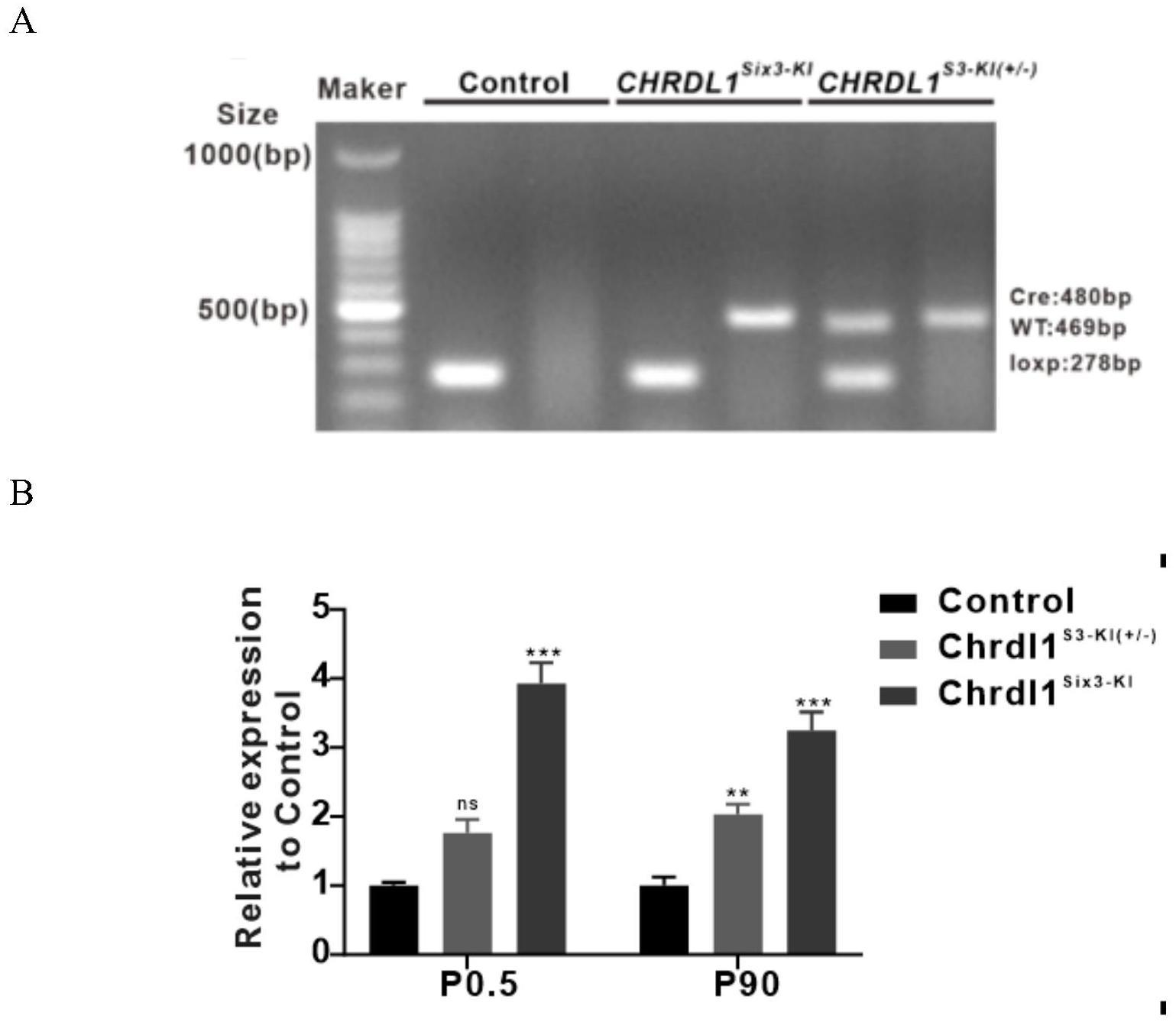
16、本发明制备得到的小鼠模型,可将基因敲进效率提高近20倍、且快速、便捷,提高了成功率,节约了成本,缩短了周期,更有利于工业化及大规模的商业应用。经检测chrdl1在chrdl1基因敲入小鼠模型的视网膜中成功过表达。
技术特征:
1.chrdl1基因敲入小鼠的打靶载体,其特征在于,所述打靶载体的核苷酸序列如seqid no.1所示。
2.根据权利要求1所述的chrdl1基因敲入小鼠的打靶载体,其特征在于,所述打靶载体包含核苷酸序列如seq id no.2所示的dna片段结构cag pr-loxp-stop-loxp-ege-zk-037cds-wpre-pa,其中,所述cag为启动子,所述pr-loxp-stop-loxp为调控元件;ege-zk-037cds-wpre-pa为表达元件,且包含zk-037cds的5’端和3’端的同源臂。
3.一种chrdl1基因敲入小鼠模型的构建方法,其特征在于,所述方法包括:
4.一种采用权利要求3所述的方法获得的chrdl1基因敲入小鼠模型。
5.权利要求4所述的chrdl1基因敲入小鼠模型在制备过表达人源性chrdl1蛋白或者筛选药物中的应用。
6.一种用于构建chrdl1基因敲入小鼠模型的成套核酸分子,其特征在于,所述成套核酸分子包括:
技术总结
本发明提供了一种CHRDL1基因敲入小鼠模型及其构建方法,所述方法包括:获得活性的sgRNA12,所述sgRNA12的核苷酸序列如SEQ ID NO.3所示;获得有活性的Cas9mRNA,所述Cas9核苷酸序列如SEQ ID NO.4所示;将所述有活性的sgRNA12、Cas9mRNA和核苷酸序列如SEQ ID NO.1所示的打靶载体混合后显微注射到小鼠受精卵中,获得F0代小鼠;选择F0代阳性小鼠与野生型小鼠进行交配,从而获得具有稳定基因型的F1代小鼠;后筛选获得CHRDL1基因敲入模式小鼠。该方法基因编辑效率高、该转基因鼠可高表达人CHRDL1蛋白。
技术研发人员:沈吟,刘冬梅
受保护的技术使用者:武汉大学
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!