一种使用pH梯度进行阳离子层析的抗体纯化方法与流程
本发明属于生物制药,特别是涉及一种使用ph梯度进行阳离子层析洗脱的抗体纯化方法,具体而言是通过使用ph梯度来进行蛋白质单体与聚体的分离,达到去除聚体的目的。
背景技术:
1、在抗体药物研发过程中,蛋白质聚集是一种可能发生与生产过程各步骤的现象,包括发酵和纯化等步骤;而蛋白质发生聚集会影响抗体质量、安全性和功效。特别是对于双特异性抗体,蛋白的稳定性更具有挑战性。因此,寻求快速有效的分离方式以降低抗体中的多聚体对于抗体生产具有非常重要的意义。
2、ph梯度洗脱:由于蛋白静电荷具有ph依耐性,因此可通过改变洗脱缓冲液中的ph将蛋白从离子层析柱上洗脱下来,通过增加或者降低缓冲液的ph,样品或层析柱填料上不同的带点基团被逐渐滴定,直到他们变成中性或者与填料相反的电荷此时样品被洗脱下来。
3、目前的现有技术,抗体纯化的方式一般为三步纯化:包括亲和层析、阳离子交换层析和阴离子交换层析。通常精纯是流穿模式的例如阴离子交换层析。
技术实现思路
1、为了更快速有效地降低抗体中的多聚体,本发明提供了一种使用ph梯度进行阳离子层析洗脱的抗体纯化方法,可以分离和提纯双特异性抗体,具体而言是通过使用ph梯度来进行蛋白质单体与聚体的分离,达到去除聚体的目的。
2、本发明所要解决的技术问题在于提供一种分离抗体药物的方法,能够快速有效的去除抗体中的多聚体,得到多聚体明显降低的抗体药物,且极大的缩短了纯化时间。
3、为解决上述缺陷,本发明第一方面提供一种使用ph梯度进行阳离子层析来纯化抗体的方法,所述方法包括以下步骤:
4、上样、平衡、洗涤和洗脱;其中,所述洗脱使用包含缓冲液a和缓冲液b的溶剂体系,从0%-100%缓冲液b,进行梯度洗脱,收集产品;所述梯度洗脱优选进行18~35个柱体积;
5、所述的缓冲液a为10~20mm柠檬酸,ph为4.5~5.5,所述的缓冲液b为10~20mm十二水合磷酸氢二钠,ph为7.5~8.5。
6、本发明的术语“梯度洗脱”指的是在同一个分析周期中,按一定程度不断改变流动相的浓度配比。梯度洗脱(gradient elution),又称为梯度淋洗或程序洗脱。其中,线性梯度洗脱为本领域技术人员所理解的技术手段,0%缓冲液b时是100%缓冲液a,缓冲液b逐渐增加的过程即缓冲液a逐渐减少的过程,当达到100%缓冲液b时,缓冲液a为0%。线性梯度洗脱过程中两种缓冲液的浓度由整个洗脱过程设定的总洗脱体积决定,例如柱体积为5ml、20个柱体积的洗脱,总洗脱缓冲液为100ml,缓冲液b的浓度按每毫升1%的速度增加。
7、在某些实施方案中,所述的缓冲液a为20mm柠檬酸,ph为5.0,所述的缓冲液b为20mm十二水合磷酸氢二钠,ph为8.0。
8、在某些实施方案中,所述方法满足以下条件的一种或多种:
9、所述梯度洗脱为线性梯度洗脱;
10、所述梯度洗脱进行20个柱体积;
11、所述的缓冲液a配制时使用0.5m十二水合磷酸氢二钠调节ph;
12、所述的缓冲液b配制时使用1m柠檬酸调节ph。
13、在某些实施方案中,所述方法使用的阳离子填料为capto s impact。
14、在某些实施方案中,
15、所述平衡使用20mm柠檬酸,ph为5.0,和/或,
16、所述平衡进行5~15个柱体积,优选所述平衡进行5个柱体积。
17、在某些实施方案中,所述洗涤使用缓冲液a,和/或,
18、所述洗涤进行5~15个柱体积,
19、优选所述洗涤进行5个柱体积。
20、在某些实施方案中,所述阳离子层析之前还包括亲和层析的步骤;所述亲和层析包括上样、平衡、洗涤和洗脱,以获得应用于阳离子层析的抗体溶液。
21、在某些实施方案中,所述亲和层析后还包括对所述抗体溶液进行离心换液;优选地,所述离心换液使用的缓冲液的ph为5.0,电导小于4ms/cm;
22、更优选地,所述缓冲液为10mm组氨酸,10mm天冬氨酸。
23、在某些实施方案中,所述方法满足以下条件的一种或多种:
24、所述抗体溶液为双特异性抗体的溶液;
25、所述亲和层析使用的填料为mabselecttmprisma;
26、所述亲和层析的平衡使用10~30mm pb,120~180mm nacl,ph 6.5~7.5,进行5~15个柱体积;
27、所述亲和层析的洗涤使用0.1~1m醋酸钠,0.2~0.8m nacl,ph 4.5~5.5,进行5~15个柱体积;
28、所述亲和层析的洗脱使用0.1~1m醋酸钠,ph 3.0~4.2,进行3~12个柱体积。
29、所述双特异性抗体包含分别靶向sars-cov-2的s蛋白以及cd3(或p-钙粘蛋白)的第一蛋白结构域和第二蛋白结构域。
30、在某些实施方案中,所述第一蛋白结构域的重链序列如seq id no:3所示;所述第一蛋白结构域的轻链序列如seq id no:2所示。
31、在某些实施方案中,所述第一蛋白结构域为igg结构。
32、在某些实施方案中,所述第二蛋白结构域为scfv,其vh的氨基酸序列如seq idno:5所示,蛋白结构域其vl的氨基酸序列如seq id no:6所示。
33、在某些实施方案中,所述第一蛋白结构域和第二蛋白结构域使用linker例如(g4s)n连接;所述n代表大于零的整数,例如n=3或4。优选所述第二蛋白结构域通过(g4s)4连接在所述第一蛋白结构域的c端。
34、在某些实施方案中,所述scfv的氨基酸序列如seq id no:4所示。
35、在某些实施方案中,所述双特异性抗体的重链序列如seq id no:1所示,轻链序列如seq id no:2所示。
36、在某些实施方案中,所述方法满足以下条件的一种或多种:
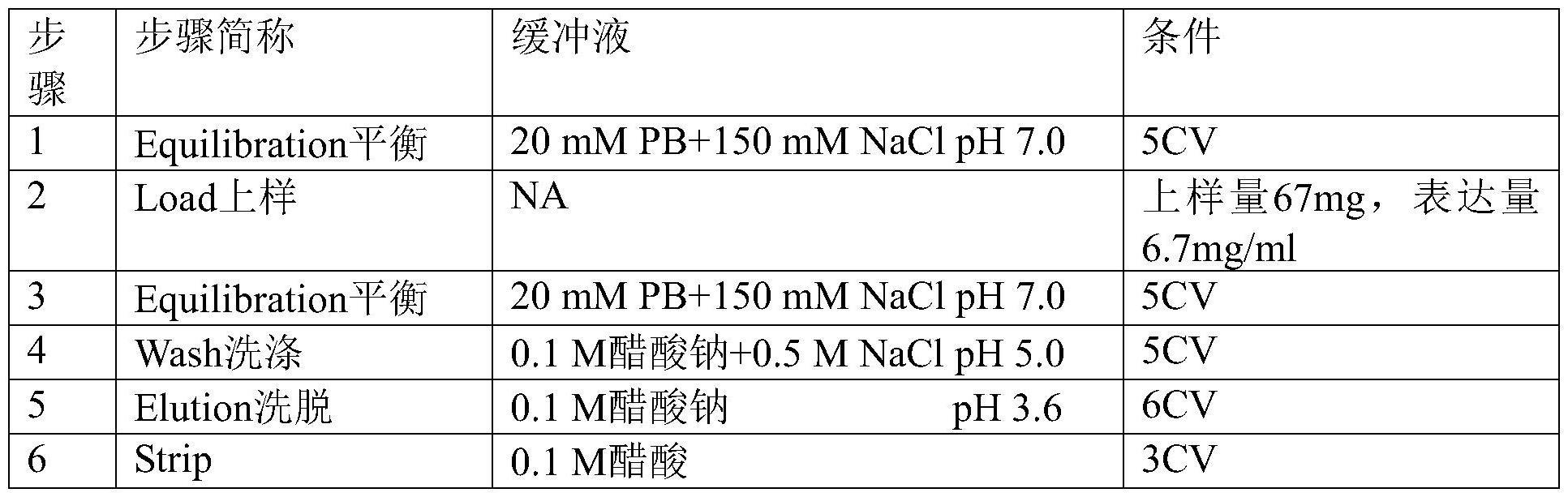
37、所述亲和层析的上样量为67mg,
38、所述亲和层析的平衡使用20mm pb,150nacl,ph 7.0,进行5个柱体积,
39、所述亲和层析的洗涤使用0.1m醋酸钠,0.5m nacl,ph 5.0,进行5个柱体积,
40、所述亲和层析的洗脱使用0.1m醋酸钠,ph 3.6,进行6个柱体积。
41、在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
42、本发明所用试剂和原料均市售可得。
43、本发明的积极进步效果在于:本发明可以使用亲和层析和阳离子层析两步纯化,将蛋白纯度提高到96%以上,样品回收率可达到61%,节约纯化时间,提高收率。
技术特征:
1.一种使用ph梯度进行阳离子层析来纯化抗体的方法,其特征在于,所述方法包括以下步骤:
2.如权利要求1所述的方法,其特征在于,所述的缓冲液a为20mm柠檬酸,ph为5.0,所述的缓冲液b为20mm十二水合磷酸氢二钠,ph为8.0。
3.如权利要求1所述的方法,其特征在于,所述方法满足以下条件的一种或多种:
4.如权利要求1所述的方法,其特征在于,所述方法使用的阳离子填料为capto simpact。
5.如权利要求1所述的方法,其特征在于,
6.如权利要求5所述的方法,其特征在于,
7.如权利要求1所述的方法,其特征在于,所述阳离子层析之前还包括亲和层析的步骤;所述亲和层析包括上样、平衡、洗涤和洗脱,以获得应用于阳离子层析的抗体溶液。
8.如权利要求7所述的方法,其特征在于,所述亲和层析后还包括对所述抗体溶液进行离心换液;优选地,所述离心换液使用的缓冲液的ph为5.0,电导小于4ms/cm;
9.如权利要求7所述的方法,其特征在于,所述方法满足以下条件的一种或多种:
10.如权利要求9所述的方法,其特征在于,所述方法满足以下条件的一种或多种:
技术总结
本发明公开了一种使用pH梯度进行阳离子层析洗脱的方法,所述方法包括以下步骤:上样、平衡、洗涤和洗脱;其中,所述洗脱使用缓冲液A和缓冲液B的溶剂体系进行梯度洗脱,梯度洗脱从0%‑100%缓冲液B,收集产品;所述的缓冲液A为10~20mM柠檬酸,pH为4.5~5.5,所述的缓冲液B为10~20mM十二水合磷酸氢二钠,pH为7.5~8.5。本发明仅使用亲和层析和阳离子层析两步纯化,将蛋白纯度提高到96%以上,节约纯化时间,提高收率。
技术研发人员:夏松,高宏海,倪天琪
受保护的技术使用者:鼎康(武汉)生物医药有限公司
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!