一种HCVE2重组蛋白、抗HCVE2蛋白的单克隆抗体及制备方法和应用与流程
本发明属于生物工程,具体涉及hcv e2重组蛋白、抗hcv e2蛋白的单克隆抗体及制备方法和应用。
背景技术:
1、丙型肝炎是由丙型肝炎病毒(hcv)引起的肝脏疾病,是一种对全球健康威胁的疾病。
2、hcv具有高度的遗传异质性,目前分为11种基因型,每种基因型包含80种亚型;然而,一些疗法对某些基因型有效,但不是对所有的基因型都有效。开发一种安全有效的hcv疫苗仍然是全球控制hcv感染的重要目标。因此,对hcv感染的抗体介导的中和作用的深入了解可能成为疫苗设计的关键。实现有效免疫的主要挑战之一是hcv病毒的遗传多样性。可能需要产生许多中和抗体来克服这种变异性。据报道,hcv的e2糖蛋白可与细胞受体直接相互作用,并早已被认为是保护性免疫的重要免疫原性目标。
3、hcv诱导的细胞和体液免疫反应已被广泛研究。新的研究表明,单克隆抗体和多克隆抗体可以防止hcv感染。针对e2包膜糖蛋白的广义中和和被动转导的单克隆抗体可以预防hcv感染。因此,筛查hcv e2抗体可促进有效疫苗的开发。人血清e2特异性抗体、e1-e2免疫小鼠的多克隆igg和针对hcv包膜糖蛋白的单克隆抗体可以在体外中和hcvcc(培养的hcv细胞)。到目前为止,丙型肝炎疫苗的开发主要集中在t细胞免疫反应上。一些观察表明,e2n端高变异区1(hvr1)可能参与hcv中和,该区域含有细胞毒性t细胞表位和一些b细胞表位,而且该区域的抗体被证明可以阻止病毒结合。然而,hcv基因组的多样性严重阻碍了针对hcv感染的疫苗开发。
技术实现思路
1、本发明的第一个目的在于提供一种hcv重组e2蛋白及其制备方法。
2、本发明的第二个目的在于提供基于hcv e2重组蛋白为抗原通过细胞融合得到的3株单克隆抗体及制备方法。
3、本发明的第三个目的在于提供了3株单克隆抗体识别的表位。
4、为了实现上述目的,本发明采用的技术方案是:
5、一种hcv e2重组蛋白,其氨基酸序列如seq id no1所示;编码其基因的核苷酸序列如seq id no2所示。
6、一种hcv e2重组蛋白的制备方法,包括以下步骤:
7、根据uniprot蛋白质数据库登录号o92972获取hcv e2蛋白氨基酸序列,按照hek293f密码子偏好性优化,设计3对引物合成至puc57质粒载体上,并引入酶切位点xhoⅰ/hindⅲ,在hcv e2蛋白的n端依次添加分泌信号肽和his标签,中间由linker连接,构建至pcaggs载体上,得到重组质粒pcaggs-e2;
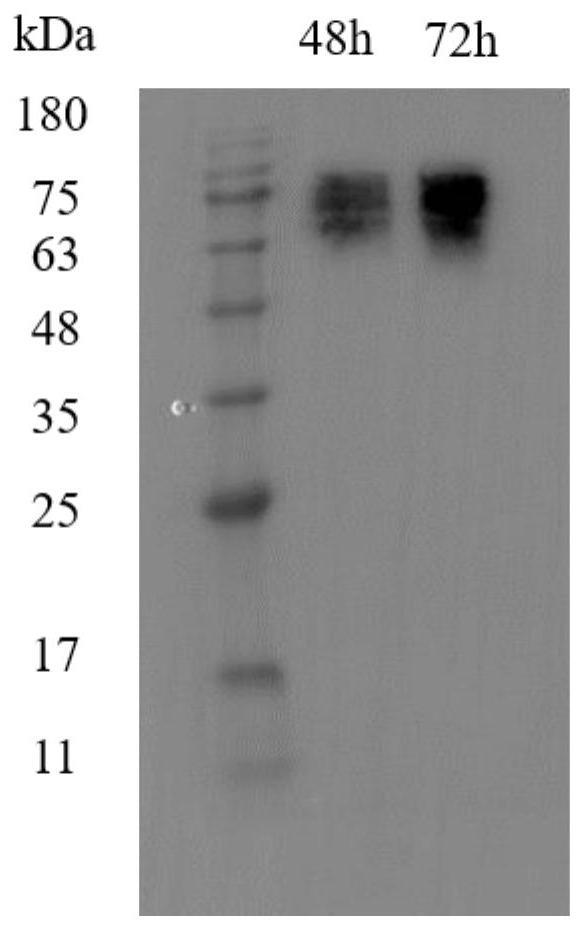
8、将pcaggs-e2去内毒素质粒转染至密度为3×106cells/ml的hek293f细胞中,培养72h离心收集细胞上清,加入终浓度为1%的蛋白酶抑制剂,经0.45μm微孔滤膜过滤,再使用ni亲和层析纯化,得到纯化的重组hcv e2蛋白。
9、所述的3对引物为(seq id no:12-17):
10、e2-f1 tcggacaccaccaccaccatcacggcggctctgagactcacactaccg
11、e2-f2 cttcctcctgctactctggctcccagataccaccggagagctcggacaccaccac
12、e2-f3 ccgctcgaggccaccatggaaaccccagcgcagcttctcttcctcctgctactc
13、e2-r1 tcgcggtcttccaggttgcaacgctcgccacgg
14、e2-r2 ctgcggtcgcggtcttccaggttgcaacgc
15、e2-r3 cccaagcttttactcgctgcggtcgcggtct。
16、纯化方法为:采用含20mm tris、150mm nacl、20-50mm咪唑的溶液洗去杂质,然后用200mm的咪唑洗脱目的蛋白,随后通过超滤管浓缩蛋白并除去咪唑。
17、所述的单克隆抗体为3株,编码3株单克隆抗体重链可变区的核酸序列如seq idno:3-5所示,轻链可变区的核酸序列如seq id no:6-8所示。
18、所述单克隆抗体的重链为包括igg1和igg2a型,轻链为kappa型。
19、3株单克隆抗体的特异性识别的表位分别为516vgttdrsgvptyswge531(seq id no:9)、527yswgenetdvmllnntr543(seq id no:10)和649gercnledrdrse661(seq id no:11)。
20、所述的单克隆抗体的制备方法,包括以下步骤:
21、选择6-8周龄的balb/c小鼠3只,将纯化后的重组hcv e2蛋白经弗氏完全佐剂乳化,用乳化后的蛋白按每只20μg的用量给小鼠皮下多点注射,3周后加强免疫,更换为弗氏不完全佐剂乳化后的蛋白,按每只20μg的用量注射,加强免疫2次后尾部采血,测定血清抗体效价,当抗体效价达到1万-5万时,则进行单克隆抗体的制备;
22、取小鼠脾脏,使用200目滤网使脾脏变成脾细胞单个悬液,与小鼠骨髓瘤细胞sp2/0混合离心后,使用融合剂peg1500进行细胞融合,在hat选择培养基中培养7-10天,培养至小鼠骨髓瘤细胞sp2/0 3-5×106个;使用纯化的重组hcve2蛋白包被elisa板,吸取细胞上清作为一抗,羊抗鼠作为二抗,检测并筛选阳性杂交瘤细胞,随后利用有限稀释法进行亚克隆,进而筛选到3株单克隆抗体,分别为2f4-5f、3c8-10g、6e3-11b。
23、所述的单克隆抗体在hcv疫苗制备中的应用。
24、本发明的有益效果:
25、本发明利用hcv包膜糖蛋白e2在真核系统中以正确的空间折叠构象表达。通过细胞融合技术建立了小鼠单克隆细胞系,并通过western blot、免疫荧光检测确定抗体亚型等方法进行表征。最后,根据截短的蛋白片段与mabs的反应确定表位区域,为hcv疫苗的研制提供了理论基础。
26、本发明筛选得到的3株单克隆抗体3c8-10g、6e3-11b、2f4-5f,其效价分别为1:2.0×106、1:2.0×106和1:4.1×106,亲和力常数最高达4.6×108l/mol,3株单克隆抗体能识别3个不同的表位区域。序列比对发现,这3个表位在多个毒株中高度保守,故该3个表位是用于hcv诊断的潜在抗原靶点。
27、本发明建立的3株单克隆抗体具有高亲和力、强特异性等优点,识别的3个b细胞表位为首次报道,且位于e2蛋白的非高变区,在多个毒株序列中高度保守,该3个表位是hcv诊断试剂的潜在应用靶点。
28、本发明通过e2蛋白结构域免疫显性表位区域的确定,对hcv诊断和多肽疫苗的研发具有重要价值。
技术特征:
1.一种hcv e2重组蛋白,其特征在于,其氨基酸序列如seq id no1所示。
2.根据权利要求1所述的hcv e2重组蛋白,其特征在于,编码其基因的核苷酸序列如seq id no2所示。
3.一种权利要求1所述的hcv e2重组蛋白的制备方法,其特征在于,所述方法包括以下步骤:
4.根据权利要求3所述的hcv e2重组蛋白的制备方法,其特征在于,所述的3对引物为:
5.利用权利要求3所述的hcv e2重组蛋白的制备方法,其特征在于,纯化方法为:采用含20mm tris、150mm nacl、20-50mm咪唑的溶液洗去杂质,然后用200mm的咪唑洗脱目的蛋白,随后通过超滤管浓缩蛋白并除去咪唑。
6.一种基于权利要求1所述的hcv e2重组蛋白制备的单克隆抗体,其特征在于,所述的单克隆抗体为3株,编码3株单克隆抗体重链可变区的核酸序列如seq id no:3-5所示,轻链可变区的核酸序列如seq id no:6-8所示。
7.根据权利要求6所述的单克隆抗体,其特征在于,所述单克隆抗体的重链为包括igg1和igg2a型,轻链为kappa型。
8.根据权利要求6所述的单克隆抗体,其特征在于,3株单克隆抗体的特异性识别的表位分别为516vgttdrsgvptyswge531、527yswgenetdvmllnntr543和649gercnledrdrse661。
9.一种权利要求6所述的单克隆抗体的制备方法,其特征在于,该方法包括以下步骤:
10.一种权利要求6-8所述的单克隆抗体在hcv疫苗制备中的应用。
技术总结
本发明涉及一种HCV E2重组蛋白、抗HCV E2蛋白的单克隆抗体及制备方法和应用。本发明利用HCV包膜糖蛋白E2在真核系统中以正确的空间折叠构象表达。通过细胞融合技术建立了小鼠单克隆细胞系,并通过Western blot、免疫荧光检测确定抗体亚型等方法进行表征。最后,根据截短的蛋白片段与mAbs的反应确定表位区域。本发明建立的3株单克隆抗体具有高亲和力、强特异性等优点,识别的3个B细胞表位为首次报道,位于E2蛋白的非高变区,在多个毒株序列中高度保守,这3个表位是HCV诊断试剂的潜在应用靶点。本发明通过E2蛋白结构域免疫显性表位区域的确定,对HCV诊断和多肽疫苗的研发具有重要价值。
技术研发人员:张改平,王爱萍,周景明,陈玉梅,刘红亮,丁培阳,梁超,朱习芳,刘恩平
受保护的技术使用者:龙湖现代免疫实验室
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!