一种基于铜和L-组氨酸配位的手性纳米酶及其制备方法和应用
本发明属于手性催化,具体涉及一种基于铜和l-组氨酸配位的手性纳米酶及其制备方法和对l/d-酪氨醇选择性催化的应用。
背景技术:
1、生命体中大部分的生物化学反应都依赖于天然酶高效且特定的催化作用。天然酶能够调节有机体的代谢,传递遗传信息,维持生命活性以及催化生物化学反应。因其具有很高的催化效率,特别是对手性底物的高效区分,天然酶被广泛应用于工业生产、医疗与生物化学领域。然而,天然酶的固有缺陷,如制备与纯化成本高,运行稳定性差,催化效率依赖反应条件,难以回收及重复利用等,限制了其实际生产应用。为了满足当前巨大的应用需求,成本更低的人工酶作为天然酶的替代品逐渐被开发使用。与天然酶和传统人工酶相比,纳米酶是一种具有类酶活性的纳米材料,具有结构稳定、效率高、活性可调、成本低、可大规模制备和可回收等优点。
2、尽管纳米酶具有很好的应用前景,但现有的纳米酶研究仍面临许多挑战,相比天然酶,纳米酶选择性与特异性较差。此外纳米酶的合成设计与机理研究依旧十分有限,不利于手性纳米酶的进一步发展。因此,提高纳米酶的手性选择性催化效果是当前迫切需要解决的问题。
技术实现思路
1、为了创造高手性选择性的纳米酶,本申请依据纳米酶和天然酶之间存在规律的结构-活性关系,模拟天然酪氨酸酶(tyr)的结构,以金属铜为催化活性位点,l-组氨酸作为手性识别配体,将天然酶的催化原理结合到纳米酶的合成设计中。在这种仿生策略的基础上,成功合成了一种基于铜和l-组氨酸配位的手性纳米酶;同时提供了该手性纳米酶的制备方法,然后还提供了其在选择性催化l/d-酪氨醇上的应用。
2、本发明的技术方案如下:
3、一种基于铜和l-组氨酸配位的手性纳米酶,所述的手性纳米酶,采用氯化铜、l-组氨酸经过水热反应制备得到。
4、进一步地,所述的氯化铜为二水合氯化铜cucl2·2h2o;所述的氯化铜与l-组氨酸所需量的摩尔比为(0.1-10):(1-100)。
5、优选地,所述的氯化铜为二水合氯化铜cucl2·2h2o;所述的氯化铜与l-组氨酸所需量的摩尔比为1:10。
6、优选地,水热反应的条件为:150-230℃下反应8h-18h。
7、本发明的另一目的保护上述基于铜和l-组氨酸配位的手性纳米酶的制备方法,包括以下步骤:
8、(1)称取氯化铜、l-组氨酸,溶解在水或乙醇或n,n-二甲基甲酰胺(dmf)中,搅拌混合均匀,得到混合溶液;
9、(2)将步骤(1)中得到的混合溶液转入水热反应釜中反应,在反应结束后得到悬浊液;
10、(3)冷却至室温,离心去除上层清液,将沉淀用水清洗后离心;干燥后,得到灰棕色粉末,即为cu@l-his手性纳米酶。
11、本发明的另一目的保护上述方法制备的手性纳米酶或者权利要求1所述的手性纳米酶在选择性催化l/d-酪氨醇上的应用。
12、本发明的原理:本发明受天然酪氨酸酶(tyr)活性中心位点结构的启发,以金属铜为催化活性位点,l-组氨酸作为手性识别配体,构建了一种具有高对映体选择性的人工过氧化物酶(cu@l-his)。其核心创新点是cu@l-his对l-酪氨醇(l-tyrosinol)显示出更高的选择性,具有偏向性的亲和力和催化活性。本发明合成的纳米酶粒径在200 nm以下,具有优异的生物相容性,细胞毒性低,在复杂的巨噬细胞环境中也同样展示出对l-酪氨醇的高选择性。
13、本发明的有益效果
14、(1)本发明基于对天然酶结构的合理模拟,利用纳米材料的独特性质,结合天然酶的选择性和纳米酶的稳定性,在纳米体系中构建活性位点与选择位点,使其形成类似天然酶的催化口袋的结构,构造了一种具有高对映体选择性及高催化活性的人工过氧化物酶。
15、(2)相较于已存在的发明中复杂的手性区分纳米酶合成方式,本发明不需要经历多步合成,仅以金属铜为催化位点,l-组氨酸作为手性识别配体,利用两者之间的简单配位,一步合成具有高对映体选择性及高催化活性的手性区分纳米酶。
16、(3)cu@l-his具有比肩天然辣根过氧化物酶(hrp)的过氧化物酶活性,大大提高了手性选择性催化的效率。且cu@l-his对l型异构体显示出更高的选择性,具有偏向性的亲和力和催化活性。
17、(4)这种优异的对映体选择催化能力可以通过紫外吸收光谱和荧光光谱等多种方式进行检测,具有检测稳定性,受外界环境的影响小。
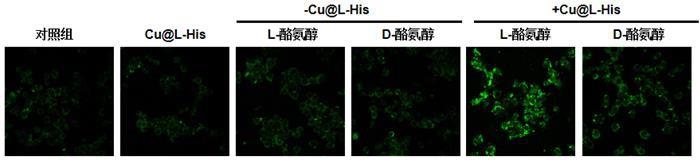
18、(5)本发明具有生物相容性,细胞毒性低,其手性选择性催化能力能够在复杂的细胞环境中实现,cu@l-his在巨噬细胞中也同样展示出对映体选择性催化效果,能够选择性催化更多的l型异构体。
19、(6)本发明制备方法简单快速,无需昂贵的仪器设备;材料绿色环保,制备原料均无生物毒性,制备过程中无需添加有机类表面活性剂等对环境产生影响的试剂;制备成本低廉,原材料成本较低且易得;适合工业化生产。
20、(7)本发明制备的cu@l-his手性纳米酶具有良好的形貌和纳米级别的尺寸,粒径分布均匀,合成过程中无需聚乙烯吡咯烷酮等常用稳定剂的加入。
21、(8)本工作将对手性选择性纳米酶的设计与合成提供新的见解。在手性区分领域具有非常广泛的应用前景。
技术特征:
1.一种基于铜和l-组氨酸配位的手性纳米酶,其特征在于,所述的手性纳米酶,采用氯化铜、l-组氨酸经过水热反应制备得到。
2.根据权利要求1所述的基于铜和l-组氨酸配位的手性纳米酶,其特征在于,所述的氯化铜为二水合氯化铜cucl2·2h2o;所述的氯化铜与l-组氨酸所需量的摩尔比为(0.1-10):(1-100)。
3.根据权利要求1或2所述的基于铜和l-组氨酸配位的手性纳米酶,其特征在于,所述的氯化铜为二水合氯化铜cucl2·2h2o;所述的氯化铜与l-组氨酸所需量的摩尔比为1:10。
4.根据权利要求1所述的基于铜和l-组氨酸配位的手性纳米酶,其特征在于,水热反应的条件为:150-230℃下反应8h-18h。
5.权利要求1-4任一所述的基于铜和l-组氨酸配位的手性纳米酶的制备方法,其特征在于,包括以下步骤:
6.采用权利要求5所述的方法制备的手性纳米酶或者权利要求1所述的手性纳米酶在选择性催化l/d-酪氨醇上的应用。
技术总结
本发明属于手性催化技术领域,具体涉及一种基于铜和L‑组氨酸配位的手性纳米酶及其制备方法和对L/D‑酪氨醇选择性催化的应用。依据纳米酶和天然酶之间存在规律的结构‑活性关系,模拟天然酪氨酸酶(TYR)的结构,以金属铜为催化活性位点,L‑组氨酸作为手性识别配体,将天然酶的催化原理结合到纳米酶的合成设计中。在这种仿生策略的基础上,成功合成了一种基于铜和L‑组氨酸配位的手性纳米酶;同时提供了该手性纳米酶的制备方法,然后还提供了其在选择性催化L/D‑酪氨醇上的应用。
技术研发人员:孔维恒,聂玲玉,渠凤丽,赵岩,张丽媛,赵明珠
受保护的技术使用者:曲阜师范大学
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!