一种跨膜蛋白41B(TMEM41B)基因敲除小鼠动物模型的构建方法和应用
本发明属于生物医药,具体涉及一种跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型的构建方法以及通过该构件方法得到的跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型在血管内膜新生或冠状动脉狭窄疾病研究中的应用,还涉及一种跨膜蛋白41b(tmem41b)作为药物靶点在制备用于治疗血管内膜新生或冠状动脉狭窄的药物中的应用。
背景技术:
1、心血管病是近十年来威胁人类健康的全球性疾病,心肌缺血导致的心力衰竭在心血管疾病中占有重要地位。冠状动脉狭窄是引起心肌缺血的主要原因,经皮冠状动脉介入治疗(pci)、球囊血管成形术或冠状动脉搭桥术(cabg)是治疗狭窄性动脉粥样硬化病变最常见的血管重建治疗策略。冠状动脉狭窄患者及时送往医院手术治疗,实现血流再通,有着立竿见影的效果。但是,这些血管介入性手术(包括治疗血管狭窄和闭塞的经皮腔内血管成形术和血管支架植入术等)不可避免的会损伤血管内膜,引发血管内膜新生。内膜的异常新生是患者支架内再狭窄的重要原因,也是预后不良的关键因素。研究发现,接受pci治疗的患者发生再狭窄的发生率最高可达50%,甚至部分患者需要在6个月内进一步接受血管重建手术。这无疑是对患者在精神、身体以及经济上再次打击。因此进一步探寻血管内膜新生机制并筛选干预靶点是一项具有积极意义的临床课题。
2、血管内膜新生在支架术后再狭窄的发生中扮演重要角色,同时也是动脉粥样硬化、静脉移植、高血压等疾病的共同病理学基础。血管平滑肌细胞具有很强的可塑性,在病理刺激下会发生表型转化,即由原来的收缩型细胞转化为合成型细胞(以高增殖、迁移和蛋白合成能力为特征)。平滑肌细胞的表型转化是血管内膜新生必经病理学过程。既往研究发现,内膜新生的主要原因是平滑肌细胞会发生过度增殖与迁移。因此,阐明血管平滑肌细胞过度增殖的分子机制,并有效抑制血管内膜新生,对研发干预血管再狭窄的药物、优化治疗措施、提高患者术后生存质量至关重要。
3、tmem41b(跨膜蛋白41b,也称为stasimon)最初发现是由于脊柱运动神经元(smn)蛋白丧失而引起的剪接功能障碍的靶点。tmem41b同时也是是一种位于内质网(er)的跨膜蛋白,其位于er与线粒体的接触部位。近年研究发现,tmem41b是自噬形成的新型调节分子,同时具有磷脂翻转酶的活性,参与调控脂质稳态。此外,tmem41b也参了黄病毒和冠状病毒(包括sars-cov-2)感染宿主的过程。但是,迄今为止tmem41b血管内膜新生的作用以及机制尚未报道。因此揭示tmem41b在内膜新生过程中的作用以及机制,为治疗内膜新生提供新的思路和靶点。
技术实现思路
1、鉴于此,本发明的目的在于提供一种跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型的构建方法以及通过该构件方法得到的跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型在血管内膜新生或冠状动脉狭窄疾病研究中的应用。
2、为实现上述目的,本发明所采取的解决方案如下:
3、第一个方面,本发明提供一种跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型的构建方法,包括如下步骤:
4、步骤(1),小鼠胚胎细胞中在tmem41b基因的3号和5号外显子插入floxp位点,通过胚胎打靶技术构建tmem41b-floxp转基因小鼠;
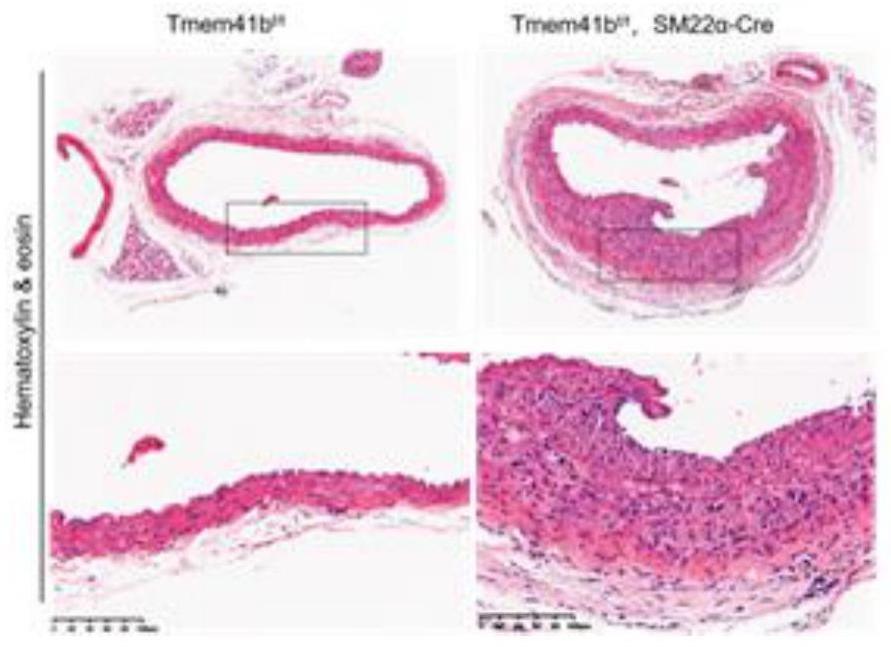
5、步骤(2),根据cre-flox敲除鼠构建系统,运用sm22α-cre工具鼠与tmem41b-floxp转基因小鼠进行杂交繁育,获得平滑肌细胞特异性组成性敲除tmem41b转基因小鼠(tmem41bf/f,sm22α-cre);
6、步骤(3),根据cre-flox敲除鼠构建系统,运用myh11-ertcre工具鼠与tmem41b-floxp转基因小鼠进行杂交繁育,获得平滑肌细胞特异性条件性敲除tmem41b-floxp转基因小鼠(tmem41bf/f,myh11-ert2cre)。
7、优选地,步骤(2)获得的平滑肌细胞特异性组成性敲除tmem41b转基因小鼠(tmem41bf/f,sm22α-cre)饲养至6-8周自发性发生血管内膜新生。
8、优选地,步骤(3)获得的平滑肌细胞特异性条件性敲除tmem41b-floxp转基因小鼠(tmem41bf/f,myh11-ert2cre)饲养至6周,连续腹腔注射tamoxifen(60-100mg/kg)5天,饲养至16周,自发性发生血管内膜新生。
9、第二个方面,本发明还提供一种通过如上所述的跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型的构建方法得到的跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型。
10、第三个方面,本发明还提供一种如上所述的跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型在血管内膜新生或冠状动脉狭窄疾病研究中的应用。
11、第四个方面,本发明提供一种跨膜蛋白41b(tmem41b)作为药物靶点在制备用于治疗血管内膜新生或冠状动脉狭窄的药物中的应用。
12、优选地,血管平滑肌细胞的跨膜蛋白41b的缺失或突变会自发引起血管内膜新生或者由此导致的冠状动脉狭窄疾病、pci后的再狭窄。
13、第五个方面,本发明还提供一种跨膜蛋白41b(tmem41b)的促进剂在制备用于治疗血管内膜新生或冠状动脉狭窄的药物中的应用。
14、第六个方面,本发明还提供一种用于治疗结血管内膜新生或冠状动脉狭窄的药物组合物,所述药物组合物包括药学上可接受的载体和有效量的活性成分,所述活性成分包括如上所述的跨膜蛋白41b(tmem41b)的促进剂。
15、优选地,所述药物组合物的剂型选自片剂、粉剂、注射剂、胶囊、混悬剂、糊剂、凝胶、涂布剂、药膜剂、缓释剂和微球中的任意一种。
16、在本发明中,本发明根据cre-loxp重组酶系统原理构建平滑肌细胞tmem41b特异性敲除小鼠,成功获得转基因敲除鼠,并且发现tmem41b平滑肌细胞缺失的转基因小鼠可自发性发生血管内膜新生。与传统的导丝损伤诱导方法相比,操作简便、疾病模型稳定,并为临床tmem41b缺失病人提供治疗依据,这类人群可能更易发生血管内膜新生导致的冠状动脉狭窄疾病或者pci后的再狭窄。
技术特征:
1.一种跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型的构建方法,其特征在于,包括如下步骤:
2.根据权利要求1所述的方法,其特征在于,步骤(2)获得的平滑肌细胞特异性组成性敲除tmem41b转基因小鼠(tmem41bf/f,sm22α-cre)饲养至6-8周自发性发生血管内膜新生。
3.根据权利要求1所述的方法,其特征在于,步骤(3)获得的平滑肌细胞特异性条件性敲除tmem41b-floxp转基因小鼠(tmem41bf/f,myh11-ert2cre)饲养至6周,连续腹腔注射tamoxifen(60-100mg/kg)5天,饲养至16周,自发性发生血管内膜新生。
4.一种通过权利要求1-3任一项所述的跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型的构建方法得到的跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型。
5.如权利要求4所述的跨膜蛋白41b(tmem41b)基因敲除小鼠动物模型在血管内膜新生或冠状动脉狭窄疾病研究中的应用。
6.跨膜蛋白41b(tmem41b)作为药物靶点在制备用于治疗血管内膜新生或冠状动脉狭窄的药物中的应用。
7.根据权利要求6所述的应用,其特征在于,血管平滑肌细胞的跨膜蛋白41b的缺失或突变会自发引起血管内膜新生或者由此导致的冠状动脉狭窄疾病、pci后的再狭窄。
8.跨膜蛋白41b(tmem41b)的促进剂在制备用于治疗血管内膜新生或冠状动脉狭窄的药物中的应用。
9.一种用于治疗结血管内膜新生或冠状动脉狭窄的药物组合物,其特征在于,所述药物组合物包括药学上可接受的载体和有效量的活性成分,所述活性成分包括如权利要求8所述的跨膜蛋白41b(tmem41b)的促进剂。
10.根据权利要求7所述的药物组合物,其特征在于,所述药物组合物的剂型选自片剂、粉剂、注射剂、胶囊、混悬剂、糊剂、凝胶、涂布剂、药膜剂、缓释剂和微球中的任意一种。
技术总结
本发明属于生物医药技术领域,具体涉及一种跨膜蛋白41B(TMEM41B)基因敲除小鼠动物模型的构建方法以及通过该构件方法得到的跨膜蛋白41B(TMEM41B)基因敲除小鼠动物模型在血管内膜新生或冠状动脉狭窄疾病研究中的应用,还涉及一种跨膜蛋白41B(TMEM41B)作为药物靶点在制备用于治疗血管内膜新生或冠状动脉狭窄的药物中的应用。本发明根据Cre‑loxP重组酶系统原理构建平滑肌细胞TMEM41B特异性敲除小鼠,成功获得转基因敲除鼠,并且发现TMEM41B平滑肌细胞缺失的转基因小鼠可自发性发生血管内膜新生。与传统的导丝损伤诱导方法相比,操作简便、疾病模型稳定,并为临床TMEM41B缺失病人提供治疗依据,这类人群可能更易发生血管内膜新生导致的冠状动脉狭窄疾病或者PCI后的再狭窄。
技术研发人员:孙爱军,洪文轩,葛均波,刘进
受保护的技术使用者:复旦大学附属中山医院
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!