一种可荧光示踪的心肌细胞核酸适配体及其制备方法和应用
本发明属于生物大分子功能化修饰领域,尤其涉及一种可荧光示踪的心肌细胞核酸适配体及其制备方法和应用。
背景技术:
1、人工合成的核酸适配体与蛋白质靶标具有高特异性和亲和性,能够有效抑制蛋白质功能,因此被广泛应用于新药的开发。心肌的收缩和舒张由细胞内ca2+控制,ca2+浓度由肌膜和肌质网(sr)调节。肌质网中的ca2+-atpase2a(serca2a)蛋白负责心脏sr对ca2+的摄取,其活性受另一种心脏sr膜蛋白磷蛋白(pln)调节[参看maclennan等,nat rev mol cellbiol.2003.47:566-577.]。之前,科学家已经通过selex等技术发现了一种对pln具有高亲和力的核酸适配体rna-apt30(简称apt30),其能够通过pln的介导实现对serca2a的抑制[参看sakai h等,j mol cell cardiol.2014,76:177-85.]。因此,核酸适配体apt30的荧光示踪对于其在生物医学领域的应用和推广非常重要,但目前对于apt30荧光功能化修饰还未见报道。
2、金纳米团簇(auncs)是指由十几至几百个金属原子构成的金纳米粒子,不仅粒径小,而且具有与尺寸相关的光致发光等性质。科学家们此前已经报道了一系列具有荧光特性的auncs。荧光auncs作为一种新型的荧光材料,具有易制备、易修饰、尺寸超小、制备条件温和、生物相容性良好等优势,在生化分析、环境检测、医学成像和肿瘤治疗等方面得到广泛应用。
技术实现思路
1、有鉴于此,本发明的目的在于提供一种可荧光示踪的心肌细胞核酸适配体,能够监测其与心肌细胞的结合情况。
2、本发明的目的还在于提供一种可荧光示踪的心肌细胞核酸适配体的制备方法,具有工艺简单、快速高效、质量稳定的优势。
3、为了实现上述发明目的,本发明提供了以下技术方案:
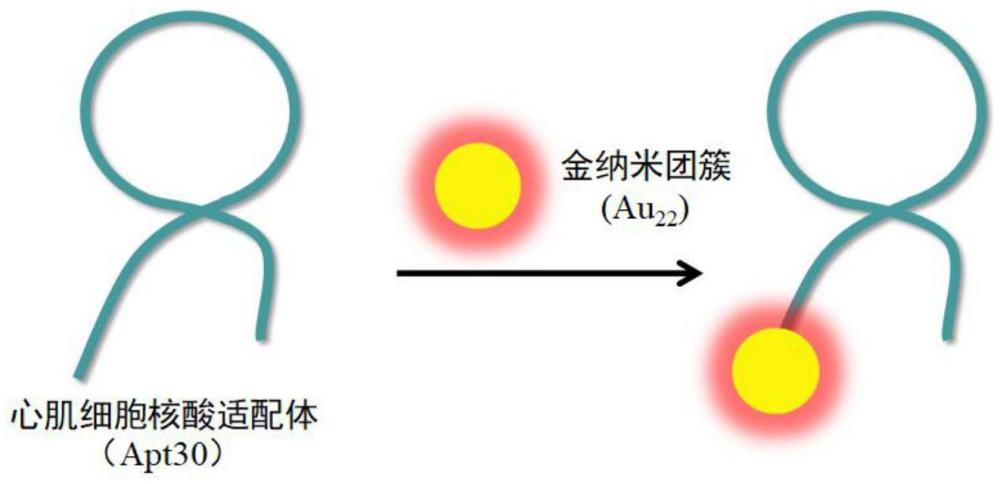
4、本发明提供了一种可荧光示踪的心肌细胞核酸适配体,采用荧光金团簇对心肌细胞核酸适配体进行荧光修饰得到;所述荧光金团簇为au22,所述心肌细胞核酸适配体为apt30。
5、优选的,所述apt30的核酸序列如seq id no.1所示。
6、本发明还提供了上述心肌细胞核酸适配体的制备方法,包括如下步骤:于au22水溶液中加入apt30,磁力搅拌,反应得到apt30-au22粗产物;apt30-au22粗产物于超滤管中离心,滤过液即为apt30-au22。
7、优选的,所述au22水溶液的浓度为8~9μg/ml。
8、优选的,所述apt30的添加量为2~8od/5ml。
9、优选的,所述磁力搅拌转速为450~550r/min。
10、优选的,所述反应温度为25~35℃,所述反应时间为6~24h。
11、优选的,所述超滤管的分子量为50kda。
12、优选的,所述离心转速为4000~5000r/min,离心时间为25~35min。
13、本发明还提供了上述心肌细胞核酸适配体在制备和/或筛选治疗心脏疾病药物中的应用。
14、本发明的有益效果:
15、本发明利用自发荧光的au22实现对核酸适配体荧光修饰,较现有技术通常采用荧光染料而言,产物结构稳定,水溶性好,操作简单,省时省力,能够有效监测核酸适配体与心肌细胞的结合情况,用于制备和/或筛选治疗心脏疾病相关药物。
技术特征:
1.一种可荧光示踪的心肌细胞核酸适配体,其特征在于,采用荧光金团簇对心肌细胞核酸适配体进行荧光修饰得到;所述荧光金团簇为au22,所述心肌细胞核酸适配体为apt30。
2.根据权利要求1所述的心肌细胞核酸适配体,其特征在于,所述apt30的核酸序列如seq id no.1所示。
3.权利要求1~2任意一项所述的心肌细胞核酸适配体的制备方法,其特征在于,包括如下步骤:于au22水溶液中加入apt30,磁力搅拌,反应得到apt30-au22粗产物;apt30-au22粗产物于超滤管中离心,滤过液即为apt30-au22。
4.根据权利要求3所述的制备方法,其特征在于,所述au22水溶液的浓度为8~9μg/ml。
5.根据权利要求3所述的制备方法,其特征在于,所述apt30的添加量为2~8od/5ml。
6.根据权利要求3所述的制备方法,其特征在于,所述磁力搅拌转速为450~550r/min。
7.根据权利要求3所述的制备方法,其特征在于,所述反应温度为25~35℃,所述反应时间为6~24h。
8.根据权利要求3所述的制备方法,其特征在于,所述超滤管的分子量为50kda。
9.根据权利要求3所述的制备方法,其特征在于,所述离心转速为4000~5000r/min,离心时间为25~35min。
10.权利要求1~2任意一项所述的心肌细胞核酸适配体在制备和/或筛选治疗心脏疾病药物中的应用。
技术总结
本发明提供了一种可荧光示踪的心肌细胞核酸适配体及其制备方法和应用,属于生物大分子功能化修饰领域。本发明采用荧光金团簇对心肌细胞核酸适配体进行荧光修饰得到;所述荧光金团簇为Au<subgt;22</subgt;,所述心肌细胞核酸适配体为Apt30。本发明还提供了心肌细胞核酸适配体的制备方法,可以得到结构稳定,水溶性好的Apt30‑Au<subgt;22</subgt;,并且操作简单,省时省力。本发明所述Apt30‑Au<subgt;22</subgt;能够有效监测Apt30与心肌细胞的结合情况,用于制备和/或筛选治疗心脏疾病相关药物。
技术研发人员:李磊,李烨莹,丁佳罗,钱凯,郭佳敏,金梦珊,陈李天,徐晨箫,苏宇,林振坤
受保护的技术使用者:温州医科大学附属第二医院(温州医科大学附属育英儿童医院)
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!