醋酸阿比特龙的合成方法与流程
本发明涉及原料药合成和和中间体合成,具体涉及醋酸阿比特龙的合成方法。
背景技术:
1、醋酸阿比特龙是雄性激素合成中关键酶17α-羟化酶-c17,20-裂合酶(也曾称为类固醇17α-单加氧酶抑制剂或人细胞色素p45017α)的有效选择性口服抑制剂,可用于治疗前列腺癌。2011年4月28日,fda批准醋酸阿比特龙联合泼尼松治疗之前使用过多西他赛化疗患者的转移性去势耐药前列腺癌。醋酸阿比特龙的化学名称为(3β)-17-(3-吡啶基)-雄甾-5,16-二烯-3-醇醋酸酯。
2、目前醋酸阿比特龙的制备主要是通过以下四种方法来制备:
3、①方法一:路线如图1所示,要使用价格很高且毒性较大的三氟甲磺酸酐和二乙基(3-吡啶基)硼烷,二乙基(3-吡啶基)硼烷的合成原料二乙基硼酸甲酯由于闪点较低,易燃易爆,运输不方便。整个工艺副产物很多,不易纯化,因此该工艺不利于工业化生成。
4、②方法二:路线如图2所示,3-吡啶溴化锌制备时需要在-78℃下,因此对于工业化生成还是存在一定限制。
5、③方法三:路线如图3所示,也要用到价格很高二乙基(3-吡啶基)硼烷,另外生产成本高,不利于产业化。
6、④方法四:路线如图4所示,收率偏低,格氏试剂用量大,成本高。
技术实现思路
1、有鉴于此,本发明目的是提供醋酸阿比特龙的合成方法的合成方法,解决上述现有技术问题中的一个或者多个。
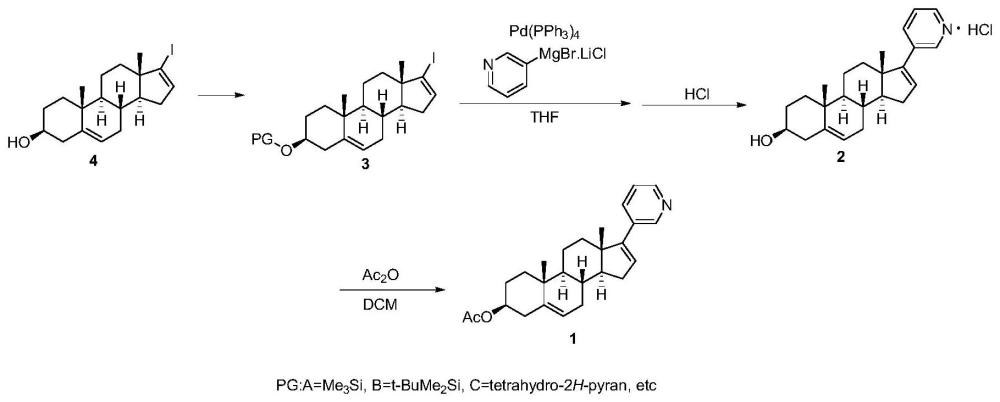
2、为实现上述目的,本发明提供的醋酸阿比特龙的合成方法,包括以下步骤:
3、1)将17-碘-雄甾-5,16-二烯-3β-醇、吡啶或其盐或咪唑中的一种以及有机溶剂加入反应体系,温度控制在20-50℃,在氮气氛围下加入保护剂并搅拌,至原料反应完全,清洗、浓缩、干燥后得到中间产物3,所述中间产物3具有以下结构式:
4、
5、2)将3-溴吡啶和无水氯化锂加入四氢呋喃中,降温至0-5℃,滴加l异丙基氯化镁的四氢呋喃溶液,滴加完毕,升温至室温,搅拌2h,冷却至0-5℃得到格式试剂待用;
6、3)将化合物3、三苯基膦以及四氢呋喃加入反应体系,氮气置换,加入四三苯基膦钯,氮气置换多次,将反应体系加热至50-60℃,滴加格式试剂,滴毕,50-60℃保温4-6h,降温至20℃,滴加水,滴毕后搅拌10-15min,浓缩、过滤、洗涤、干燥后得到中间产物2,所述中间产物2具有以下结构:
7、
8、4)将中间产物2、4-二甲氨基吡啶以及二氯甲烷加入反应体系,搅拌,滴加乙酸酐,滴毕,搅拌,向反应体系加入甲醇,搅拌,加入l-半胱氨酸溶液,搅拌分层,洗涤后分出有机相,浓缩,加入甲醇升温至60℃,脱色、过滤,加入水,降温至25℃,过滤得到目标产物醋酸阿比特龙。
9、在一些实施方式中,所述吡啶盐为对甲苯磺酸吡啶盐。
10、在一些实施方式中,所述有机溶剂为n,n-二甲基甲酰胺、二氯甲烷或甲苯中的一种。
11、在一些实施方式中,所述保护剂为三甲基氯硅烷、叔丁基二甲基氯硅烷或3,4-二氢-2h-吡喃中的一种。
12、在一些实施方式中,所述清洗步骤为使用饱和碳酸氢钠溶液、hci溶液或者碳酸钠溶液中的一种进行清洗。
13、在一些实施方式中,所述步骤3中,所述浓缩、过滤、洗涤、干燥步骤包括:浓缩后加入甲苯,活性炭以及树脂,搅拌,过滤,室温下向滤液滴加浓盐酸,升温至40℃搅拌,降温至室温,过滤,洗涤,将固体转入水中,控制温度至20-30℃,通过氢氧化钠溶液调节ph至9-10,过滤,水洗,加入丙酮,在50-60℃下搅拌2h,降温,过滤、洗涤、烘干得到中间产物2。
14、与现有技术对比,本发明的有益效果在于:
15、提供了一种新的合成醋酸阿比特龙的工艺路线,先对中间体的羟基进行保护,再通过kumada反应来制备醋酸阿比特龙中间体,增加了氯化锂作催化剂,使反应收率大大提高,并在工艺过程中采用了连续化设计,减少了污染,提高了收率,降低了成本。
技术特征:
1.醋酸阿比特龙的合成方法,其特征在于,包括以下步骤:
2.如权利要求1所述的合成方法,其特征在于,所述吡啶盐为对甲苯磺酸吡啶盐。
3.如权利要求1所述的合成方法,其特征在于,所述有机溶剂为n,n-二甲基甲酰胺、二氯甲烷或甲苯中的一种。
4.如权利要求1所述的合成方法,其特征在于,所述保护剂为三甲基氯硅烷、叔丁基二甲基氯硅烷或3,4-二氢-2h-吡喃中的一种。
5.如权利要求1所述的合成方法,其特征在于,所述清洗步骤为使用饱和碳酸氢钠溶液、hcl溶液或者碳酸钠溶液中的一种进行清洗。
6.如权利要求1所述的合成方法,其特征在于,所述步骤3中,所述浓缩、过滤、洗涤、干燥步骤包括:浓缩后加入甲苯,活性炭以及树脂,搅拌,过滤,室温下向滤液滴加浓盐酸,升温至40℃搅拌,降温至室温,过滤,洗涤,将固体转入水中,控制温度至20-30℃,通过氢氧化钠溶液调节ph至9-10,过滤,水洗,加入丙酮,在50-60℃下搅拌2h,降温至20-30℃,过滤、洗涤、烘干得到中间产物2。
技术总结
本发明公开了一种新的合成醋酸阿比特龙的工艺路线,先对中间体的羟基进行保护,再通过Kumada反应来制备醋酸阿比特龙中间体,增加了氯化锂作催化剂,使反应收率大大提高,并在工艺过程中采用了连续化设计,减少了污染,提高了收率,降低了成本。
技术研发人员:汪成进,陈一鸣,何俊丽,权明琦,季平,吕峰
受保护的技术使用者:江苏希迪制药有限公司
技术研发日:
技术公布日:2024/3/12
- 还没有人留言评论。精彩留言会获得点赞!