一种基于KLRB1基因提高动物抗菌及毒素的方法
本发明属于基因工程,具体涉及一种基于klrb1基因提高动物抗猪多杀性巴氏杆菌及其毒素的方法。
背景技术:
1、多杀性巴氏杆菌(pasteurella multocida,pm)是一种革兰阴性兼性厌氧球菌,根据荚膜抗原不同,可分为a、b、d、e、f五个血清群。猪多杀性巴氏杆菌属a与d型,能产生一种多杀性巴氏杆菌皮肤坏死毒素(pasteurella multocida toxin,pmt),该毒素是由toxa基因编码的大小约为146kda的不耐热蛋白质。该毒素是猪萎缩性鼻炎的主要毒力因子,对小鼠的ld50为0.2μg/kg,对猪的ld100为40μg/kg。猪多杀性巴氏杆菌属于条件致病菌,当猪场广泛使用抗生素时一般不会引起该病的大爆发,但随着抗生素的滥用,造成了耐药菌株的产生。
2、由klrb1基因编码的cd161蛋白是一种潜在的抑制性受体,使用crispr/cas9基因编辑技术使t细胞中的klrb1基因失活,能够增强了t细胞对肿瘤细胞的杀伤作用。目前并未有关于klrb1基因及其编码的蛋白在动物抗病育种中的报道,针对宿主基因来优化抗病育种的领域还处于空白。
技术实现思路
1、本发明所要解决的技术问题为:提供一种提高动物抗猪多杀性巴氏杆菌的方法。
2、本发明的技术方案为:
3、抗klrb1蛋白抗体或klrb1基因敲除载体或klrb1基因沉默载体在制备提高动物对猪多杀性巴氏杆菌和/或猪多杀性巴氏杆菌毒素抗性的产品中的应用。
4、进一步地,所述klrb1蛋白的氨基酸序列如seq id no.1所示。
5、进一步地,所述抗klrb1蛋白抗体为兔抗klrb1蛋白抗体。
6、进一步地,所述klrb1基因的cds序列如seq id no.2所示。
7、进一步地,所述动物为猪或小鼠。
8、一种构建抵抗猪多杀性巴氏杆菌和/或猪多杀性巴氏杆菌毒素动物模型的方法,包括使动物缺失编码klrb1蛋白的基因。本发明对使动物缺失编码klrb1蛋白的基因的方式没有严格要求,采用常规技术手段即可,如通过基因编辑敲除或rnai沉默动物的klrb1基因。
9、进一步地,所述动物模型为猪或小鼠模型。
10、与现有技术相比,本发明具有以下有益效果:
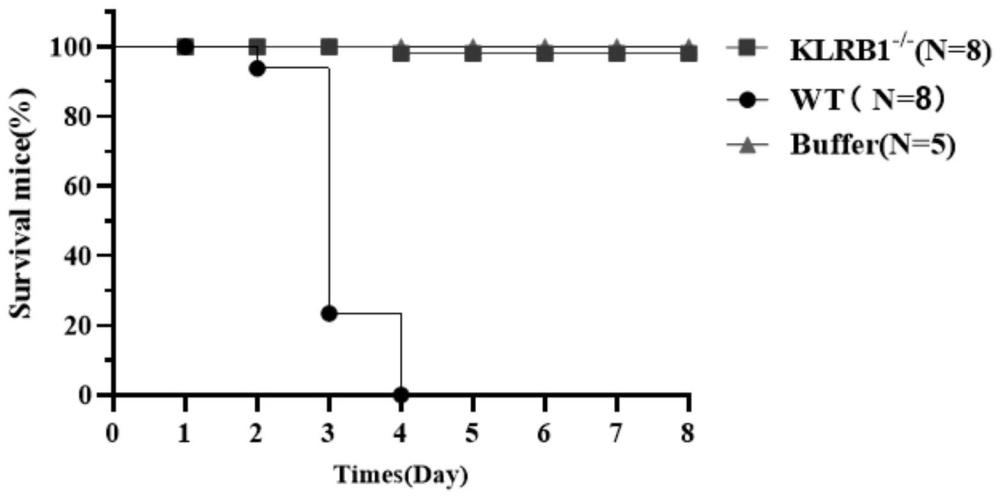
11、本发明首次证明了klrb1蛋白与猪多杀性巴氏杆菌及重组猪多杀性巴氏杆菌毒素对动物的致命作用相关,klrb1蛋白缺失或缺失编码klrb1蛋白的基因的动物能够抵抗猪多杀性巴氏杆菌及重组猪多杀性巴氏杆菌毒素的致命作用。因此,抗klrb1蛋白抗体或klrb1基因敲除载体或klrb1基因沉默载体,能够阻断猪多杀性巴氏杆菌和/或猪多杀性巴氏杆菌毒素对动物的致命作用。通过开发klrb1基因敲除动物,能提高动物对多杀性巴氏杆菌的抗病能力。
技术特征:
1.抗klrb1蛋白抗体或klrb1基因敲除载体或klrb1基因沉默载体在制备提高动物对猪多杀性巴氏杆菌和/或猪多杀性巴氏杆菌毒素抗性的产品中的应用。
2.根据权利要求1所述的应用,其特征在于,所述klrb1蛋白的氨基酸序列如seq idno.1所示。
3.根据权利要求1所述的应用,其特征在于,所述抗klrb1蛋白抗体为兔抗klrb1蛋白抗体。
4.根据权利要求1所述的应用,其特征在于,所述klrb1基因的cds序列如seq idno.2所示。
5.根据权利要求1所述的应用,其特征在于,所述动物为猪或小鼠。
6.一种构建抵抗猪多杀性巴氏杆菌和/或猪多杀性巴氏杆菌毒素动物模型的方法,其特征在于,通过基因编辑敲除或rnai沉默动物的klrb1基因。
7.根据权利要求1所述的方法,其特征在于,所述动物模型为猪或小鼠模型。
技术总结
本发明公开了一种基于KLRB1基因提高动物抗菌及毒素的方法,属于基因工程技术领域;本发明首次证明了KLRB1蛋白与猪多杀性巴氏杆菌及重组猪多杀性巴氏杆菌毒素对动物的致命作用相关,KLRB1蛋白缺失或缺失编码KLRB1蛋白的基因的动物能够抵抗猪多杀性巴氏杆菌及重组猪多杀性巴氏杆菌毒素的致命作用。因此,抗KLRB1蛋白抗体或KLRB1基因敲除载体或KLRB1基因沉默载体,能够阻断猪多杀性巴氏杆菌和/或猪多杀性巴氏杆菌毒素对动物的致命作用,加快动物抗病育种进程。
技术研发人员:曹三杰,袁建林,赵勤,黄小波,杜森焱,王一平,文翼平,颜其贵,伍锐,郎一飞
受保护的技术使用者:四川农业大学
技术研发日:
技术公布日:2024/5/8
- 还没有人留言评论。精彩留言会获得点赞!