微流控芯片及体外检测系统的制作方法
本实用新型涉及体外诊断技术领域,尤其是涉及一种微流控芯片及体外检测系统。
背景技术:
体外诊断行业(invitrodiagnosis,ivd)属于医药生物行业,是指将血液、体液、组织等样本从人体中取出,使用体外检测试剂、仪器等对样本进行检测与校验,以便对疾病进行预防、诊断、治疗检测、后期观察、健康评价、遗传疾病预测等。体外诊断按照方法学分为生化诊断、免疫诊断和分子诊断三大类,以及从生化、免疫和分子诊断中分化出来的床旁快速诊断poct。干化学反应是生化诊断的一种,是利用生化试剂与特定的底物反应,再通过仪器定量检测出标的物浓度,推算出人体的某些生化指标。传统生化诊断需要在大型生化仪上进行检测,由此导致试剂消耗多、灵活性不够等问题;一般的干式生化poct诊断方式则在测试通量上较低,一般一次只能测验一个或几个样本、一个或几个项目。微流控芯片技术(microfluidics)能把生物、化学、医学分析过程的样品制备、反应、分离、检测等基本操作单元集成在芯片上,自动完成分析全过程,极大的提高了检测效率,同时具有小型化、自动化等优点,因而在poct领域中应用越来越广泛。
在生化检测领域中,以美国的abaxis公司为代表,率先开发了用于生化检测的微流控芯片,国内如天津微纳芯、成都斯马特等都有类似微流控芯片开发。传统产品的芯片对全血样本的定量与分配过程,往往需要将全血的分离和血清的定量过程分开,因此需要进行多次的离心分离和定量,使得样本处理的时间比较长,导致检测时间过于延长。
技术实现要素:
基于此,有必要提供一种能够提高样本处理效率的微流控芯片和含有该微流控芯片的体外检测系统。
一种微流控芯片,具有分离定量单元,所述分离定量单元包括加样腔体、第一连接微流道、定量腔体、第一废液腔体、溢流微流道和第二废液腔体;所述加样腔体具有加样孔;所述定量腔体通过所述第一连接微流道与所述加样腔体连通;所述第一废液腔体与所述定量腔体连通;所述第二废液腔体通过所述溢流微流道与所述定量腔体连通;
所述分离定量单元具有在离心时靠近旋转中心的近心端;所述加样腔体较所述定量腔体靠近所述近心端;所述定量腔体较所述第一废液腔体靠近所述近心端;当所述定量腔体中填满液体后,多余的液体能够经由所述溢流微流道进入所述第二废液腔体,所述第二废液腔体整体距离所述近心端的距离不大于所述定量腔体距离所述近心端的距离。
在其中一个实施例中,所述加样孔较所述加样腔体与所述第一连接微流道的连接位置更靠近所述近心端。
在其中一个实施例中,所述加样腔体还具有第一透气孔,所述第一透气孔较所述加样腔体与所述第一连接微流道的连接位置更靠近所述近心端。
在其中一个实施例中,所述加样腔体与所述第一连接微流道的连接处呈漏斗状。
在其中一个实施例中,所述微流控芯片还包括质控腔体,所述质控腔体与所述第二废液腔体连通,所述质控腔体较所述第二废液腔体远离所述近心端。
在其中一个实施例中,所述微流控芯片还包括与所述第二废液腔体连通的第二连接微流道,所述第二连接微流道自与所述第二废液腔体连接的一端逐渐向靠近所述近心端的方向延伸,并在另一端设有第二透气孔。
在其中一个实施例中,所述微流控芯片还包括第三连接微流道,所述第一废液腔体通过所述第三连接微流道与所述定量腔体连通。
在其中一个实施例中,所述微流控芯片还包括出液微流道,所述出液微流道的一端与所述定量腔体连通,另一端具有渗透孔。
在其中一个实施例中,所述出液微流道包括毛细流道,所述毛细流道的一端与所述第三连接微流道连接,另一端设有所述渗透孔;
所述毛细流道自与所述第三连接微流道连接的一端逐渐向靠近所述近心端的方向延伸并弯折后向远离所述近心端的方向延伸;所述毛细流道的弯折顶点位置较所述定量腔体与所述第一连接微流道的连接位置处更靠近所述近心端。
在其中一个实施例中,所述出液微流道还包括第四连接微流道,所述第四连接微流道的一端与所述第三连接微流道连接,另一端与所述毛细流道连接。
在其中一个实施例中,所述第四连接微流道自与所述第三连接微流道连接的一端逐渐向靠近所述近心端的方向延伸以与所述毛细流道连接。
在其中一个实施例中,各所述微流控芯片上设有一个所述分离定量单元。
在其中一个实施例中,所述微流控芯片上还具有用于安装在离心设备上的卡接部。
在其中一个实施例中,所述卡接部位于所述近心端。
一种体外检测系统,包括上述任一实施例所述的微流控芯片和检测机构,所述检测机构与所述定量腔体连通,所述检测机构用于检测所述定量腔体内的样本。
在其中一个实施例中,所述体外检测系统还包括用于安装在离心设备上的离心托盘,所述离心托盘上设有用于放置所述微流控芯片的安装位。
在其中一个实施例中,所述离心托盘的中部具有旋转安装部,所述安装位有多个,多个所述安装位围绕所述旋转安装部设置。
在其中一个实施例中,所述离心托盘在所述安装位设有至少一个用于观察所述微流控芯片状态和/或检测结果的观察孔。
在其中一个实施例中,所述检测机构为干化学试纸。
在其中一个实施例中,所述干化学试纸包括支撑层和在所述支撑层上依次层叠设置的反应指示层和扩散层,所述反应指示层中含有能够与待测样本中目标物质反应的反应试剂和指示试剂,所述扩散层通过所述进样口面向于所述渗透孔。
在其中一个实施例中,所述微流控芯片围绕所述分离定量单元的渗透孔设有安装槽,所述检测机构镶嵌在各所述安装槽中。
上述微流控芯片的分离定量单元具有加样腔体、第一连接微流道、定量腔体、第一废液腔体、溢流微流道和第二废液腔体,各腔体与微流道配合构成连通器的结构,在向加样腔体中加入样本溶液后,通过旋转离心,样本溶液经由第一连接微流道进入定量腔体和第一废液腔体中,并逐渐填满第一废液腔体和定量腔体,多余的样本溶液经由溢流微流道溢流进入第二废液腔体中,通过进一步离心可以将样本溶液中的固体杂质等与待测溶液分离,固体杂质等被离心沉淀至第一废液腔体中,待测溶液留在靠近于近心端的定量腔体中,从而实现对样本溶液的分离和定量。需要检测时,可以使用检测机构对定量腔体中定量的待测溶液进行检测。
该微流控芯片在加入样本溶液后只需要一次离心就可以实现样本溶液中杂质和目标待测溶液的分离和定量,无需过多的离心操作,因而操作简便,需要等待的时间短,样本处理的效率显著提高。
进一步,该微流控芯片设置有包括毛细流道的出液微流道,毛细流道自与第三连接微流道连接的一端逐渐向靠近近心端的方向延伸并弯折后向远离近心端的方向延伸,并且毛细流道的弯折顶点位置较定量腔体与第一连接微流道的连接位置处更靠近于近心端,这样在样本溶液的离心分离和定量时,由于离心力大于毛细流道内的毛吸力,样本溶液不会突破毛细流道的弯折顶点,该毛细流道即可起到“阀门”的关闭作用,后续在检测时,在低速离心的情况下,存在定量腔体内的待测溶液就会在毛吸力的作用下沿毛细流道不断前进,并突破毛细流道的弯折顶点位置,“阀门”打开,在虹吸作用下,待测溶液继续前进并渗透孔渗出至检测机构被检测。
通过毛细流道来作为控制样本与检测机构接触反应的阀门,可以代替传统的水溶性膜或阀门等延时打开机构,使进样检测过程更加稳定可靠,同时简化了芯片组装工艺,有利于降低生产成本。
更进一步,通过采用微流控芯片与离心托盘相分离的形式,一个离心托盘上可自由装配多个微流控芯片,实现对检测项目和检测样本的自由搭配,有利于整体提高体外检测系统的灵活性。
附图说明
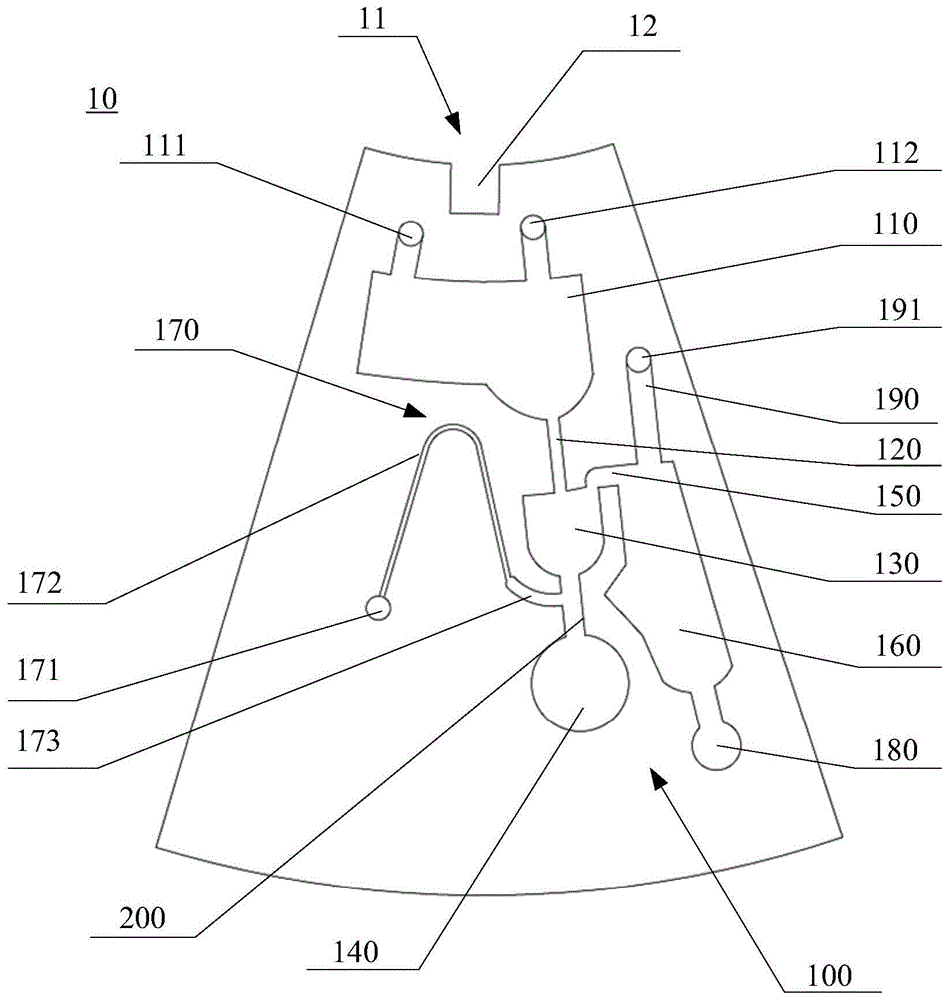
图1、图2和图3分别为本实用新型一实施例的微流控芯片的正面、背面和侧面示意图;
图4和图5分别为与图1所示微流控芯片相匹配的离心托盘的正面和背面结构示意图;
图6为图1所示微流控芯片与图4所示离心图片的组装示意图;
图7-1、图7-2和图7-3分别为图1所示微流控芯片实现对样本溶液的分离和定量的流程示意图,图7-2-1为局部放大示意图;
图8-1和图8-2分别为使用图1所示微流控芯片的检测流程示意图。
附图标记说明如下:
10:微流控芯片,11:近心端,12:卡接部;13:芯片本体,14:透明盖膜,15:安装槽;
100:分离定量单元,110:加样腔体,111:加样孔,112:第一透气孔,120:第一连接微流道,130:定量腔体,140:第一废液腔体,150:溢流微流道,160:第二废液腔体,170:出液微流道,171:渗透孔,172:毛细流道,172a、172b和172c分别为毛细流道的不同位置,173:第四连接微流道,180:质控腔体,190:第二连接微流道,191:第二透气孔,200:第三连接微流道;
20:离心托盘,21:安装位,22:旋转安装部,23:检测孔,24:质控孔。
具体实施方式
为了便于理解本实用新型,下面将参照相关附图对本实用新型进行更全面的描述。附图中给出了本实用新型的较佳实施例。但是,本实用新型可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本实用新型的公开内容的理解更加透彻全面。
需要说明的是,当元件被称为“设于”另一个元件,它可以直接在另一个元件上或者也可以存在居中的元件。当一个元件被认为是“连接”、“连通”另一个元件,它可以是直接连接到另一个元件或者可能同时存在居中元件。
除非另有定义,本文所使用的所有的技术和科学术语与属于本实用新型的技术领域的技术人员通常理解的含义相同。本文中在本实用新型的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本实用新型。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
请结合图1和图2,本实用新型一实施例提供了一种微流控芯片10,其具有分离定量单元100。分离定量单元100包括加样腔体110、第一连接微流道120、定量腔体130、第一废液腔体140、溢流微流道150和第二废液腔体160。
加样腔体110具有加样孔111。样本溶液可自加样孔111加入至加样腔体110中。定量腔体130通过第一连接微流道120与加样腔体110连通。定量腔体130用于实现待测溶液的定量。第一废液腔体140与定量腔体130连通。第一废液腔体140用于填装多余的样本溶液和分离后的固定杂质沉淀等。第二废液腔体160通过溢流微流道150与定量腔体130连通。第二废液腔体160用于填装多余的样本溶液。
在本实施例中,分离定量单元100具有在离心时靠近旋转中心的近心端11。加样腔体110较定量腔体130靠近近心端11。定量腔体130较第一废液腔体140靠近近心端11。当定量腔体130中填满液体后,多余的液体能够经由溢流微流道150进入第二废液腔体160,第二废液腔体160整体距离近心端11的距离不大于定量腔体130距离近心端11的距离。
在向加样腔体110中加入样本溶液后,通过旋转离心,样本溶液可经由第一连接微流道120进入定量腔体130和第一废液腔体140中,并逐渐填满第一废液腔体140和定量腔体130,多余的样本溶液经由溢流微流道150溢流进入第二废液腔体160中,通过进一步离心可以将样本溶液中的固体杂质等与待测溶液分离(例如将全血样本中的血细胞与血清(血浆)分离),固体杂质等被离心沉淀至第一废液腔体140中,待测溶液留在靠近于近心端11的定量腔体130中,从而实现对样本溶液的分离和定量。需要检测时,可以使用检测机构对定量腔体130中定量的待测溶液进行检测。
该微流控芯片10在加入样本溶液后只需要一次离心就可以实现样本溶液中杂质和目标待测溶液的分离和定量,无需过多的离心操作,因而操作简便,需要等待的时间短,样本处理的效率显著提高。
在一个具体示例中,加样孔111较加样腔体110与第一连接微流道120的连接位置更靠近近心端11,这样可以避免在离心操作时,样本溶液自加样孔111倒流出去。
在一个具体示例中,加样腔体110还具有第一透气孔112,第一透气孔112较加样腔体110与第一连接微流道120的连接位置更靠近近心端11。通过设置第一透气孔112,在加样时,可以及时有效地将加样腔体110中的空气排出,保证加样的顺利进行。
在一个具体示例中,加样腔体110与第一连接微流道120的连接处呈漏斗状,这样更有利于将加样腔体110中的样本溶液经由第一连接微流道120导入至定量腔体130中。
在其中一个实施例中,该微流控芯片10还包括质控腔体180。质控腔体180与第二废液腔体160连通,质控腔体180较第二废液腔体160远离近心端11。进入第二废液腔体160中的样本溶液是在定量腔体130中充满样本后才会流入的,多余的样本溶液在第二废液腔体160中会进一步流入至远离近心端11的质控腔体180中,通过观察质控腔体180中有无液体,即可判断定量腔体130中是否填满样本溶液。
在一个具体示例中,该微流控芯片10还包括与第二废液腔体160连通的第二连接微流道190,第二连接微流道190自与第二废液腔体160连接的一端逐渐向靠近近心端11的方向延伸,并在另一端设有第二透气孔191。通过在第二废液腔体160的靠近近心端11的一侧设置第二透气孔191,可以在样本溶液溢流至第二废液腔体160中时,及时将第二废液腔体160中的空气排出,保证溢流的顺利进行。
在一个具体示例中,微流控芯片10还包括第三连接微流道200,第一废液腔体140通过第三连接微流道200与定量腔体130连通。通过设置第三连接微流道200,可以将第一废液腔体140与定量腔体130隔开,避免第一废液腔体140中沉积的杂质进入定量腔体130中。
在一个具体示例中,该微流控芯片10还包括出液微流道170。出液微流道170的一端与定量腔体130连通,另一端具有渗透孔171。出液微流道170用于将定量腔体130中定量的待测溶液自渗透孔171导出至检测机构中。
进一步,出液微流道170包括毛细流道172。毛细流道172的一端与第三连接微流道200连接,另一端设有渗透孔171。进一步,毛细流道172自与第三连接微流道200连接的一端逐渐向靠近近心端11的方向延伸并弯折后向远离近心端11的方向延伸。毛细流道172的弯折顶点位置较定量腔体130与第一连接微流道120的连接位置处更靠近近心端11。通过设置毛细流道172,毛细流道172可以起到“阀门”的作用,在样本溶液的分离和定量时,“阀门”关闭,待测样本溶液不会突破毛细流道172的弯折顶点而从渗透孔171渗透出;在后续检测时,在毛细流道172的毛细力的作用下,配合低速离心,定量在定量腔体130中的待测溶液会在虹吸作用下,沿毛细流道172不断前进,并可自渗透孔171渗出被检测。
在一个具体示例中,该出液微流道170还包括第四连接微流道173。第四连接微流道173的一端与第三连接微流道200连接,另一端与毛细流道172连接。通过设置第四连接微流道173,可以在检测时,更便于将定量腔体130中定量的待测溶液导入至毛细流道172中。优选地,第四连接微流道173自与第三连接微流道200连接的一端逐渐向靠近近心端11的方向延伸以与毛细流道172连接。
在样本溶液的离心分离和定量时,由于离心力大于毛细流道172内的毛吸力,样本溶液不会突破毛细流道172的弯折顶点,该毛细流道172即可起到“阀门”的关闭作用,后续在检测时,在低速离心的情况下,存在定量腔体130内的待测溶液就会在毛吸力的作用下沿毛细流道172不断前进,并突破毛细流道172的弯折顶点位置,“阀门”打开,在虹吸作用下,待测溶液继续前进并渗透孔171渗出至检测机构被检测。
通过毛细流道172来作为控制样本与检测机构接触反应的阀门,可以代替传统的水溶性膜或阀门等延时打开机构,使进样检测过程更加稳定可靠,同时简化了芯片组装工艺,有利于降低生产成本。
在一个具体示例中,各微流控芯片10上设有一个分离定量单元100。该微流控芯片10整体上可呈但不限于扇形的结构,可以安装在离心托盘等装置上,实现对样本的单项目检测。
进一步,在一个具体示例中,微流控芯片10上还具有用于安装在离心设备上的卡接部12。卡接部12用于卡接在外接的离心托盘等装置上,具有定位和稳定装配的功能。
更具体地,在一个示例中,该卡接部12可位于但不限于微流控芯片10的近心端11。
如图3所示,在一个具体示例中,微流控芯片10包括芯片本体13和覆盖在芯片本体13上的透明盖膜14。芯片本体13与透明盖膜14配合形成各腔体结构和流道结构。具体地,各腔体结构和流道结构的沟槽等均预形成在芯片本体13上,如图2所示,各孔均开口在芯片本体13的背面,而各腔体结构和流道结构的沟槽则开口在芯片本体13的正面,后续通过透明盖膜12覆盖并密封在芯片本体11的正面即可形成完成对腔体结构和流道结构的封装,形成完整的腔体结构和流道结构。
透明盖膜14可以是但不限于透明胶带或者透明压敏胶等,其与芯片本体13配合构成整个微流控芯片10,装配简单,无需使用复杂、昂贵的超声焊接技术,直接粘接即可,可以显著降低制作成本。可理解,在其他具体示例中,微流控芯片10也可以采用成本较高的超声焊接技术焊接形成,或者采用3d打印技术一体成型。
本实用新型进一步还提供了一种体外检测系统,其包括上述微流控芯片10和检测机构,检测机构通过渗透孔171与定量腔体130连通,检测机构用于检测定量腔体130内的样本。
在一个具体示例中,检测机构为干化学试纸。更具体地,干化学试纸包括支撑层和在支撑层上依次层叠设置的反应指示层和扩散层,反应指示层中含有能够与待测样本中目标物质反应的反应试剂和指示试剂,扩散层通过进样口面向于渗透孔171。可理解,在其他具体示例中,检测机构也不限于干化学试纸,也可以是各类其他试纸条或者反应器等。
在一个具体示例中,如图2所示,微流控芯片10围绕分离定量单元100的渗透孔171设有安装槽15,检测机构镶嵌在各安装槽15中。
在一个具体示例中,如图4、图5和图6所示,该体外检测系统还进一步包括用于安装在离心设备上的离心托盘20。离心托盘20上设有用于放置微流控芯片10的安装位21。
更具体地,该离心托盘20的中部具有旋转安装部22。安装位21有多个,多个安装位21围绕旋转安装部22设置。
更进一步,该离心托盘20在安装位21设有至少一个用于观察微流控芯片10状态和/或检测结果的观察孔。例如在图示的具体示例中,该离心托盘20对应于检测机构设有检测孔23,并设有用于观察质控腔体180状态的质控孔24。
以下以图1所示的具体微流控芯片和图4所述的离心托盘对全血样本进行检测为例,对样本溶液的分离和定量以及检测过程进行进一步详细的说明。该离心托盘20上可安装多个微流控芯片10,可根据具体的检测项目需求和样本需求安装相应数量的微流控芯片10,对于缺位情况,可使用空白的微流控芯片10填补,以保证离心托盘20各位置处的基本平衡。
微流控芯片10实现对全血样本的分离和定量过程可参考但不限于如下:
如图7-1所示,将全血样本经由加样孔111加入至加样腔体110中,将离心托盘20安装至具有离心功能的检测设备上,开启设备,转动离心托盘20。
如图7-2所示,随着离心的进行,加样腔体110中的全血样本经由第一连接微流道120进入定量腔体130和第一废液腔体140中,多余的全血样本经由溢流微流道150进入质控腔体180和第二废液腔体160中,当检测到质控腔体180中有全血样本时,说明定量腔体13中填充满全血样本。如图7-2-1所示,由于毛细流道172的弯折顶点位置较定量腔体130的最上方更靠近于近心端11,在高速离心(如4000-6000rpm)时,离心力大于毛细流道172中毛吸力,全血样本溶液只会进入毛细流道172的172a段,而不会突破毛细流道172的弯折顶点172b而流至172c段。
如图7-3所示,继续离心过程,填装在定量腔体130中的全血样本中血细胞会与血清(血浆)分离被沉积在第一废液腔体140中,进而实现了全血样本的分离和定量。
使用该微流控芯片10实现对全血样本的检测过程可参考但不限于如下:
如图8-1和图8-2所示,在全血样本定量结束后,暂停转动离心托盘20,定量在定量腔体130中的血清(血浆)会在毛细流道172的毛吸力的作用下不断沿着毛细流道172前进,并突破毛细流道172的弯折顶点172b处,优选地,开启设备低速离心(如1000-2500rpm),血清(血浆)从毛细流道172的172c段自渗透孔171渗出,在虹吸作用下,定量腔体130中的血清(血浆)不断排出直至全部排空而被检测。
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述实施例仅表达了本实用新型的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对实用新型专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本实用新型构思的前提下,还可以做出若干变形和改进,这些都属于本实用新型的保护范围。因此,本实用新型专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!