基于荧光染料作为内标物的化学发光免疫分析法及其应用的制作方法
本发明涉及新型纳米材料研究应用以及预防与诊断医学检验领域
技术领域:
,尤其涉及一种基于荧光染料作为内标物的化学发光免疫分析法及其应用。
背景技术:
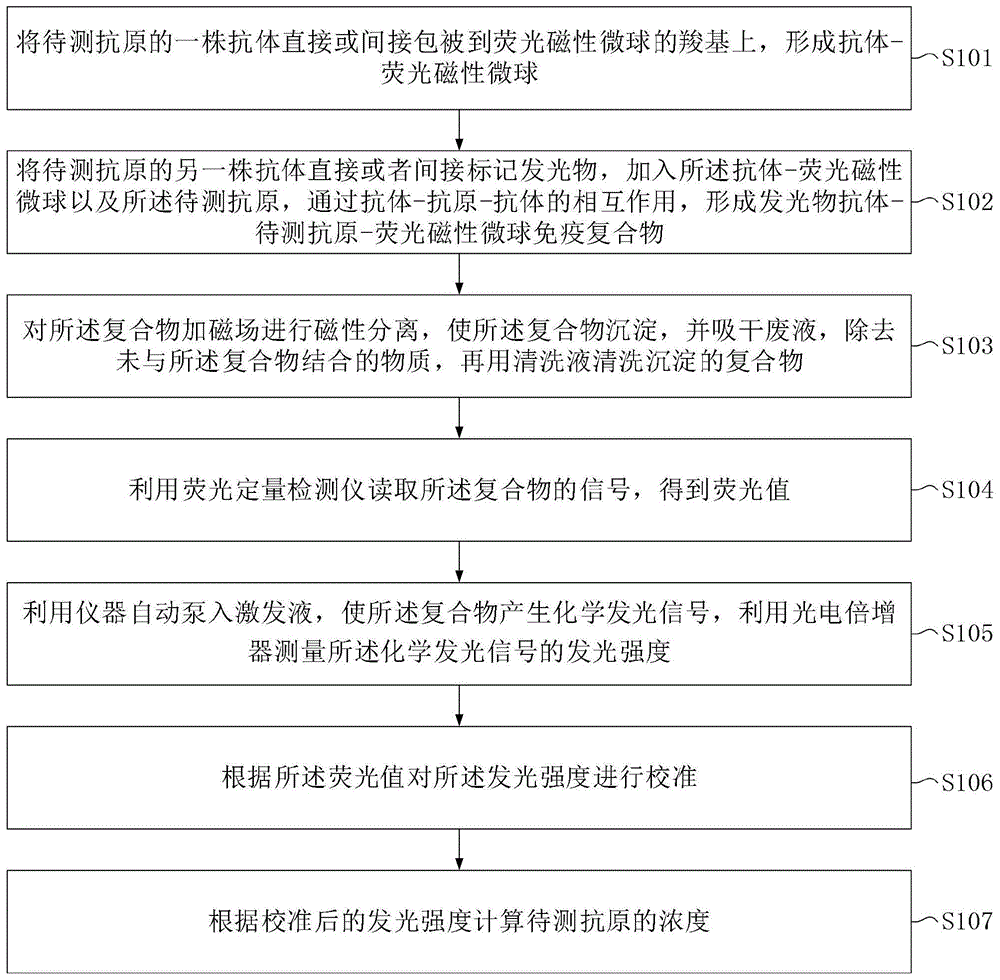
:化学发光免疫分析法是将具有高灵敏度的化学发光测定技术与高特异性的免疫反应相结合,用于各种抗原、半抗原、抗体、激素、酶、脂肪酸、维生素和药物等的检测分析技术。化学发光免疫分析法是继放免分析、酶免分析、荧光免疫分析和时间分辨荧光免疫分析之后发展起来的一项最新免疫测定技术。化学发光免疫分析法实际上是利用化学发光的原理而建立起来的一种免疫分析方法。化学发光免疫分析法的特点较为明显,主要表现在化学发光不需要任何光源,同时在实践的过程中,化学发光免疫分析法与其他方法相比较,其灵敏度也较高。此外,线性范围宽和仪器简单也是化学发光免疫分析法的特点之一。磁微粒化学发光免疫分析是将磁性分离技术、化学发光技术、免疫分析技术三者结合起来的一种新兴分析方法。该技术充分利用了磁性分离技术的快速易自动化性,化学发光技术的高灵敏度性,以及免疫分析的特异性。正是基于这些特点,磁微粒化学发光免疫分析在环境化学、临床检验、药物分析等领域得到十分广泛的应用和研究。目前,国内外有较多化学发光免疫产品上市。但是,国内外各大厂家推出的产品性能差异较大。其中,精密度是衡量各个厂家化学发光免疫产品质量的重要参数之一。精密度是在一定条件下所获得的独立的测定结果间的一致程度,以不精密度表示。传统的磁微粒化学发光免疫分析技术中,不精密度的主要来源为随机误差,在化学发光免疫分析系统测试过程中,则体现在加样过程、磁分离过程以及清洗过程的随机误差,这些随机误差导致现有的化学发光免疫分析法的精密度有待提高。技术实现要素:本发明的目的在于提供一种基于荧光染料作为内标物的化学发光免疫分析法,以解决现有的化学发光免疫分析法的精密度有待提高的问题。本发明的另一目的在于提供上述基于荧光染料作为内标物的化学发光免疫分析法的应用。本发明采用的技术方案如下:第一方面,本发明提供一种基于荧光染料作为内标物的化学发光免疫分析法,包括:将待测抗原的一株抗体直接或间接包被到荧光磁性微球的羧基上,形成抗体-荧光磁性微球;将待测抗原的另一株抗体直接或者间接标记发光物,加入所述抗体-荧光磁性微球以及所述待测抗原,通过抗体-抗原-抗体的相互作用,形成发光物抗体-待测抗原-荧光磁性微球免疫复合物;对所述复合物加磁场进行磁性分离,使所述复合物沉淀,并吸干废液,除去未与所述复合物结合的物质,再用清洗液清洗沉淀的复合物;利用荧光定量检测仪读取所述复合物的信号,得到荧光值;利用仪器自动泵入激发液,使所述复合物产生化学发光信号,利用光电倍增器测量所述化学发光信号的发光强度;根据所述荧光值对所述发光强度进行校准;根据校准后的发光强度计算待测抗原的浓度。结合第一方面,在第一方面的第一种可选的实施方式中,所述荧光磁性微球为表面含羧基,粒径为500-3000纳米,具有磁信号响应功能、表面基团功能化以及荧光特性的荧光磁性微球。结合第一方面的第一种可选的实施方式,在第一方面的第二种可选的实施方式中,所述荧光磁性微球通过以下方法制备:在氮气保护及预设搅拌速度下,将fe2+、fe3+按一定比例混合,采用共沉淀方法制备出纳米fe3o4颗粒;洗涤去除多余的氯离子,干燥得到纳米fe3o4颗粒;对所述纳米fe3o4颗粒进行油酸改性,制备fe3o4磁流体;基于细乳液复合液滴成核的乳液聚合制备方法,通过聚合反应在所述fe3o4磁流体表面进行苯乙烯和丙烯酸的共聚,制备出表面含羧基的磁性高分子微球;通过溶胀分散技术将荧光染料嵌入所述表面含羧基的磁性高分子微球内部,制得所述荧光磁性微球。结合第一方面的第二种可选的实施方式,在第一方面的第三种可选的实施方式中,所述发光物为n-(4-氨丁基)-n-乙基异鲁米诺,吖啶酯,吖啶磺酰胺,辣根过氧化物酶,碱性磷酸酶中的任意一种可以和激发液或者底物作用产生化学发光的物质。结合第一方面的第三种可选的实施方式,在第一方面的第四种可选的实施方式中,所述荧光染料为fitc、rhodamine、alexa488、cy3、cy5、dio、dii、dir中的任意一种具有吸收某一波长的光波后,能发射出另一波长大于吸收光的光波性质,且在与所述发光物的联合使用中,所述荧光染料不与所述发光物干扰的物质。结合第一方面,在第一方面的第五种可选的实施方式中,根据所述荧光值对所述发光强度进行校准的步骤中,根据:对所述发光强度进行校准,其中,r为校准后计算得发光强度,f0为荧光磁性微粒的初始荧光强度,f1为荧光检测仪测量荧光强度,r1为光电倍增器测量发光强度。第二方面,本发明提供上述的任一种基于荧光染料作为内标物的化学发光免疫分析法在制备化学发光免疫检测试剂盒中的应用。第三方面,本发明提供一种化学发光免疫检测试剂盒,基于上述的任一种基于荧光染料作为内标物的化学发光免疫分析法制备,所述化学发光免疫检测试剂盒还包含化学发光激发液系统。结合第三方面,在第三方面的第一种可选的实施方式中,所述试剂盒为检测肌钙蛋白i的磁化学发光免疫分析试剂盒。结合第三方面的第一种可选的实施方式中,在第三方面的第二种可选的实施方式中,所述检测肌钙蛋白i的磁化学发光免疫分析试剂盒包含:肌钙蛋白i的一株单克隆抗体包被的共价偶联了链亲和素的磁性微粒、标记吖啶酯的肌钙蛋白i的另一株单克隆抗体、第一激发液以及第二激发液,所述第一激发液为含有0.5wt%过氧化氢溶液的0.2m的硝酸溶液,所述第二激发液为含有1wt%tween-20的0.5m氢氧化钠溶液,所述肌钙蛋白i的一株单克隆抗体和肌钙蛋白i的另一株单克隆抗体为配对抗体。本发明的有益效果如下:本发明的基于荧光染料作为内标物的化学发光免疫分析法及其应用,首先,通过将待测抗原的一株抗体直接或间接包被到荧光磁性微球的羧基上,形成抗体-荧光磁性微球,然后将待测抗原的另一株抗体直接或者间接标记发光物,加入抗体-荧光磁性微球以及待测抗原,形成发光物抗体-待测抗原-荧光磁性微球免疫复合物,在对复合物清洗分离后,利用荧光定量检测仪读取复合物的信号,得到荧光值,接着利用仪器自动泵入激发液,使复合物产生化学发光信号,利用光电倍增器测量化学发光信号的发光强度,再根据荧光值对发光强度进行校准,最后可根据校准后的发光强度计算待测抗原的浓度,本发明在传统的磁化学发光免疫分析技术基础上,引入荧光物质作为发光信号的校正系统,通过对已知量的荧光物质进行测量,从而校正免疫复合物上标记物的发光值,降低系统产生的随机误差,提升分析的精密度。附图说明为了更清楚地说明本发明的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,对于本领域普通技术人员而言,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。图1为本发明实施例提供的基于荧光染料作为内标物的化学发光免疫分析法的流程图。图2为本发明实施例提供的荧光磁性微球制备流程图。图3为本发明实施例提供的基于荧光染料作为内标物的化学发光免疫分析法的技术路线示意图。图4为仅磁性微粒做固相的检测体系和荧光磁性微粒做固相校正体系的ctni检测重复性对比示意图。图5为仅磁性微粒做固相的检测体系和荧光磁性微粒做固相校正体系的ctni检测室内精密度对比示意图。图6为0-1ng/mlctn仅磁性微粒体系与雅培对比图。图7为0-1ng/mlctn荧光磁性微粒体系与雅培对比图。图8为0-40ng/mlctn仅磁性微粒体系与雅培对比图。图9为0-40ng/mlctn荧光磁性微粒体系与雅培对比图。图10为仅磁性微粒做固相的检测体系和荧光磁性微粒做固相校正体系灵敏度对比示意图。具体实施方式为使本发明的目的、技术方案和优点更加清楚,下面将结合本发明具体实施例及相应的附图对本发明技术方案进行清楚、完整地描述。显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。以下结合附图,详细说明本发明各实施例提供的技术方案。请参阅图1,图1为本发明实施例提供的一种基于荧光染料作为内标物的化学发光免疫分析法的流程图,包括:步骤s101,将待测抗原的一株抗体直接或间接包被到荧光磁性微球的羧基上,形成抗体-荧光磁性微球。其中,所述荧光磁性微球为表面含羧基,粒径为500-3000纳米,具有磁信号响应功能、表面基团功能化以及荧光特性的荧光磁性微球,如图2所示,所述荧光磁性微球可以通过以下方法制备:步骤s201,在氮气保护及预设搅拌速度下,将fe2+、fe3+按一定比例混合,采用共沉淀方法制备出纳米fe3o4颗粒。步骤s202,洗涤去除多余的氯离子,干燥得到纳米fe3o4颗粒。步骤s203,对所述纳米fe3o4颗粒进行油酸改性,制备fe3o4磁流体。步骤s204,基于细乳液复合液滴成核的乳液聚合制备方法,通过聚合反应在所述fe3o4磁流体表面进行苯乙烯和丙烯酸的共聚,制备出表面含羧基的磁性高分子微球。本发明通过基于细乳液复合液滴成核的乳液聚合制备方法,实现了粒径单分散、高饱和磁化强度磁性微球的可控制备,磁性胶体粒子为聚合种子。通过聚合反应在磁流体表面进行苯乙烯和丙烯酸的共聚,制备了表面含羧基的磁性高分子微球,通过溶胀分散技术将荧光染料嵌入微球内部制备荧光磁性微球,此微球具有高磁响应性和高羧基含量和稳定荧光强度性质。步骤s205,通过溶胀分散技术将荧光染料嵌入所述表面含羧基的磁性高分子微球内部,制得所述荧光磁性微球。上述过程首先用化学共沉淀法制备出纳米级具有高磁响应性和活性基团的磁流体,再基于细乳制备方法机理的基础上,以核壳结构磁性复合微球为核,采用丙烯酸为共聚单体,制备表面具有羧基功能基团的磁性复合微球,羧基含量高。同时,通过溶胀分散技术将荧光染料嵌入微球内部制备荧光磁性微球,溶胀分散法是溶胀剂先将微球溶胀使其表面和内部出现空隙,随后荧光染料一同进入到微球内部,再将溶胀剂除去的过程。最终得到具有荧光特性的磁性微球。若将有机染料直接在磁珠表面结合,直接暴露于外界,容易受离子浓度、温度等环境条件的影响从而出现光漂白和淬灭现象。而将染料溶胀在的纳米颗粒内部具有更高的亮度和稳定性,在实际应用中表现出更好地重现性。本发明提出了一种简单的合成方法,使用聚苯乙烯和丙烯酸作为主要合成材料,用于制备具有高品质的核壳结构纳米微球,同时含有荧光物质作为内标以及羧基基团用于偶联抗体,本发明所采用的合成方法具有步骤简单,产量高,成本低等优点,为构建新型的高精密度检测体系用于体外检测试剂盒的研发与临床应用提供更优方案。步骤s102,将待测抗原的另一株抗体直接或者间接标记发光物,加入所述抗体-荧光磁性微球以及所述待测抗原,通过抗体-抗原-抗体的相互作用,形成发光物抗体-待测抗原-荧光磁性微球免疫复合物。在本实施例中,所述发光物可以为n-(4-氨丁基)-n-乙基异鲁米诺,吖啶酯,吖啶磺酰胺,辣根过氧化物酶,碱性磷酸酶中的任意一种可以和激发液或者底物作用产生化学发光的物质。由于发光物质主要分为两大类,一类是直接发光,如:吖啶酯,n-(4-氨丁基)-n-乙基异鲁米诺,直接加激发液可产生光子。吖啶磺酰胺,辣根过氧化物酶,碱性磷酸酶等为酶促发光,标记的并非发光物,而是激发发光物的酶,因此需要在激发液里有酶作用的底物产生光子。在本实施例中,所述荧光染料可以为fitc(异硫氰酸荧光素及其衍生物)、rhodamine(罗丹明及其衍生物)、alexa488(alexa系列染料)、cy3和cy5(cy类荧光染料)、dio、dii、dir(长链的亲脂性二烷基碳菁类荧光染料家族)中的任意一种具有吸收某一波长的光波后,能发射出另一波长大于吸收光的光波性质,且在与所述发光物的联合使用中,所述荧光染料不与所述发光物干扰的物质。荧光染料是荧光免疫微球中的核心原材料之一,经过激发光的激发作用后,可以发射一定波长范围的发射光,从而被荧光检测器接收。根据这种特性,发现不同浓度的荧光染料在激发后最大吸收波长位置呈现出一定的规律性。步骤s103,对所述复合物加磁场进行磁性分离,使所述复合物沉淀,并吸干废液,除去未与所述复合物结合的物质,再用清洗液清洗沉淀的复合物。步骤s104,利用荧光定量检测仪读取所述复合物的信号,得到荧光值。步骤s105,利用仪器自动泵入激发液,使所述复合物产生化学发光信号,利用光电倍增器测量所述化学发光信号的发光强度。步骤s106,根据所述荧光值对所述发光强度进行校准。在本实施例中,根据所述荧光值对所述发光强度进行校准的步骤中,可以根据:对所述发光强度进行校准。其中,r为校准后计算得发光强度,f0为荧光磁性微粒的初始荧光强度,f1为荧光检测仪测量荧光强度,r1为光电倍增器测量发光强度。本发明利用了荧光物质对发光信号的校正作用。荧光信号和发光信号在检测中不互相干扰,已知的荧光物质强度可作为检测过程中的内参物进行校正,当测试发生荧光强度偏离期望值,则可能由于加样过程,或清洗磁珠免疫复合物过程等系统随机误差导致,可通过公式进行补偿发光信号。在这一系列过程中,极大改善仪器系统误差导致的不精密度。本发明采用与标记发光物质无干扰的荧光染料作为内参物,在传统的磁化学发光免疫分析技术系统内引入一种与检测物质无干扰的荧光染料物质,由于引入的荧光物质为已知参数,可以用来校正系统产生的误差,如加样臂误差,清洗免疫复合物损失误差等。步骤s107,根据校准后的发光强度计算待测抗原的浓度。请参阅图3,本发明实施例提供的基于荧光染料作为内标物的化学发光免疫分析法,选用以上述荧光羧基微球作为固相,通过羧基可以直接或间接偶联捕获抗体,标记抗体标记发光物质,当待测物与捕获抗体和标记抗体在微球表面形成免疫复合物后,加磁场沉淀,去掉上清液,用清洗液清洗沉淀复合物,并吸干废液,除去未与磁性微粒结合的物质,再将反应杯送入测量室中。首先经过荧光定量检测仪读取复合物的信号,量化荧光强度。然后仪器自动泵入两种激发液,使复合物产生化学发光信号,通过光电倍增器测量发光强度。通过荧光信号首先对发光信号进行校准,在通过工作曲线计算得出检测待测物浓度。本发明在传统化学发光免疫分析法的基础上引入内标法,可以极大程度校正这些系统过程导致的随机误差,从而可以提升系统精密度。内标法常被应用到色谱分析法中,是结合了峰面积归一法和外标法的优点的一种方法,它在加入内标物后,按峰面积归一法的分析方法进行分析,这就避免了由于进样的一致性及样品歧视效应导致的偶然误差。因而,它的分析精密度也是比较高的,是一种比较理想的定量分析方法。本发明还提供上述任一种基于荧光染料作为内标物的化学发光免疫分析法在制备化学发光免疫检测试剂盒中的应用。本发明提供一种化学发光免疫检测试剂盒,基于上述任一种基于荧光染料作为内标物的化学发光免疫分析法制备,所述化学发光免疫检测试剂盒还包含化学发光激发液系统。本发明以此基于荧光染料作为内标物的化学发光免疫分析法的技术平台为基础,开发不同的免疫学检测试剂盒,以解决现有基于clia的检测试剂盒的精密度较差的问题。本发明能在现有clia检测技术基础上系统精密度提升50%以上。作为一种可选的实施方式,所述试剂盒可以是检测肌钙蛋白i(ctni)的磁化学发光免疫分析试剂盒。所述检测肌钙蛋白i的磁化学发光免疫分析试剂盒可以包含:肌钙蛋白i的一株单克隆抗体包被的共价偶联了链亲和素的磁性微粒、标记吖啶酯的肌钙蛋白i的另一株单克隆抗体、第一激发液以及第二激发液,所述第一激发液为含有0.5wt%过氧化氢溶液的0.2m的硝酸溶液,所述第二激发液为含有1wt%tween-20的0.5m氢氧化钠溶液,所述肌钙蛋白i的一株单克隆抗体和肌钙蛋白i的另一株单克隆抗体为配对抗体。具体地,上述试剂盒制备包括如下步骤:制备磁流体:称取30克fecl2·4h20和75克fecl3·6h20溶解于100克去离子水中(经加热除氧)得到透明黄色溶液,为加快溶解,使用玻璃棒搅拌并辅以超声。将上述溶液置入250m1的三口烧瓶中后将反应装置放入恒温水浴中,通氮升温至75度,加入160ml氨水,反应体系颜色立即变为黑色,75度保温维持2小时后,加入8ml油酸,再继续通氮保温反应1小时,然后撤去氮气与冷凝管,搅拌下将未反应完的氨蒸发除去,直至发现停止搅拌后,体系中的黑色颗粒马上与水分层并沉淀下来即告反应结束,将得到的黑色悬浮液在磁场作用下收集、去离子水洗涤数次后,测试上清液为中性后,再用无水乙醇洗涤3次后再将得到的黑色颗粒用去离子水洗涤三次,然后加入100ml的正己烷,黑色磁颗粒瞬间转入已烷相中,使用玻璃棒搅拌使磁性粒子与正己烷充分接触,至无明显的团块物。制备羧基磁性微球:首先称取1.5gsds和4.5g十六醇用1000ml纯化水分散与三口瓶中,通氮气30min,然后进入预乳化阶段:将温度设置为55度后,接通冷凝管,先开启超声后使用搅拌器进行搅拌设置350转/分钟20min,体系变为白色乳液状,预乳化完成。取上述制备得到的磁流体转移至烧瓶中,再加入110ml苯乙烯、加入1.25g2-2偶氮二异丁腈、加入甲基丙烯酸丁酯25ml手动摇匀后,将烧杯放入冰水浴中200w超声20min后得到黑色的均匀分散液,将上述黑色分散液从烧瓶口中用滴管逐滴加入预乳化完成的三口瓶中,温度设置55度。滴加完成后,用玻璃塞将瓶口封闭,继续保持搅拌和超声30min,使得体系充分乳化,在加入2.5g过硫酸铵。继续超声40min,温度升高65度,保持加热继续反应20h。每隔30min向体系内加入1ml丙烯酸,全部加完继续反应2小时。制备荧光羧基磁性微球:将羧基化磁性微球乳液(2wt%)加入到150.0ml烧瓶中,同时向其加入40.0ml去离子水和10.0ml2%的十二烷基磺酸钠。将fitc溶解于溶胀剂二氯甲烷之后加入离心管,混合物在25℃下以分散均质仪进行30min的溶胀反应,之后放置于通风橱进行4小时的挥发,除去有机溶剂。通过去离子水和离心(10000*g,20min)对收集到的荧光微球乳液进行多次洗涤,进一步除去有机溶剂及未加载的荧光物质。制备共价偶联了链亲和素的磁性微粒:以下操作需避光处理。用活化缓冲液活化磁性微粒表面化学基团,活化完成后使用偶联缓冲液清洗磁性微粒,加入相当于磁性微粒质量的1/20的链亲和素,反应后使用封闭缓冲液封闭磁性微粒上空余的活化基团,得到共价偶联了链亲和素的磁性微粒。ctni的单克隆抗体标记生物素:ctni的单克隆抗体中加入一定比例摩尔的nhs活化的生物素。生物素化反应完成后,将生物素化的抗体加入上述偶联了链亲和素的磁性微粒中,利用链亲和素-生物素体系间接包被后得到抗体包被的荧光磁性微球。ctni的另一支单克隆抗体标记吖啶酯:ctni的另一株单克隆抗体中加入一定比例摩尔的nhs活化的吖啶酯。配制激发液1和激发液2:激发液1为含有0.5%过氧化氢溶液的0.2m的硝酸溶液;激发液2为含有1%tween-20的0.5m氢氧化钠溶液。上述ctni的两株单克隆抗体为配对抗体。下面结合具体的实验过程及数据来说明本发明的有益效果。1.实验仪器和试剂:a.实验仪器:加热磁力搅拌器(德国ika),透射电子显微镜(日本jeol),恒温水浴锅(hh-60,常州国华电器有限公司),恒温摇床(太仓市科教器材厂),微量移液器(thermo公司),离心机(德国eppendorf公司),磁分离架(天津倍思乐色谱技术开发中心),透析袋(上海泰伯),全自动化学分析仪6800(基蛋生物)。b.实验试剂:ctni标准品(基蛋生物),ctni单克隆抗体(hytest公司),pbs-t缓冲液(kh2po43.35g/l,na2hpo4-12h2o17.9g/l,kcl0.2g/l,nacl8.77g/l,tween-200.5g/l,ph6.96),小牛血清(gibco公司),ctni标准品稀释液为含20%小牛血清的pbs-t缓冲液,其它试剂以及耗材若无特殊说明,均购自sigma-aldrich公司。试剂批号:cci19004。c.实验样本:精密度样本:level1(临床混合人血清):0.46ng/ml;level2(临床混合人血清):16.04ng/ml。相关性样本:84例ctni阳性血清样本,雅培赋值。lob样本:5个空白样本(采用免疫吸附法分离患者血清标本中的ctni)。lod样本:5个低水平样本(浓度1-1.5pg/ml)。loq样本:5个低水平粗晒样本(浓度2-10pg/ml),5个低水平确认样本(浓度6.21、675、6.52、6.32、6.16pg/ml,雅培赋值)。2.实验方法:2.1.荧光磁性微球的制备:(1)正己烷基fe3o4磁流体的制备称取30克fecl2·4h20和75克fecl3·6h20溶解于100克去离子水中(经加热除氧)得到透明黄色溶液,为加快溶解,使用玻璃棒搅拌并辅以超声。将上述溶液置入250m1的三口烧瓶中后将反应装置放入恒温水浴中,通氮升温至75度,加入160ml氨水,反应体系颜色立即变为黑色,75度保温维持2小时后,加入8ml油酸,再继续通氮保温反应1小时,然后撤去氮气与冷凝管,搅拌下将未反应完的氨蒸发除去,直至发现停止搅拌后,体系中的黑色颗粒马上与水分层并沉淀下来即告反应结束,将得到的黑色悬浮液在磁场作用下收集、去离子水洗涤数次后,测试上清液为中性后,再用无水乙醇洗涤3次后再将得到的黑色颗粒用去离子水洗涤三次,然后加入100ml的正己烷,黑色磁颗粒瞬间转入已烷相中,使用玻璃棒搅拌使磁性粒子与正己烷充分接触,至无明显的团块物。(2)羧基磁性微粒的制备首先称取1.5gsds和4.5g十六醇用1000ml纯化水分散与三口瓶中,通氮气30min,然后进入预乳化阶段:将温度设置为55度后,接通冷凝管,先开启超声后使用搅拌器进行搅拌设置350转/分钟20min,体系变为白色乳液状,预乳化完成。取上述制备得到的磁流体转移至烧瓶中,再加入110ml苯乙烯、加入1.25g2-2偶氮二异丁腈、加入甲基丙烯酸丁酯25ml手动摇匀后,将烧杯放入冰水浴中200w超声20min后得到黑色的均匀分散液,将上述黑色分散液从烧瓶口中用滴管逐滴加入预乳化完成的三口瓶中,温度设置55度。滴加完成后,用玻璃塞将瓶口封闭,继续保持搅拌和超声30min,使得体系充分乳化,在加入2.5g过硫酸铵。继续超声40min,温度升高65度,保持加热继续反应20h。每隔30min向体系内加入1ml丙烯酸,全部加完继续反应2小时。(3)荧光磁性微球制备将羧基化磁性微球乳液(2wt%)加入到150.0ml烧瓶中,同时向其加入40.0ml去离子水和10.0ml2%的十二烷基磺酸钠。将fitc溶解于溶胀剂二氯甲烷之后加入离心管,混合物在25℃下以分散均质仪进行30min的溶胀反应,之后放置于通风橱进行4小时的挥发,除去有机溶剂。通过去离子水和离心(10000*g,20min)对收集到的荧光微球乳液进行多次洗涤,进一步除去有机溶剂及未加载的荧光物质。2.2.将链霉亲和素偶联至荧光磁性微球上(在避光条件下操作):(1)先将整瓶磁珠超声1min,使磁珠分散均匀,再取5ml上述制备荧光磁性微球(10mg/ml)于10ml离心管中,吸去磁珠储存液,加入5ml100mmmes重新分散,超声1min,吸去液体,重新加入5ml100mmmes。(2)称取一定量的edc,配制成100mg/ml,edc加入量设置为25mg;迅速加入到磁珠悬液中,并置于37度,220转/分钟反应15min。(3)将edc清洗干净,清洗两遍,去悬液,重新加入5ml100mmmes。(4)将链霉亲和素清洗干净,去上清后,加入5ml清洗液,清洗两遍后,再加入5ml磁珠储存液转移至50ml离心管中,补加15ml储存液,使用磁珠储存液再次清洗一遍。2.3.生物素标记ctni抗体:取2.0ml离心管,准确量取0.54mg待标记抗体溶液加到离心管底部;准确量取4.0ul的生物素加到离心管中间部位内壁上;将离心管呈45℃倾斜,准确量取ul标记缓冲溶液(磷酸盐缓冲液,20mmol/lph=7.5±0.2)沿管壁将管壁上的生物素冲进去,震荡混匀,37.0℃水浴反应60min后取出。(注:标记缓冲液体积为使反应体系总体积为540ul需要补足的量),在上述反应管中加入72ul封闭液混合,置于37℃水浴锅中反应0.5h后取出。将反应好的标记抗体,进行透析纯化,回收生物素标记物。2.4.ctni单克隆抗体标记吖啶酯:(1)取2.0ml离心管,准确量取0.30mg待标记抗体溶液加到离心管底部;准确量取12.8ul的吖啶酯加到离心管中间部位内壁上;将离心管呈45℃倾斜,准确量取ul标记缓冲溶液(0.05mol/l碳酸盐缓冲液,ph应在9.6±0.2,若ph不符,需重新配置,备用。)沿管壁将管壁上的吖啶酯冲进去,震荡混匀,37.0℃水浴反应60min后取出。(标记缓冲液体积为使反应体系总体积为300ul需要补足的量),在上述反应管中加入40ul封闭液混合,置于37℃水浴锅中反应0.5h后取出。(2)将反应好的标记抗体,进行透析处理,回收吖啶酯标记物。2.5化学发光免疫分析法测定样品中肌钙蛋白浓度的实验:将上述制备的链霉亲和素包被的荧光磁性微粒/仅链亲和素包被磁性微粒用缓冲液稀释为1.25mg/ml的工作液,再将已制备的生物素化抗体母液和吖啶酯化抗体母液分别用含蛋白缓冲液稀释400倍和2500倍制备为生物素抗体工作液和吖啶酯抗体工作液。将50μl样本、50μl生物素标记的ctni单克隆抗体、50μl吖啶酯标记的另一株ctni单克隆抗体以及10μl链霉亲和素包被的荧光磁性微粒/仅链亲和素包被磁性微粒加入反应杯内,37℃温育条件下反应10分钟,抗体捕获样本中的抗原,形成抗原抗体夹心复合物。检测读数:温育结束后,加磁场沉淀,去掉上清液,用清洗液清洗沉淀复合物,并吸干废液,除去未与磁性微粒结合的物质,再将反应杯送入测量室中,首先经过荧光定量检测仪读取复合物的信号,量化荧光强度。再通过仪器自动泵入两种激发液,使复合物产生化学发光信号,通过光电倍增器测量发光强度。仪器自动通过工作曲线计算得出检测结果并用荧光信号对发光强度进行校正。校正公式如下:其中,r为校准后计算得发光强度,f0为荧光磁性微粒的初始荧光强度,f1为荧光检测仪测量荧光强度,r1为光电倍增器测量发光强度。2.6.激发液系统的配制:a.激发液1的:含有0.5wt%过氧化氢溶液的0.2m的硝酸溶液。b.激发液2的:含有1wt%tween-20的0.5m氢氧化钠溶液。2.7仅磁性微粒检测系统和荧光磁性微粒校正检测系统的精密度实验:精密度研究将在clsiep5-a2的指导下进行,并在clsiep15-a3的指导下进行验证,对比验证仅磁性微粒检测系统和荧光磁性微球校正体系的精密度。该方案使用了一个嵌套的方差设计,每个样本有20个测试日,每个测试日运行两次,每次运行两次重复测量(一个20×2×2的设计)。所有测试在一个地点用一个仪器进行。我们对每种ctni试剂使用两种不同浓度的ctni混合人血清。分别用仅磁性微粒检测系统和荧光磁性微球校正体系使用上述方案研究。2.8仅磁性微粒检测系统和荧光磁性微粒校正检测系统的相关性实验:对比验证仅磁性微粒检测系统和荧光磁性微粒校正检测系统与对照试的相关性,选取雅培为对照试剂,分别使用两种体系测试84例雅培赋值的阳性血清。2.9仅磁性微粒检测系统和荧光磁性微粒校正检测系统的灵敏度实验:检测能力是临床实验室测量程序的基本性能特征,通常用来表示测量程序测量区间的低端边界。然而,理解和评估检测能力可能经常是令人困惑的,因为不同类型的估计、实验方案和制造商产品声明中使用的术语,以及过去几十年的科学文献中使用的术语都是不同的。我们选用空白限lob、检出限lod、定量限loq来评价试剂的灵敏度。lobandlod:为了满足lob和lod的要求,选择如下所列的实验设计。α=β=0.05的默认值被用于i和ii型错误的风险。一批试剂(cci19004),两个检测系统(磁性微粒检测系统和荧光磁性微粒校正检测系统),测试五天,五个空白样品,5个低水平样本,每个样品重复测试4遍,每个试剂空白和低水平样本测量5天×5样本×4重复。loq:本次loq测试基于c.ricos等人提供的生物变异数据库中的理想te规范,loq的精度目标是总误差(te)为20%:te=|bias|+2s上述实验中lob/lod测试的数据用于指导loq的初始估计。loq测试采用了以下实验设计:一个试剂批次(cci19004),两个检测系统(磁性微粒检测系统和荧光磁性微粒校正检测系统),三个测试天,四个重复次数,对每个试剂组的每个样品的试剂量(3天×5个样品×4个重复),5个低水平样品,60个总低水平样品。3.实验数据:3.1精密度实验:表1.仅磁性微粒检测系统实验数据表2.仅磁性微粒检测系统精密度评价总结表3.仅磁性微粒检测系统下不同ctni水平样本cv的95%置信区间表4.荧光磁性微球校正体系实验数据表5.荧光磁性微球校正体系精密度评价总结表6.荧光磁性微球校正体系下不同ctni水平样本cv的95%置信区间考察精密度最重要的两个指标为重复性和室内精密度(总精密度),磁性微粒系统重复性水平1样本分别为:3.30%;水平2样本分别为:3.43%。荧光磁性微粒系统三批重复性,水平1样本分别为:1.65%;水平2样本分别为:1.47%。磁性微粒系统室内精密度,水平1样本分别为:5.73%,水平2样本分别为:4.91%。荧光磁性微粒系统三批重复性:水平1样本分别为:2.92%;水平2样本分别为:2.33%。由图4和图5可知,荧光磁性微粒体系明显比仅磁性微粒体系在重复性和室内精密度方面存在较大的优势。3.2相关性实验:表7.雅培测试样本浓度数据将上述数据按0-1ng/ml和0-40ng/ml做散点图,由图6~图9可知,0-1ng/ml的仅磁性微粒体系r2为0.9089,对应的荧光磁性微粒体系为0.9899;0-40ng/ml的仅磁性微粒体系r2为0.9919,对应的荧光磁性微粒体系为0.9963。荧光磁性微粒体系总体上比仅磁性微粒体系相关性好,特别是低值部分优势跟明显。荧光磁性微粒体系应用内参可以矫正测值,较少随机波动能够有效的减少方法学比对的离散性,从而提高与对照试剂的相关性,特别是随机误差较大的低值部分,相关性有明显提高。3.3灵敏度实验:仅磁性微粒检测系统:(a)空白限表8.ctni空白限的测试结果表9.空白样本的百分比排序其中b=100是每批试剂的空白样品测量数量。由于顺序位置是整数,所以顺序位置95对应的值是lob。表中包含了已分类的空白测量结果的较高排序,此试剂批次的lob为1.19pg/ml。(b)检出限表10.ctni检出限的测试结果表11.ctni检出限结果处理样本数量sd低值样本1200.1494低值样本2200.1700低值样本3200.2179低值样本4200.2624低值样本5200.3003sdl/0.22704cp/1.64934lod:/1.56447接下来对每个试剂批次的低水平样品结果进行分析,如上表所示的计算表给出了每个样品的单sds。这些结果合并以得出sdl。cp乘子因子按公式计算,在上面确定的lob基础上得出lod。结果为1.56pg/ml。则1.56pg/ml为测量程序的lod。(c)定量限loq表示相对于预定的精度目标,可以测量的最低测量和浓度。它是度量过程的一个特征,包括用于定义精度目标的特定性能属性,以及被认为是可接受的值。验收要求越严格,loq可能越大。考虑到loq定义的灵活性,在报告loq估计值时,有必要包括潜在的准确性目标。根据定义,loq是仅适用于定量测量过程的性能属性。表12.ctni检出限结果处理对于每批试剂,以观察到的平均值减去参考值,计算每个低水平样品的偏差。这与所观察到的sd值相结合,得到te,te表示为相关样本参考值的百分比。表13.低浓度样本的处理结果样本名称标识浓度(pg/ml)bias(pg/ml)te(%)低值样本12.00.017525%低值样本24.00.093324%低值样本36.0-0.054819%低值样本48.0-0.118720%低值样本510.00.176816%从平均te与参考值的关系中推断,loq可能达到6pg/ml左右。在此基础上,以6.0pg/ml的标称目标量制备了5个混合样品。样品采用罗氏赋值,并确定其在所需的测量和浓度范围内(6.0±1.0pg/ml)。5个样品中的每一个都在3天的测试时间里,分别用三个试剂批次各检测3份。每批试剂产生45个重复。样品的观察结果和参考值汇总在下表中。表14.样品的观察结果和参考值计算每个试剂批次样品相对于参考值的平均值、sd和偏差。这些值用于计算每个样品的te,用%te表示每个样品相对于各自的参考值。计算结果见下表。表15.ctni定量限的数据处理结果每个试剂批次所有样品的计算te均满足%te≤20%的精度目标;因此,loq标准被认为是满足的。试剂批次一满足准确度目标的最低样品浓度为6.31pg/ml。则6.31pg/ml为测量程序的loq。荧光磁性微粒校正检测系统:(a)空白限表16.ctni空白限的检测结果表17.空白样本的百分比排序百分比排序测值pg/ml931.08941.09951.09961.09971.09981.09lob:1.09其中b=100是每批试剂的空白样品测量数量。由于顺序位置是整数,所以顺序位置95对应的值是lob。表中包含了已分类的空白测量结果的较高排序,此试剂批次的lob为1.09pg/ml。(b)检出限表18.ctni检出限的测试结果表19.ctni检出限结果处理样本名称数量sd低值样本1200.0675低值样本2200.0897低值样本3200.1004低值样本4200.1278低值样本5200.1586sdl/0.11329cp/1.64934lod:/1.27685接下来对每个试剂批次的低水平样品结果进行分析,如上表所示的计算表给出了每个样品的单sds。这些结果合并以得出sdl。cp乘子因子按公式计算,在上面确定的lob基础上得出lod。次试剂批次的lod为1.28pg/ml。定量限loq:loq表示相对于预定的精度目标,可以测量的最低测量和浓度。它是度量过程的一个特征,包括用于定义精度目标的特定性能属性,以及被认为是可接受的值。验收要求越严格,loq可能越大。考虑到loq定义的灵活性,在报告loq估计值时,有必要包括潜在的准确性目标。根据定义,loq是仅适用于定量测量过程的性能属性。表20.定量限的结果对于每批试剂,以观察到的平均值减去参考值,计算每个低水平样品的偏差。这与4所观察到的sd值相结合,得到te,te表示为相关样本参考值的百分比。表21.低浓度样本的处理结果样本名称标识浓度(pg/ml)bias(pg/ml)te(%)低值样本12.0-0.006820%低值样本24.00.002914%低值样本36.0-0.135719%低值样本48.0-0.193814%低值样本510.0-0.222613%从平均te与参考值的关系中推断,loq可能达到4pg/ml左右。在此基础上,以4.0pg/ml的标称目标量制备了5个混合样品。样品采用罗氏赋值,并确定其在所需的测量和浓度范围内(4.0±1.0pg/ml)。5个样品中的每一个都在3天的测试时间里,分别用三个试剂批次各检测3份。每批试剂产生45个重复。样品的观察结果和参考值汇总在下表中。表22.样品的观察结果和参考值汇总计算每个试剂批次样品相对于参考值的平均值、sd和偏差。这些值用于计算每个样品的te,用%te表示每个样品相对于各自的参考值。计算结果见下表。表23.定量限的数据处理结果每个试剂批次所有样品的计算te均满足%te≤20%的精度目标;因此,loq标准被认为是满足的。满足试剂批次一准确度目标的最低样品浓度为4.54pg/ml。试剂批次的loq为4.54pg/ml。综上可得图10,仅磁性微粒系统的lob:1.19pg/ml,lod:1.56pg/ml,loq:6.35pg/ml。荧光磁性微粒系统的lob:1.09pg/ml,lod:1.28pg/ml,loq:4.54pg/ml。荧光磁性微粒系统的灵敏度明显优于仅磁性微粒系统。以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1