一种基于二硫化钨的柔性生物传感器及其制备方法
1.本发明属于新型功能材料与生物传感检测技术领域,具体涉及一种基于二硫化钨的柔性生物传感器及其制备方法。
背景技术:
2.二硫化钨薄膜生物传感器利用沟道内的电导会随器件表面修饰情况的变化而发生变化,从而导致电流的变化,进而实现对生物分子的检测。并且超薄二硫化钨纳米材料具有很好的韧性,容易沉积到柔性基底上,并且其机械强度可以很好地适应人体的曲线表面,适用于柔性生物传感器的制备,可以实时监测人体状态,对癌症疾病的早期筛查具有重要意义。
技术实现要素:
3.本发明的目的在于一种基于二硫化钨的柔性生物传感器及其制备方法。该柔性生物传感器能够应用于抗原的非侵入、高灵敏、特异性检测。
4.第一方面,本发明提供一种基于二硫化钨的柔性生物传感器,其包括pen基体、二硫化钨薄膜和抗体。二硫化钨薄膜设置在pen基体上;二硫化钨薄膜与pen基体之间设置有叉指电极;抗体结合在二硫化钨薄膜经pase修饰形成的位点上。
5.作为优选,该柔性生物传感器还包括二抗;二抗为能够与目标抗原发生特异性结合,且与修饰在二硫化钨薄膜上的抗体不同的另一种抗体。二抗用于在被测样本滴加到柔性生物传感器后滴加,与柔性生物传感器上已有的抗体、抗原形成夹心结构,实现信号放大。
6.作为优选,所述叉指电极的间距为100-200μm。
7.第二方面,本发明提供前述的基于二硫化钨的柔性生物传感器的制备方法,具体如下:
8.s1:对二硫化钨薄膜表面进行pase(1-芘丁酸n-羟基琥珀酰亚胺酯,1-pyrenebutanoic acid succinimidyl ester)修饰。
9.s2:抗体修饰二硫化钨膜表面。
10.作为优选,步骤s1具体为:将二硫化钨薄膜用由dmso(二甲基亚砜)稀释的pase溶液浸泡后用pbs缓冲液冲洗并吹干。
11.作为优选,步骤s1中所述的pase的浓度为5mmol l-1
,浸泡时间为2-4h。
12.作为优选,步骤s2具体为:将由pbs缓冲液稀释的抗体,滴加到二硫化钨薄膜表面上并孵育预设时长后,用pbs缓冲液冲洗并吹干。
13.作为优选,步骤s2中的孵育时间为2-4h,温度为室温。
14.作为优选,步骤s2执行后,在二硫化钨薄膜表面滴加bsa(牛血清白蛋白)溶液,室温孵育后用pbs缓冲液冲洗并吹干。
15.作为优选,滴加滴加bsa溶液后的孵育时间为0.5-2h。
16.第三方面,本发明提供一种二硫化钨薄膜在柔性生物传感器中的应用。
17.第四方面,本发明提供前述的柔性生物传感器在非诊断目的的抗原检测中的应用。
18.本发明的有益效果是:
19.1.本发明使用的二硫化钨薄膜,易于沉积到柔性基底上,并可以实现目标抗原的监测。二硫化钨纳米材料具有较大的比表面积,可以增强其生物传感性能,由于存在合适的带隙,基于二硫化钨的传感器件的总体灵敏度要比没有带隙或带隙很小的石墨烯或石墨烯氧化物的要大得多。并且二硫化钨纳米片之间由弱的范德华力相连,很容易剥离为单层或少层,单层的二硫化钨器件能够提供较高的通断比,这对于生物传感器的构建是十分有利的。
20.2.本发明使用的二硫化钨纳米材料具有较大的比表面积,能够有效固定大量的修饰物。
21.3.本发明用于抗原检测的操作过程简单,成本低,无需昂贵的检测装置。
附图说明
22.图1为二硫化钨薄膜在-5-5v扫描电压下的i-v测试曲线图。
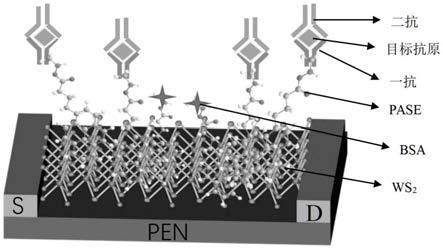
23.图2为本发明的二硫化钨柔性生物传感器的检测原理示意图。
具体实施方式
24.下面结合具体实施例对本发明作进一步说明,但是本发明所要保护的范围并不限于此。
25.一种基于二硫化钨的柔性生物传感器的制备方法如下
26.(1)二硫化钨膜表面的pase修饰
27.首先,将二硫化钨膜叠置到带有叉指电极的pen柔性基底上,并将所得器件在室温下浸泡于5mmol
·
l-1
的pase-dmso溶液中2h,pase通过一端的芘基基团与二硫化钨膜之间的π-π配位作用,修饰在二硫化钨膜表面。之后用pbs缓冲液(1
×
)冲洗3次,氮气吹干。此时,二硫化钨膜的表面末端修饰上了nhs-酯基,以便与抗体实现特异性结合。
28.(2)抗体修饰二硫化钨膜
29.取20μl由pbs缓冲液稀释的抗体,滴加在二硫化钨膜表面,在室温下孵育约2h。之后用pbs缓冲液(1
×
)冲洗3次,除去未反应的抗体,氮气吹干。为防止非特异性吸附,在传感器表面滴加bsa溶液,封闭pase上未与抗体(一抗)结合的位点,室温下孵育1h左右。之后用pbs缓冲液(1
×
)冲洗3次,除去未反应的bsa溶液,氮气吹干。至此,得到基于二硫化钨的柔性生物传感器。
30.该基于二硫化钨的柔性生物传感器的使用过程如下:
31.(1)抗原抗体特异性结合
32.在传感器表面滴加20μl由pbs缓冲液稀释的被测样本,并于室温孵育1h左右。之后用pbs缓冲液(1
×
)冲洗3次,除去未反应的抗原,氮气吹干。
33.(2)添加二抗
34.在传感器表面滴加20μl由pbs稀释的抗体(二抗),并于室温孵育2h。
35.(3)使用kickstart 2450数字源来表实时监测叉指电极源漏极之间的电流变化。并根据该电流变化判断被测样本是否存在对应的抗原。
36.二硫化钨薄膜在-5~5v的扫描电压下呈现的是非线性的肖特基i-v特性曲线如图1所示。
37.搭建生物传感器定量检测特定抗原的平台如图2所示,以二硫化钨膜为传输通道。在二硫化钨上以pase作为交联剂,将抗体固定在二硫化钨膜表面。引入目标抗原后,通过抗原抗体之间的特异性结合来定量检测目标抗原,最后加入二抗,通过抗体-抗原-二抗之间形成三明治夹心结构实现检测信号的放大,一定程度上提高传感器的灵敏度。
38.以上对本发明的优选实施例及原理进行了详细说明,对本领域的普通技术人员而言,依据本发明提供的思想,在具体实施方式上会有改变之处,而这些改变也应视为本发明的保护范围。
技术特征:
1.一种基于二硫化钨的柔性生物传感器,其特征在于:包括pen基体、二硫化钨薄膜和抗体;二硫化钨薄膜设置在pen基体上;二硫化钨薄膜与pen基体之间设置有叉指电极;抗体结合在二硫化钨薄膜经pase修饰形成的位点上。2.根据权利要求1所述的一种基于二硫化钨的柔性生物传感器,其特征在于:还包括二抗;二抗为能够与目标抗原发生特异性结合,且与修饰在二硫化钨薄膜上的抗体不同的另一种抗体;二抗用于在被测样本滴加到柔性生物传感器后滴加,与柔性生物传感器上已有的抗体、抗原形成夹心结构,实现信号放大。3.根据权利要求1所述的一种基于二硫化钨的柔性生物传感器,其特征在于:所述叉指电极的间距为100-200μm。4.如权利要求1所述的一种基于二硫化钨的柔性生物传感器的制备方法,其特征在于:包括以下步骤:s1:对二硫化钨薄膜表面进行pase修饰;s2:抗体修饰二硫化钨膜表面。5.根据权利要求4所述的制备方法,其特征在于:步骤s1具体为:将二硫化钨薄膜用由dmso稀释的pase溶液浸泡后用pbs缓冲液冲洗并吹干;步骤s1中所述的pase的浓度为5mmol l-1
,浸泡时间为2-4h。6.根据权利要求4所述的制备方法,其特征在于:步骤s2具体为:将由pbs缓冲液稀释的抗体,滴加到二硫化钨薄膜表面上并孵育预设时长后,用pbs缓冲液冲洗并吹干;步骤s2中的孵育时间为2-4h,温度为室温。7.根据权利要求4所述的制备方法,其特征在于:步骤s2执行后,在二硫化钨薄膜表面滴加bsa溶液,室温孵育后用pbs缓冲液冲洗并吹干。8.根据权利要求4所述的制备方法,其特征在于:滴加滴加bsa溶液后的孵育时间为0.5-2h。9.一种二硫化钨薄膜在柔性生物传感器中的应用。10.如权利要求1所述的一种基于二硫化钨的柔性生物传感器在非诊断目的的抗原检测中的应用。
技术总结
本发明公开了一种基于二硫化钨的柔性生物传感器及其制备方法。本发明利用柔性的二硫化钨薄膜作为传感器的敏感材料,通过交联剂PASE与二硫化钨之间形成的π-π配位作用固定在二硫化钨表面,为传感器表面提供了NHS-酯基。之后通过NHS-酯基与抗体表面的氨基之间形成的酰胺键实现抗体的固定,为了防止非特异性吸附,引入BSA,以封闭PASE上未与抗体结合的位点。利用抗原抗体之间的异性结合实现目标抗原的捕获,最后引入第二抗体(二抗),与之前的抗体,抗原形成抗体-抗原-二抗的三明治免疫夹心结构,从而实现传感器信号的放大。该方法操作简单,设备要求低,易实现,信号放大效果良好,可实现对目标抗原的实时监测。可实现对目标抗原的实时监测。可实现对目标抗原的实时监测。
技术研发人员:李杜娟 孙宏宇 洪锐 杨伟煌 董林玺 王高峰 樊凯
受保护的技术使用者:杭州电子科技大学
技术研发日:2021.12.24
技术公布日:2022/4/5
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1