猪源性小肠粘膜下基质材料中活性蛋白的表征方法和应用与流程
本发明涉及生物,具体涉及一种猪源性小肠粘膜下基质材料中活性蛋白的表征方法和应用。
背景技术:
1、公开该背景技术部分的信息仅仅旨在增加对本发明的总体背景的理解,而不必然被视为承认或以任何形式暗示该信息构成已经成为本领域一般技术人员所公知的现有技术。
2、细胞外基质材料是一类来源于猪、牛等动物心包、小肠粘膜下组织经生物、化学和物理脱细胞工艺处理得到的生物医用材料,具有可吸收特性、免疫原性低、超微结构与人体组织相近等优点。经处理的细胞外基质材料中主要含有胶原蛋白、蛋白多糖和氨基多糖等生物化学成分,有利于细胞粘附、力学传导、募集生长因子和促进组织重塑能力。其中,总蛋白与胶原蛋白差值大概是15%。与植入体内后最后转归为组织纤维疤痕修复的惰性材料(如不可降解的金属、陶瓷和塑料以及常规的可降解合成高分子材料等)不同,细胞外基质材料具有独特的物理、化学和生物学特性。例如,具有较高的比表面积、对机体无毒且容易代谢的降解产物、与组织重塑和再生相匹配的降解性能等。
3、在细胞外基质材料的脱细胞工艺过程中,因多糖损耗,细胞去除,蛋白成分在细胞外基质材料中的占比会增加。这些蛋白为细胞外基质材料在组织再生修复中的关键功能蛋白,有利于细胞的粘附、迁移、增殖和分化。但是,因为存在细胞外基质材料样品制备难题和缺少有效的分析手段,目前尚未建立针对这些活性蛋白定性定量的分析技术。因此,如果能对细胞外基质材料进行有效处理,对其中关键功能蛋白进行检测并建立表征方法,将会为细胞外基质材料相关产品的开发提供强有力的支持。
4、目前,国内外对细胞外基质材料中蛋白的检测采用的是将材料机械剪碎并酶解的方法。该方法虽然操作简便,但是因为细胞外基质材料一般都经过交联工艺处理,关键功能蛋白被包裹在产品内部,如果缺少对剪碎的蛋白进行有效的前处理,就会存在酶解不充分,蛋白暴露不完全,无法完全富集,且对样品单纯机械处理会造成蛋白活性降低,后续的检测方法敏感性降低的缺点。
技术实现思路
1、为了解决现有技术中存在的技术问题,本发明公开了一种猪源性小肠粘膜下基质材料中活性蛋白的表征方法和应用,利用高速低温匀质法对猪源性小肠粘膜下细胞外基质材料进行研磨处理,利用酸化胃蛋白酶对细胞外基质材料进行酶解,在37℃条件下将酶解的产物诱导成凝胶,然后通过离心得出固体沉淀物和含有可溶性蛋白的上清液,通过蛋白检测试剂盒测得总蛋白含量后,利用聚丙酰胺凝胶电泳获得固体沉淀物和上清中的蛋白条带,富集后再采用蛋白质谱方法对蛋白进行分析,从而对样品中蛋白进行定性定量表征。
2、具体地,本发明的技术方案如下所述:
3、一种猪源性小肠粘膜下基质材料中活性蛋白的表征方法,包括以下步骤:
4、(1)将猪小肠粘膜下细胞外基质材料采用高速低温匀质法进行处理,得到均匀匀浆,向匀浆中加入胃蛋白酶和盐酸溶液温育搅拌诱导凝胶化,得到凝胶化的产物;调节凝胶化的产物的ph至7.4,离心分离出上清液与沉淀;
5、(2)将所述沉淀重悬于1×pbs溶液中,得到沉淀悬浮液,将所述沉淀悬浮液剧烈振荡后均匀化处理,得到均匀化的沉淀,保存备用;
6、(3)将所述上清液冻干,得到冻干产物,将所述冻干产物再水化,将水化后的产物离心获得澄清溶液,吸取澄清溶液,稀释至体积与所述上清液体积相同,保存备用;
7、(4)将所述凝胶化的产物、所述均匀化的沉淀以及所述澄清溶液通过蛋白检测试剂盒对总蛋白含量进行检测;
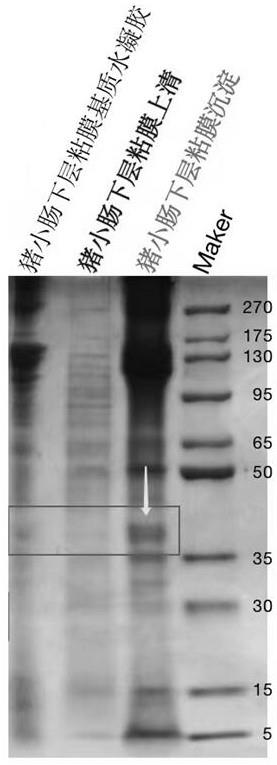
8、(5)将所述均匀化的沉淀以及所述澄清溶液用丙酮沉淀法提取蛋白,复溶后进行聚丙酰胺凝胶电泳,对所述均匀化的沉淀以及所述澄清溶液中的蛋白进行定性定量检测;
9、(6)将所述均匀化的沉淀以及所述澄清溶液分别通过液质联用进行分析,得到蛋白质谱分析结果。
10、在一种具体的实施方式中,步骤(1)中将猪小肠粘膜下细胞外基质材料采用高速低温匀质法进行处理,得到均匀匀浆的具体步骤为:将猪小肠粘膜下细胞外基质材料剪碎,置于匀质仪器中,在转速6500-8000r/min下,采用液氮冷却研磨至均匀匀浆;
11、在一种具体的实施方式中,步骤(1)中胃蛋白酶的浓度为0.5-1.5mg/ml,盐酸溶液的浓度为0.005-0.015m,ph为2.0。
12、在一种具体的实施方式中,步骤(1)中温育搅拌诱导凝胶化的具体步骤为:37℃温育搅拌46-50小时诱导凝胶化。
13、在一种具体的实施方式中,步骤(2)中将所述沉淀悬浮液剧烈振荡后均匀化处理,得到均匀化的沉淀的具体步骤为:将所述沉淀悬浮液剧烈振荡后通过移液管尖端并加压通过300μm过滤器,得到均匀化的沉淀。
14、在一种具体的实施方式中,步骤(2)中保存备用的保存温度为−80°c。
15、在一种具体的实施方式中,步骤(3)中将所述冻干产物再水化的具体步骤为:将所述冻干产物用无菌水以其原始体积的10%比例再水化。
16、在一种具体的实施方式中,步骤(3)中保存备用的保存温度为−80°c。
17、在一种具体的实施方式中,步骤(4)中的蛋白检测试剂盒为pierce™ bca 蛋白检测试剂盒(thermo scientific™,23227)。
18、在本发明的第二方面,提供一种第一方面所述猪源性小肠粘膜下基质材料中活性蛋白的表征方法在细胞外基质材料检测中的应用。
19、本发明具有以下有益效果:
20、本发明采用高速低温匀质法对猪源性小肠粘膜下细胞外基质材料进行研磨处理,在不破坏产品中蛋白活性的前提下将样品中蛋白充分暴露。
21、本发明利用酸化胃蛋白酶对样品进行酶解,在37℃条件下将酶解的产物诱导成凝胶,然后通过离心进一步处理非蛋白成分,采用聚丙酰胺凝胶电泳法富集出样品中关键蛋白分子,采用蛋白质谱采集的raw文件,经过软件maxquant(2.1.4.0)数据库检索,得到鉴定蛋白,此方法样品制备和处理对蛋白保护性好,可有效鉴定出活性蛋白,为后续的深化研究和产品设计开发提供支持。
技术特征:
1.一种猪源性小肠粘膜下基质材料中活性蛋白的表征方法,其特征在于,包括以下步骤:
2.如权利要求1所述的表征方法,其特征在于,步骤(1)中将猪小肠粘膜下细胞外基质材料采用高速低温匀质法进行处理,得到均匀匀浆的具体步骤为:将猪小肠粘膜下细胞外基质材料剪碎,置于匀质仪器中,在转速6500-8000r/min下,采用液氮冷却研磨至均匀匀浆。
3.如权利要求1所述的表征方法,其特征在于,步骤(1)中胃蛋白酶的浓度为0.5-1.5mg/ml,盐酸溶液的浓度为0.005-0.015m,ph为2.0。
4.如权利要求1所述的表征方法,其特征在于,步骤(1)中温育搅拌诱导凝胶化的具体步骤为:37℃温育搅拌46-50小时诱导凝胶化。
5.如权利要求1所述的表征方法,其特征在于,步骤(2)中将所述沉淀悬浮液剧烈振荡后均匀化处理,得到均匀化的沉淀的具体步骤为:将所述沉淀悬浮液剧烈振荡后通过移液管尖端并加压通过300μm过滤器,得到均匀化的沉淀。
6.如权利要求1所述的表征方法,其特征在于,步骤(2)中保存备用的保存温度为−80°c。
7.如权利要求1所述的表征方法,其特征在于,步骤(3)中将所述冻干产物再水化的具体步骤为:将所述冻干产物用无菌水以其原始体积的10%比例再水化。
8.如权利要求1所述的表征方法,其特征在于,步骤(3)中保存备用的保存温度为−80°c。
9.如权利要求1所述的表征方法,其特征在于,步骤(4)中的蛋白检测试剂盒为pierce™ bca 蛋白检测试剂盒(thermo scientific™,23227)。
10.权利要求1~9任一项所述的猪源性小肠粘膜下基质材料中活性蛋白的表征方法在细胞外基质材料检测中的应用。
技术总结
本发明涉及生物技术领域,具体涉及猪源性细胞外基质材料中活性蛋白的检测方法,方法包括:(1)将猪小肠粘膜下细胞外基质材料处理得到凝胶化的产物,离心分离出上清液与沉淀;2)将沉淀重悬于1×PBS溶液中,得到沉淀悬浮液,均匀化处理得到均匀化的沉淀;3)将上清液冻干,将冻干产物再水化,将水化后的产物离心获得澄清溶液,保存备用;4)将凝胶化的产物、均匀化的沉淀以及澄清溶液通过蛋白检测试剂盒对总蛋白含量进行检测;5)对均匀化的沉淀以及澄清溶液中的蛋白进行定性定量检测;6)将均匀化的沉淀以及澄清溶液分别通过液质联用进行分析,得到蛋白质谱分析结果。本发明的方法对蛋白保护性好,可有效鉴定出活性蛋白。
技术研发人员:刘成虎,孙晓霞,林振华,阮文婷,屈秋锦,王国伟
受保护的技术使用者:山东省医疗器械和药品包装检验研究院
技术研发日:
技术公布日:2024/1/16
- 还没有人留言评论。精彩留言会获得点赞!