一种评价体外扩增CD8+T细胞的杀伤能力的方法与流程
本发明属于免疫治疗,具体涉及一种评价体外扩增cd8+t细胞的杀伤能力的方法。
背景技术:
1、细胞毒性t淋巴细胞(ctl细胞),通常称为cd8+t细胞,是一种抗原特异性t细胞,是适应性免疫系统的关键组成部分,监视机体并清除感染,尤其是在消除细胞内感染和恶性细胞中发挥关键作用,同时可提供长期保护性免疫(cd8+t cell metabolismin infectionand cancer.nat rev immunol.2021nov;21(11):718-738.)。cd8+t细胞在人外周血单核细胞的t细胞中的占比仅为5~30%,经过体外扩增的cd8+t细胞在体外扩增的t细胞中的占比远高于在人外周血单核细胞中的,同时静息的cd8+t细胞通过体外扩增能够成为细胞毒性效应细胞,体外扩增的cd8+t细胞还可生成多种有助于宿主防御的细胞因子(包括ifnγ和tnfα)。因此评价体外扩增cd8+t细胞的杀伤能力具有重要意义。
2、体外扩增cd8+t细胞的杀伤能力可通过检测cd107a分子表达反映,但目前的研究表明cd107a分子表达不稳定。脱颗粒是穿孔素和颗粒酶依赖性靶细胞杀伤途径的关键过程,也是抗原特异性cd8+t细胞介导的细胞杀伤功能的最主要途径。脱颗粒过程中,cd8+t细胞的溶细胞颗粒膜与活化的质膜融合,同时cd107a膜蛋白被合并到活化cd8+t细胞的质膜中,导致cd107a分子暴露于cd8+t细胞表面。因此cd107a分子是cd8+t细胞脱颗粒的一种敏感标志,与细胞毒活性直接相关,可反映细胞毒性t细胞的杀伤能力。但是cd107a在脱颗粒结束后会从细胞表面内吞,进入酸性内体或溶酶体室,cd107a在cd8+t细胞表面的表达会减少甚至消失的,因此cd107a的表达是动态、不稳定的,所以针对体外扩增cd8+t细胞的cd107a表达的检测更具有挑战性。
3、目前的研究主要利用流式细胞术检测体外扩增cd8+t细胞的cd107a的膜表达,但是这些流式细胞术检测方法中存在诸多问题:如对样本的处理操作繁琐、费时致真实性不足、成本高、检测结果分析有一定主观性、无法准确定量、指标判断单一、敏感度低。
技术实现思路
1、本发明的目的在于提供一种评价体外扩增cd8+t细胞的杀伤能力的方法,简单特异、成本低、真实和稳定性好,敏感性高。
2、本发明提供了一种评价体外扩增cd8+t细胞的杀伤能力的方法,包括以下步骤:(1)将体外培养的cd8+t细胞分为实验组和同型对照组,其中利用cd8和cd107a抗体对所述实验组避光染色,利用同型抗体对所述同型对照组避光染色;
3、(2)依次利用流式细胞仪检测实验组和同型对照组的cd107a的阳性率和平均荧光强度,当cd8+t细胞表面的cd107a的阳性率>8%,且实验组与同型对照组的cd107a平均荧光强度的比值>2,说明所述cd8+t细胞有活化杀伤能力。
4、优选的,步骤(1)中将体外培养的cd8+t细胞分为实验组和同型对照组前,还包括对细胞悬液进行计数。
5、优选的,步骤(1)体外培养的cd8+t细胞的细胞悬液的培养天数为12~21天。
6、优选的,所述cd8+t细胞来源于人体或动物。
7、优选的,步骤(1)所述同型抗体包括与实验组的一抗完全相同种属来源、相同亚型及荧光标记的抗体。
8、优选的,在步骤(1)所述避光染色结束后,还包括利用洗液洗涤并离心,离心结束后,用洗液重悬洗涤后的细胞,而后进行流式细胞仪检测;所述洗液包括生理盐水或pbs。
9、优选的,所述避光染色的时间为50~70min。
10、优选的,所述避光染色的温度为34~38℃。
11、优选的,所述离心的离心力为150~500g。
12、优选的,所述离心的时间为4~10min。
13、优选的,步骤(2)所述流式细胞仪检测,包括:根据前向散射光、侧向散射光调整电压大小和增益参数,使目标细胞团位置处于视野范围内,并且能与细胞碎片分开;选取目标细胞并设门;通过同型对照组设阴性置信区;完成样品数据的获取。
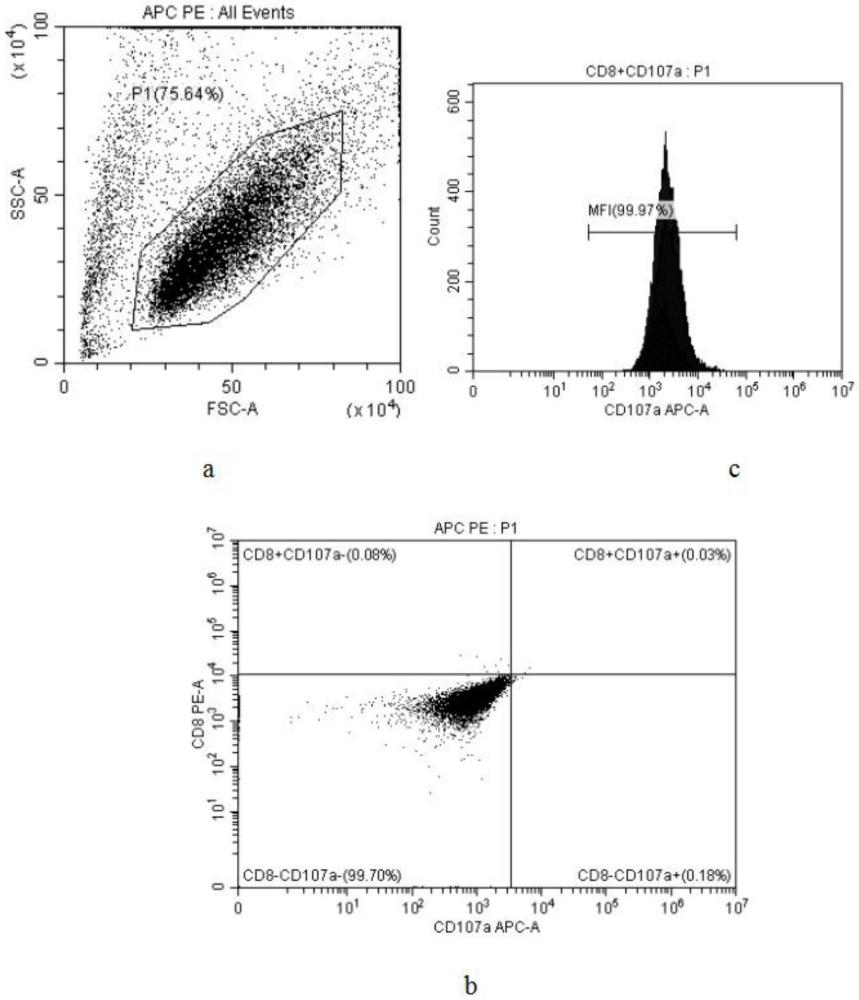
14、优选的,所述同型对照组设阴性置信区,包括:设定cd8/cd107a散点图中十字门的左下方为阴性置信区,使得阴性置信区细胞百分比≥99%。
15、有益效果:本发明提供了一种评价体外扩增cd8+t细胞的杀伤能力的方法,利用cd107a评价体外扩增cd8+t细胞的杀伤能力的流式细胞术检测方法,使用抗体标记cd8+t细胞表面膜蛋白cd107a,并采用流式细胞仪检测细胞cd107a的阳性率和平均荧光强度,通过cd8+t细胞表面cd107a的表达水平评价该cd8+t细胞的杀伤能力。本发明以体外扩增的cd8+t细胞的cd107a的表达作为评价标准,直接用培养的细胞悬液作为样本,减少了实验步骤和降低了实验成本,同时能够真实的反映出体外扩增cd8+t细胞的cd107a膜表达量。本发明在评价时,设置了同型对照组,对同型对照界定阴性置信区的细胞数量百分比进行了限定,解决了不能准确定量和具有一定主观性的问题。本发明利用cd107a的阳性率和平均荧光强度两个指标评价体外扩增cd8+t细胞的cd107a的表达能力,相对于现有技术更敏感。本发明在检测的过程中无需染色前洗涤和加入肽库的刺激,未来对开发和改造cd8+t细胞的培养工艺起到一定的促进作用。
技术特征:
1.一种评价体外扩增cd8+t细胞的杀伤能力的方法,其特征在于,包括以下步骤:(1)将体外培养的cd8+t细胞分为实验组和同型对照组,其中利用荧光标记cd8和cd107a抗体对所述实验组避光染色,利用同型抗体对所述同型对照组避光染色;
2.根据权利要求1所述方法,其特征在于,步骤(1)中将体外培养的cd8+t细胞分为实验组和同型对照组前,还包括对细胞悬液进行计数。
3.根据权利要求1或2所述方法,其特征在于,步骤(1)体外培养的cd8+t细胞的细胞悬液的培养天数为12~21天。
4.根据权利要求3所述方法,其特征在于,所述cd8+t细胞来源于人体或动物。
5.根据权利要求1所述方法,其特征在于,步骤(1)所述同型抗体包括与实验组的一抗完全相同种属来源、相同亚型及荧光标记的抗体。
6.根据权利要求1所述方法,其特征在于,在步骤(1)所述避光染色结束后,还包括利用洗液洗涤并离心,离心结束后,用洗液重悬洗涤后的细胞,而后进行流式细胞仪检测;所述洗液包括生理盐水或pbs。
7.根据权利要求6所述方法,其特征在于,所述避光染色的时间为50~70min,避光染色温度为34~38℃。
8.根据权利要求6所述方法,其特征在于,所述离心的离心力为150~500g,离心的时间为4~10min。
9.根据权利要求1所述方法,其特征在于,步骤(2)所述流式细胞仪检测,包括:根据前向散射光、侧向散射光调整电压大小和增益参数,使目标细胞团位置处于视野范围内,并且能与细胞碎片分开;选取目标细胞并设门;通过同型对照组设阴性置信区;完成样品数据的获取。
10.根据权利要求9所述方法,其特征在于,所述同型对照组设阴性置信区,包括:设定cd8/cd107a散点图中十字门的左下方为阴性置信区,使得阴性置信区细胞百分比≥99%。
技术总结
本发明公开了一种评价体外扩增CD8+T细胞的杀伤能力的方法,属于免疫治疗技术领域。本发明提供的一种评价体外扩增CD8+T细胞的杀伤能力的方法,使用抗体标记CD8+T细胞表面的膜蛋白CD107a,并采用流式细胞仪检测细胞CD107a的阳性率和平均荧光强度,通过CD8+T细胞表面CD107a的表达水平来评价该CD8+T细胞的杀伤能力。本发明所述方法简单特异、成本低、真实和稳定性好,敏感性高,能够更好的监视体外扩增的CD8+T细胞的杀伤能力,未来对开发和改造CD8+T细胞的培养工艺起到一定的作用。
技术研发人员:张菊,王静雪,吴修泉,洪辅安,孙乙天
受保护的技术使用者:深圳锦时生物科技有限公司
技术研发日:
技术公布日:2024/8/26
- 还没有人留言评论。精彩留言会获得点赞!