联合检测待测样品中多种抗生素的方法及试剂盒与流程
本发明涉及生物检测领域,具体涉及联合检测待测样品中多种抗生素的方法及试剂盒。
背景技术:
1、抗生素,又称为抗菌素,是指由微生物(包括细菌、真菌、放线菌属)或高等动植物在生活过程中所产生的具有抗病原体或其他活性的一类次级代谢产物,能干扰其他生活细胞发育功能的化学物质。抗生素的使用对医学产生了巨大的影响,是医院中日常用量较大的抗感染药物,但抗生素在全世界范围内滥用的现象相当普遍,病人在生病预防感染中会使用一种或或多种抗生素,同时,由于在养殖过程中,对家禽及水产生物也会使用抗生素,人在食用含有抗生素的食物会导致抗生素在人体内累积,当人体内积累部分抗生素增加到一定量时,会影响人体的正常生理机能,甚至导致耐药菌的产生和变异,从而使一些常用抗生素失去功效,催生了抗生素治不死的超级细菌,故各个国家对于抗生素的监测越来越重视,合理使用抗生素、规避抗生素滥用,对疾病的预防和治疗有有十分重要意义。
2、已提出基于抗生素浓度水平的治疗药物监测(tdm)来优化暴露。免疫测定法作为一种实施tdm的方法被广泛使用。然而,它们在体内常受人抗体的影响,缺乏特异性和准确性,且检测成本较高。高效液相色谱(hplc)检测仪器是可靠的,但检测效率较低,且检测时间较长。液相色谱串联质谱法(lc-ms/ms)方法作为一种相对较新的技术,克服了检测周期长、样品采集量大的缺点,在实验室监测中得到广泛应用。然而,大多数lc-ms/ms方法只能同时检测少量抗生素,且很少能够检测抗真菌药物。
3、因此,如何一次性准确监测人体内多种抗生素,包括抗真菌药物的浓度水平非常重要。
技术实现思路
1、发明目的:解决上述相关技术中的技术问题之一。
2、技术方案:联合检测待测样品中多种抗生素的方法,包括
3、第一步,校准曲线和质控样本准备,包括储备液制备、校准曲线与质控品配制、同位素内标配制。
4、第二步,将待测样品进行处理,所述待测样品为离体的血清样本;
5、第三步,将样本进行液相色谱分离-质谱检测;
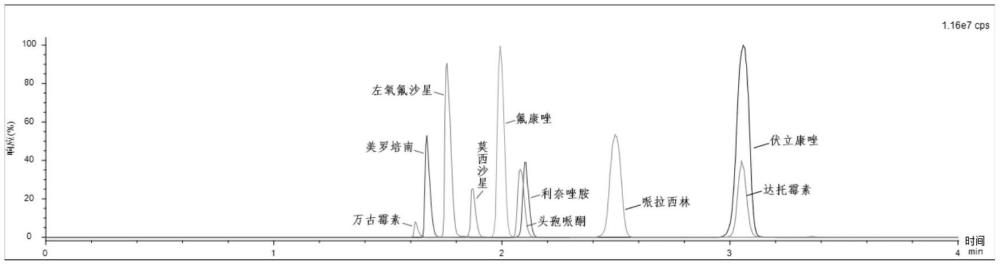
6、第四步,基于液相色谱分离-质谱检测结果,确定所述待测样品中各抗生素的含量,所述抗生素包括万古霉素、美罗培南、左氧氟沙星、莫西沙星、利奈唑胺、氟康唑、头孢哌酮、哌拉西林、伏立康唑、达托霉素;
7、所述液相色谱分离-质谱检测中,色谱柱温箱40℃;流动相a为0.1%甲酸水,流动相b为0.1%甲酸乙腈/甲醇(1:1),流速为0.5ml/min,进样体积10μl,样品室温度8℃;洗脱程序如表1所示:
8、表1
9、
10、
11、质谱条件为:电喷雾电离方式,正离子模式下进行检测;扫描方式:多重反应监测模式。离子源参数如下:毛细管电压4kv,真空接口温度115℃,去溶剂气温度400℃,雾化气流速1.5l/min,去溶剂气流速8l/min,反吹气流速2l/min;分析物离子对参数如表2;
12、表2
13、
14、进一步,所述的储备液配制:使用十万分之一天平称量10个目标物于50ml离心管中,万古霉素称量21.05mg,达托霉素称量40.82mg,美罗培南称量23.04mg,利奈唑胺称量4.02mg,伏立康唑称量4.01mg,头孢哌酮称量85.29mg,哌拉西林称量100mg,左氧氟沙星称量8.24mg,莫西沙星称量4.58mg,氟康唑称量10.02mg,溶解于10ml dmso/甲醇/水溶液中(v:v:v=1:10:9),储存与-80℃。
15、进一步,所述的校准曲线与质控品配制:储备液与无药物空白血
16、清混合,使得万古霉素、美罗培南、氟康唑、头孢哌酮、利奈唑胺、左氧氟沙星、哌拉西林、莫西沙星、伏立康唑、达托霉素在工作校准曲中的最高浓度分别为99.99mg/l、99.99mg/l、49.10mg/l、400.01mg/l、19.90mg/l、40.38mg/l、480.50mg/l、22.67mg/l、19.65mg/l、200.02mg/l;校准曲线其他浓度点为最高浓度与空白血清混合,梯度稀释而来;
17、所述的质控品配制:万古霉素的浓度为3.81mg/l-35.19mg/l;美罗培南的浓度为4.46mg/l-40.21mg/l;氟康唑的浓度为1.38mg/l-13.44mg/l;头孢哌酮的浓度为15.26mg/l-146.72mg/l;利奈唑胺的浓度为0.96mg/l-8.6mg/l;左氧氟沙星的浓度为1.14mg/l-10.57mg/l;哌拉西林的浓度为13.49mg/l-125.85mg/l;莫西沙星的浓度为0.79mg/l-7.4mg/l;伏立康唑的浓度为0.72mg/l-7.21mg/l;达托霉素的浓度为10.56mg/l-85.58mg/l
18、在校准曲线最高浓度点和质控品配制过程中,为保证血清的完整性,水、甲醇、dmso的总含量的最终体积保持在≤10%。
19、进一步,所述的同位素内标的配制:内标伏立康唑-[13c2,d3],美罗培南-[d6],利奈唑胺-[d3],哌拉西林-[d5],左氧氟沙星-[d3]的储备液浓度为1mg/ml,莫西沙星-[d4]的储备液浓度为2mg/m,去甲万古霉素的储备液浓度40mg/ml。内标工作液中伏立康唑-[13c2,d3],利奈唑胺-[d3]的浓度为0.1mg/ml,美罗培南-[d6],哌拉西林-[d5],左氧氟沙星-[d3],莫西沙星-[d4]的浓度为0.2mg/ml,去甲万古霉素的浓度为4mg/ml,混合于甲醇溶液中,使用前存放于-80℃。
20、进一步,所述的样品处理:血清校准曲线各个点和低、中、高三水平质控品与内标工作液混合,试管涡旋混合,离心,用0.1%甲酸水稀释上清,然后将样品注入lc-ms/ms中,进行监测所有分析物的反应。
21、有益效果:
22、1、检测结果在测试浓度范围内呈线性。
23、2、对精密度数据进行分析,每个分析物三水平质控品的批内精密度均≤10%,每个分析物三水平质控品大部分批间精密度也≤10%,除了莫西沙星低浓度质控品的批间精密度为11%。
24、3、信号交叉贡献;每个分析物在定量上限自然发生的同位素转换在所选内标mrm离子对产生的交叉信号贡献为所设定的内标浓度信号的<5%。在所选内标溶液中的无分析物信号干扰。
25、4、通过先检测最高校准曲线浓度,然后再检测双空白血清提取物来进行评估。跟进检测结果,十种分析物在空白样品的响应不超过分析物定量限响应的10%,其中万古霉素的残留比例为0.00%。
技术特征:
1.联合检测待测样品中多种抗生素的方法,其特征在于,包括
2.根据权利要求1所述的联合检测待测样品中多种抗生素的方法,其特征在于,所述的储备液配制:使用十万分之一天平称量10个目标物于50ml离心管中,万古霉素称量21.05mg,达托霉素称量40.82mg,美罗培南称量23.04mg,利奈唑胺称量4.02mg,伏立康唑称量4.01mg,头孢哌酮称量85.29mg,哌拉西林称量100mg,左氧氟沙星称量8.24mg,莫西沙星称量4.58mg,氟康唑称量10.02mg,溶解于10ml dmso/甲醇/水溶液中(v:v:v=1:10:9),储存与-80℃。
3.根据权利要求1或2所述的联合检测待测样品中多种抗生素的方法,其特征在于,所述的校准曲线与质控品配制:储备液与无药物空白血清混合,使得万古霉素、美罗培南、氟康唑、头孢哌酮、利奈唑胺、左氧氟沙星、哌拉西林、莫西沙星、伏立康唑、达托霉素在工作校准曲中的最高浓度分别为99.99mg/l、99.99mg/l、49.10mg/l、400.01mg/l、19.90mg/l、40.38mg/l、480.50mg/l、22.67mg/l、19.65mg/l、200.02mg/l;校准曲线其他浓度点为最高浓度与空白血清混合,梯度稀释而来;
4.根据权利要求1或2所述的联合检测待测样品中多种抗生素的方法,其特征在于,所述的同位素内标的配制:内标伏立康唑-[13c2,d3],美罗培南-[d6],利奈唑胺-[d3],哌拉西林-[d5],左氧氟沙星-[d3]的储备液浓度为1mg/ml,莫西沙星-[d4]的储备液浓度为2mg/m,去甲万古霉素的储备液浓度40mg/ml。内标工作液中伏立康唑-[13c2,d3],利奈唑胺-[d3]的浓度为0.1mg/ml,美罗培南-[d6],哌拉西林-[d5],左氧氟沙星-[d3],莫西沙星-[d4]的浓度为0.2mg/ml,去甲万古霉素的浓度为4mg/ml,混合于甲醇溶液中,使用前存放于-80℃。
5.根据权利要求1或2所述的联合检测待测样品中多种抗生素的方法,其特征在于,所述的样品处理:血清校准曲线各个点和低、中、高三水平质控品与内标工作液混合,试管涡旋混合,离心,用0.1%甲酸水稀释上清,然后将样品注入lc-ms/ms中,进行监测所有分析物的反应。
技术总结
本发明是一种联合检测样品中多种抗生素和病毒的方法,根据本发明的所述,包括:①校准曲线和质控样本准备;②将待测离体的血清样品进行处理;③将样本进行液相色谱分离‑质谱检测;④基于液相色谱分离‑质谱检测结果,确定所述待测样品中各抗生素的含量,相比现有技术,本发明检测的数据量更多,成本与时间都降低,同时从不同侧面展示了检测方法的可靠性:包括检测限、准确度、批间及批内精密度、残留等信息。
技术研发人员:刘婷婷,陈晓敏,李洪霞,曹彬,朱平,张关璇子,蔡云枫
受保护的技术使用者:中国人民解放军总医院第二医学中心
技术研发日:
技术公布日:2024/11/26
- 还没有人留言评论。精彩留言会获得点赞!