经皮系统、装置和方法与流程
本发明涉及涉及医疗装置和手术装置。更具体地,本发明涉及经导管系统和相应的治疗装置和方法。本发明作为机械循环支持系统,例如用于治疗循环衰竭、心力衰竭、需要循环辅助仪器的心脏状况尤其有益,但也具有广泛的用途。
背景技术:
机械循环支持系统(MCS)的实例包括心室辅助装置(VAD)。VAD是可以支持心脏功能和血液流动的机械泵装置。具体而言,VAD帮助心脏的一个或两个心室通过循环系统泵送血液。目前可获得左心室辅助装置(LVAD)、右心室辅助装置(RVAD)和两心室辅助装置(BiVAD)。并且,循环支持系统可以包括心肺支持(CPS,ECMO),其提供血氧合和血液泵送。在心脏手术或严重的心脏病(例如,心力衰竭、心肺骤停、心律不齐、或心源性休克)治疗之前和/或之后可能需要这种装置。
传统上,VADs配备在通过胸部开刀的心内直视手术过程,该过程涉及穿刺左心室的尖端通过外部泵重新形成血液从主动脉到心室的路线。外科手术中使用的VAD的一个示例是HeartMate II设备。这种手术明显具侵略性,因需要大量的康复时间并有感染和创伤风险而不适合于较弱的患者。尤其是在对儿童的治疗中,现有的外科手术仪器和设备相对较笨重和更具侵略性,鉴于所涉及的仪器和方法,减小设备的尺寸如果不是不可能也通常是很困难的。此外,这些设备的使用需要医院中一群熟练的手术人员,因此可用性较低且昂贵。
更多程序是非手术性的以及涉及通过患者的腹股沟处的小切口插入VAD。这种所谓经皮VAD的一种常见类型是TandemHeart装置。通过邻近患者腹股沟的切口引入管子,并沿着股骨颈脉和下腔静脉前行,横穿内心房隔膜进入左心房,由此来自左心房的氧合血被送入位于患者身体外部的泵装置并通过流出管再循环进入股骨动脉。虽然此设备具有满意的效果,但它只能提供短期支持(最长至两周)而不能用于长期治疗。外部泵体积庞大,只要配有该设备就要求患者不能移动。并且,腹股沟切口附近还有威胁生命的感染风险因该切口在治疗过程中始终是开放的,并且有主动脉大出血的风险。此外,TandemHeartTM的管子终止于左心房内,血液从左心房泵出并导至患者的身体外部。这种血液进入系统可能会被阻塞,如果未被阻塞,如果周围组织被意外吸入,会导致该系统功效丧失。
另一种常见的经皮VAD是Impella设备,它被插入股动脉和下行的主动脉。Impella设备包括细长的末端,其被植入横穿天然的主动脉瓣并将一血液入口置于左心室内以及一血液出口置于主动脉瓣上方。泵使血液从入口循环到出口。在使用过程中,动力传动系统外化经过股骨动脉,具有和TandemHeartTM以及其他当前的经皮MCS系统一样的使用局限性。此设备最多能提供支持一周。因此需要一种装置,其具有降低的感染和出血风险以及增强的机械稳定性,可用作短期"复苏桥"治疗的一部分或允许病患者活动长期治疗。此外,泵的效率是有限的因为无法插入一具有使用经皮动脉通道提供合适的血流量所必需的尺寸的泵。目前,经皮MCS的有限的泵容量和持续时间的问题以及上述所有的潜在问题是通过手术插入较大的体内泵或选择体外泵来解决的。
现有的机械循环支持系统是拯救生命的。然而,他们仍然昂贵、复杂、临床潜力有限且大多数患者仍无助逝世。
目前可用的经皮治疗依靠患者的尚未损坏的解剖学上的血管结构的主要结构。然而,很多心脏病患者是有先天性心脏缺陷的儿童或者常伴有解剖学上的血管异常,例如,钙化和心脏瓣膜疾病的老年患者。通过手术可以克服这种限制但随之而来的是手术创伤有关的风险。因此需要一种可以安全并可预见地通过经皮获取从一个解剖结构到另一个解剖结构的通道而实施的方法和设备,因为这将允许在无手术创伤的同时安全传递更高效的泵。
技术实现要素:
本发明的目的是缓解上述问题。
根据本发明的第一方法,经导管系统包括穿过至少一个解剖壁体内流体连通两解剖隔室的连接器。更具体地,连接器配置为接收一体内流动调节装置。
在本发明的语境中,经导管包括经皮、经心房、经股动脉(穿过大腿)、经心尖(肋骨间的胸部内)、和经主动脉(上胸部内)。较优的实施方式是经皮系统、装置和方法。
根据本发明的系统是经导管系统,因此无需侵略性的有创伤手术(该手术对于安置HeartMate系统是必需的)。此外,连接器和流动调节装置都是体内的,这样无需主要的外部部件。无需像在使用HeartMate系统的情况下完全固定患者,在该情况下需要体外泵。因此,本系统可被用于短期、中期、长期治疗。此外,通过穿过一个或两个解剖壁连接两解剖隔室,本系统可绕过有缺陷的或异常的解剖学上的部分。不用修复或替代现存有问题的解剖学上的部分,根据本发明的系统有效地为流体循环建立新的路径。因此,这是一种包容性更强更通用的治疗程序。
连接器可以对抗由流体(血液)流动施加的压力而维持解剖学上的结构和组织的完整性,由此流动调节装置防止隔室崩塌。
在一较优的实施方式中,当流动调节装置联结于连接器时,流体可从第一隔室流至第二隔室,而当流动调节装置不联结于连接器时,流体不能从第一隔室流至第二隔室。因此,流体调节装置行使连接器的致动器的功能,因此在没有流体调节装置的情况下,流体不能在隔室间流动。连接器通过经皮或经导管插入,之后跟着也通过经皮或经导管插入的流动调节装置。因此,流动调节装置在原位联结连接器。这是相对于现有系统(使用体外泵或在患者的体外装有VAD然后以一个体积庞大的设备插入的系统)的显著区别。本发明的优点尤其在于体内装置允许使用较小组件从而实现微创医疗过程。此外,本医疗程序对于小患者更理想,例如用于儿科用途。同样有趣的是,如下文所将详细阐述,流动调节装置和/或连接器是可收缩的。
在于当一个或两个隔室是循环系统的隔室时,本发明尤其有利。一个较优的实施方式涉及左心房-主动脉的过程。但是,其它隔室对可包括但不限于,右心室-主动脉,左心室-主动脉、右心房-上腔静脉、左心房-降主动脉、左心房-升主动脉、右心室-肺动脉。
当被用于治疗心力衰竭、舒张性心力衰竭、收缩性心力衰竭、左心室衰竭、右心室衰竭、儿科心脏异常和/或分流时,本发明尤其有利。可选地或额外地,一个或两个隔室是胸腔或腹腔内的隔室。
较优地,至少一个解剖壁是隔室的外壁。例如,对心脏进行本治疗后,人工流体通道是心外通道。在本发明的语境中,术语“心外通道”指心脏的内部和心脏的外部之间。
流体连通穿过的壁的数目取决于要连接的隔室。例如,左心房到主动脉的连接涉及穿过两个解剖壁的穿刺和流体连通(即,左心房的顶和主动脉壁),而右心房到左心房的连接只涉及一个解剖壁(即,心房隔膜)。建立流体连通穿过内解剖壁而不穿过外壁,例如皮肤组织。较优地,解剖隔室由两解剖壁分割。更优地,连接器连接解剖学上的不相邻的隔室。这意味着,例如两隔室互相非常靠近,但并不是解剖学地直接接触。这还可包括虽然两隔室的某些部分存在解剖学上的接触,但在该两隔室非解剖学的接触部分通过本发明的系统连接。举例来说,心脏的主动脉和左心房在某些部分解剖学上相接触,但形成的连接穿过左心房的顶和主动脉壁,两隔室在此处无解剖学上的接触。
较优地,连接器包括用于从一个隔室到另一个隔室的流体通道的颈部和使颈部横跨解剖壁的稳固装置。在使用中,连接器的颈部较优地横嵌入解剖壁,并且如果合适,横嵌入两解剖隔室/壁之间的间隙空间。较优地,颈部包括将流动调节装置固定或可拆卸地固定至连接器的装置。
颈部的一个实施例可以包括从一个隔室到另一个隔室的流体通路的通道。较优地,流体的通道沿着颈部的中心纵轴。颈部较优地被密封,这样就不会有流体侧漏进入解剖壁和/或进入分隔两解剖壁的任何空间。
颈部可能是容易移动的,不只因为患者的活动,还因为心脏跳动机制本身,因此包括将稳固或锚定颈部横跨解剖壁的装置。因此,稳固装置还包括从颈部的第一端延伸的锚部。所述锚部可以是可膨胀的。更优地,在稳固位置,锚部基本平行于解剖壁放置。在较优的实施例中,锚部可以基本垂直于颈部的第一端延伸并基本平行于解剖壁布置。较优地,锚部位于递送流体的解剖隔室内。锚部稳固颈部,因此连接器横跨解剖壁,但也辅助维持解剖壁的完整性。
在一个实施例中,(展开的)锚部基本呈圆盘形。在另一个实施例中,锚部包括多个可展开的臂。较优地,可展开的臂弯曲或可包括一个或多个肘部。
连接器还可被稳固于解剖壁,例如通过使用由可膨胀材料制成的颈部,这样颈部在未膨胀状态时被插入,随着释放而膨胀以便紧密地接触穿过解剖壁的开口。
较优地,连接器包括防止组织妨碍穿过颈部的流体通路的装置。流体通路,尤其是在使用泵装置的情况下,形成将周围的组织吸向连接器的颈部的吸力。阻止装置可包括从所述的颈部的第二端延伸的屏蔽。屏蔽可以是可膨胀的。屏蔽防止周围的组织陷入连接器的颈部,还防止流体通路被阻碍。本类型的屏蔽还可用作将连接器的颈部稳固在其正确位置的装置。较优地,屏蔽位于移出流体的解剖隔室内。较优地,屏蔽在膨胀状态基本呈伞形或碗形。此实施例的优点在于周围的组织不直接摩擦屏蔽并且不被吸入屏蔽,这样可以避免擦伤和损伤。优选网状或格状材料以便最小化引入患者体内的外源材料。屏蔽防止组织的阻碍,但还稳固穿过解剖壁的连接器并辅助维持解剖壁的完整性。
在一个实施例中,(展开的)屏蔽基本呈碗形或伞形。在另一个实施例中,屏蔽包括多个可展开的臂。较优地,可展开的臂弯曲。
尽管在此描述的较优的连接器包括一个锚部和一个屏蔽,还可设置连接器包括一个锚部或一个屏蔽,两个锚部或两个屏蔽。
如上所述,解剖壁的完整性由于流体/血液流动所施加的压力和流动调节装置可以妥协。根据本发明的系统包括维持解剖壁完整性的装置,具体为例如,连接器的锚部和屏蔽。当将本发明用于脆弱的解剖壁,例如主动脉壁时,本发明尤为可贵。操作主动脉壁时必须极其小心,因为主动脉破裂或任何栓塞可能产生严重的如果不是致命的后果。本发明提供一种方法、系统和设备,其允许安全的穿刺、递送、插入和植入。
在一较优的实施例中,连接器全部或部分地由形状记忆性材料制成。因此,非展开的连接器可插入一鞘用于经导管引入患者体内。较优地,锚部和/或屏蔽由形状记忆性材料制成。通过一传递鞘,连接器可以以非展开的细长状态被引入。
较优地,颈部包括一门,该门选择性地阻止或允许穿过颈部的流体通路。在关闭状态,该门阻止从一个到另一个解剖隔室的流体通路。该门可被机械地启动、打开并维持在开放状态,例如通过上述的流动调节装置。
较优地,该装置包括将流动调节装置固定于连接器的固定装置。这种固定装置的一个实施例是如上所述的门,该门在流动调节装置的颈部周围关闭。在另一个实施例中,连接器和流动调节装置可包括互相配合的固定装置(例如拧紧装置),较优地,该固定装置位于连接器的颈部的内表面和流动调节装置的中间部的外表面。
在另一个实施例中,连接器的锚部和/或屏蔽包括多个臂。臂从颈部的一端或两端延伸以形成锚部和/或屏蔽。臂可沿着颈部的内表面延伸以形成将流动调节装置固定至连机器的拧紧装置。
拧紧装置的优点尤其在于流动调节装置可被(可拆卸地)固定于连接器,但还可被用于辅助流动调节装置向前穿过连接器并定位。
连接器可包括用于防止连接器和流动调节装置或固定装置之间的联结界面上不需要的流体流动的密封装置。在一较优的实施例中,连接器和流动调节装置包括互相配合的拧紧装置,密封装置包括镜像反映拧紧装置的螺旋轮廓的密封材料条带。因此,在使用时,密封装置夹在连接器的拧紧装置和流动调节装置的拧紧装置之间。
在一较优的实施例中,密封装置是可膨胀的。在其膨胀状态,密封装置是基本呈矩形的密封材料条带。在其收缩状体,密封装置基本呈螺旋形。密封装置可由柔性材料和/或形状记忆性材料制成。密封装置可包括将密封装置固定至连接器和/或流动调节装置的装置。
在一较优的实施例中,本系统还包括用于调节两解剖隔室之间流体流动的体内装置。此流动调节装置可使从一个隔室到另一个隔室的流体流动被中断或开启,或可调节该流体的流速。这一点尤其有利是因为本发明建立了穿过解剖壁的人造开口的流体连通,因此不存在调节解剖隔室间流体流动的天然机构。例如,在循环系统中,血液循环是通过心脏肌肉和天然开口调节的,例如动脉瓣膜或二尖瓣膜。本发明不依靠天然开口也不试图修复有缺陷的天然开口,但建立新的人工血液路径。
较优地,流动调节装置包括可以允许或阻止流体穿过体内连接器的致动器。因此,可以使用致动器开启或终止穿过连接器从一个解剖隔室到另一个解剖隔室的流体连通,较优地通过打开或关闭连接器的颈部的门。在一较优的实施例中,当流动调节装置机械地联结连接器,流体连通开启,当上述两装置被分开,流体连通则终止。
在一较优的实施例中,流动调节装置包括在使用时位于第一隔室的第一部、在使用时位于第二隔室的第二部、和在使用时穿过解剖壁的中间部。
较优地,在使用时,(即当流动调节装置正确地植入并横穿解剖壁时)中间部穿过并固定于连接器的颈部。更优地,在使用时,中间部穿过连接器的门。在一较优的实施例中,流动调节装置的中间部的外尺寸基本和连接器的颈部的内尺寸互相配合。
较优地,第一部包括一个或多个孔用于第一和第二隔室之间的流体连通。较优地,中间部包括用于第一和第二隔室之间流体连通的通道。较优地,第二部包括一个或多个个孔用于第一和第二隔室之间的流体连通。
在一较优的实施例中,当流动调节装置的中间部联结连接器时,流体可从第一隔室流至第二隔室,而当流动调节装置的中间部不联结连接器时,流体不能年从第一隔室流至第二隔室。
较优地,流动调节装置包括泵。由此,可以调节参数,例如两解剖隔室之间的流体流速和/或流体流动的时机。较优地,泵位于流动调节装置中的第一部。
本系统可包括治疗或处理流体的装置。在一些例子中,流体,例如血液,可能是有缺陷的或需要治疗。如果流通的血液缺氧,则可使其氧合。流动调节装置可包括输送氧气的装置,较优地,通过附加一外部氧合器线路至该装置,这样氧气可通过跨膜通路(膜氧合)释放或者通过微孔直接进入血液(泡氧合)。
此外,可通过将一种或多种药物化合物输送至流体治疗血液或相同地,当流体流经本发明的系统时可设计将一组分(例如污染物)从流体去除。这种输送或去除装置可以是化学过滤器,膜和/或连着物质传输线路的装置上的一个或多个开口。有利地,用于调节流体流动的体内装置包括流体治疗装置。如果需要,本系统还可从流体去除氧和/或其他气体。如果需要,也可以实现其他治疗,例如对流体加热或冷却。
流体治疗装置可以实现将一种或多种用于治疗流体或用于传送的药物化合物引入一个或两个隔室内和/或引入一个或多个气体,例如氧气。流动调节装置可包括调节治疗参数的控制器,例如时机、浓度和剂量。还可设计一缓慢或可控释放机构用于传送药物。
较优地,本系统包括将流动调节装置固定于连接器的装置。连接器和/或流动调节装置可包括一个或多个用于互相连接的固定装置。此两装置可以可拆卸或不可拆卸地互相固定。当由于解剖学上的活动(例如心脏肌肉的活动)、患者的活动、和/或流体流动而存在上述两装置意外脱离的风险时,固定装置尤为有利。
在一较优的实施例中,流动调节装置的第二部包括用于抵靠解剖壁或连接器的可膨胀锚部的一个或多个凸缘,由此固定流动调节装置到解剖壁和连接器。
较优地,中间部由可膨胀材料制成以紧密接触连接器的颈部的内表面,由此将流动调节装置固定于连接器。
在一较优的实施例中,第一部的横截面的直径比中间部的横截面的直径大。此特征的益处在于两个原因。第一,具有较小直径的中间部穿过解剖壁和/或连接器并且可被第一部和第二部固定定位。第二,流体被吸入具有较大直径的第一部并且流过具有较小直径的中间部,由此形成文丘里效应(Venturi effect)促进流动调节装置的泵送效率。
较优地,第二部基本呈锥形这样以利于流动调节装置插入并穿过连接器和/或解剖壁并使创伤的风险最小化。更优地,为了实现无损伤插入,第二部包括圆形的远尖端。
在一较优的实施例中,流动调节装置配置为接收穿过其中的导线。较优地,第一部、第二部和/或中间部包括包括接收穿过其中的导线的孔。较优地,流动调节装置配置为接收沿着其纵轴的导线。更优地,第一部、第二部和/或中间部包括接收穿过其中的导线的通道。最优地,通道沿着流动调节装置的纵轴设置。
在一较优的实施例中,流动调节装置是可收缩的。较优地,流动调节装置可被配置为以第一构型插入并穿过鞘,并以第二构型工作。较优地,流动调节装置包括一外壳。外壳较优地由柔性材料制成。这一点尤其有利因为它增大经导管传送的泵的潜在尺寸(由此提高效率),其还提高经导管磁驱动泵长期使用的能力。
在一较优的实施例中,流动调节装置可包括支撑至少一个叶片的可旋转轴,该叶片配置为沿轴的纵向延伸以进入插入构型,以及沿轴的纵向松弛以进入工作构型。
叶片在轴的横向方向的尺寸在工作构型时大于其在插入构型时。由此,叶片以及流动调节装置可容易地被插入鞘中。
较优地,叶片是螺旋形叶片。叶片可以是一片连续的叶片和/或蛇形叶片。较优地,叶片由弹性(记忆性)材料制成由此叶片可在轴的纵向延伸或伸展。
处于插入构型的流动调节装置可通过传递鞘或导管被传送到其工作位置。当流动调节装置离开鞘后,其展开进入工作构型并定位于横跨解剖壁的工作位置。在一较优的实施例中,流动调节装置的可伸缩外壳内包括轴和叶片组件。轴和叶片组件可在纵向伸展以进入插入构型从而使叶片横向方向的尺寸减小。
在另一实施例中,流动调节装置包括反向螺旋泵。在此实施例中,螺旋或叶片被形成在流动调节装置的内表面,因此流体从第一隔室被吸入第二隔室。
较优地,流动调节装置部分或全部地由磁性材料制成。例如,装置的一个或多个部件(例如,外壳、叶片、磁性轴承、磁性驱动器等)由磁性材料制成。
当一个或两个解剖隔室是循环系统的隔室时,本系统尤其有利。循环系统的隔室包括例如,左心房、右心房、左心室、右心室、主动脉、肺动脉、上腔静脉以及外周血管系统的动脉、静脉和其他隔室。更优地,根据本发明的系统建立相邻隔室之间的流体连通。
较优地,流体包括或是血液,其可被氧合或脱氧。根据本发明的系统有利地用作机械支撑系统,较优地用作机械循环支持系统,例如心室辅助装置。
在另一实施例中,连接器和流动调节装置构建为一个装置。
根据本发明的第二方面,提供一种如上所述的体内连接器。
根据本发明的第三方面,提供一种如上所述的体内流动调节装置。
根据本发明的第四方面,提供一种经导管插入装置,该装置包括具有整体形成的穿刺头的导线。该经导管插入装置使解剖学上的结构穿刺成为可能,例如分隔解剖隔室的解剖壁,并且对于具有较大组织抗力的解剖隔室的外壁穿刺尤其有利。较优地,穿刺头形成极尖锐的末端以利于使用者在使用的关键阶段获得更高的精度和更好的控制。通常不会使用这么尖锐的末端是因为存在意外穿刺和/或受伤的风险。但是在本发明中,经导管插入装置被配置为防止这种意外,这将在下文中详细阐述。
此外,插入装置用作导线,本发明系统的各种部件例如体内连接器或体内流动调节装置可越过该导线插入患者。由此,可以使用一个装置既用于穿刺步骤也用于穿刺过程中的的插入/传递步骤。在传统方法中,穿刺装置是通过使用一个单独的穿刺针工作的,其在穿刺之后被去除并紧跟着引入一导线。这在本发明不是必需的。在一已知的插入系统中,使用一中空的针刺穿皮肤。导线穿过针的通道插入,将针移除而将导线留下。然后沿导线插入导管,再取出导线将导管留下。在本发明中,穿刺由导线的远端,尤其是导线的穿刺头形成。这样可以形成平缓、无损伤并准确的切口,并且当刺穿解剖隔室的外壁,例如,为了形成心脏至心外(例如一个从心脏隔室到主要血管)的穿刺时,尤其有利。
较优地,穿刺头包括固体远尖端。换句话说,穿刺头非中空,或者不包括传统血管穿刺针的远端孔,因为这会导致不必要的较大切口并且通常需要施加为了穿刺成功而不希望有的力。不希望形成较大切口,那样有可能引起血液危险地高速流动。对于解剖壁的穿刺,例如主动脉壁,鉴于主动脉破裂的风险不推荐使用传统针。在另一常用的方法中,可使用标准导线进行穿刺。但是,标准导线具有圆形或扁平的头而无法实施准确的穿刺并且如果意外地从将被穿刺的解剖壁偏移会发生危险。更优地,本穿刺头包括锥形的远尖端。
在一较优的实施例中,锥形尖端的底的直径基本与导线的直径相等。
在一较优的实施例中,导线可以围着穿刺头绕圈。较优地,导线包括邻接穿刺头的柔性远端部和较刚性的近端部。这些特征在防止由穿刺体的锐度造成的损伤方面尤其有利。一旦形成穿刺,穿刺头和扩张器一起进入第二隔室。当扩张器被被取出,导线的柔性部变得没有支撑并且围着锚定的穿刺头绕圈从而提供穿刺头和周围组织之间的有效的屏蔽。更优地,导线由形状记忆性材料制成,因此导线可配制成围绕穿刺头的屏蔽。
较优地,插入装置还包括扩张器。更优地,穿刺头最宽处的横截面的尺寸基本等于扩张器的远端的尺寸。
较优地,插入装置包括传递鞘。更优地,插入装置包括内传递鞘和外传递鞘。在一较优的实施例中,插入装置包括具有穿刺头的导线、扩张器、内传递鞘和外传递鞘。
插入装置允许解剖壁的穿刺以及鞘或导管穿入患者为了随后引入经导管装置,并且插入装置还可包括引导鞘的装置。当医疗程序涉及穿过两层解剖壁的插入和植入时,本发明尤其有利。这是因为插入装置可推动一个壁接触另一个这样壁有利于穿刺和随后的插入以及植入。
本系统可以以包括体内连接器、体内流动调节装置和/或经导管插入装置的工具盒的形式呈现。
根据本发明的第五方面,提供一种经导管方法,该方法用于提供由至少一个解剖壁分隔的两解剖隔室之间的流体连通,该方法包括(a)穿刺分隔隔室的壁;(b)通过穿刺孔插入体内连接器;以及(c)将体内流动调节装置联结至体内连接器。较优地,步骤(c)在体内进行。
较优地,穿刺步骤通过使用如上文任意一段所述的插入装置实施。
较优地,体内连接器是如上文任意一段所述的连接器。
较优地,体内流动调节装置是上文任意一段所述的流动调节装置。
较优地,解剖隔室由两解剖壁分隔。更优地,此两解剖隔室在解剖学上不相邻。本发明的一个优点是可以通过人工流体连通路径在解剖学上明显区分的隔室之间形成流体通路。
较优地,本方法还包括在使用插入装置进行穿刺步骤(a)之前推挤两解剖壁以使其接触。
较优地,插入步骤(b)是通过使用插入装置实施的。插入装置的穿刺头可被用于执行步骤(a)以对解剖壁进行穿刺,以及使用导线执行插入过程中的步骤(b)。因此,在一较优的实施例中,插入装置包括具有整体形成的穿刺头的导线。
较优地,本方法包括使用穿刺头对分隔隔室的壁进行穿刺,以及使用导线引导体内连接器穿过穿刺孔。
较优地,本方法还包括插入流动调节装置并将其定位在相对于连接器的联结位置。
较优地,本方法包括使用插入装置的导线引导流动调节装置。
在一较优的实施例中,体内连接器和/或体内流动调节装置以收缩的状态插入体内。
较优地,本方法还包括将连接器固定于解剖壁。
较优地,本方法还包括将流动调节装置固定于连接器。
较优地,本方法还包括防止组织妨碍穿过流动调节装置的流体通路。
较优地,本方法还包括通过包括泵的流动调节装置调节流体的流动。
较优地,本方法还包括处理流体的步骤。在一较优的实施例中,对流体的处理,包括使流体接触一种或多种药物化合物,是通过使用上述的处理装置实施的。较优地,本方法包括使流体接触一种或多种气体,例如氧气。
在一较优的实施例中,本方法还包括从连接器分离开并取回流动调节装置。本发明对于永久或半永久性使用是理想的。但是,在一些情况下,流动调节装置可能需要被取回,例如出于替换和/或修复的目的。
较优地,分离并取回流动调节装置是通过使用取会装置实施的。更优地,取回装置包括抓取流动调节装置的装置。
较优地,一个或两个隔室是循环系统的隔室。更优地,隔室之一是心脏的左心房和/或主动脉的隔室。最优地,解剖壁是左心房的顶和主动脉壁。
根据本发明的第六个方面,提供一种插入经导管系统的方法,包括使用如上所述的插入装置刺穿分隔两解剖隔室的至少一个解剖壁。
较优地,解剖隔室由两解剖壁分隔。更优地,两解剖隔室在解剖学上不相邻。
较优地,穿刺方法包括将插入装置插入患者的循环系统直至穿刺头邻接将被刺穿的解剖壁。
较优地,穿刺方法包括使用插入装置推挤两解剖隔室使其互相接触。
较优地,穿刺方法包括使用穿刺头刺穿分隔隔室的壁以及使用导线引导经皮装置穿过穿刺孔。
较优地,穿刺方法包括防止穿刺头对患者造成解剖学上的创伤。
较优地,穿刺方法包括将本系统从股骨动脉和/或下腔静脉插入。
较优地,一个隔室是心脏的左心房和/或主动脉的隔室。更优地,解剖壁是左心房的顶和主动脉壁。
根据本发明的第七方面,提供一种将流动调节装置联结于连接器或将流动调节装置从连接器分离的装置。联结/分离装置包括可拆卸地联结流动调节装置的装置。因此,联结/分离装置可为了联结或分离以及植入或取回流动调节装置而抓取流动调节装置。较优地,联结装置包括一个或多个突出部啮合流动调节装置。
较优地,联结/分离装置包括遥控联结装置的装置,这样可遥控联结/分离装置可选择地抓取或释放流动调节装置。较优地,联结/分离装置可以旋转,这样可遥控联结/分离装置可选择地从连接器拧紧或拧松流动调节装置。
较优地,联结/分离装置包括导管和远端联结装置。较优地,导管包括一个或多个弯头,这样导管可向前穿过患者体内而不扭结。
当被用于治疗心力衰竭、舒张性心力衰竭、收缩性心力衰竭、左心室衰竭、右心室衰竭、儿科心脏异常和/或分流时,本发明的系统和装置尤其有利。
本发明还涉及:用于创建两单独隔室之间穿过解剖壁的人工连通(而不是天然存在的解剖学开口)的经导管方法,包括使用如上所述的经导管插入装置的步骤;用于处理和/或治疗流体的经导管方法,包括使用如上所述的流动调节装置的步骤;用于插入如上所述的体内连接器的方法;用于插入如上所述的体内流动调节装置的方法。本发明涉及的其他方法将在下文中以示例的方式阐述。
在本发明的语境中,术语“经皮”指任何医疗程序中进入内部器官或其他组织是通过穿过皮肤(和/或血管系统)的穿刺和/或切口完成的,例如进入循环系统,而不是开放手术过程。因此,经皮的方法涉及到部件的经皮传送,以及可能涉及允许经皮传送的(例如用手术刀形成的)切口。在一较优的实施例中,该方法为了建立解剖学上隔开但相邻的胸器官之间的流体连通,在通过穿刺或切口进入血管系统之后,提供心血管内一个或多个装置的传送。可在不同的可能进入血管的位点,例如腹股沟、腋下、胸部或腹部内形成穿刺或切口。
附图说明
下文将参考附图进一步阐述本发明,其中:
图1是根据本发明的体内连接器和流动调节装置的示意图;
图2A至2C是根据本发明的体内连接器的示意图;
图3是根据本发明的体内连接器的示意图;
图3A和3B是根据本发明的体内连接器的门的示意图;
图4A和4B是根据本发明的流动调节装置的示意图;
图5A至5C是根据本发明的体内连接器的示意图;
图6A至6C是根据本发明的经皮插入装置的示意图;
图7A至7C是根据本发明的经皮插入装置的示意图;
图7D是根据本发明的经皮插入装置在基本直线构型和盘绕构型时的示意图;
图8A至8J是根据本发明方法的刺穿、插入、定位步骤的示意图;
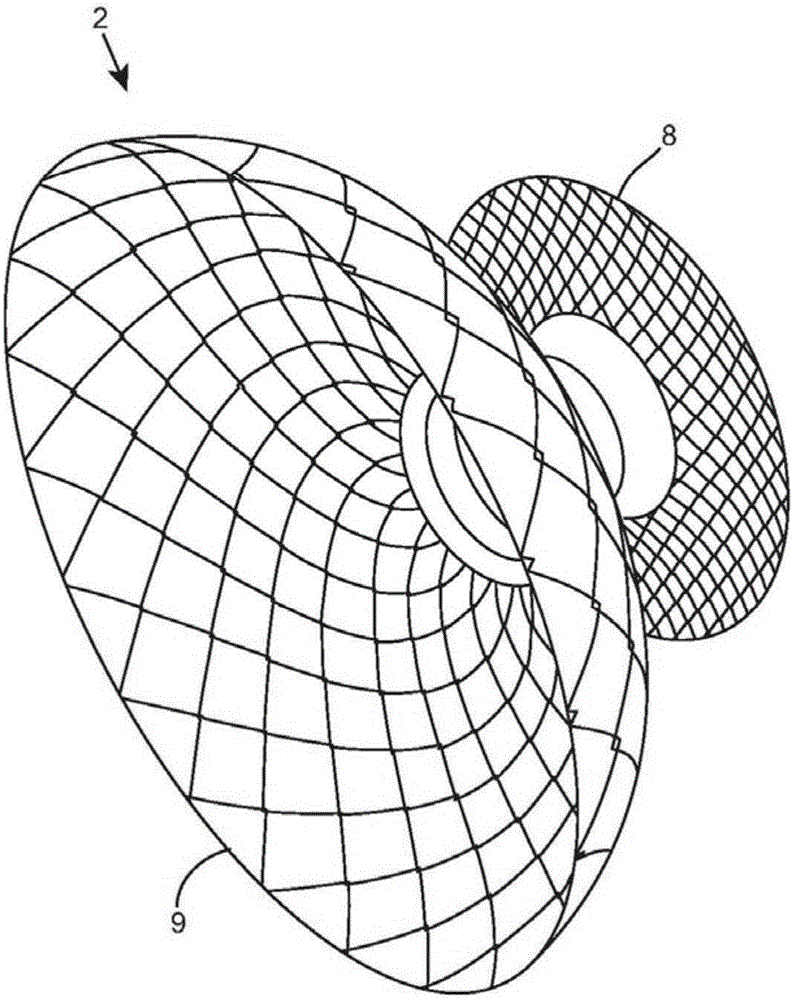
图9示出了根据本发明方法的插入路线;
图10A和10B是根据本发明的体内连接器处于压缩状态时的示意图;
图11是根据本发明的体内连接器在原位的示意图;
图12是根据本发明的流动调节装置处于插入过程时的示意图;
图13是根据本发明的系统在原位的示意图;
图14和15是根据本发明的第一较优的流动调节装置处于插入状态时的示意图;
图16是根据本发明的第二较优的流动调节装置处于插入状态时的示意图;
图17是如图15所示的可压缩流动调节装置的部分示意图;
图18是如图16所示的可压缩流动调节装置在插入过程中的示意图;
图19是如图18所示的可压缩流动调节装置的部分示意图;
图20A是本发明使用的第一密封件处于展开位置和两选择性工作位置的示意图;
图20B是本发明使用的第二密封件的示意图;
图21A至21D是根据本发明的具有包括多个臂的锚部和屏蔽的连接器的俯视图和仰视图;
图21E是根据本发明的连接器的部分示意图;
图22是根据本发明的包括反向螺旋泵的流动调节装置的示意图;
图23是根据本发明的联结/分离装置的示意图。
具体实施方式
参见图1,如图所示的经皮穿刺系统1,在原位,包括穿过至少一个壁5、6并用于流体连通两解剖隔室3、4的体内连接器2。在本图中,第一解剖隔室是心脏的左心房3,第二解剖隔室是主动脉4,第一解剖壁左心房3的顶部5,第二壁是主动脉4的壁6。
连接器2被设计为维持并支撑通常抵抗洪流施加的压力的解剖壁和隔室的结构完整,但是也用于经皮穿刺设备的插入、植入和取回过程中。
下文将结合图1和图2A至2C阐述根据本发明的体内连接器2。该连接器2包括腰部或颈部7,和锚部8和屏蔽9。流体,在这里即血液,可穿过门道10流经颈部7。连接器2是由一种及以上可生物相容性材料制成,根据需要,可在治疗完成后留在病人体内。
典型地,颈部7是由半柔性至基本刚性材料制成,由此来自周围组织的压力不会使颈部7压缩以及不会妨碍流体流动。颈部7包括可生物相容性或外科手术用材料,例如,金属或塑性材料。门道10由弹性材料制成(例如塑性材料或形状记忆性材料)由此可处于允许流体流动的s开放位置或阻止流体流动的关闭位置。颈部7可包括如图1-3所示的固体表面,或可由如图21E所示的网形表面构成。
在致动器不动的情况下,门道10维持在关闭位置。门道10的两个例子如图3A和3B所示。在图3A中,门道10由在关闭位置可配合在一起的几个部分组成,并可被推开以形成开口。在图3B中,门道10包括开口10A,该开口在关闭位置阻止血液流动,但可被拉伸至开放位置以允许血液流动。
在此实施例中,系统1将左心房3连接至主动脉4,左心房3和主动脉4彼此相对较近。但是,当隔室的位置有异或相距较远,可对颈部7的形状和尺寸进行调整。例如,可使颈部7足够有韧性以弯曲至合适的位置或设置其为铰接。
锚部8从颈部7的第一端部延伸。锚部8由弹性材料制成,例如形状记忆性材料,由此可将其以收缩状态(如图10A和10B所示)嵌入,以及以展开状态(如图1和2所示)安装。在其收缩状态,锚部8基本为圆柱形。在其展开状态,锚部8可被布置为防止连接器2在解剖壁5、6内移动或从解剖壁5、6移出。在本实施例中,处于展开状态的锚部8被附接于颈部7的端部并从该端部基本垂直地延伸,由此其抵靠于和/或基本平行于解剖壁,即主动脉壁6。
屏蔽9从颈部7的第二端部延伸。屏蔽9是由弹性材料制成,例如形状记忆性材料,由此可将其以收缩状态(如图10A和10B所示)嵌入,以及以展开状态(如图1和2所示)安装。屏蔽9包括网形或栅格形材料,并可由与锚部8相同或不同的材料制成。在其收缩状态,屏蔽9基本为圆柱形。在其展开状态,屏蔽9可被布置为阻止周围的组织穿过解剖壁5、6被吸入穿刺。屏蔽9扩展开,因此周围的组织不接触屏蔽。这使由穿过网的吸力或摩擦屏蔽所致的损害的风险最小化。在此实施例中,屏蔽9展开基本为碗状或伞状。
在图1-3中,锚部8为盘状,屏蔽为碗状。二者皆由网形材料制成。在另一或可选实施例中,连接器2包括多个臂,所述多个臂从连接器2的一端或两端延伸以形成锚部8和/或屏蔽9。所述多个臂可以是弯曲的和/或包括一个或多个肘部,并且是可/不可展开的。所述多个臂可沿颈部7的内表面延伸以形成拧紧装置用于将流动调节装置11固定至连接器2。此种连接器的示例如图21A至21E所示。
下文将结合图4和5阐述根据本发明的流动调节装置11。
装置11包括远端部11A,中间部11B和近端部11C。在使用中,远端部11A的远端或尖端延伸入一解剖隔室4内,近端部11C的近端或尖端延伸入第二解剖隔室内。中间部11B部分或全部位于连接器2的颈部7内。在本发明的范围内,术语“远端”指在插入方向上最接近病人的位置,术语“近端”指在该方向上最接近医疗人员的位置。换句话说,最先插入装置的远端,最后插入装置的近端。
装置11包括一通道(未示出)作为血液从装置11的近端部11C穿过其远端部11A的通路。近端包括一个或多个开口12以允许血液流入装置11,远端包括一个或多个开口13以允许血液流出装置11。装置11的远端为圆形以使创伤最小化并且突出为尖状以使插入更容易。
流动调节装置11包括将装置11固定至连接器2的装置,并且这种固定装置的示例由图5A至5B示出。在图5A中,装置11的远端部包括一个或多个肋部14或突出部,其用于防止装置11逆着流体的流动而移动。在图5B中,中间部11B的部分或全部由弹性或可膨胀材料制成,该材料使装置11保持在其位置。可通过修饰中间部11B的外表面从而向连接器颈部的内表面提供更好的握持。在图5C中,装置11的远端部11A包括皮瓣15或突出部,其可展开以防止装置11逆着流体的流动而移动或可在插入过程中收缩。
固定装置的另一实例是通过门道10呈现的。在插入过程中,装置11的远端被推过并打开门道10,以及,在插入位置,中间部11B部分或全部位于连接器2的颈部7内,穿过门道10。因此,门道材料在装置11的远端部11A周围弹性地关闭并将装置11固定至连接器2。根据本发明的插入过程,装置11的远端部11A或该远端部11A的远端,通过打开门道10以及允许血液从左心房流至主动脉,充当连接器2的致动器。
可选地或额外地,连接器2和流动调节装置11可包括补充固定装置,例如拧紧装置,其位于连接器2的颈部7的内表面以及流动调节装置11的中间部11B的外表面。拧紧装置的优点尤其在于可将流动调节装置(可拆卸地)固定至连接器,但是还可被用于辅助推进并定位流动调节装置穿过连接器。
在另一较优实施例中,连接器2和流动调节装置11可通过扭锁机构连接,这样的实例如图21E所示。在此实施例中,颈部7可包括两条或多条用于锁定的通道或纵向突部。
连接器2还可包括密封装置用于防止不需要的流体在连接器和流动调节装置的联结界面流动或固定装置。例如,连接器和流动调节装置包括补充拧紧装置,密封装置包括镜像反映拧紧装置的螺丝轮廓的一条密封材料。由此,在使用时,密封装置被夹在连接器的拧紧装置和流动调节装置的拧紧装置之间。
所用的可展开的密封装置在其展开状态,基本呈密封材料的矩形条带状。在其收缩状态,密封装置基本为螺旋状。密封装置可由柔性材料和/或形状记忆性材料制成。密封装置可包括将密封装置固定至连接器的固定装置和/或流动调节装置。
流动调节装置11包括通道34,通过该通道34接收导线19b。在一较优的是实施例中,通道34从流动调节装置11的近端延伸到远端。较优地,通道34沿着流动调节装置11的中心纵轴延伸。
流动调节装置11包括内泵16。泵送参数由体内或体外控制器(未示出)调节。若使用体外控制器,首选无线控制器。可通过电导线17将电流提供给泵16,或者装置11可包括内部电池。如果使用可充电电池,优选无需插入病人体内的设备的充电机构,例如,磁充电机构。如果使用非充电电池,则在使用之后可拆走并替换或丢弃装置11。电导线17或其他导管可被用作在使用后将装置11从病人身上移除的拉绳或者可附加一条专用拉绳。
如果从隔室3泵送的流体在被输送到隔室4前需要治疗或处理,合适的装置(未示出)可被并入装置11。例如,一给药设备可通过装置11使血液接触一种或多种药物;或者可利用一供氧设备或膜在血液流出装置11前对血液充氧。在给药情况下,装置11与药物容器整合一体或装置11被连接至一外部药物容器。也可设计一缓慢释放或可控释放机构。根据本发明的系统1还可被看作是随或不随血液流动的体内给药系统,其中药物被输送至目标隔室内。
流动调节装置11是独立自给的,因此所有的元件,包括泵16、给药或给氧设备,根据需要可并入流动调节装置11的壳体内。
下文结合图16-19阐述本发明中使用的较优的流动调节装置11。该装置11是上述设备的变形,可包括关于上文中所述装置11的任何特征。
流动调节装置11包括远端部11A、中间部11B和近端部11C。近端部11C形成部分或全部包围泵16的一壳体。近端部11C还包括一可拆卸基座11D。基座11D可通过旋转附接,例如通过旋拧或卡口装置。此可拆卸基座11D包括一个或多个开口27,这样流体可从第一解剖隔室流入基座开口27,穿过装置11流出位于装置11的远端部11A的开口13流入第二解剖隔室。
基座11D包括支撑至少一个叶片16B的可旋转轴16A。该叶片16B是从轴16A延伸出的螺旋型叶片。叶片的近端可从轴16A延伸。叶片16B的远端可被/不被附接于装置11的近端部11C的远端或装置11的中间部11B的近端。设置且构造螺旋型叶片16B以使得其可在轴16A的纵向延伸或伸展从而使其容易插入工作鞘21。处于延伸构型时,旋转叶片16B纵向伸展由此叶片16B的整体直径比其处于松弛构型的直径小。当叶片16B从鞘21穿出时,叶片16B回到其初始松弛构型,即:其工作构型。在此工作构型,叶片16B的整体直径比其在伸展构型的直径大。因此,当螺旋型叶片16B处于伸展构型时,叶片16B可以容易地穿过鞘21,而在工作构型时,叶片16B的尺寸尽量增大以获得最佳能效。这还意味着可以使使用具有较大螺旋圈数形成单位长度(由此更高效)的叶片16B。装置11的任一部分,尤其是,装置11的近端部11C和/或叶片16B,可以由弹性(或形状记忆性)材料制成,材料可以是相同的或不同的。在较优的实施例中,可延伸的泵由装置11的近端部11C包围,而近端部11C由弹性材料制成由此可被压缩以适于放入鞘内以及随后使用时展开。此在实施例中,基座11D较优地由刚性材料制成。
在如图22所示的另一实施例中,流动调节装置11包括反向罗纹泵机构,该机构的螺纹和/或叶片33被设置在流动调节装置11的可旋转内表面,这样流体从第一隔室被吸入第二隔室。在此实施例中,血液在流动调节装置内的中心流动。此设置的优点还在于可容易地沿着流动调节装置11的中心纵轴放置导线。
基座11D可包括隔室(未示出),该隔室具有泵电机、泵运行所需要的其它部件、如上所述的流体治疗和/或处理装置。或者,基座11D或近端部11C可包括一个或多个用于给药和/或氧的凸脊。例如,凸脊可被置于轴16A的周围。装置11和病人身体外部之间的连接件17可被附接于基座11D。
使用可展开的经皮穿刺部件(例如可膨胀的连接器和流动调节装置)的宗旨是在于满足微型化的需求。换句话说,可以将完整尺寸的部件以折叠或压缩状态穿过小切口插入病人的血管系统,使其在正确的部位展开并随后以折叠或压缩状态从病人身体移除,而无需将部件的尺寸缩减(从而导致能效降低)。这提供了在尺寸和形状方面更加通用的系统,尤其是儿童将会从中获得很大利益。这还意味着,不只可以使用皮下传动系,还可以使用外部传动系和可展开部件穿过静脉系统。因此,如果可以避开主动脉,感染和大出血的风险会大大降低。
下文将结合图6-8阐述根据本发明的经皮插入装置18。
经皮插入装置18包括与导线19b和扩张器19c构成整体的穿刺头19a。插入装置还包括工作鞘21和一外鞘23。使用插入装置18插入根据本发明的方法所需的任何设备或部件。如下文更详细地描述,针19,尤其是穿刺头19a用于穿刺一个或多个解剖壁;导线19用于在插入过程中指导部件;扩张器19c用于伸展穿刺头19a形成的穿刺孔;工作鞘21用于插入、运输并定位系统1的设备;以及外鞘23用于形成插入系统1的设备的安全通道。
在此实施例中,穿刺头19a,例如通过焊接,被连接至导线19b的远端。穿刺头19a具有一固体尖,即,没有标准插入针或注射针的中空通道。穿刺头19a成圆锥形并形成一极锐利的尖端。圆锥形穿刺头19a的底部的直径比导线19b的直径大。导线19b可滑动地穿过扩张器19c。圆锥形穿刺头19a的底部的直径基本等于扩张器19c的远端的直径以形成一平齐、平滑的过渡。
在另一实施例中(未示出),圆锥穿刺头19a的底部的直径基本等于导线19b的直径,这样导线19b是具有一锋利的锥形尖头的锥形导线。在此实施例中,穿刺头19a和导线19b形成一个整体。导线19b的直径基本等于扩张器的远端的直径以形成一平齐、平滑的过渡;尽管如此,当锥形导线19b作为针时可以不需要扩张器19c。
在导线19b的远端使用锐利的穿刺头19a使得插入装置18成为无损伤且精准的穿刺装置。穿刺头19a、导线19b和扩张器19c的相对尺寸使穿刺孔逐渐温和地增大。
较优地,导线19b包括具有不同刚性的两段或三段,例如,材料刚性较强的远端部,材料柔性的中间部,和材料刚性较强的近端部。刚性上的差异使操作和引导穿过病人体内的导线成为可能。
参见图7D,导线19a包括至少具有不同刚性的两段,即:材料刚性较强的近端部用于引导并推送穿刺头19a穿过患者体内,和材料较柔性的远端部。柔性部尤其有利于防止病人体内受到伤害,例如,当推进导线19b或插入并定位体内装置时。例如,柔性部可围绕穿刺头19a卷成圈以保护周围的组织并防止穿刺头19a意外移动。
如下文更详细地描述,插入部件18使得为插入、安装、移除系统1的各种部件创立一条安全的路径成为可能。更具体地,根据本发明的插入装置18的尤其有利于解剖壁的穿刺,例如具有较大组织抵抗力的解剖隔室的外壁的穿刺。插入装置18使得形成非常精确且小的创口成为可能,这对于涉及高压血流的创口是非常重要的。插入部件18的一个较优的用途是用于体内器官的外壁的穿刺,例如外心脏穿刺。
下文将结合左心房-主动脉连接的例子阐述根据本发明的方法。
第一步是插入导线,可通过本领域中的已知技术实现。将带着导线的针置于患者的腹股沟部位,邻近股骨动脉。施加压力使针尖刺穿患者的皮肤被并穿过皮肤和组织进入股骨动脉。一旦就位,导线沿着股骨动脉前行并上行至下腔静脉25。参见图9,导线在下腔静脉25并进入右心房26。左右心房之间的隔膜穿刺可通过现有技术进行。现在,导线从患者体外延伸,通过皮肤穿刺进入股骨动脉、下腔静脉25、右心房26、心房隔膜和左心房3,较优地暂定于左上肺静脉。然后,可将一可操纵的大支撑鞘沿着导线放入左心房以便于整个过程中的最后步骤。使用本发明的插入装置18可同等地实施的皮肤穿刺和/或隔膜穿刺,尽管当实施如下所述的心外穿刺时插入装置18是最有利的。
第二步是插入并安装本发明所述的插入装置18。较优地,通过专用的鞘21和23使针19穿过腹股沟并沿着上文所述路线前进。导线19b包括较柔性的远端部,该部分邻近穿刺头且在较刚性的近端部之前,这样导线19b的柔性部自行折叠由此形成U形。该柔性部先前行,随后是刚性近端部。由此,导线19b可防止损伤地穿过传递鞘或穿过患者的血管。需要时,通过轻拉近端并将远端部重定位于其最前端可使导线19b被拉直。穿刺头19a被拉向扩张器19c的远端。
第三步是使用本发明的插入装置18进行左心房的心外穿刺。外鞘23的远端抵靠在左心房3的顶端并被推靠在所述壁从而使左心房3的顶端接触主动脉壁。穿刺头前行从而在左心房3的顶部形成穿刺。此尖锐的圆锥形使医疗人员能够以平滑无损伤的方式形成微小且精确的心外切口。穿刺头19a和扩张器19c穿过穿刺向主动脉壁前行。外鞘23用于推着左心房的壁抵靠主动脉壁并控制两壁一起辅助主动脉壁的穿刺。一旦主动脉壁被刺穿,扩张器20可撑开两穿刺孔以便于工作鞘21插入。可将扩张器19c移除而留下并定位导线19b和工作鞘21在主动脉4内。外鞘23可保留在左心房3内。
穿刺头19a进一步前行进入主动脉4内。随着扩张器19c退出,导线19b的柔性部将围着穿刺头19a盘绕,由此锚定并屏蔽穿刺头19a使其和周围组织分隔开。额外地或可选地,通过现有技术可将一接收导管置于主动脉4的内部用于接收并保护主动脉内的穿刺头19a。
因此,可以理解支撑鞘23可被用于安全地传输体内设备但也辅助解剖壁的穿刺,尤其是涉及一个以上解剖壁的穿刺的方法。
第四步是插入根据本发明的体内连接器2。参见图10A和10B,处于折叠或压缩状态的体内连接器2沿着导线19b被插入的工作鞘21。当连接器2到达左心房的顶部,其被沿着导线19b推着穿过解剖壁5、6上的切口直至颈部7被正确地置于解剖壁5、6之间并且锚部8和屏蔽9分别在壁5、6两边的主动脉4和左心房3内展开(图11)。随着连接器2从工作鞘21的远端离开,连接器2逐渐展开。
如本发明的图4或图15所示,第五步是体内流动调节装置11的插入。参见图12,将体内流动调节装置11插入并使其沿着导线19b向前穿过鞘21直至其到达连接器2。远端部11A,尤其是连接器2的远尖端作为致动器通过拉伸门道10的开口10A从而打开连接器2的颈部7的门道10。流动调节装置11的中间部11B位于连接器2的颈部7并被安全地定位。流动调节装置11可通过门道10的弹性材料的压力和肋部14而被固定。额外地或可选地,流可通过将流动调节装置11的中间部11B拧紧至连接器2的颈部7而固定流动调节装置11。此拧紧机构还使流动调节装置11被安全地引导至连接器2的内部。在提供密封装置的情况下,密封装置防止穿过流动调节装置11和连接器2之间的联结界面的任何渗漏。除非有进一步需求,工作鞘21现在可被移除。
因此,可以理解根据本发明的插入装置18提供双重用途。第一,穿刺头19可被用于以安全、可控且防止损伤的方式刺穿解剖壁。第二,插入装置18可被用作整合的导线19b。因此,不需要在两个单独的步骤中分别使用针和单独的导线。这减小了意外的风险并简化了插入程序。
如图16至19所示的可压缩/可膨胀的流动调节装置,装置11的基座11D从近端部11C分离,叶片16B被拉伸至其展开位置。例如,基座11D是旋转的或未拧紧的,因此同时地,基座11D从近端部11C分离并且叶片16B延伸。装置11进入鞘21的远端,并且装置11的远端部11A适当定位准备启动门道10。基座11D被重新附连在装置11的近端部11C,例如通过旋转扭紧装置,由此,叶片16B松弛进入工作构型。流动调节装置11的远端部11A现在可被推着穿过门道10以允许流体流动。
可通过可视化技术,例如X射线、荧光透视、超声心动描记术、超声波技术促进上述插入和安装方法。
发动泵16,可调节左心房3和主动脉4之间的血液流动。血液从左心房3流入装置11的近端,穿过装置并从装置11的远端上的孔13流入主动脉4。
可控制并调节血液流动、血液流动的时机、温度和其它参数。类似地,随着血液流经装置11,可加入药物和/或氧和/或从血液移除污染物。随着血液被吸入装置11,通过屏蔽9阻止周围组织妨碍血液通道。血流具有将装置11推回左心房的倾向,但如上所述的固定装置使的装置11固定不动。
当治疗完成,如果需要充电维修或替换,可从患者身体移除流动调节装置11。鞘21、23插入并穿过患者,并且使用专用的联结/分离装置35,其包括联结流动调节装置11的装置。联结/分离装置附连于流动调节装置11,例如通过一个或多个啮合突出部36a啮合流动调节装置11内相应的凹部36b。附连装置是可远程操控的。联结/分离装置包括用于将流动调节装置11从连接器2旋开的旋转装置,并且可通过鞘21、23安全地取回流动调节装置11。联结/分离装置还可被用于插入过程使流动调节装置11向前穿过鞘21、23并将流动调节装置11旋拧至连接器2。
移除装置11后,门11关闭并且血液流动暂停,连接器2被留在原位或被移除。
尽管如上文所述的本发明是关于左心房到主动脉的过程,所述系统和方法还可用于其它传送点,其包括但不限于右心房–主动脉、腔静脉–肺动脉、腔静脉–主动脉。因此,本发明可宽泛地用作例如左心辅助仪器(LVAD)、右心辅助仪器(RVAD)或者双心辅助仪器(BiVAD),用于心肺支持(CPS)、或用于体内膜式氧合(ICMO)或泡式氧合、或用于治疗有压力问题的其它器官(例如胃的或神经性治疗)。本发明是通用型的,并且因此使用范围广泛。
通过以上阐述,可以理解,本发明构成了一种新的替代现有经皮穿刺程序的方法。本发明的经皮穿刺程序需要有限的机械装置和设备,提供了一个简单的、更安全、更低廉的替代现有程序的方法。所有部件均是经皮插入和植入的,所以步需要进行创伤性开放手术。此外,在此描述的设备可以很容易地用于儿科治疗。
重要的是注意到本发明依赖于人工创建的流体通道。心肺或循环系统崩溃和心衰可以由各种获得性或先天条件所导致,并且可以影响心脏和循环系统以及呼吸系统的不同解剖部位。现有治疗程序往往寻求修复或替换存在缺陷的解剖部位。本发明提供一种包容性更强的治疗程序,因其依赖于人工创建的绕过循环系统缺陷部分的通道,并允许使用与目前的治疗方法相比新的治疗理念和技术。
但是,设计本发明使其用于以下情况:通过自然通路的流体流动不足、有缺陷或不受控制,以及有必要恢复通路或流体流动。例如,所述情况是重度肺动脉瓣狭窄、严重主动脉瓣狭窄、闭锁、或重度二尖瓣狭窄。
通过使用包括上述导线和整体式穿刺头的插入装置,本发明允许安全且无损伤的在结构上敏感的解剖壁上的穿刺。本发明使用如上文所述的连接器,允许流动调节装置的安全植入、定位和工作,其提供了结构上敏感的解剖壁上的完整性。本发明允许对可能具有解剖学的缺陷而无法接受常规治疗的患者进行治疗。本发明适用于更小的患者,例如儿童,或者无法使用或引入大仪器的情况。本发明提供最低限度创伤的治疗,其不影响患者的术后移动性。
本系统具有安全、稳定、可预测的结构,可将改进的治疗仪器穿过更短和更有益的路线从一个隔室传递到另一个隔室。
本发明的更进一步的方面可见于以下段落。
1.经皮系统包括用于穿过至少一个解剖壁流体连通两解剖隔室的体内连接器。
2.根据段1的系统,其中所述连接器包括提供从一个隔室到另一个隔室的流体通路的颈部和固定横闯解剖壁的颈部的装置。
3.根据段2的系统,其中所述固定装置包括从所述颈部的第一端延伸的可膨胀的锚部。
4.根据段3的系统,其中所述锚部在其膨胀状态与所述解剖壁基本平行放置。
5.根据段2-4中任意一段所述的系统,其中所述连接器包括防止组织妨碍穿过颈部的流体通路的防止装置。
6.根据段5的系统,其中所述防止装置包括从所述颈部的第二端延伸的可膨胀的屏蔽。
7.根据段6的系统,其中所述屏蔽在其膨胀状态基本不接触所述解剖壁。
8.根据前述任意一段的系统,其中所述连接器完全地或部分地由形状记忆性材料制成。
9.根据段2-8中任意一段所述的系统,其中所述颈部包括选择性地阻止或允许穿过所述颈部的流体通道的门。
10.根据前述任意一段的系统,还包括用于调节所述两解剖隔室间的流体流动的体内的流动调节装置。
11.根据段10的系统,其中流动调节装置包括用于允许或阻止流体流过体内的连接器的致动器。
12.根据段11或12的系统,其中所述流动调节装置包括泵。
13.根据前述任意一段的系统,还包括处理流体的流体处理装置。
14.根据段13的系统,其中所述流体处理装置包括使所述流体接触一个或多个药物化合物的装置。
15.根据段13或14的系统,其中所述流体处理装置包括使所述流体接触一个或多个气体,例如氧气的装置。
16.根据段10-15中任意一段所述的系统,还包括将所述流动调节装置固定至所述连接器的装置。
17.根据段10-16中任意一段所述的系统,其中所述流动调节装置包括支撑至少一个叶片的可选转轴,所述叶片适于在所述轴的长度方向上延展进入插入构型。
18.根据段17的系统,其中所述叶片适于在所述轴的长度方向上松弛进入工作构型。
19.根据段18的系统,其中所述叶片在所述轴的横向方向上的尺寸在所述工作构型时大于其在插入构型时。
20.根据段17-19中任意一段所述的系统,其中所述叶片是螺旋型叶片。
21.根据段17-20中任意一段所述的系统,其中所述叶片由长度上的弹性材料制成。
22.根据前述任意一段的系统,其中一个或两个解剖隔室是循环系统的隔室。
23.根据前述任意一段的系统,其中所述流体是血液。
24.根据前述任意一段的系统,其中所述系统是心室辅助装置。
25.根据前述任意一段的系统,还包括具有针的经皮插入装置,所述针包括针体、导线和穿刺头。
26.根据段25的系统,其中所述穿刺头包括固体尖。
27.根据段25或26的系统,其中所述穿刺头最宽的横截面的尺寸基本等于所述导线的远端的横截面的尺寸。
28.根据段25-27中任意一段所述的系统,其中所述插入装置还包括扩张器。
29.根据段28所述的系统,其中所述穿刺头最宽的横截面的尺寸基本等于所述扩张器的远端的横截面的尺寸。
30.根据段25-29中任意一段所述的系统,其中所述插入装置还包括引导一鞘的装置。
31.前述任意一段所述的体内连接器。
32.如段10-21中任意一段所述的体内流动调节装置。
33.如段25-30中任意一段所述的经皮插入装置。
34.一种用于提供两解剖隔室之间的流体连通的经皮方法,所述方法包括以下步骤:刺穿分离所述隔室的壁,以及穿过两隔室之间的穿刺孔插入体内连接器。
35.根据段34的方法,其中所述穿刺步骤是通过使用如段25-30中任意一段所述的插入装置实施的。
36.根据段34或35的方法,其中所述体内连接器是如段1-30中任意一段所述的连接器。
37.根据段34-36中任意一段所述的方法,还包括调节所述两解剖隔室之间的流体流动的步骤。
38.根据段37所述的方法,使用如段10-30中任意一段所述的体内流动调节装置调节所述流体流动。
39.根据段34-38中任意一段所述的方法,还包括处理所述流体的步骤。
40.根据段38的方法,其中所述处理流体是通过使用如段13-15中任意一段所述的处理装置实施的。
41.根据段34-40中任意一段所述的方法,其中一个或两个隔室是循环系统的隔室。
- 还没有人留言评论。精彩留言会获得点赞!