本发明涉及用于治疗骨骼破裂和/或骨骼缺损的方法,尤其涉及促进破裂愈合的方法,并且涉及用于此类方法的组合物、可注射的原位储库(depot)形成制剂和贴剂。本发明还涉及用于此类方法的骨骼填充物、医疗装置和骨骼植入物。本发明尤其涉及破裂和缺损的短期局部治疗。
发明背景
骨骼破裂是骨骼的完全或不完全断裂。骨骼破裂可以是强力冲击或应力的结果,或者是由于某些使骨骼变弱的医学病况导致的轻微损伤。骨骼破裂被称为创伤性破裂,即由创伤导致的破裂,例如由跌倒或事故(例如交通事故)导致的破裂。由使骨骼变弱的潜在疾病(例如骨质疏松症、佩吉特氏病(Paget's disease)或骨癌)导致的骨骼破裂被称为病理性破裂。当覆盖在其上的皮肤未被破坏并且骨骼不暴露于空气时,将破裂称为简单的(或闭合的)。若皮肤被破坏并且骨骼暴露,则将破裂称为复合(或开放)破裂。
破裂愈合分成三个部分重叠的阶段,即发炎阶段、修复阶段和重塑阶段。在发炎阶段期间,在破裂之后的前几个小时和几天内,在破裂部位内产生血肿。包括巨噬细胞、单核细胞、淋巴细胞和多形核细胞的炎性细胞以及纤维母细胞浸润骨骼,其导致肉芽组织形成、脉管组织生长和间叶细胞迁移。在修复阶段期间,血肿从破裂部位去除并且被肉芽组织取代,其导致在修复部位形成软骨痂。骨母细胞和软骨细胞的分化在此阶段期间发生。软骨痂重塑为硬骨痂,并且新骨骼由成骨细胞形成。破裂愈合在重塑阶段期间完成,其中骨骼经由组织化的骨母细胞/破骨细胞活性恢复成其原始形状、结构和机械强度。重塑缓慢地发生并且需要数月至数年才完成。
骨骼缺损是骨骼中的间隙或空隙,其可以是多种原因的结果,例如创伤(例如事故和/或破裂)或由手术移除骨骼片段(例如移除恶性骨瘤)。当前骨骼缺损的治疗主要需要使用骨骼填充物,例如骨水泥和去矿物质骨基质。骨水泥进一步用于使植入物黏着至现存骨骼。使用骨骼填充物的主要缺点为缺乏新骨骼的重塑或替代或者新骨骼的限制性重塑或替代以及随后不能黏着至现存骨骼。骨水泥以及骨骼植入物的另一重要缺点为无菌性松脱。无菌性松脱是围绕假体填充物和/或植入物产生空隙,尤其在骨骼与植入物/填充物彼此邻近的部位。无菌性松脱可以是不充分的初始固定、随时间推移的固定损失或由围绕植入物的粒子诱发骨质溶解导致的固定损失的结果。无菌性松脱也可以由骨水泥/植入物界面的空隙引起。此类空隙在植入物引入之后始终存在,并且通常主要由仅含有若干细胞和血管的纤维组织填充。例如在移动期间的重复的机械应力可以在界面诱发创伤并且最终使骨骼-植入物界面松脱。无菌性松脱甚至可以使过早替换植入物成为必需。
目前,仅存在有限的有效治疗是可用的,其辅助骨骼破裂愈合,尤其是在破裂已发生之后的早期阶段中促进创伤和/或复杂破裂愈合。
双膦酸盐对破骨细胞骨骼再吸收具有抑制作用。它们已用于具有增加的骨骼再吸收的疾病,例如骨质疏松症、佩吉特氏病和骨癌。认为双膦酸盐的活性通过抑制破骨细胞介导的骨骼再吸收来预防骨质流失和改善骨骼强度。然而,仅发现双膦酸盐降低破裂的风险,但不具有愈合破裂骨骼或产生骨组织的功能。实际上,通常认为在骨骼破裂之后的骨骼愈合期间用双膦酸盐进行治疗是有害的,因为破骨细胞在破裂愈合期间对于重塑阶段中使骨痂重塑为骨骼是必需的。
在许多动物研究中,已显示双膦酸盐对骨痂尺寸和骨骼矿物质含量具有积极作用。然而,这从未导致增加骨骼强度或促进愈合,从而确认破骨细胞在骨痂重塑中必不可少的作用。Einhorn,TA(2010)提供了在动物模型中药理学治疗骨骼破裂的概述。据报道,双膦酸盐导致骨痂尺寸增加,但也在长期治疗破裂之后导致骨痂重塑和/或骨骼形成减少。描述了短期研究,其报道了在用双膦酸盐进行全身性治疗之后骨痂尺寸增加和骨骼矿物质含量增加。局部施用双膦酸盐也增加骨痂尺寸和骨骼矿物质含量,但这并未转变为骨痂强度增加。作者得出结论,局部施用双膦酸盐可对破裂愈合过程具有抑制作用,并且长期的双膦酸盐治疗可以是有价值的治疗。
双膦酸盐也已用于植入骨骼中的螺钉的涂层,参见例如Wermelin K等人(2008)和Aspenberg P等人(2008)。Wermelin K等人(2008)报道,钛植入物在骨骼中的固定通过双膦酸盐涂层来改善。Aspenberg P等人(2008)使用双膦酸盐与甲状旁腺激素(PTH)的组合,所述甲状旁腺激素是增加血清钙水平的84氨基酸多肽。连续的PTH暴露刺激破骨细胞活性,而间歇暴露刺激骨母细胞,并且在骨质疏松症中的总体作用为PTH对骨骼形成具有积极作用。Aspenberg P等人(2008)报道,作为不锈钢螺钉上的涂层的PTH和双膦酸盐对螺钉在骨骼中的固定具有累加作用。
Xue等人(2014)的随机对照试验的近期综合分析确认了在动物研究中获得的结果。Xue等人报道,其综合分析显示出双膦酸盐对短期和长期骨骼愈合不具有作用。
睪酮是影响骨母细胞活性和增加骨生成的同化剂。对于在具有低睪酮水平(其中所述睾酮导致骨密度的较少增加)的男性中使用睪酮来预防骨质疏松症或在骨质疏松症已经诊断之后预防进一步的骨质流失,已经进行了临床试验。然而,由于对肝脏和心血管系统的不良作用,睪酮尚未用于此类应用。Cheng等人(2013)描述了睪酮对小鼠中的创伤性骨骼破裂的作用。在骨架中局部施用睪酮诱发骨痂形成并且增加骨痂中的破骨细胞数。未报道对骨痂重塑和所得骨骼强度的作用。
WO 98/23274描述了用双膦酸盐与雄激素进行的组合治疗。然而,此文件未提出对骨骼破裂或骨骼缺损的治疗。相反地,其涉及包括骨骼再吸收的疾病的治疗,所述疾病例如骨质疏松症和佩吉特氏病,其病理过程在很大程度上不同于在例如破裂或缺损之后的骨骼损伤和修复。所述文件还未涉及骨骼的局部治疗。
在骨骼愈合过程期间,患者的活动严重受到妨碍并且可能经历对生活质量的实质性影响。患者例如经历进行普通日常活动的困难和工作能力的限制,从而导致受限制的生产力、独立性损失、自尊降低和可能的慢性疼痛。如上所述,全部愈合过程需要数月至数年来完成。因此需要辅助骨骼破裂愈合的医学治疗。此类医学治疗优选促进破裂后的骨骼愈合,以使破裂愈合的总时间减少。还需要骨骼缺损的改善治疗,其解决与使用以上所述的骨骼填充物和骨骼植入物相关的缺点。另外,需要对骨骼破裂或缺损的医学治疗,其避免双膦酸盐的不良作用,包括在除以上所述的破裂部位以外的位置抑制骨更新,以及例如在口服施用后的低钙血症和上部GI不良作用,以及同化药物的不良作用,例如对肝脏或其他器官、生殖系统、心血管系统及血清脂质分布和行为的不良作用,但同时提供对破裂部位的持续治疗。
发明概述
本发明的目的为提供辅助破裂愈合过程的治疗骨骼破裂的方法,所述骨骼破裂包括病理性、创伤性和复杂性破裂。本发明的另一目的为提供治疗骨骼缺损的方法,其刺激骨骼形成并且抑制骨骼再吸收,以便改善例如骨骼植入物和骨骼填充物对现存骨骼的连接。
因此,本发明提供治疗患者(优选人类患者)的骨骼破裂或缺损的方法,其包括向破裂部位或缺损部位施用贴剂或可注射的原位储库形成制剂,所述贴剂或制剂包含至少一种可生物降解的聚合物和雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合,和/或包括向骨骼破裂部位或骨骼缺损部位或向该部位内引入包含至少一种可生物降解的聚合物和雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合的骨骼填充物,或者具有涂层的骨骼填充物、医疗装置或骨骼植入物,所述涂层包含至少一种可生物降解的聚合物和雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合。
在另一方面,本发明提供用于治疗骨骼破裂或骨骼缺损的方法的组合物,所述组合物包含雄激素受体激动剂和双膦酸盐或其药学上可接受的盐。所述方法优选包括向破裂部位或缺损部位施用可注射的原位形成的储库制剂或贴剂,所述制剂或贴剂包含至少一种可生物降解的聚合物和雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合,和/或向骨骼破裂部位或骨骼缺损部位或向该部位内引入包含至少一种可生物降解的聚合物和雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合的骨骼填充物,或者具有涂层的骨骼填充物、医疗装置或骨骼植入物,所述涂层包含至少一种可生物降解的聚合物和雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合。
在另一方面,本发明提供雄激素受体激动剂和双膦酸盐或其药学上可接受的盐的用途,其用于制备治疗骨骼破裂或骨骼缺损的药物。所述治疗优选包括向破裂部位或缺损部位施用可注射的原位形成的储库制剂或贴剂,所述制剂或贴剂包含至少一种可生物降解的聚合物和雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合,和/或向骨骼破裂部位或骨骼缺损部位或向该部位内引入包含至少一种可生物降解的聚合物和雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合的骨骼填充物,或者具有涂层的骨骼填充物、医疗装置或骨骼植入物,所述涂层包含至少一种可生物降解的聚合物和雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合。
在另一方面,本发明提供组合物,其包含至少一种可生物降解的聚合物、雄激素受体激动剂和双膦酸盐或其药学上可接受的盐。
在另一方面,本发明提供可注射的原位形成的储库制剂、贴剂、涂层和骨骼填充物,其包含含有至少一种可生物降解的聚合物、雄激素受体激动剂和双膦酸盐或其药学上可接受的盐的组合物。
发明详述
本发明涉及骨骼修复,尤其涉及骨骼破裂或骨骼缺损的治疗,更尤其涉及骨骼破裂或骨骼缺损的局部治疗。因此,组合物、贴剂和制剂优选用于局部施用于骨骼和/或骨骼的局部治疗。如本文所用的术语“骨骼破裂”包括完全与不完全破裂以及创伤性破裂和病理性破裂。“完全破裂”是指在骨骼的整个直径上的断裂,而“不完全断裂”是指不跨越骨骼的整个直径的部分破裂。如本文所用的“创伤性破裂”是指由创伤导致的破裂,例如由跌倒或事故(例如交通事故)导致的破裂。如本文所用的“病理性破裂”是指由使骨骼变弱的潜在疾病(例如骨质疏松症或骨癌)导致的骨骼破裂。术语“骨骼缺损”是指骨骼中的间隙或空隙。可以成为此类空隙或间隙产生的基础的因素的实例包括但不限于创伤,例如由跌倒或事故导致的创伤;(椎骨)挤压破裂;骨囊肿;癌症诱发的缺损,例如骨肿瘤,包括原发性骨肿瘤和例如其他类型的转移两者或癌症(例如乳腺癌、前列腺癌、肺癌或肾癌)或者多发性骨髓瘤;以及此类肿瘤的外科移除。此类骨骼缺损通常通过向缺损部位中引入骨骼空隙填充物或骨骼植入物来治疗。
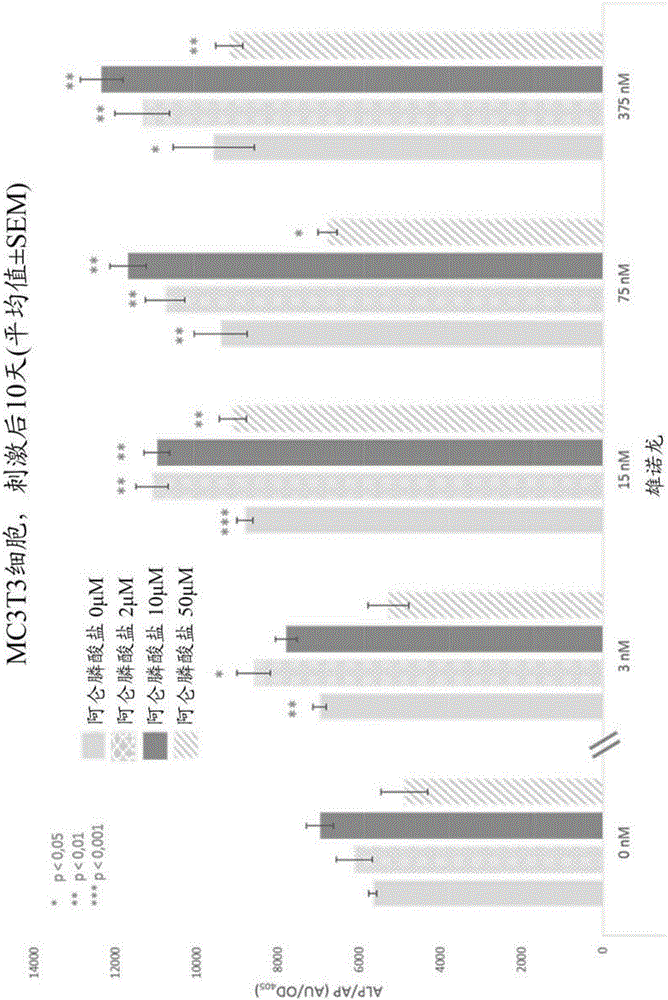
不希望受理论束缚,认为在骨骼破裂部位或缺损部位局部施用时,用雄激素受体激动剂(优选为睪酮或其衍生物)与双膦酸盐或其药学上可接受的盐进行的组合治疗的活性至少部分为两种活性化合物的协同作用的结果,尤其是雄激素受体激动剂的同化作用与双膦酸盐的抗分解代谢作用的协同作用的结果。如图1所示,与仅有双膦酸盐相比,双膦酸盐与雄激素受体激动剂的组合导致成骨细胞活性的大幅和显著的增加。双膦酸盐通过抑制细胞内甲羟戊酸途径(其导致受损的膜定位,进而导致受损的破骨细胞信号传导分子鸟苷三磷酸酶)或通过被代谢为ATP的非水解性类似物来抑制破骨细胞介导的骨骼再吸收,两者均导致破骨细胞凋亡。雄激素受体激动剂通过经由与雄激素受体结合以增强骨母细胞增殖和分化来影响骨骼产生。认为雄激素受体激动剂(优选为睪酮)与双膦酸盐的组合局部作用尤其在破裂之后的早期阶段(至多4个月)预防骨质流失和改善骨骼强度中起协同作用。
本发明的组合物、制剂和贴剂包含两种活性化合物,即雄激素受体激动剂与双膦酸盐或其药学上可接受的盐的组合。如本文所用的“雄激素受体激动剂”是指与雄激素受体(AR)结合并且激活该雄激素受体的任何天然或合成化合物。优选的雄激素受体激动剂为同化类固醇,更优选为睪酮或其衍生物。术语“同化类固醇”在本领域中是熟知的并且是指与睪酮有关的一类类固醇激素。同化类固醇在Kicman AT,British Journal of Pharmacology(2008)154,502-521中进行了综述。如本文所用的“睪酮或其衍生物”是指睪酮、睪酮酯、睪酮前体、睪酮代谢物和睪酮类似物。适用于本发明的组合物和方法的衍生物的实例为睪酮酯,环戊丙酸睪酮、癸酸睪酮、庚酸睪酮、异己酸睪酮、苯丙酸睪酮、丙酸睪酮和十一酸睪酮;睪酮前体,雄烯二酮、4-雄烯二酮、5-雄烯二酮、雄烯二醇、5-雄烯二醇、4-雄烯二醇和脱氢表雄酮;睪酮代谢物,二氢睪酮和本胆烷醇酮;睪酮类似物,甲基睪酮、雄酮、表雄酮、诺龙(nandrolone)、17α-乙基睪酮和氟羟甲睪酮。因此,睪酮或衍生物优选地选自:睪酮、环戊丙酸睪酮、癸酸睪酮、庚酸睪酮、异己酸睪酮、苯丙酸睪酮、丙酸睪酮、十一酸睪酮、雄烯二酮、4-雄烯二酮、5-雄烯二酮、雄烯二醇、5-雄烯二醇、4-雄烯二醇、脱氢表雄酮、诺龙、二氢睪酮、本胆烷醇酮、甲基睪酮、雄酮、表雄酮、17α-乙基睪酮和氟羟甲睪酮。更优选地,睪酮或衍生物选自睪酮、诺龙和二氢睪酮。最优选地,雄激素受体激动剂为睪酮。
根据本发明局部施用于骨骼破裂部位或缺损部位的雄激素受体激动剂(优选为同化类固醇,更优选为睪酮或其衍生物)的量优选使得不发生雄激素受体激动剂的全身性作用并且因此避免雄激素受体激动剂的不良作用,例如对肝脏或其他器官、生殖系统、心血管系统和血清脂质分布的不良作用。这意指雄激素受体激动剂的剂量优选不导致超过血清睪酮在人中的平均浓度四倍(优选两倍)的血清水平。因此,根据本发明局部施用的睪酮或衍生物(优选睪酮)的优选量为1μg至10mg,更优选为5μg至5mg,更优选为15μg至2.5mg,更优选为20μg至1.5mg,最优选为约50μg。此量优选存在于根据本发明的贴剂或可注射的储库形成制剂中。以医疗装置或植入物的涂层局部施用于骨骼破裂部位或缺损部位的雄激素受体激动剂(优选为同化类固醇,更优选为睪酮或其衍生物)的量可以甚至更低。根据本发明局部施用的睪酮或衍生物在此类涂层中的优选量为10ng至2.5μg/cm2涂布表面。
若使用如本文所定义的另一雄激素受体激动剂或睪酮衍生物替代睪酮,则其局部施用量优选等效于上述的睪酮量。例如,雄酮为睪酮类似物,其具有约为睪酮效能的1/7的效能。因此,若根据本发明使用雄酮,则施用量优选为睪酮的以上所示量的7倍。
术语“双膦酸盐”在本领域是熟知的并且是指具有两个膦酸根(PO3)基团的因其对破骨细胞骨骼再吸收的抑制作用而已知的一类药物。根据本发明使用的优选双膦酸盐选自:阿仑膦酸盐(alendronate)、利塞膦酸盐(risedronate)、伊班膦酸盐(ibandronate)、帕米膦酸盐(pamidronate)、氯屈膦酸盐(clodronate)、唑来膦酸盐(zoledronate)、依替膦酸盐(etidronate)、替鲁膦酸盐(tiludronate)、米诺膦酸盐(minodronate)、奥帕膦酸盐(olpadronate)、奈立膦酸盐(neridronate)、因卡膦酸盐(incadronate)及其混合物。更优选的双膦酸盐选自含氮双膦酸盐,其优选地选自:阿仑膦酸盐、利塞膦酸盐、伊班膦酸盐、帕米膦酸盐、唑来膦酸盐、米诺膦酸盐、奥帕膦酸盐、奈立膦酸盐、因卡膦酸盐。特别优选的双膦酸盐和盐为阿仑膦酸盐或阿仑膦酸钠。如本文所用的短语“药学上可接受的盐”是指双膦酸盐的盐,其适用于治疗哺乳动物(优选为人)而基本上无不良作用,例如毒性和过敏反应。根据本发明局部施用于骨骼破裂部位的双膦酸盐或其盐(优选为阿仑膦酸盐或阿仑膦酸钠)的量优选使得不发生双膦酸盐的全身性作用并且因此避免双膦酸盐的不良作用,例如在除破裂部位以外的其它位置抑制骨更新、低钙血症和上部GI不良作用。根据本发明局部施用的双膦酸盐或其盐的优选量为0.1μg至1mg,更优选为0.1μg至500μg,更优选为1μg至250μg,更优选为1.5μg至150μg,更优选为2μg至100μg,最优选为约50μg。此量优选存在于根据本发明的贴剂或可注射的储库形成制剂中。以医疗装置或骨骼植入物的涂层局部施用于骨骼破裂部位或缺损部位的双膦酸盐或其盐的量可以甚至更低。根据本发明局部施用的双膦酸盐或其盐在此类涂层中的优选量为20ng-500ng至2.5μg/cm2涂布表面。若双膦酸盐或其盐为阿仑膦酸盐或阿仑膦酸钠,则优选使用这些量。若根据本发明使用唑来膦酸盐或其盐,则施用量优选比以上所示的量低20-80倍,因为唑来膦酸盐与阿仑膦酸盐相比活性高约20-80倍。因此,若根据本发明以贴剂或可注射的储库形成制剂局部施用唑来膦酸盐,则其量优选为1ng至50μg,更优选为1ng至25μg,更优选为12.5ng至12.5μg,更优选为20ng至7.5μg,更优选为25ng至5μg。根据本发明局部施用的唑来膦酸盐或其盐在涂层中的优选量为0.25ng-25ng/cm2涂布表面。
包含至少一种可生物降解的聚合物、雄激素受体激动剂和双膦酸盐或其药学上可接受的盐的根据本发明的组合物可以是固体形式或者液体或半固体形式。组合物优选局部施用于骨骼,尤其是骨骼破裂或骨骼缺损。
在优选实施方案中,根据本发明的组合物在室温(即在约37℃下)下和在体内为固体形式。在此种情况下,包含本发明的组合物或由本发明的组合物组成的植入物可以例如以贴剂形式植入患者体内。因此,也提供包含根据本发明的组合物的贴剂。如本文所用的“贴剂”是指一块固体,优选为柔韧的材料,例如包含可生物降解的聚合物和根据本发明的活性化合物的组合的片材。根据本发明的贴剂尤其适用于刺激复合性破裂和/或复杂性破裂的愈合,其中破裂部位可在无需侵入性方法的情况下接近和/或其中破裂部位需要例如通过矫形外科医师接近以进行破裂骨骼或周围组织或脉管系统的补充治疗。根据本发明的贴剂优选施用于破裂部位,更优选地,用贴剂覆盖破裂部位。或者,根据本发明的贴剂优选施用于骨骼缺损部位,更优选地,用贴剂覆盖缺损部位。以这种方式,活性化合物的逐渐释放将集中于破裂部位。因此,贴剂优选局部施用于骨骼,尤其是骨骼破裂或骨骼缺损。
为了辅助破裂愈合,贴剂仅需要向破裂骨骼释放活性组分,即活性化合物的释放仅需要在一个方向上,该方向朝向破裂部位。类似地,为了刺激骨骼填充物或植入物附着至现存骨骼,贴剂仅需要向骨骼缺损部位释放活性组分,即活性化合物的释放仅需要在一个方向上,该方向朝向缺损部位。因此,也提供包含根据本发明的组合物的贴剂,其包含含有根据本发明的所述组合物的第一层和可生物降解的第二层,所述第二层对于所述雄激素受体激动剂和所述双膦酸盐或其药学上可接受的盐是基本上不可渗透的。所述第二层优选还包含至少一种可生物降解的聚合物或由其组成,所述可生物降解的聚合物可以是存在于根据本发明的组合物中(即在贴剂的第一层中)的相同的可生物降解的聚合物或者是不同的可生物降解的聚合物。当施用于破裂骨骼或骨骼缺损时,第一层为贴剂的内层,其面向破裂骨骼或缺损,并且第二层为贴剂的外层,其背对破裂骨骼或缺损。所述层的存在预防在除骨骼破裂部位或缺损部位以外的其它位置释放至患者体内的活性化合物或至少减小其量。这可以减少活性化合物的不需要的作用并且减少需要存在于贴剂中的活性化合物的量。如本文所用,“基本上不可渗透”意指随时间从贴剂的第二层释放至贴剂的第一层内的活性化合物的量或从贴剂的第二层穿过贴剂的第一层释放的活性化合物的量是从贴剂的第二层向破裂的或缺损的骨骼方向释放的药物量的最多1/5,优选为最多1/10,更优选为最多1/100。
根据本发明的贴剂可以通过例如将两种活性化合物分散或溶于包含至少一种可生物降解的聚合物的溶液中来制备,所述两种活性化合物为雄激素受体激动剂(优选为同化类固醇,更优选为睪酮或其衍生物,更优选为睪酮)和双膦酸盐或其药学上可接受的盐(优选为阿仑膦酸盐)。在凝固和任选地进一步加工组合物之后,这产生贴剂,其中两种活性化合物或多或少地均匀分布在贴剂中或在贴剂的第一层中。或者,可制备两种独立的组合物,其中各活性化合物独立地分散或溶于包含至少一种相同或不同的可生物降解的聚合物的溶液中。各组合物随后凝固并且任选地分别进一步处理,其后通过将两种固体制剂(包含至少一种可生物降解的聚合物和雄激素受体激动剂的第一制剂以及包含至少一种可生物降解的聚合物和双膦酸盐或其药学上可接受的盐的第二制剂)组合形成贴剂。两种固体制剂的组合产生包含两个部分的单一组合物或贴剂,一个部分包含雄激素受体激动剂并且第二部分包含双膦酸盐或其盐。
进一步提供包含根据本发明的组合物的可注射制剂。此类可注射制剂在储存温度(通常为2-8℃)和/或室温(通常为15-25℃)下是液体的、胶化的或半固体的,但在原位(即在约37℃的温度下)凝固。如本文所用,术语“可注射制剂”是指可以通过注射施用于破裂骨骼并且旨在凝固以及因此保留在注射部位的制剂。此类可注射制剂也可以施用于骨骼缺损部位。如本文所用,“原位凝固”是指可注射制剂在向患者施用后黏度增加足以允许制剂保留在注射部位,例如为固体、半固体、糊状或凝胶状形式。本发明的可注射制剂具有在室温下时适用于注射(例如可使用注射器注射)的黏度。可注射的原位储库制剂的黏度优选为300mPas至800mPas。此类可注射制剂为例如液体或凝胶形式。在注射位置(其为骨骼破裂部位或骨骼缺损部位)凝固之后,制剂用作储库制剂,其随时间逐渐释放至少雄激素受体激动剂,优选睪酮或其衍生物,更优选睪酮、诺龙或二氢睪酮。由于双膦酸盐在释放之后在骨骼中积聚并且因此即使其在短时间段内释放仍可以在延长的时间段发挥其活性,因此双膦酸盐无需从储库制剂或贴剂逐渐释放。优选地,储库制剂逐渐释放两种活性化合物,即雄激素受体激动剂和双膦酸盐或其药学上可接受的盐。因此,根据本发明的可注射制剂优选为可注射的原位储库形成制剂。因此可注射制剂优选局部施用于骨骼,尤其是骨骼破裂或骨骼缺损。
根据本发明的可注射的原位储库制剂例如通过遍及骨骼破裂部位施用该制剂来应用,以使所得储库制剂在凝固之后覆盖大部分破裂部位,即至少25%,优选至少50%,更优选至少75%。最优选地,由凝固的储库制剂覆盖基本上全部破裂部位。可注射的原位储库形成制剂可以以单次注射或通过多次注射施用于破裂部位。
还提供包含根据本发明的组合物的骨骼填充物。如本文所用的术语“骨骼填充物”在本领域是熟知的并且也称为“骨骼空隙填充物”。该术语是指可以用于填充骨骼中的间隙或空隙的材料。最常见的骨骼填充物类型为骨水泥和去矿物质骨基质。去矿物质骨基质(DBM)是来自经捐赠的人类组织的已去除无机矿物质以及大多数细胞以使胶原基质保留的同种异体移植骨骼。然后去矿物质骨骼与生物相容性载体组合以提供去矿物质骨基质。适合用作生物相容性载体的材料为透明质酸、葡聚糖以及聚氧化乙烯与聚丙烯的普朗尼克(pluronic)嵌段共聚物。“骨水泥”在本领域是熟知的,并且是指可在骨骼中或围绕骨骼施用例如以填充间隙或空隙,或在骨骼植入物与周围骨骼之间施用以将植入物或螺钉或板固定至现存骨骼的材料。最常见的骨水泥类型为包含聚甲基丙烯酸甲酯(PMMA)或PMMA与MMA共聚物掺混物的水泥和磷酸钙水泥(例如包含无水磷酸四钙、磷酸三钙和/或磷酸二钙)或其复合物。骨水泥通常以双组分材料提供。将基于PMMA/MMA的水泥的两种组分混合,接着诱发聚合,从而导致水泥黏度变化以使其可局部施用,其后其在施用部位硬化为固体水泥。磷酸钙水泥通常由粉末和液相组成。当与水混合时,粉末组合物形成羟基磷灰石。
包含可生物降解的聚合物、雄激素受体激动剂(优选为睪酮或其衍生物)和双膦酸盐的根据本发明的组合物例如与骨水泥组分中的一种或多种(或在这些组分混合和硬化之前)混合或与去矿物质骨基质混合。本发明的组合物例如与一种或多种骨水泥组分混合或者与构成微球形式的去矿物质骨基质的组分混合,然后在骨骼缺损部位或破裂部位施用并且因此填充物硬化。因此,提供包含根据本发明的组合物的骨骼填充物。优选地,所述组合物以微球形式存在于骨骼填充物中。因此,提供包含微球的骨骼填充物,所述微球包含根据本发明的组合物。微球例如具有1μm至1000μm的平均尺寸。骨骼填充物优选为骨水泥或去矿物质骨基质。
或者,根据本发明的组合物可以以涂层形式施用于骨骼填充物表面。包含根据本发明的组合物的此类涂层也适用于与医疗装置和骨骼植入物一起使用。因此,涂层优选局部施用于骨骼部位,尤其是骨骼破裂或骨骼缺损。因此,还提供涂层,其优选用于骨骼填充物、骨骼植入物和/或医疗装置,所述涂层包含含有至少一种根据本发明的可生物降解的聚合物、雄激素受体激动剂和双膦酸盐或其药学上可接受的盐的组合物。也提供具有根据本发明的涂层的骨骼填充物、医疗装置或骨骼植入物。根据本发明的涂层可以通过例如将两种活性化合物分散或溶于包含至少一种可生物降解的聚合物的溶液中来制备,所述两种活性化合物为雄激素受体激动剂(优选为同化类固醇,更优选为睪酮或其衍生物,更优选为睪酮)和双膦酸盐或其药学上可接受的盐(优选为阿仑膦酸盐)。涂层可以施用于适当对象并且其后例如通过冷却凝固。如本文所用,术语“涂层”包括完全覆盖骨骼填充物、医疗装置或骨骼植入物表面的涂层或其部分。涂层优选覆盖骨骼填充物、医疗装置或骨骼植入物表面的至少50%。如本文所用的术语“医疗装置”是指可以在人或动物身体中(优选在骨骼组织中或围绕骨骼组织)使用的任何类型的装置,并且包括但不限于螺钉、骨板、销钉和脊椎棒。此类医疗装置优选为用于骨骼组织的医疗装置。如本文所用的术语“骨骼植入物”是指可以引入骨骼中或与骨骼连接的任何类型的植入物,并且包括但不限于牙齿植入物、脊椎植入物和替换关节,所述替换关节包括但不限于膝、髋、踝、肩、肘和腕关节。
如本文先前所示,当在骨骼破裂部位或缺损部位局部施用时,用雄激素受体激动剂(优选为睪酮或其衍生物)与双膦酸盐或其药学上可接受的盐进行的组合治疗至少部分为两种活性化合物的协同作用的结果,尤其是雄激素受体激动剂的同化作用与双膦酸盐的抗分解代谢作用的协同作用的结果。当用作医疗装置或骨骼植入物的涂层以及在骨骼填充物中或在其表面上使用时,认为雄激素受体激动剂(优选为睪酮或其衍生物)与双膦酸盐或其药学上可接受的盐的组合刺激新骨骼形成,尤其在骨骼填充物和/或植入物已在骨骼破裂部位或缺损部位引入之后的早期阶段。因此,骨骼填充物、医疗装置(例如螺钉、板或销钉)和骨骼填充物和/或植入物与现存骨骼的连接被改善并且较迅速地发生,并且破裂的愈合(若存在)受到刺激。
如以上所述的根据本发明的贴剂或可注射的储库形成制剂也适用于刺激骨骼缺损中形成新骨骼,其中骨骼空隙填充物和/或骨骼植入物已经引入骨骼缺损部位。将贴剂或可注射的储库形成制剂以上文所解释的方式施用于骨骼缺损部位,所述方式为所述贴剂或可注射的储库形成制剂覆盖骨骼与骨骼填充物和/或骨骼植入物之间的界面。在此类途径或可注射的储库制剂中的雄激素受体激动剂(优选为睪酮或其衍生物)与双膦酸盐或其药学上可接受的盐的组合活性刺激骨骼填充物和/或骨骼植入物与现存骨骼连接。
当在骨骼破裂部位局部施用时,根据本发明的贴剂、储库制剂、骨骼填充物和涂层逐渐释放两种活性化合物中的至少一种。优选地,从储库制剂、贴剂、骨骼填充物或涂层中逐渐释放至少雄激素受体激动剂(优选睪酮或其衍生物)。由于双膦酸盐在释放之后在骨骼中积聚并且因此即使其在较短时间段内释放仍可以在延长的时间段发挥其活性,因此双膦酸盐无需从储库制剂、贴剂、骨骼填充物或涂层中逐渐释放。优选地,储库制剂、贴剂、骨骼填充物或涂层逐渐释放两种活性化合物,即雄激素受体激动剂和双膦酸盐或其药学上可接受的盐。如本文所用,“逐渐”优选意指雄激素受体激动剂(优选为睪酮或其衍生物)或两种活性化合物在施用或应用于破裂部位或缺损部位后在1天至4个月的时间段内从储库制剂、贴剂、骨骼填充物或涂层中释放。优选地,雄激素受体激动剂或两种活性化合物在1天至12周,更优选为1天至10周,最优选为2周至10周(例如约4、5、6、7或8周)的时间段内从储库制剂、贴剂、骨骼填充物或涂层中释放。在包含两个独立部分(各包含活性化合物之一)的根据本发明的固体组合物或贴剂中,可以选择各部分中的可生物降解的聚合物以使雄激素受体激动剂和双膦酸盐或其盐的释放特征不同。例如,可以选择聚合物的类型、分子量和量以使双膦酸盐或盐与雄激素受体激动剂相比在较短的时间段内释放。
根据本发明的组合物、可注射制剂、贴剂、骨骼填充物和涂层还包含至少一种可生物降解的聚合物。优选地,组合物、可注射制剂、贴剂和涂层全部可生物降解。因此,提供根据本发明的可生物降解的组合物、可注射制剂、贴剂和涂层。如本文所用的术语“可生物降解”是指在体内逐渐溶解、分解、水解和/或侵蚀的材料。通常,本文中的“可生物降解的聚合物”为可水解的聚合物,和/或通过水解和/或酶作用在体内降解的聚合物。如本文所用的术语“可生物降解的聚合物”包括可以使用并且在体内可降解的任何可生物降解的合成聚合物和天然聚合物。使用可生物降解的聚合物的优势为根据本发明的组合物、可注射制剂、贴剂和涂层不需要在已经释放活性化合物之后从患者的身体中被除去。
本领域已知的可以用于在体内逐渐释放活性化合物的任何可生物降解的聚合物或共聚物均可以用于本发明的组合物、可注射制剂和贴剂。例如,WO 2011/161531、WO 2010/018159、WO 2005/068533、WO 2013/015685、WO 2012/175746和WO 2012/175748描述了适合的可生物降解的聚合物和共聚物以及方法,所述专利通过引用并入本文。适合的可生物降解的聚合物和共聚物的实例包括但不限于聚丙交酯、聚乙交酯、聚己内酯、聚二氧环己酮、聚碳酸酯、聚羟基丁酸酯、聚草酸亚烷基酯、聚酸酐、聚酰胺、聚氨酯、聚酰胺酯、聚缩醛、聚缩酮、聚原碳酸酯、聚磷腈、聚羟基戊酸酯、聚琥珀酸亚烷基酯、聚苹果酸、聚原酸酯,及其共聚物、嵌段共聚物和混合物,例如聚D,L-丙交酯(PDLLA)、丙交酯与乙交酯的共聚物(PLGA)、丙交酯与ε-己内酯的共聚物、聚(丙交酯-ε-己内酯)(PLA-ε-CL)共聚酯和聚丙交酯-三亚甲基碳酸酯共聚物,以及基于氨基酸的聚合物,例如基于酪氨酸的聚芳酯和聚碳酸酯以及基于亮氨酸和/或赖氨酸的聚酯氨基甲酸酯和聚酰胺酯。优选的可生物降解的聚合物为聚丙交酯、聚乙交酯、聚(乙交酯-ε-己内酯)、聚(乙交酯-D,L-丙交酯)、聚(DL-丙交酯)、聚(乙交酯-ε-己内酯)、基于氨基酸的聚酯氨基甲酸酯和基于氨基酸的聚酰胺酯。
用于本发明的组合物、制剂、贴剂、骨骼填充物和涂层的可生物降解的聚合物的种类、聚合物(单一单体或共聚物)的类型、可生物降解的聚合物的分子量和可生物降解的聚合物的量的选择通常取决于贴剂、储库制剂、骨骼填充物和涂层的所需特性。例如,可生物降解的聚合物的类型、分子量和量可影响活性化合物从贴剂、储库制剂、骨骼填充物和涂层释放的时间周期,如以上所示。除了活性化合物释放的时间周期之外,释放的动力学可以受聚合物或聚合物组合的种类、类型、量、分子量等的选择影响。例如,可以选择聚合物以使活性化合物之一或两者的初始突释在将根据本发明的可注射的原位贴剂、储库制剂、骨骼填充物和涂层施用于破裂部位或缺损部位之后发生。在此情况下,例如1%、5%、10%或甚至更高的活性化合物之一或两种活性化合物在例如施用于破裂部位4或8小时内释放。然而,优选地,此类初始突释受到阻止,并且两种活性化合物的释放经由零级动力学发生,其意指活性化合物从贴剂、储库制剂、骨骼填充物和涂层的释放随时间基本上是线性的。因此,在优选实施方案中,储库制剂、贴剂、骨骼填充物或涂层对于雄激素受体激动剂(优选为睪酮或其衍生物,更优选为雄激素受体激动剂)和双膦酸盐或其药学上可接受的盐(优选为阿仑膦酸盐或阿仑膦酸钠)表现出零级释放动力学。
此外,所需黏度也决定用于本发明的组合物、可注射制剂、贴剂、骨骼填充物和涂层中的可生物降解的聚合物的类型、种类和量。例如,若将根据本发明的组合物用于产生可注射的原位储库形成制剂,则优选地选择在室温下具有适用于注射并且在约37℃温度下凝固的黏度的可生物降解的聚合物或聚合物组合。或者,若将根据本发明的组合物用于制备贴剂或涂层,则优选地选择具有在高温下(例如高于42℃,优选高于50℃)适合溶解或分散活性化合物并且在室温和约37℃的温度下为固体的黏度的可生物降解的聚合物或聚合物组合。
在优选实施方案中,至少一种可生物降解的聚合物为基于氨基酸或含氨基酸的聚合物。尤其优选为可生物降解的基于氨基酸的聚酯氨基甲酸酯和可生物降解的基于氨基酸的聚酰胺酯。此类聚合物例如具有以下优势:可以选择它们以使其主要通过酶活性在体内降解,因此活性化合物的释放主要遵循零级动力学。特别地,优选的基于氨基酸的聚合物在WO 2012/175746和WO 2012/175748中进行了描述。本文描述了下式的基于氨基酸的聚酰胺酯(PEA):
其中:
-m在0.1至0.9变化;p在0.9至0.1变化;n在50至150变化;
-各R1独立地为(C1-C20)亚烷基;
-各R2独立地为氢或(C6-C10)芳基(C1-C6)烷基;
-各R3独立地为氢、(C1-C6)烷基、(C2-C6)烯基、(C2-C6)炔基或(C6-C10)芳基(C1-C6)烷基;并且
-各R4独立地为(C2-C20)亚烷基。
优选地,m在0.01至0.99变化;p在0.2至3变化并且q在0.10至1.00变化,由此n为5至100;R1为-(CH2)8;R3和R4在主链单元中,m和p为亮氨酸,-R5为己烷,并且R6为以下结构式的1,4:3,6-双失水己醣醇的双环片段:
R7选自H或苄基并且R8为-(CH2)4-。
特别地,WO 2012/175746和WO 2012/175748所述的优选的基于氨基酸的PEA共聚物具有式
其中
-m+p在0.9-0.1变化并且q在0.1至0.9变化;
-m+p+q=1,由此m或p可以为0;
-n在5至300变化;
-R1独立地选自(C2-C20)亚烷基、(C2-C20)亚烯基、-(R9-CO-O-R10-O-CO-R9)-、-CHR11-O-CO-R12-COOCR11-及其组合;
-R3和R4在单个主链单元中,m或p分别独立地选自氢、(C1-C6)烷基、(C2-C6)烯基、(C2-C6)炔基、(C6-C10)芳基、(C1-C6)烷基、-(CH2)SH、-(CH2)2S(CH3)、-CH2OH、-CH(OH)CH3、-CH2)4NH3+、--(CH2)3NHC(=NH2+)NH2、-CH2COOH、-(CH2)COOH、-CH2-CO-NH2、-CH2CH2-CO-NH2、-CH2CH2COOH、CH3-CH2-CH(CH3)-、(CH3)2-CH-CH2-、H2N-(CH2)4-、Ph-CH2-、CH=C-CH2-、HO-p-Ph-CH2-、(CH3)2-CH-、Ph-NH-、
-R5选自(C2-C20)亚烷基、(C2-C20)亚烯基、烷氧基或寡聚乙二醇;
-R6选自下式的1,4:3,6-双失水己醣醇的双环片段:
-R7选自由(C6-C10)芳基(C1-C6)烷基;
-R8为-(CH2)4-;
-R9或R10独立地选自C2-C12亚烷基或C2-C12亚烯基;
-R11或R12独立地选自H、甲基、C2-C12亚烷基或C2-C12亚烯基,并且由此a为至少0.05,b为至少0.05并且a+b=1。
此类基于氨基酸的PEA可以使用本领域已知的方法来制备,例如如WO 2012/175746和WO 2012/175748的方案1所述。其描述了通过对甲苯磺酸二胺盐与活化二酸的溶液缩聚来合成聚酰胺酯。通常,将二甲亚砜或二甲基甲酰胺用作溶剂并且将三乙基酰胺用作碱,反应通常在惰性氛围和60℃下于持续搅拌下进行24-72小时。然后将反应混合物经由水沉淀,然后有机沉淀和过滤来纯化,然后在减压下干燥以得到聚酰胺酯。
在另一优选实施方案中,至少一种可生物降解的聚合物为多嵌段共聚物,其包含至少两种衍生自两种不同预聚物的可水解片段。特别地,优选为多嵌段共聚酯,其由乙交酯-ε-己内酯片段和丙交酯-乙交酯片段组成。此类共聚物例如具有以下优势:可以选择它们以使其主要经由表面磨蚀在体内降解,因此活性化合物的释放主要遵循零级动力学。特别地,优选的多嵌段共聚物在WO 2005/068533和WO 2013/015685中进行了描述。
WO 2005/068533描述了多嵌段共聚物,其包含至少两种衍生自预聚物A和B的可水解片段,所述片段通过多官能增链剂连接并且选自预聚物A和B以及三嵌段共聚物ABA和BAB,其中多嵌段共聚物在生理(身体)条件下是非晶形的。所述增链剂优选衍生自双官能脂肪族化合物,优选二异氰酸酯,例如1,4-丁烷二异氰酸酯。所述预聚物(A)优选包含至少一种环状单体与至少一种选自二醇、二羧酸和羟基羧酸的非环状引发剂的反应产物,其中所述环状单体优选地选自:乙交酯、丙交酯(L、D或DL)、ε-己内酯、δ-戊内酯、三亚甲基碳酸酯、四亚甲基碳酸酯、1,4-二噁烷-2-酮(对二氧环己酮)、1,5-二氧杂环庚烷-2-酮和/或环状酸酐(例如氧杂环庚烷-2,7-二酮)。所述预聚物(B)优选包含ε-己内酯、δ-戊内酯、三亚甲基碳酸酯、对二氧环己酮、DL-丙交酯和/或乙交酯,更优选地,所述预聚物(B)含有d,l-丙交酯,并且优选为聚(d,l-丙交酯)或聚(丙交酯-乙交酯(50/50)),其中预聚物(B)优选具有高于300的数均分子量(Mn)。
WO 2013/015685描述了半结晶、相分离、热塑性多嵌段共聚物,该共聚物特征在于:
a)其包含至少一个可水解预聚物(A)片段和至少一个可水解预聚物(B)片段,
b)所述多嵌段共聚物在生理条件下具有37℃或低于37℃的玻璃化转移温度(Tg)和110-250℃的熔点(Tm);
c)所述片段通过多官能增链剂连接;
d)所述片段在聚合物链上随机分布;
e)至少部分预聚物(A)片段衍生自水溶性聚合物。所述增链剂优选为双官能脂肪族增链剂,优选为二异氰酸酯,例如1,4-丁烷二异氰酸酯。所述预聚物(A)优选包含环状单体和/或非环状单体的反应产物,其中所述非环状单体优选地选自琥珀酸、戊二酸、己二酸、癸二酸、乳酸、乙醇酸、羟基丁酸、乙二醇、二甘醇、1,4-丁二醇和/或1,6-己二醇,并且其中所述环状单体优选地选自乙交酯、丙交酯、ε-己内酯、δ-戊内酯、三亚甲基碳酸酯、四亚甲基碳酸酯、l,5-二氧杂环庚烷-2-酮、l,4-二噁烷-2-酮(对二氧环己酮)和/或环状酸酐例如氧杂环庚烷-2,7-二酮。所述预聚物(B)片段优选包含一定量和比率的衍生自羟基烷酸酯、乙交酯、L-丙交酯或D-丙交酯(优选L-丙交酯预聚物和D-丙交酯预聚物)的可结晶聚合物,以使实现L-丙交酯与D-丙交酯之间的立体复合,更优选地,所述预聚物(B)为具有1000g/mol或多于1000g/mol的Mn的聚(L-乳酸)。
此类共聚物尤其优选用于本发明的组合物中。此类多嵌段共聚物可以使用本领域已知的方法来制备,例如通过用等量的双官能分子(优选脂肪族分子,例如二异氰酸酯,例如1,4-丁烷二异氰酸酯)以所需比率使含有单体的预聚物的混合物链增长来实现,如WO 2005/068533和WO 2013/015685所述。
两种活性化合物(雄激素受体激动剂和双膦酸盐或其药学上可接受的盐)例如在聚合物为液体的温度(便利地,例如室温)下或在组合物于室温下为固体的情况下在高温下溶解或分散于至少一种可生物降解的聚合物的溶液中。可以通过无菌生产或在生产后的灭菌来获得无菌产品。
任选地,根据本发明的组合物含有一种或多种赋形剂。可以将赋形剂添加至至少一种可生物降解的聚合物的溶液中。例如,可存在以下赋形剂,其修饰可生物降解的聚合物的物理和/或机械性质,例如改善聚合物和/或活性化合物的溶解度;改善活性化合物在聚合物溶液中的分散度或调节活性化合物从根据本发明的储库制剂、贴剂、骨骼填充物或涂层的释放。另外,用作可生物降解的聚合物的溶剂的赋形剂可包括在本发明的组合物中。适合的赋形剂的实例在本领域是熟知的,并且包括但不限于溶剂、表面活性剂、分散剂和增稠剂,更特别地,甲醇、乙醇、丙二醇、吐温(Tween)、聚(乙二醇)、聚乙烯醇、乳酸、乙酸、褐藻酸、羧甲基纤维素、明胶、壳聚糖、瓜尔豆胶、羟乙基纤维素、羟乙基甲基纤维素、淀粉、预胶凝淀粉、羟丙基淀粉、甲基纤维素、果胶、甘油、N,N-二甲基乙酰胺、苯甲酸苯甲酯、聚氧乙基化脂肪酸、卵磷脂、大豆油、植物油和棉籽油。赋形剂浓度通常为以组合物的重量计1%至50%,优选为组合物的1重量%至30重量%,更优选为组合物的1重量%至20重量%。
本发明的组合物、可注射的原位储库形成制剂、贴剂、骨骼填充物和涂层适用于治疗骨骼破裂和/或骨骼缺损。特别地,所述组合物、制剂、贴剂、骨骼填充物和涂层适用于促进破裂愈合。所述组合物、制剂、贴剂、骨骼填充物和涂层还尤其适用于促进骨骼填充物和/或植入物与现存骨骼的连接。因此,提供组合物,其包含雄激素受体激动剂(优选为同化类固醇,更优选为睪酮或其衍生物,更优选为睪酮、诺龙或二氢睪酮)和双膦酸盐或其药学上可接受的盐(优选为阿仑膦酸盐或阿仑膦酸钠),用于治疗骨骼破裂或骨骼缺损的方法。还提供组合物,其包含雄激素受体激动剂(优选为同化类固醇,更优选为睪酮或其衍生物,更优选为睪酮、诺龙或二氢睪酮)和双膦酸盐或其药学上可接受的盐(优选为阿仑膦酸盐或阿仑膦酸钠),用于骨骼破裂愈合的方法。所述方法优选包括向破裂部位或缺损部位施用包含至少一种可生物降解的聚合物、雄激素受体激动剂和双膦酸盐或其药学上可接受的盐的根据本发明的组合物,更优选地向破裂部位或缺损部位施用根据本发明的可注射的原位形成的储库制剂或贴剂。或者,所述方法包括向骨骼破裂部位或骨骼缺损部位或者向骨骼破裂部位或骨骼缺损部位内引入包含根据本发明的组合物的骨骼填充物或具有根据本发明的涂层的骨骼填充物、医疗装置或植入物。在另一实施方案中,所述方法包含其组合并且因此包括向骨骼破裂部位或骨骼缺损部位或者向骨骼破裂部位或骨骼缺损部位内引入包含根据本发明的组合物的骨骼填充物或具有根据本发明的涂层的骨骼填充物、医疗装置或植入物,以及向破裂部位或缺损部位施用根据本发明的可注射的原位形成的储库制剂或贴剂。所述储库制剂、贴剂、骨骼填充物或涂层最优选地包含睪酮和阿仑膦酸盐或其盐。
还提供雄激素受体激动剂(优选为同化类固醇,更优选为睪酮或其衍生物,更优选为睪酮、诺龙或二氢睪酮)和双膦酸盐或其药学上可接受的盐(优选为阿仑膦酸盐或阿仑膦酸钠)的用途,其用于制备治疗骨骼破裂或骨骼缺损的药物。所述治疗优选包括向破裂部位或缺损部位施用包含至少一种可生物降解的聚合物、雄激素受体激动剂和双膦酸盐或其药学上可接受的盐的根据本发明的组合物,更优选地向破裂部位或缺损部位施用根据本发明的可注射的原位形成的储库制剂或贴剂。或者,所述方法包括向骨骼破裂部位或骨骼缺损部位或者向骨骼破裂部位或骨骼缺损部位中引入包含根据本发明的组合物的骨骼填充物或具有根据本发明的涂层的骨骼填充物、医疗装置或植入物。在另一实施方案中,所述方法包含其组合,并且因此包括向骨骼破裂部位或骨骼缺损部位或向骨骼破裂部位或骨骼缺损部位中引入包含根据本发明的组合物的骨骼填充物或具有根据本发明的涂层的骨骼填充物、医疗装置或植入物,以及向破裂部位或缺损部位施用根据本发明的可注射的原位形成的储库制剂或贴剂。所述储库制剂、贴剂、骨骼填充物或涂层最优选地包含睪酮和阿仑膦酸盐或其盐。
本发明还提供治疗患者(优选人类患者或其他哺乳动物)的骨骼破裂或缺损的方法,其包括向破裂部位或缺损部位施用根据本发明的贴剂或可注射的原位储库形成制剂。还提供骨骼破裂愈合的方法,其包括向破裂部位施用根据本发明的贴剂或可注射的原位储库形成制剂。所述贴剂或可注射的原位储库形成制剂优选包含治疗有效量的睪酮、诺龙或二氢睪酮,更优选为睪酮和阿仑膦酸盐或阿仑膦酸钠,最优选为阿仑膦酸钠。本发明还提供治疗患者(优选人类患者或其他哺乳动物)的骨骼破裂或缺损的方法,其包括向骨骼破裂部位或骨骼缺损部位或者向骨骼破裂部位或骨骼缺损部位内引入包含根据本发明的组合物的骨骼填充物或具有根据本发明的涂层的骨骼填充物、医疗装置或植入物。还提供治疗患者(优选人类患者或其他哺乳动物)的骨骼破裂或缺损的方法,其包括向破裂部位施用根据本发明的贴剂或可注射的原位形成的储库制剂,以及向骨骼破裂部位或骨骼缺损部位或者向骨骼破裂部位或骨骼缺损部位中引入包含根据本发明的组合物的骨骼填充物或具有根据本发明的涂层的骨骼填充物、医疗装置或骨骼植入物。如本文所用的术语“患者”是指可能患有骨骼破裂或骨骼缺损的人和任何非人个体。优选地,如本文所用的患者为哺乳动物。患者的优选实例包括但不限于人、狗和其他犬科动物、猫和其他猫科动物、马、母牛和其他牛科动物、小鼠、大鼠、兔、天竺鼠和其他啮齿动物、猴和其他灵长类动物、猪(pig)和猪(swine)及其类似者。尤其优选的患者为人患者。
还提供骨骼破裂愈合的方法,其包括向破裂部位施用根据本发明的贴剂或可注射的原位储库形成制剂。所述贴剂、可注射的原位储库形成制剂、骨骼填充物或涂层优选包含治疗有效量的睪酮、诺龙或二氢睪酮,更优选为睪酮和阿仑膦酸盐或阿仑膦酸钠,最优选为阿仑膦酸钠。
如本文所用的术语“骨骼破裂”包括创伤性破裂和病理性破裂、简单破裂与复合破裂两者。本发明的用途和方法尤其适用于治疗复杂的骨骼破裂,优选创伤性复杂的骨骼破裂。如本文所用,术语“复杂破裂”是指伴随有周围组织(例如神经和血管)和/或周围器官损伤的破裂。复杂破裂通常(但不一定)为复合或开放性破裂。本发明的用途和方法还尤其适用于治疗病理性骨骼破裂。根据本发明治疗的优选破裂为需要由矫形外科医师治疗的破裂。矫形外科医师例如使用螺钉来使破裂稳定。此类破裂尤其通过施用根据本发明的贴剂来有利治疗。根据本发明有利治疗的破裂的实例为脊椎、腿和手臂的破裂。根据本发明有利治疗的破裂的另一实例为脊椎压缩破裂。当脊柱中的一种或多种的骨骼破裂或崩塌时,通常当脊椎例如由于老化或使骨骼变弱的疾病(例如骨质疏松症、佩吉特氏病或骨癌)而已经变弱时,此类破裂发生。另一实例为完全破裂,其特征在于骨骼部分或片段之间存在间隙。通常,此类破裂的自发愈合发生得极其缓慢。因此,此类破裂尤其受益于由本发明提供的治疗。因此,提供根据本发明的方法或用途,其中所述破裂为复杂破裂(优选为创伤性复杂破裂)或病理性破裂。根据本发明治疗的患者优选为患有复杂破裂(优选创伤性复杂破裂)或病理性破裂的患者。用贴剂或可注射的原位储库形成制剂治疗的另一优选破裂为脊椎压缩破裂。
为了清楚和简洁描述的目的,本文可以将特征描述为本发明的相同或单独方面或实施方案的部分。本领域技术人员应了解,本发明的范围可以包括具有所有或一些本文所述特征的组合作为相同或单独实施方案的部分的实施方案。
以下实施例进一步解释了本发明。所述实施例并不限制本发明的范围,而仅仅用以阐明本发明。
附图简述
图1.通过阿仑膦酸盐、二羟基睪酮(雄诺龙(Stanolone))及其组合诱发MC3T3细胞的活性。ALP:碱性磷酸酶,AP:酸性磷酸酶。
实施例
材料和方法
细胞和处理
将MC3T3-E1(ECACC,登记号99072810)在补充有100U/ml青霉素、100ug/ml链霉素(Invitrogen,Carlsbad,CA)和5%胎牛血清(Hyclone,GE Heathcare)的α-MEM(Invitrogen,Carlsbad,CA)中培养。将细胞在标准条件(37℃、5%CO2和95%湿度)下生长。将MC3T3-E1细胞以26000个细胞/cm2的密度接种,并且将细胞的接种视为第0天时间点。在平板接种后第1天,用成骨培养基(补充有50μg/ml抗坏血酸(Sigma)的以上所述的培养基)、10nMβ-甘油磷酸酯(Sigma)替代MC3T3-E1细胞的培养基,并且在平板接种后第3天,添加激素或媒介物(0.1%乙醇)。
所测试的化合物为与阿仑膦酸盐组合的雄诺龙(二羟基睪酮(DHT))或仅为阿仑膦酸盐。所用的最终雄诺龙浓度为:含3nM、15nM、75nM和375nM雄诺龙(TCI Europe N.V.)的0.1%乙醇以及含2μM、10μM、50μM阿仑膦酸盐(TCI Europe N.V.)的milliQ。培养物的最终乙醇浓度为0.1%。每2-3天改变培养基。
碱性磷酸酶和酸性磷酸酶活性测定
用裂解缓冲液(100mM磷酸钾、含有0.2%Triton X-100(pH 7.8)的蛋白酶抑制剂混合液(Roche))裂解细胞10分钟。为了测定碱性磷酸酶活性,将CDP-star(Roche)添加至裂解物中并且在96孔光学板(optiplate)中于暗处孵育30分钟。用Filtermax F5(Molecular Devices)测量发光(1秒)。
通过向细胞裂解物添加新鲜制备的p-NPP缓冲液(含4-硝基苯基磷酸酯(Sigma)的0.1M NaAc+0.1%Triton X-100,pH 5.5)并且在37℃和5%CO2下孵育1.5小时来测定细胞的酸性磷酸酶活性。通过添加10μl NaOH停止反应。在405nm处用Filtermax F5(Molecular Devices)测量吸光度。
统计分析
所有数据均以平均值±SEM所示。使用学生t检验(Student's t-test)与仅用阿仑膦酸盐(0nM雄诺龙)相比在*p<0.05或**p<0.01或***p<0.001下分析数据。
结果
为了测试阿仑膦酸盐和阿仑膦酸盐与DHT(雄诺龙)的组合是否能够诱发成骨细胞的活性,将MC3T3细胞在培养基+/-化合物中刺激总共10天。然后通过分析ALP酶(其为骨细胞活性的公认标记)的量来测量成骨细胞的活性。然后针对酸性磷酸酶校正最终数据以校正细胞的总数。所获得的数据显示,仅用阿仑膦酸盐(0nM雄诺龙)处理MC3T3细胞在2μM和10μM的浓度下导致较小的ALP/AP活性增加,而50μM降低ALP/AP活性(图1)。相反,与仅用阿仑膦酸盐相比,用阿仑膦酸盐与雄诺龙(3nM、15nM、75nM和375nM雄诺龙)结合处理导致较强并且显著的ALP活性增加(图1)。
参考文献
Aspenberg P,Wermelin K,Tengwall P,Fahlgren A.Additive effects of PTH and bisphosphonates on the bone healing response to metaphyseal implants in rats.Acta Orthop.2008Feb;79(1):111-5.
Cheng BH,Chu TM,Chang C,Kang HY,Huang KE.Testosterone delivered with a scaffold is as effective as bone morphologic protein-2in promoting the repair of critical-size segmental defect of femoral bone in mice.PLoS One.2013Aug 5;8(8):e70234.
Einhorn,TA.Can an anti-fracture agent heal fractures?Clin Cases Miner Bone Metab.2010Jan;7(1):11-4.
Wermelin K,Aspenberg P,P,Tengvall P.Bisphosphonate coating on titanium screws increases mechanical fixation in rat tibia after two weeks.J Biomed Mater Res A.2008 Jul;86(1):220-7.
Xue D,Li F,Chen G,Yan S,Pan Z.Do bisphosphonates affect bone healing?A meta-analysis of randomized controlled trials.J Orthop Surg Res.2014 Jun 5;9:45.
- 该技术已申请专利。仅供学习研究,如用于商业用途,请联系技术所有人。
- 技术研发人员:让·艾伯特·戈森;
- 技术所有人:奥斯特优制药有限公司;
- 我是此专利的发明人
- 该领域下的技术专家
- 如您需求助技术专家,请点此查看客服电话进行咨询。
- 1、司老师:1.制浆造纸 2.植物资源精细化工与化学 3.生物质精炼 4.天然产物化学
- 2、薛老师:1.CRISPR-Cas系统 2.基因编辑 3.基因修复 4.天然产物合成 5.单分子技术开发与应用
- 3、戴老师:1.天然药物(中药)合成生物学研究 2.酵母生物学与工程化研究
- 4、孟老师:1. 基于糖类的抗肿瘤药物的合成和活性评价及糖类疫苗的研制 2.功能糖类的化学酶法合成及构效关系研究 3.多糖及仿生材料功能的开发及应用
- 5、满老师:1.天然产品的提取分离与活性研究 2.天然产物活性与安全性评价 3.中药组方配伍机制研究
- 如您是高校老师,可以点此联系我们加入专家库。
- 还没有人留言评论。精彩留言会获得点赞!