烟酰胺作为抗真菌药物增效剂的用途的制作方法
本发明涉及医药技术领域,具体地说,是烟酰胺作为抗真菌药物增效剂的新用途。
背景技术:
侵袭性真菌感染近年来已成为许多国家重症加强护理病房(ICUs)的重要死亡因素之一。然而临床上可选用的抗真菌药物种类比较少、毒副作用大,并且临床耐药菌株被不断的分离并报道出来,这使得真菌感染的治疗面临着越来越严峻的挑战。唑类、棘白菌素类及多烯类等抗真菌药物是临床上常用的能有效治疗深部及浅表部真菌感染的抗真菌药,如唑类中的氟康唑和伏立康唑等;棘白菌素类中的卡泊芬净;多烯类中的两性霉素B等。但随着临床上的耐药菌株越来越普遍,致使不得不加大用药剂量,某些抗真菌药物甚至加大用药量也无效。加大用药剂量必然会增加毒副作用,尤其如两性霉素B等对肝脏或心脏有毒副作用的药物。此外卡泊芬净、伏立康唑等原本价格高昂的药物的应用将受到限制。
烟酰胺(Nicotinamide),又名烟碱酰胺、尼克酰胺,是维生素B3的酰胺形式,它同时也是辅酶I和辅酶II的重要组成部分,其结构如式(I)所示。
临床实践中,烟酰胺是一种具有广泛用途的药物,如用于糙皮病、天疱疮、病态窦房结综合征、房室传导阻滞等的治疗。近年来,烟酰胺更是作为一种在高给药剂量下也安全、有效的药物用于非黑色素瘤皮肤癌、日光性角化症和弗里德希氏共济失调的治疗,且相关的研究进行到了三期临床试验阶段。但至今未见烟酰胺可作为唑类、棘白菌素类或多烯类等抗真菌药物增效剂的报道。
技术实现要素:
本发明的目的在于提供一种烟酰胺作为抗真菌药物增效剂的新用途。
本发明的第一方面,提供烟酰胺作为抗真菌药物增效剂的新用途,即,烟酰胺在制备抗真菌药物增效剂中的应用。
优选的,所述的抗真菌药物是唑类、棘白菌素类或多烯类等抗真菌药物。
优选的,所述的抗真菌药物是氟康唑、伏立康唑、卡泊芬净或两性霉素B等抗真菌药物。
优选的,所述的烟酰胺的用量为在抗真菌药物有效浓度中加入0.8~35mg/ml。例如,在每毫升含氟康唑、伏立康唑、卡泊芬净或两性霉素B 0.0078~8微克的液体制剂中,加入烟酰胺0.8~35毫克;或者在每毫升含氟康唑、伏立康唑、卡泊芬净或两性霉素B 0.0078~8微克的固体制剂中加入烟酰胺0.8~35毫克。
优选的,所述的真菌是白色念珠菌、热带念珠菌或新生隐球菌。
在本发明的实施例中,所述的真菌是白色念珠菌38、白色念珠菌901、白色念珠菌885、白色念珠菌953、白色念珠菌557;热带念珠菌2718、热带念珠菌ATCC750、热带念珠菌112936;新生隐球菌553、新生隐球菌20186、新生隐球菌041。
本发明的第二方面,提供一种抗真菌的药物组合物,所述的药物组合物的活性成分是抗真菌药物和烟酰胺。
优选的,所述的抗真菌药物是唑类、棘白菌素类或多烯类等抗真菌药物。
更优选的,所述的抗真菌药物是氟康唑、伏立康唑、卡泊芬净或两性霉素B等抗真菌药物。
经实验表明,当抗真菌药物与烟酰胺合用时,烟酰胺能降低抗真菌药物的用药剂量,不仅能在减少抗真菌药物用药量的情况下确保其对真菌的抗菌效果,而且对于临床分离的耐药性菌株、热带念珠菌或新生隐球菌均具有明显的增效作用。侵袭性真菌感染的动物模型显示,烟酰胺能增强氟康唑的治疗效果。因此烟酰胺可用作抗真菌药物的增效剂,用于不同真菌感染的治疗。
本发明优点在于:
本发明为烟酰胺开辟了一种新用途,作为抗真菌药物的增效剂,可降低唑类、棘白菌素类及多烯类等抗真菌药物的用药剂量,从而减轻了药物的毒副作用,特别是氟康唑、伏立康唑、卡泊芬净及两性霉素B等。尤其是烟酰胺作为抗真菌药物的增效剂,使抗真菌药物恢复对耐药真菌的作用,有效治疗真菌感染特别是耐药性真菌感染,降低药物的毒性并减轻病人用药的经济负担,此外还能增强抗真菌药物对热带念珠菌及新生隐球菌的作用,具有重要的临床应用价值。
附图说明
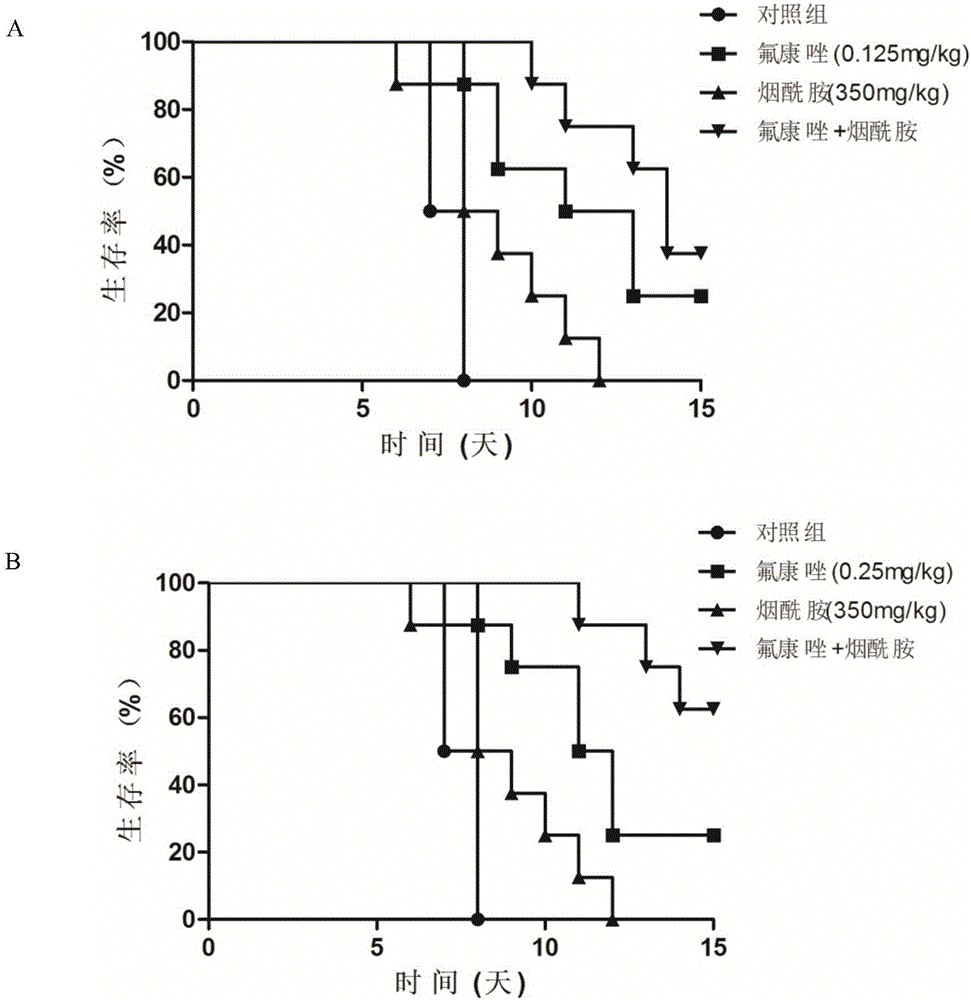
图1.烟酰胺对氟康唑治疗小鼠侵袭性真菌感染效果的影响。小鼠由尾静脉注射0.2ml白色念珠菌(5×106个/ml),烟酰胺单用或与氟康唑联用的药液由腹腔注射。图A为单独或联合腹腔注射0.125mg/kg氟康唑、350mg/kg烟酰胺时,系统性真菌感染小鼠生存率变化的曲线;图B为单独或联合腹腔注射0.25mg/kg氟康唑、350mg/kg烟酰胺时,系统性真菌感染小鼠生存率变化的曲线。
具体实施方式
下面结合实施例对本发明提供的具体实施方式作详细说明。
实施例1:烟酰胺和氟康唑合用对不同临床真菌菌株的作用
材料和方法
1.试药:
烟酰胺:美国sigma试剂公司(下同)。
氟康唑:美国sigma试剂公司(下同)。
二甲亚砜:中国医药(集团)上海化学试剂公司。
烟酰胺用培养液配成浓度为200mg/ml的母液,氟康唑用二甲亚砜配成浓度为6.4mg/ml的母液,受试药物于-20℃保存。实验前,将药物贮存液取出置35℃温箱融化,充分混匀,分别进行药效学试验。
2.菌株:
白色念珠菌、热带念珠菌和新生隐球菌临床株,由上海长海医院真菌室提供,均经形态学和生化学鉴定。
所有实验用菌株均于沙堡葡萄糖琼脂培养基(SDA)划板活化,于35℃培养1周后,分别挑取单克隆再次划板活化,取第二次所得单克隆置SDA斜面,用上述方法培养后于4℃保存备用。
3.培养液:
RPMI 1640培养液:RPMI 1640(Gibco BRL公司)10.0g,NaHCO3 2.0g,吗啡啉丙磺酸(Sigma)34.5g,加三蒸水900ml溶解,1N NaOH调pH至7.0,定容至1000ml,滤过消毒,4℃保存。
沙堡葡萄糖琼脂(SDA)培养基:蛋白胨10g,葡萄糖40g,琼脂18g,加三蒸水900ml溶解,加入浓度为2mg/ml氯霉素水溶液50ml,调整pH至7.0,定容至1000ml,高压灭菌后4℃保存。
YEPD培养液:酵母浸膏10g,蛋白胨20g,葡萄糖20g,加三蒸水900ml溶解,加入浓度为2mg/ml氯霉素水溶液50ml,定容至1000ml,高压灭菌后4℃保存。
4.仪器:
隔水式电热恒温培养箱(上海跃进医疗器械厂);
THZ-82A台式恒温振荡器(上海跃进医疗器械厂);
511型酶标分析仪(上海第三分析仪器厂);
5.菌液制备:
(1)念珠菌菌液
从4℃保存的SDA培养基上挑取念珠菌少量,接种至1mlYEPD培养液,于30℃以200rpm振荡培养活化,使真菌处于指数生长期后期。取该菌液至1mlYEPD培养液中,用上述方法再次活化16小时后,用血细胞计数板计数,以RPMI 1640培养液调整菌液浓度至3×103~5×103个/ml。
(2)新生隐球菌菌液
从4℃保存的SDA培养基上挑取新生隐球菌少量,接种至1mlYEPD培养液,于30℃以200rpm振荡培养活化,使真菌处于指数生长期后期。取该菌液至1mlYEPD培养液中,用上述方法再次活化16小时后,用血细胞计数板计数,以RPMI 1640培养液调整菌液浓度至3×103~5×103个/ml。
6.药敏板制备:
将烟酰胺母液用RPMI1640培养液稀释为25.6~0.8mg/ml。取无菌96孔板,于每排1~12号孔加入含有或不含一定浓度烟酰胺的RPMI1640培养液100μl;2号孔再分别加入相应的培养液196μl和氟康唑溶液4μl,或加入148.8μlRPMI1640培养液和烟酰胺溶液51.2μl。
对2~11号孔进行倍比稀释,使2~11号孔的最终氟康唑浓度分别为64、32、16、8、4、2、1、0.5、0.25和0.125μg/ml;烟酰胺浓度为25.6、12.8、6.4、3.2、1.6、0.8、0.4、0.2、0.1和0.05mg/ml;再于每排2~12号孔加入菌液100μl,使得1号孔为不含药物的RPMI 1640培养液,作为阴性对照,12号孔为不含药物的菌液,作为阳性对照。各药敏板于振荡器上振荡混匀5分钟后于30℃培养。
7.MIC80值判定:
含菌96孔板分别于30℃培养48小时后,按常规用酶标分析仪于620nm测各孔OD值。与阳性对照孔比,以OD值下降80%以上的最低浓度孔中的药物浓度为MIC80(真菌生长80%被抑制时的药物浓度)。
当药物的MIC80值超过测定浓度范围时,按以下方法进行统计:氟康唑MIC80值高于最高浓度64μg/ml时,计为“>64μg/ml”;烟酰胺MIC80值高于最高浓度25.6mg/ml时,计为“>25.6mg/ml”。上述实验均平行操作2到3次,当MIC80值能准确重复时才被接受;当MIC80值相差一个浓度以上时,则需要重新实验,直到符合要求为止。
实验结果见表1,表2。
表1烟酰胺与氟康唑单用和合用时,5株临床白色念珠菌的MIC80值
注:fluconazole的单位为μg/ml,nicotinamide的单位为mg/ml(下同)
表2烟酰胺与氟康唑单用和合用时,6株热带念珠菌及新生隐球菌的MIC80值
由表1和表2可见,合用时,12.8~25.6mg/ml的烟酰胺可使白色念珠菌对氟康唑的MIC80值下降16~32倍,3.2~25.6mg/ml的烟酰胺可使临床热带念珠菌对氟康唑的MIC80值下降8~64倍,6.4~25.6mg/ml的烟酰胺可使临床新生隐球菌对氟康唑的MIC80值下降8~64倍,说明烟酰胺能明显增强氟康唑的抗真菌作用。
实施例2:烟酰胺和伏立康唑合用对不同临床真菌菌株的作用
材料和方法
1.试药:
烟酰胺:美国sigma试剂公司(下同)。
伏立康唑:美国sigma试剂公司(下同)。
二甲亚砜:中国医药(集团)上海化学试剂公司。
烟酰胺用培养液配成浓度为200mg/ml的母液,伏立康唑用二甲亚砜配成浓度为6.4mg/ml的母液,受试药物于-20℃保存。实验前,将药物贮存液取出置35℃温箱融化,充分混匀,分别进行药效学试验。
2.菌株:
白色念珠菌、热带念珠菌和新生隐球菌,由上海长海医院真菌室提供,经形态学和生化学鉴定确认。
其它实验步骤与方法同实施例1。
实验结果见表3、表4。
表3烟酰胺与伏立康唑单用和合用时,5株临床白色念珠菌的MIC80值
注:voriconazole的单位为μg/ml,nicotinamide的单位为mg/ml(下同)
表4烟酰胺与伏立康唑单用和合用时,6株热带念珠菌及新生隐球菌的MIC80值
由表3和表4可见,合用时,12.8~25.6mg/ml的烟酰胺可使白色念珠菌对伏立康唑的MIC80值下降>256倍,3.2~12.8mg/ml的烟酰胺可使临床热带念珠菌对伏立康唑的MIC80值下降>8~>128倍,6.4~12.8mg/ml的烟酰胺可使临床新生隐球菌对伏立康唑的MIC80值下降1~>256倍,说明烟酰胺能明显增强伏立康唑的抗真菌作用。
实施例3:烟酰胺和卡泊芬净合用对不同临床真菌菌株的作用
材料和方法
1.试药:
烟酰胺:美国sigma试剂公司(下同)。
卡泊芬净:美国sigma试剂公司(下同)。
二甲亚砜:中国医药(集团)上海化学试剂公司。
烟酰胺用培养液配成浓度为200mg/ml的母液,卡泊芬净用二甲亚砜配成浓度为0.2mg/ml的母液,受试药物于-20℃保存。实验前,将药物贮存液取出置35℃温箱融化,充分混匀,分别进行药效学试验。
2.菌株:
白色念珠菌、热带念珠菌和新生隐球菌,由上海长海医院真菌室提供,经形态学和生化学鉴定确认。
其它实验步骤与方法同实施例1。
实验结果见表5,表6。
表5烟酰胺与卡泊芬净单用和合用时,5株临床白色念珠菌的MIC80值
注:caspofungin的单位为μg/ml,nicotinamide的单位为mg/ml(下同)
表6烟酰胺与卡泊芬净单用和合用时,6株热带念珠菌及新生隐球菌的MIC80值
由表5和表6可见,合用时,0.8~12.8mg/ml的烟酰胺可使白色念珠菌对卡泊芬净的MIC80值下降 4~8倍,25.6mg/ml的烟酰胺可使临床热带念珠菌对卡泊芬净的MIC80值下降 1~32倍,6.4~12.8mg/ml的烟酰胺可使临床新生隐球菌对卡泊芬净的MIC80值下降4~64倍,说明烟酰胺能明显增强卡泊芬净的抗真菌作用。
实施例4:烟酰胺和两性霉素B合用对不同临床真菌菌株的作用
材料和方法
1.试药:
烟酰胺:美国sigma试剂公司(下同)。
两性霉素B:美国sigma试剂公司(下同)。
二甲亚砜:中国医药(集团)上海化学试剂公司。
烟酰胺用培养液配成浓度为200mg/ml的母液,两性霉素B用二甲亚砜配成浓度为2mg/ml的母液,受试药物于-20℃保存。实验前,将药物贮存液取出置35℃温箱融化,充分混匀,分别进行药效学试验。
2.菌株:
白色念珠菌、热带念珠菌和新生隐球菌,由上海长海医院真菌室提供,经形态学和生化学鉴定确认。
其它实验步骤与方法同实施例1。
实验结果见表7,表8。
表7烟酰胺与两性霉素B单用和合用时,5株临床白色念珠菌的MIC80值
注:Amphotericin B的单位为μg/ml,nicotinamide的单位为mg/ml(下同)
表8烟酰胺与两性霉素B单用和合用时,6株热带念珠菌及新生隐球菌的MIC80值
由表7和表8可见,合用时,6.4~12.8mg/ml的烟酰胺可使白色念珠菌对两性霉素B的MIC80值下降 2~4倍,12.8~25.6mg/ml的烟酰胺可使临床热带念珠菌对两性霉素B的MIC80值下降 4~256倍,6.4~25.6mg/ml的烟酰胺可使临床新生隐球菌对两性霉素B的MIC80值下降4~16倍,说明烟酰胺能明显增强两性霉素B的抗真菌作用。
实施例5:烟酰胺和氟康唑合用对小鼠体内真菌感染的治疗作用
材料和方法
1.试药:
烟酰胺:美国sigma试剂公司(下同)。
氟康唑:美国sigma试剂公司(下同)。
二甲亚砜:中国医药(集团)上海化学试剂公司。
烟酰胺用培养液配成浓度为200mg/ml的母液,氟康唑用二甲亚砜配成浓度为6.4mg/ml的母液,受试药物于-20℃保存。实验前,将药物贮存液取出置35℃温箱融化,充分混匀,分别进行药效学试验。
2.菌株:
白色念珠菌SC5314(菌株的详细信息和制备方法参考文献:Fonzi WA,Irwin MY.Isogenic strain construction and gene mapping in Candida albicans.Genetics 1993;134:717-28.)。
3.动物:
Balb/c雌性小鼠,购自上海西普尔-必凯实验动物有限公司。
4.溶液:
沙堡葡萄糖琼脂(SDA)培养基:蛋白胨10g,葡萄糖40g,琼脂18g,加三蒸水900ml溶解,加入浓度为2mg/ml氯霉素水溶液50ml,调整pH至7.0,定容至1000ml,高压灭菌后4℃保存。
YEPD培养液:酵母浸膏10g,蛋白胨20g,葡萄糖20g,加三蒸水900ml溶解,加入浓度为2mg/ml氯霉素水溶液50ml,定容至1000ml,高压灭菌后4℃保存。
PBS缓冲液:磷酸二氢钾 0.27g,磷酸氢二钠 1.42g,氯化钠 8g,氯化钾0.2g,加去离子水约800mL充分搅拌溶解,然后加入浓盐酸调pH至7.4,最后定容到1000ml,高压灭菌后4℃保存。
5.菌液制备:
从4℃保存的SDA培养基上挑取念珠菌少量,接种至1mlYEPD培养液,于30℃以200rpm振荡培养活化,使真菌处于指数生长期后期。取该菌液至1mlYEPD培养液中,用上述方法再次活化16小时后,用血细胞计数板计数,以PBS缓冲液调整菌液浓度至5×106个/ml。
6.真菌感染及治疗:
烟酰胺用PBS稀释成35mg/ml,氟康唑用PBS或35mg/ml烟酰胺溶液稀释成 0.0125mg/ml及0.025mg/ml的溶液,使得给药时的药物剂量为烟酰胺350mg/kg,氟康唑0.125mg/kg或0.25mg/kg。小鼠随机分组,每组8只,其中三组小鼠腹腔注射烟酰胺溶液0.2ml,其余小鼠腹腔注射PBS溶液0.2ml。30分钟后,由小鼠尾静脉注入0.2ml菌液,并于4小时后由腹腔注射0.2ml药液,此后1天、2天、4天及6天再次给药。以给菌当天为0天,每天观察并记录小鼠生存情况,连续观察15天。实验结果见图1。
由图1可见,合用时,350mg/kg的烟酰胺可显著增强0.125mg/kg或0.25mg/kg氟康唑对小鼠侵袭性真菌感染的治疗效果。
以上已对本发明创造的较佳实施例进行了具体说明,但本发明创造并不限于所述实施例,熟悉本领域的技术人员在不违背本发明创造精神的前提下还可做出种种的等同的变型或替换,这些等同的变型或替换均包含在本申请权利要求所限定的范围内。
- 还没有人留言评论。精彩留言会获得点赞!
- 卷柏素类化合物在作为抗真菌药物增效剂中的应用的制作方法与工艺
- 一种抗细菌兼抗真菌作用的十一烯酸接枝多聚赖氨酸轭合物胶束制剂及制备方法与流程
- 一种抗真菌药物泊沙康唑的固体分散体及制备方法与应用与流程
- Ternatusine A在制备抗人体真菌药物中的应用的制作方法与工艺
- 白薇作为抗真菌类药物的新用途的制作方法与工艺
- 一种抗真菌增效药物体内筛选方法与流程
- 一种抗真菌感染的药物组合物及其制备方法、制剂与应用与流程
- 由杂环衍生物取代的抗真菌5,6‑二氢‑4H‑吡咯并[1,2‑a][1,4]苯并‑二氮杂*类及6H‑吡咯并[1,2‑a][1,4]苯并二氮杂*类的制作方法与工艺
- 包含抗真菌剂和甾类化合物的药物组合物的制作方法与工艺
- 一种具有协同抗耐药真菌的药物组合物、制备方法以及应用与流程