虾青素和/或氯化锂在制备预防和治疗慢性有机磷中毒所致的认知障碍病症的药物中的应用的制作方法
本发明属于药物领域,具体涉及虾青素和/或氯化锂在制备预防和治疗慢性有机磷中毒所致的认知障碍病症的药物中的应用。
背景技术:
有机磷农药(organophosphate pesticides,OPS)是目前世界范围内广泛使用的杀虫剂,具有杀虫谱广、药效高、价格低廉等特点,被广泛用于家庭和农业的防虫抗害中。在我国,根据国家质量管理总局调查资料显示:食品中的农药残留现象在我国大量存在,农作物中有机磷农药超标率为1%-35%。2010年,河南省开封市OPS农药残留检出率高达14.5%,这种长期低剂量接触有机磷农药严重危害着人类健康。正因如此,OPS残留成为我们日常生活中农药残留突出的安全隐患。目前研究发现,除了传统理论认为有机磷农药的毒性能够抑制胆碱酯酶的活性外,有机磷农药的使用通过直接影响神经细胞的复制和分化,直接对脑内神经系统产生严重的损害,通过增加活性氧的产生,使得脂质和蛋白质产生氧化应激损伤,直接损害细胞DNA而导致炎症反应和神经细胞凋亡的发生,从而与认知功能障碍和神经退行性疾病的发生有关。因此,开发一种能够减轻长期有机磷残留引起的神经毒性的药物或功能制品具有重要意义。
虾青素(Astaxanthin,AST)又名虾黄质、虾红素,是一种脂溶性酮式类胡萝卜素,雨生红球藻是自然界中合成和积累虾青素最多的微生物,虾、蟹、鱼、酵母和鸟类羽毛中同样含有虾青素的成分,作为微藻类的植物营养素,AST是海洋生物体内主要的类胡萝卜素之一。虾青素具有多种神经保护功能,包括急性神经损伤及慢性神经损伤。虾青素的神经保护作用主要通过它所具有的抗氧化、抗炎、抑制凋亡的作用来发挥。有研究表明虾青素能够减少海马可塑性损伤,通过增加齿状回(DG)区血流速,增强成年大鼠海马神经发生及学习记忆特别是空间学习记忆能力,并对焦虑抑郁情绪有很好的改善作用,是预防认知障碍疾病有效的天然化合物。虾青素是一种抗氧化能力比其他β-胡萝卜素和叶黄素高出十倍的海洋来源的化合物,其可有效通过血脑屏障阻止由神经元氧化损伤引起的神经系统退行性疾病。此外,虾青素通过抗凋亡作用减少海马神经元丢失,这使得新生神经元的存活得到有效保护。
目前治疗化学物中毒所致的认知障碍以及慢性神经损伤的药物主要为依达拉奉和石杉碱甲等药物,而这些药物大多具有药效不够持久,副作用较大等缺点。因此,研发新型低毒高效的针对慢性有机磷中毒致认知障碍的药物具有重要的经济和社会效益。国内外学者已经报道了一些关于虾青素在防治农药有机磷致雄性生殖毒性和致胚胎毒性的药物中的应用方面的专利(CN201410502878.5,CN201310018433.5),此外,虾青素还被用于制备治疗抗抑郁症药物和制备预防和治疗脑卒中药物中的用途(CN201210548264.1,CN200810195924.6)。也有学者报道,氯化锂在抗脂质过度积累诱导的心肌凋亡药物中的应用(CN201510980704.4),在甲基苯丙胺认知障碍药物中的应用(CN201610368414.9)等精神稳定剂类治疗方面的作用,但是目前还没有关于虾青素联合氯化锂在制备预防和治疗慢性有机磷中毒所致认知障碍药物的研究和应用报道。
技术实现要素:
针对现有技术中还未有针对慢性有机磷中毒致认知功能障碍的有效药物,本发明提供了虾青素和/或氯化锂在制备预防和治疗慢性有机磷中毒所致的认知障碍病症的药物中的应用。本发明提供的虾青素联合氯化锂治疗对慢性有机磷中毒导致的海马损伤具有神经保护作用,且可通过激活Akt/GSK3β/CREB信号通路来改善慢性有机磷中毒导致的认知功能障碍。
为实现上述发明目的,本发明采用下述技术方案予以实现:
本发明提供了虾青素和/或氯化锂在制备预防和治疗慢性有机磷中毒所致的认知障碍病症的药物中的应用。
进一步的:所述虾青素和氯化锂联合使用优于单独使用虾青素或氯化锂。
进一步的:所述认知障碍病症包括空间认知障碍、学习和记忆功能障碍以及精神焦虑抑郁障碍。
进一步的:所述虾青素和/或氯化锂能够显著改善有机磷中毒小鼠的认知功能,有助于小鼠学习和记忆能力的恢复。
进一步的:所述虾青素和/或氯化锂能够显著抑制慢性有机磷中毒引起的小鼠海马组织损伤,减少脑组织凋亡。
进一步的:所述虾青素以50mg/kg/day的剂量灌胃给药8周;
或者所述虾青素以50mg/kg/day的剂量灌胃给药,并联合氯化锂以2mmol/kg/day剂量腹腔注射给药,连用8周。
进一步的:所述虾青素和/或氯化锂能上调Akt/GSK3β/CREB信号通路的活化水平,抑制神经细胞凋亡,改善认知功能障碍。
进一步的:所述虾青素以50mg/kg/day的剂量灌胃给药,并联合氯化锂以2mmol/kg/day剂量腹腔注射给药,连用8周。
进一步的:所述的有机磷为久效磷、辛硫磷、对氧磷和三唑磷。
与现有技术相比,本发明的优点和积极效果是:本发明选取虾青素为研究对象,在体内水平上揭示其抑制慢性有机磷中毒导致的海马神经元损伤,改善认知功能障碍的作用。
本发明经实验证实虾青素联合氯化锂治疗具有显著的抗氧化、抑制凋亡的作用,能够对慢性有机磷中毒导致的海马损伤具有神经保护作用,且可通过激活Akt/GSK3β/CREB信号通路来改善慢性有机磷中毒导致的认知功能障碍,减轻小鼠的焦虑抑郁情绪,表明该试剂具有开发成新型预防和治疗慢性有机磷中毒所致的痴呆的药物的广阔前景。
结合附图阅读本发明的具体实施方式后,本发明的其他特点和优点将变得更加清楚。
附图说明
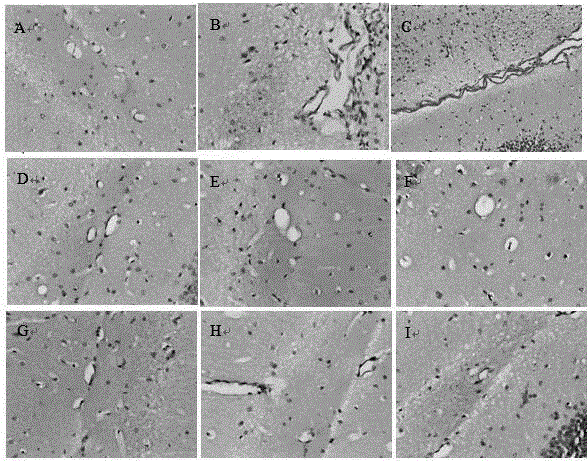
图1表明本发明试验中有机磷慢性中毒小鼠脑部海马区刚果红染色结果(400x,C图200x)。图1中,A:对照组;B和C模型组;D:虾青素组;E和F:虾青素加氯化锂组;G和H:依达拉奉组;I氯化锂组。
图2表明本发明试验中有机磷慢性中毒小鼠脑部海马CA1区TUNEL染色结果(400x)。图2中,A:对照组;B:模型组;C:虾青素组;D:依达拉奉组;E:氯化锂组;F:虾青素加氯化锂组。
图3表明本发明试验中有机磷慢性中毒小鼠脑部海马CA1区p-PI3K免疫组化结果(400x)。图3中,A:对照组;B:模型组;C:虾青素组;D:依达拉奉组;E:氯化锂组;F:虾青素加氯化锂组。
图4表明本发明试验中有机磷慢性中毒小鼠脑部海马CA3区p-GSK3β免疫组化结果(200x)。图4中,A:对照组;B:模型组;C:虾青素组;D:依达拉奉组;E:氯化锂组;F:虾青素加氯化锂组。
图5表明本发明试验中有机磷慢性中毒小鼠脑部海马CA3区p-CREB免疫组化结果(200x)。图5中,A:对照组;B:模型组;C:虾青素组;D:依达拉奉组;E:氯化锂组;F:虾青素加氯化锂组。
具体实施方式
下面结合附图和具体实施方式对本发明的技术方案作进一步详细的说明。
本发明按照国际公认的方法,评价了虾青素联合氯化锂治疗对慢性有机磷中毒导致的海马损伤的神经保护作用以及改善认知功能障碍的作用。本发明采用的虾青素采用市面销售的产品即可。
实施例1、虾青素联合氯化锂治疗对慢性有机磷中毒认知障碍小鼠行为学的影响
1)Morris水迷宫实验评价虾青素联合氯化锂治疗对染毒小鼠行为学影响
小鼠采用皮下注射染毒方法建立慢性有机磷中毒动物模型。染毒结束后应用Morris水迷宫对小鼠的记忆再现及空间记忆能力进行测试。共6天,取对照组小鼠5天内逃避潜伏期的均值为参考值,同时计算造模小鼠5天的平均逃避潜伏期与参考值之差占该鼠的平均逃避潜伏期时间的比值,该值>20%则认为模型成功,模型成功率90%。
模型制备成功后,虾青素组:虾青素以50mg/kg/day剂量给予灌胃,连续8周;依达拉奉组将依达拉奉每只给予3mg/kg腹腔注射,每日一次,连续8周;氯化锂组将氯化锂(Licl)每只给予2mmol/kg腹腔注射,隔日一次,连续8周。虾青素加抑制剂组将虾青素以50mg/kg/day剂量给予灌胃,后将氯化锂(Licl)每只给予2mmol/kg腹腔注射,隔日一次,连续8周。
定位航行实验结果如表1所示,5天的测试中,模型组小鼠找到水下隐蔽平台所用时间均显著高于对照组(P<0.05),这表明模型组小鼠存在学习记忆能力的损害;虾青素组小鼠逃避潜伏期所用时间较模型组有明显的缩短(P<0.05);依达拉奉组小鼠逃避潜伏期也随时间的改变逐渐缩短,但与模型组比较无统计学差异(P>0.05);氯化锂组小鼠逃避潜伏期较模型组小鼠也明显缩短(P<0.05);虾青素加氯化锂组逃避潜伏期较模型组有较为显著地缩短(P<0.05),该小组所需时间均短于其余治疗组的小鼠(P<0.05)。
表1本发明中各组小鼠Morris水迷宫逃避潜伏期的比较结果(x±s,n=8)
与对照组比较:#P<0.05;与模型组比较:*P<0.05
空间探索实验结果如表2所示,经过5天的定位航行训练结束后将水池中的平台取出,开始对各组小鼠进行空间探索实验测试,记录各组小鼠在目标象限(原平台所在象限)停留的时间比,以及穿越平台的次数。在目标象限停留的时间越长以及穿越平台的次数越多,表明该小鼠空间学习记忆能力越好,反之则越差。与对照组比较,模型组小鼠目标象限停留的时间比大为缩短,穿越平台的次数显著减少,这提示慢性有机磷致认知障碍小鼠的空间记忆能力出现较为严重的损伤(P<0.05);与模型组相比,虾青素治疗组、依达拉奉组、氯化锂组及虾青素加氯化锂组小鼠目标象限停留时间均有所增加,穿越平台次数亦增多明显,特别是虾青素加氯化锂组小鼠测试结果较模型组小鼠变化最为显著(P<0.05),这表明虾青素联合氯化锂抑制剂对改善由慢性有机磷中毒致认知障碍小鼠的空间学习记忆能力效果显著。
表2本发明中各组小鼠目标象限停留时间比和穿越平台次数的结果(x±s)
与对照组比较:#P<0.05;与模型组比较:*P<0.05.
2)高架十字迷宫实验评价虾青素联合氯化锂治疗对染毒小鼠行为学影响
小鼠采用皮下注射染毒方法建立慢性有机磷中毒动物模型。染毒结束并应用各种药物处理8周之后,应用高架十字迷宫实验评价药物对染毒小鼠行为学影响。将小鼠置于迷宫中央(开臂与闭臂结合处),小鼠头朝开臂,实验者距离迷宫中心至少1cm。打开录像系统,分别记录实验期(5min)内小鼠进入开臂和闭臂的次数和在两臂滞留的时间,以开臂停留时间的百分比和进入开闭次数百分比反应动物的焦虑状态。
高架十字迷宫测试结果如表3所示,模型组小鼠在开臂处停留时间的百分比、进入开臂次数百分比要显著低于对照组(均p<0.05),且模型组小鼠在测试过程中出现次数较多的刻板样重复性的焦虑动作(例如搓爪,挠头等),提示模型建立成功;虾青素治疗组小鼠处于开臂时间百分比、进入开臂次数百分比较模型组有明显的增长(P<0.05);依达拉奉组小鼠处于开臂时间百分比较模型组无统计学差异(P>0.05),进入开臂次数百分比较模型组明显缩短(P<0.05),但效果没有虾青素组明显(P<0.05);氯化锂组小鼠处于开臂时间百分比、处于开臂次数百分比较模型组有明显的增长(P<0.05);虾青素加氯化锂组小鼠处于开臂时间百分比、进入开臂次数百分比较模型组有非常显著性的增加(P<0.01),并高于其他治疗组小鼠。
表3本发明中各组小鼠开臂处停留时间的百分比和进入开臂次数百分比的比较结果(x±s)
与对照组比较:#p<0.05;与模型组比较:*p<0.05**p<0.01.
3)明暗箱实验评价虾青素联合氯化锂治疗对染毒小鼠行为学影响
小鼠采用皮下注射染毒方法建立慢性有机磷中毒动物模型。染毒结束并应用各种药物处理8周之后,应用明暗箱实验评价虾青素联合氯化锂治疗对染毒小鼠行为学影响。
明暗箱实验测试结果如表4所示,模型组小鼠在明箱区域停留时间的百分比、穿箱的频率均非常显著低于对照组(P<0.05,P<0.05),且模型组小鼠在测试过程中出现次数较多的刻板样重复性的焦虑动作(例如搓爪,挠头等);与模型组相比,虾青素治疗组、氯化锂组小鼠在明箱区域停留时间的百分比、穿箱的频率均存在明显的增长(P<0.05,P<0.05),氯化锂治疗组优于虾青素组;依达拉奉组小鼠在明箱区域停留时间的百分比较模型组小鼠无统计学意义(P>0.05);虾青素加氯化锂组小鼠在明箱区域停留时间的百分比、穿箱的频率较模型组有非常显著性的增加(P<0.01,P<0.01),并高于其他治疗组小鼠。
表4本发明中各组小鼠明箱区域停留时间的百分比和穿箱频率的比较结果(x±s)
与对照组比较:#p<0.05;与模型组比较:*p<0.05**p<0.01.
综上,Morris水迷宫实验、高架十字迷宫实验和明暗箱实验的结果表明,虾青素联合氯化锂治疗能够显著改善有机磷中毒小鼠的认知功能,有助于小鼠学习和记忆能力的恢复。
实施例2、虾青素联合氯化锂治疗对慢性有机磷中毒认知障碍小鼠海马组织形态学的影响
1)刚果红染色评价虾青素联合氯化锂治疗对染毒小鼠海马损伤的影响
小鼠采用皮下注射染毒方法建立慢性有机磷中毒动物模型。染毒结束并应用各种药物处理8周之后,打开头颅取海马组织进行石蜡切片制作,并应用刚果红染色评价虾青素联合氯化锂治疗对染毒小鼠海马损伤的影响。
刚果红染色结果如图1所示,对照组小鼠海马切片未见橘红色淀粉样沉积,海马齿状回背侧细胞带排列整齐;模型组小鼠海马组织内及邻近区域血管内皮可见橘红色淀粉样沉积,齿状回区出现较为明显的条带状橘红色沉淀,而海马组织锥体细胞并未见淀粉样沉积,这提示低剂量接触有机磷农药所导致的淀粉样沉积损伤较轻,还未出现较大面积斑块样沉淀;虾青素组、虾青素加氯化锂组小鼠海马组织内血管内皮橘红色淀粉样沉积明显减轻,分析是由于虾青素可增加脑血流量,这使得血管内皮的淀粉样沉积减轻;依达拉奉组与氯化锂组并未见明显的改善作用。
2)TUNEL法评价虾青素联合氯化锂治疗对染毒小鼠脑组织凋亡的影响
小鼠采用皮下注射染毒方法建立慢性有机磷中毒动物模型。染毒结束并应用各种药物处理8周之后,打开头颅取海马组织进行石蜡切片制作,并应用TUNEL法评价虾青素联合氯化锂治疗对染毒小鼠脑组织凋亡的影响。
TUNEL染色结果如图2所示,对照组小鼠脑组织海马CA1区凋亡细胞少或无,与对照组比较,模型组、虾青素组、依达拉奉组、氯化锂组、虾青素加氯化锂组可见不同程度的凋亡细胞(P<0.05);与模型组比较,虾青素组、依达拉奉组、虾青素加氯化锂组小鼠海马组织凋亡细胞比较有统计学意义(P<0.05),氯化锂组相比差异无统计学意义(P>0.05);虾青素组与依达拉奉组比较存在统计学意义(P<0.05);虾青素组与虾青素加氯化锂组比较无统计学差异(P>0.05),这表明,虾青素与依达拉奉均可减少慢性有机磷中毒致认知障碍小鼠海马区的细胞凋亡,虾青素治疗效果优于依达拉奉治疗组,氯化锂对慢性有机磷中毒致认知障碍小鼠海马区神经细胞凋亡的改善不明显。
总之,刚果红染色和TUNEL染色法结果表明虾青素联合氯化锂治疗能够显著抑制慢性有机磷中毒引起的小鼠海马组织损伤,减少脑组织凋亡。
实施例3、虾青素联合氯化锂治疗对慢性有机磷中毒认知障碍小鼠Akt/GSK3β/CREB信号通路活化水平的影响
1)免疫组化染色法评价虾青素联合氯化锂治疗对染毒小鼠Akt/GSK3β/CREB信号通路活化水平的影响
小鼠采用皮下注射染毒方法建立慢性有机磷中毒动物模型。染毒结束并应用各种药物处理8周之后,打开头颅取海马组织进行石蜡切片制作,并应用免疫组化染色法评价虾青素联合氯化锂治疗对染毒小鼠Akt/GSK3β/CREB信号通路活化水平的影响。
免疫组化染色结果如图3-图5所示,图3的p-PI3K免疫组织化学的结果表明,与对照组比较,模型组小鼠海马CA1区神经元边界不清且阳性细胞着色浅,平均光密度值比较差异有统计学意义(p<0.05);与模型组相比,虾青素组、氯化锂组、虾青素加氯化锂组p-PI3K的表达均升高(P<0.05),依达拉奉组与模型组比较也有升高,但差别无统计学意义(P>0.05)。
图4的p-GSK3β免疫组织化学结果表明,与对照组比较,模型组脑组织海马内p-GSK3β阳性染色较淡,胞体较小,阳性细胞显著减少,平均光密度值比较差异有统计学意义(P<0.05);与模型组相比,虾青素组、氯化锂组、虾青素加氯化锂组p-GSK3β的表达均升高(P<0.05),依达拉奉组与模型组比较也有升高,但差别无统计学意义(P>0.05)。
图5的p-CREB免疫组织化学结果表明,与对照组比较,模型组小鼠阳性细胞显著减少,p-CREB表达受到显著抑制(P<0.05);与模型组相比,虾青素组、依达拉奉组、氯化锂组、虾青素加氯化锂组p-CREB的表达均升高(P<0.05)。
表5各组小鼠海马组织内p-PI3K、p-Akt、p-GSK3β及p-CREB相对于β-actin的表达量
与对照组比较:#p<0.05;与模型组比较:*p<0.05.
2)Western blot法评价虾青素联合氯化锂治疗对染毒小鼠Akt/GSK3β/CREB信号通路活化水平的影响
小鼠采用皮下注射染毒方法建立慢性有机磷中毒动物模型。染毒结束并应用各种药物处理8周之后,取海马组织匀浆后取上清液,利用Western blot法评价虾青素联合氯化锂治疗对染毒小鼠Akt/GSK3β/CREB信号通路活化水平的影响。Western blot结果表明,与对照组相比,模型组小鼠p-PI3K、p-Akt、p-GSK3β、p-CREB表达水平显著降低,灰度值分析差异具有统计学意义(均P<0.05);与模型组相比,虾青素组、氯化锂组和虾青素加氯化锂组小鼠海马组织内p-PI3K、p-Akt、p-GSK3β、p-CREB的表达水平显著提高,灰度值分析差异具有统计学意义(P<0.05),且虾青素组与虾青素加氯化锂组p-PI3K、p-Akt、p-CREB的表达水平高于氯化锂组小鼠(P<0.05);依达拉奉组的表达水平与模型组灰度值比较无统计学差异(P>0.05)。
总之,免疫组化和western blot的结果提示虾青素联合氯化锂治疗可以上调Akt/GSK3β/CREB信号通路的活化水平,从而抑制神经细胞凋亡,改善认知功能障碍。
综上所述,本实验结果证实虾青素联合氯化锂治疗具有显著的抗氧化、抑制凋亡的作用,能够对慢性有机磷中毒导致的海马损伤具有保护作用,且可通过激活Akt/GSK3β/CREB信号通路来改善认知功能障碍,减轻小鼠的焦虑抑郁情绪,显示虾青素联合氯化锂治疗具有较好的抗慢性有机磷中毒致认知障碍活性。
本发明的虾青素来源于海洋虾蟹外壳或藻类,具有资源丰富、成本低廉和安全性高等诸多优点,并且在体内水平上证明其具有较好的抗慢性有机磷中毒致认知障碍的活性,为该类药物的开发提供了新的途径。
以上实施例仅用于说明本发明的技术方案,而非对其进行限制;尽管参照前述实施例对本发明进行了详细的说明,对于本领域的普通技术人员来说,依然可以对前述实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或替换,并不使相应技术方案的本质脱离本发明所要求保护的技术方案的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!