一种胶原膜的改性方法与流程
本发明属于生物材料领域,具体涉及一种胶原膜的改性方法。
背景技术:
牙科手术中常需要应用引导骨再生手术进行骨增量。胶原是细胞外基质的一种成分,已经广泛应用于引导骨再生术中。胶原膜有较好的生物相容性,并能促进成骨细胞黏附、增殖、迁移和分化,也能有阻挡成纤维细胞快速入侵骨组织生长位点、隔开软组织与硬组织的生长等屏障功能。
然而,作为一种外源性移植物,胶原仍然会引起一定的炎症反应,也因为它的易降解性而缺乏较好的机械性能。科学家们采用交联剂与胶原进行交联,从而提高它的机械性能。常用的交联剂是戊二醛,但它容易引发炎症和产生一定的细胞毒性。因此,胶原膜长期的保存和使用,不仅仅需要提高机械性能,更要抗炎和提高生物相容性。
表没食子儿茶素没食子酸酯(EGCG)是一种来自绿茶的多酚,它拥有众多生物学功能,近年来广受关注。科学家们发现,EGCG拥有抗癌、抗氧化、抗炎症、抗纤维化和促进成骨的作用。同时,它也可以作为一种胶原的交联剂,既可以增强胶原的机械性能,也不会破坏胶原的三股螺旋结构。因此,EGCG-胶原复合膜可以用于引导骨再生等手术中,并拥有良好的前景。
EGCG与胶原膜交联后,随着EGCG浓度的增加,胶原膜的机械性随之增加。然而,EGCG作为一种药物,较大浓度的EGCG仍然拥有一定的细胞毒性。Li等人的研究表明不同浓度的EGCG会有不同的作用,不同浓度的EGCG可以有抗癌作用也可能有促癌作用。因此,对EGCG的细胞毒性仍然需要进一步的解决。
因此,现有的胶原膜的机械性能、抗炎性和生物相容性都有待提高。
技术实现要素:
本发明针对现有技术的不足,提供一种胶原膜的改性方法,
其中,所述改性胶原膜是通过加载一种聚合物在用药物-胶原复合膜上得到的。
其中,所述改性胶原膜所述加载的聚合物为聚乙二醇(PEG)。
其中,所述改性胶原膜所用药物为:表没食子儿茶素没食子酸酯(EGCG)。
本发明还提供了聚合物改性的药物-胶原复合膜的制备方法:先用药物交联胶原膜,再加载聚合物,以得到聚合物改性的药物-胶原复合膜。
其中,所述制备方法中改性胶原膜所述加载的聚合物为:聚乙二醇(PEG)。
其中,所述制备方法中改性胶原膜所用药物为:表没食子儿茶素没食子酸酯(EGCG)。
1、一种胶原膜的改性方法,其特征在于,包括以下步骤:
A.以培养板为模板,加入胶原蛋白2mL,在-26℃低温冰箱冷冻过夜;
B.在-53℃、1 Pa条件下,将步骤A所得样品在冻干机真空冷冻干燥24 h,制备胶原膜;
C.将表没食子儿茶素没食子酸酯按照0.64%,0.064%,0.0064%梯度浓度进行溶液配制;
D. 将步骤B中制备的胶原膜置于0.64%EGCG中预交联10 min后,浸泡于含0.64%EGCG的0.05 mol/L醋酸溶液,于4℃交联24 h,lXPBS缓冲液漂洗3次。同样的方法制备加载0.064%EGCG,0.0064%EGCG的的胶原复合膜;
E. 将制备好的EGCG-胶原复合膜浸泡在1%的PEG20000中,于25℃浸泡过夜,再用PBS缓冲液冲洗三次,于-20℃条件下冷冻干燥过夜。
其中,所述步骤A中培养板的直径为3.5cm/孔,所述步骤E还包括胶原复合膜的生物相容性试验。
本发明的有益效果在于:创造性提供了一种拥有更好机械性能、抗炎性和生物相容性的胶原复合膜,提高了以前胶原膜的机械性能,克服了容易引发炎症等长期困扰本领域的技术问题,降低了药物-胶原复合膜的生物毒性,具有很好的应用前景,为引导骨再生术等相关骨增量手术提供了新选择。
附图说明
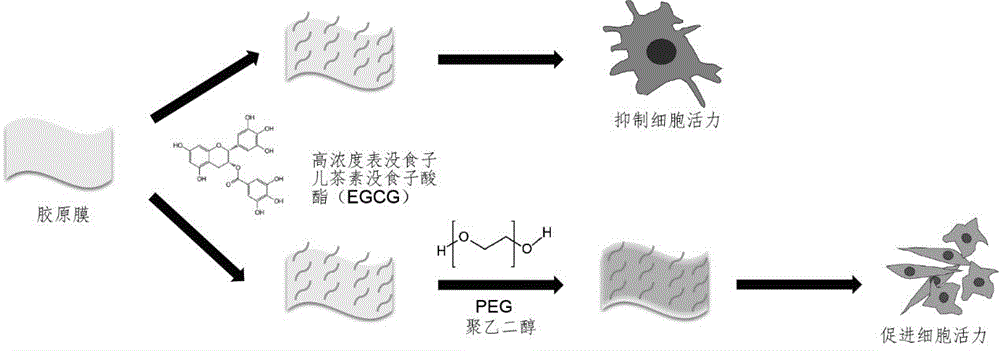
图1为本发明改性胶原膜的制备示意图。
图2为PEG改性EGCG-胶原复合膜材料表面结构图。
图3为MG63细胞在PEG改性EGCG-胶原复合膜上的形态特征图。
图4为MG63细胞在PEG改性EGCG-胶原复合膜上的活细胞数量特征图。
图5为MG63细胞在PEG改性EGCG-胶原复合膜上的CCK-8细胞活性特征图。
具体实施方式
实施例1:一种胶原膜的改性方法,包括以下步骤:
一、PEG改性的EGCG-胶原复合膜的制备
其中PEG改性的EGCG-胶原复合膜的制备示意图如图1所示。
制备流程一:胶原膜与EGCG复合,制得EGCG-胶原复合膜,该复合膜抑制细胞活力。
制备流程一:胶原膜与EGCG复合,制得EGCG-胶原复合膜,再与PEG改性,该复合膜促进细胞活力。
1、胶原膜的制备
以直径为3.5cm/孔的培养板为模具,加入胶原蛋白2 mL。-26℃低温冰箱冷冻过夜,在一53℃、1 Pa条件下,冻干机真空冷冻干燥24 h,制备胶原膜。
2、EGCG(0.64%,0.064%,0.0064%)梯度浓度溶液配制。
3、EGCG交联胶原膜
将制备的胶原膜置于0.64%EGCG中预交联10 min后,浸泡于含0.64%EGCG的0.05 mol/L醋酸溶液,于4℃交联24 h,l X PBS缓冲液漂洗3次。同样的方法制备加载0.064%EGCG,0.0064%EGCG的的胶原复合膜。
4、PEG化
将制备好的EGCG-胶原复合膜浸泡在1%的PEG20000中,于25℃浸泡过夜,再用PBS缓冲液冲洗三次,于-20℃条件下冷冻干燥过夜。
二、PEG改性的EGCG-胶原复合膜的生物相容性试验
1、细胞培养
MG63细胞株常规养于高糖DMEM培养基中(内含10%胎牛血清,100kU/L青霉素,100kU/L链霉菌)在5%CO2、37℃条件下培养,当融合度达到80%时进行处理。
2、加载EGCG、PEG的胶原膜对成骨细胞处理及观测
分多组进行:每个培养板作一组,编号A1—A15组。将各组细胞置于事先制备好的PEG改性的EGCG-胶原复合膜上进行培养,做空白组,每个培养板继续在前述环境下培养,换液时同时重新配置培养液梯度。
3、MG63细胞形态的免疫荧光染色。
用含2%多聚甲醛的PBS固定第3天的细胞,固定5分钟(pH 7.4),将样品在PBS中洗涤3次(每次5分钟),用含有1%牛血清白蛋白和0.1%Triton X-100的PBS预处理1小时,然后在1%Tween20中保温20分钟。之后用PBS洗涤5分钟后,培养在用PBS1:100稀释的Rhodamine-phalloidin (Life technologies, Thermo, USA)中15分钟。然后用PBS冲洗3次,每次5分钟。添加300nM的DAPI染色溶液(Life technologies, Thermo, USA),覆盖细胞和培养基1-5分钟,避光。然后,用PBS冲洗细胞2-3次以去除染色液,采取图像(图2)。结果显示,PEG改性后的EGCG-胶原复合膜, 明显促进了细胞的铺展, 细胞有更好的型态。
4、CCK-8法(测量细胞增殖活性)
在96孔板中, 注入成骨细胞达到7000个/孔. 贴壁后,换成含2%胎牛血清的高糖DMEM配制的各种浓度的EGCG溶液,每孔200μl。继续培养24、48h,每孔换成新鲜培养液100μl,再加入10μl CCK-8溶液,细胞培养箱中孵育1h后在酶标仪上450nm波长处读取各孔吸亮度(A)值,计算细胞增殖率,公式为=(处理组A值-空白A值)/(对照组A值-空白A值)*100%。结果见图3。结果发现PEG改性后的EGCG-胶原复合膜上的细胞活性显著高于E-Col组。
5、活死细胞染色(CCK-8)
将实验孔样品经PBS液漂洗15s后,转移至盖玻片上,用含10μg/ml Calcein-AM的PBS液孵育30min,在共聚焦显微镜下检测成像。Calcein-AM显示绿色标示活细胞。计数活细胞数量(N活)。结果发现PEG改性后的EGCG-胶原复合膜上的活细胞数量显著高于E-Col组。
- 还没有人留言评论。精彩留言会获得点赞!