一种以氢氧化铁胶体为乳液法水相制备聚合物微球的方法与流程
本发明涉及聚合物微球的制备方法,特别涉及一种以氢氧化铁胶体为乳液法水相制备聚合物微球的方法。
背景技术:
在生物医学材料领域中,生物可降解聚合物微球具有药物靶向运输、药物缓释以及模拟细胞外基质以刺激细胞响应的功能。乳液法是最常用于制备聚合物微球的方法,传统乳液法制备生物医用微球,总是需要在外水相中加入一定量的表面活性剂以稳定油相乳液滴,如聚乙烯醇(Biomaterials, 2002, 23, 1649-1656)、甲基纤维素(Journal of Biomedical Materials Research, 1992, 26, 467-479)等。但是有研究表明残留在微球上的表面活性剂会对人体产生不利的影响,比如会产生免疫反应或者致癌(Advanced Drug Delivery Reviews, 2008, 60, 939-954)。有研究表明,采用Pickering乳液法制备的生物医用聚合物微球可避免有毒表面活性剂所带来的不利影响。
Pickering乳液法,即采用固体颗粒代替表面活性剂作为乳液的稳定剂(Progress in Chemistry, 2009, 21, 1418-1426)。目前常用于Pickering乳液中的固体颗粒稳定剂主要是纳米级或者微米级颗粒,常用在生物医学材料领域的Pickering乳液固体稳定剂有羟基磷灰石(Acta Biomaterialia, 2011, 7, 821-828)、SiO2(Colloids and Surfaces B: Biointerfaces, 2012, 91, 97-105)、CaCO3(International Journal of Pharmaceutics, 2008, 351, 104-112)等。采用该方法制备的聚合物微球,微球表面会掺有部分固体颗粒稳定剂。
Fe元素是人体所必需的微量元素之一,是骨骼和牙齿中重要的微量元素,对骨组织具有一定的调节作用(Physical Review B, 2002, 66, 648-679)。研究表明掺杂Fe元素的骨水泥具有良好的生物相容性和骨诱导能力(Acta Biomaterialia, 2010, 6, 607-616)。采用氢氧化铁胶体作为Pickering乳液法的水相时,其中的Fe(OH)3胶体纳米粒子作为Pickering乳液法的固体稳定剂,制备出聚合物微球。同时,Fe(OH)3胶体纳米粒子可掺在聚合物微球表面,从而使微球表面含有微量的Fe元素,与传统乳液法所制备的聚合物微球表面成分有所差异。
技术实现要素:
本发明的目的在于提供一种以氢氧化铁胶体为乳液法水相制备聚合物微球的方法。该方法可使聚合物微球表面掺入少量的铁元素成分,同时这种方法制备得到的微球具有良好的细胞相容性,可以促使小鼠骨髓间充质干细胞的黏附和增殖。
本发明的目的通过以下技术方案实现。
一种以氢氧化铁为乳液法水相制备聚合物微球的方法,包括如下步骤:
(1)将聚合物材料添加到有机溶剂中,搅拌,得到聚合物油相溶液;
(2)将FeCl3溶液加入到沸腾的去离子水中,持续加热,水解反应制备得到氢氧化铁胶体溶液;
(3)将聚合物油相溶液分散到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌水包油的单乳液,挥发除去聚合物油相溶液中的有机溶剂,得到固化的聚合物微球,去离子水洗涤,干燥,得到所述聚合物微球。
进一步地,步骤(1)中,所述聚合物材料包括聚乳酸-羟基乙酸共聚物(PLGA)、聚左旋乳酸(PLLA)或聚己内酯(PCL)。
进一步地,步骤(1)中,所述有机溶剂包括二氯甲烷。
更进一步地,步骤(1)中,所述聚乳酸-羟基乙酸共聚物的分子量Mw=30~100 kDa;所述聚乳酸-羟基乙酸共聚物中,乳酸单体的比例为50%~90%。
更进一步地,步骤(1)中,所述聚左旋乳酸的分子量Mw=30~100 kDa。
更进一步地,步骤(1)中,所述聚己内酯的分子量Mw=50~150 kDa。
更进一步地,步骤(1)中,所述聚乳酸-羟基乙酸共聚物与二氯甲烷的质量体积比为1:5~20g/ml。
更进一步地,步骤(1)中,所述聚左旋乳酸与二氯甲烷的质量体积比为1:5~25g/ml,优选为1:10~25g/ml。
更进一步地,步骤(1)中,所述聚己内酯与二氯甲烷的质量体积比为1:5~25g/ml,优选为1:10~25g/ml。
进一步地,步骤(2)中,所述FeCl3溶液中,FeCl3的质量分数是1%~10%。
进一步地,步骤(2)中,所述FeCl3溶液与沸腾的去离子水的体积比为1:3~50。
进一步地,步骤(2)中,所述持续加热的时间为0.5~3 min。
进一步地,步骤(2)中,持续加热的温度保持在80℃以上。
进一步地,步骤(3)中,所述聚合物油相溶液与氢氧化铁胶体溶液的体积比为1:4~100。
进一步地,步骤(4)中,所述持续搅拌的转速为200~500 rpm,时间为2~24 h。
本发明采用Pickering乳液法原理,将氢氧化铁胶体粒子作为Pickering乳液法的固体乳化剂,与聚合物的二氯甲烷溶液在搅拌下形成水包油乳液;在水包油乳液中,氢氧化铁胶体粒子存在水相与油相液滴的界面上,不断搅拌使二氯甲烷挥发以使聚合物微球固化,氢氧化铁胶体粒子在微球固化过程中会留在微球表面,于是形成了表面含铁元素成分的聚合物微球。
与现有技术相比,本发明具有以下优点和有益效果:
(1)本发明方法制备的聚合物微球表面含有铁元素成分,且具有良好的细胞相容性;相对传统的聚乙烯醇(PVA)乳液法制备的微球,含有铁元素成分的聚合物微球对小鼠骨髓间充质干细胞具有促进增殖作用。
附图说明
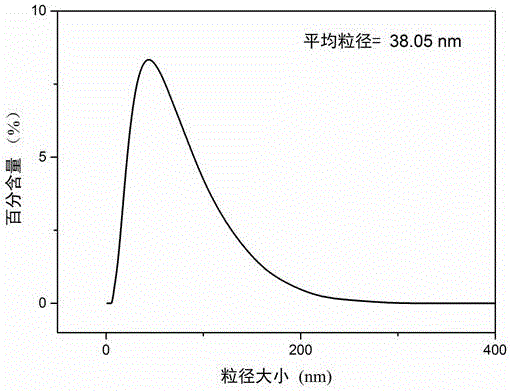
图1为实施例1制备的水相中Fe(OH)3胶体纳米粒子的粒径分布图;
图2为实施例1制备的Fe(OH)3-PLGA微球的整体形貌图;
图3为实施例1制备的Fe(OH)3-PLGA微球的表面XPS测试结果图;
图4为实施例1制备的Fe(OH)3-PLGA微球与小鼠骨髓间充质干细胞共培养5天后的活死细胞染色图;
图5为实施例2制备的PVA-PLGA微球的整体形貌图;
图6为实施例1、2制备Fe(OH)3-PLGA微球和PVA-PLGA微球的细胞增殖情况柱状图;
图7为实施例3中制备的Fe(OH)3-PLLA微球的整体形貌图;
图8为实施例4中制备的Fe(OH)3-PCL微球的整体形貌图。
具体实施方式
下面结合实施例,对本发明作进一步地详细说明,但本发明的实施方式不限于此。
实施例1
(1)称取0.5 g PLGA(LA/GA =85/15, Mw=100 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PLGA的油相溶液;
(2)取60 ml质量分数为3%的FeCl3溶液加入到240 ml 沸腾的去离子水中,持续加热2 min,制成氢氧化铁胶体溶液,作为乳液的水相;
图1为水相中Fe(OH)3胶体纳米粒子的粒径分布图,由图1可知,大部分Fe(OH)3胶体纳米粒子粒径分布于0~200nm之间,平均粒径为38.05nm;
(3)在转速为300 rpm搅拌条件下,将PLGA的油相溶液逐滴加入到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液5 h,挥发除去有机溶剂,得到表面含铁元素成分的PLGA微球;收集固化的PLGA微球,用去离子水洗涤3遍后,冷冻干燥,标记为Fe(OH)3-PLGA微球。
图2为制备的Fe(OH)3-PLGA微球的整体形貌图,由图2可知,制备得到的Fe(OH)3-PLGA微球表面光滑。
图3为制备的Fe(OH)3-PLGA微球的表面XPS测试结果图,测试结果显示,在结合能为708.5eV处有属于Fe元素2p轨道电子的峰出现,表明在微球表面含有铁元素。
图4为制备的Fe(OH)3-PLGA微球与小鼠骨髓间充质干细胞共培养5天后的活死细胞染色图,由图4可知,在第5天的时候,微球表面黏附了大量的细胞,并且没有发现死细胞,说明该微球具有良好的细胞相容性,对小鼠骨髓间充质干细胞不具有毒害作用。
实施例2
(1)称取0.5 g PLGA(LA/GA =85/15, Mw=100 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PLGA油相溶液;
(2)称取1.50 g PVA加入到250 ml 90℃的去离子水中,持续加热60min,使PVA充分溶解,冷却后得到PVA的水相溶液;
(3)在转速为300 rpm搅拌条件下,将PLGA的油相溶液逐滴加入到PVA水相溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液5 h,挥发除去有机溶剂,得到表面不含铁元素的PLGA微球;收集固化的PLGA微球,用去离子水洗涤3遍后,冷冻干燥,标记为PVA-PLGA微球。
图5为制备的PVA-PLGA微球整体形貌图,由图5可知,传统的PVA乳液法制备得到的PVA-PLGA微球的表面光滑。
图6为实施例1、2制备Fe(OH)3-PLGA微球和PVA-PLGA微球的细胞增殖情况图,由图6可知,两种方法制备的PLGA微球上,细胞均能呈现良好的增殖情况,且在相同时间点上,Fe(OH)3-PLGA微球的增殖情况比PVA-PLGA微球更好,具有显著性差异。
实施例3
(1)称取0.5 g PLLA(Mw=50 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PLLA的油相溶液;
(2)取60 ml质量分数为3%的FeCl3溶液加入到240 ml 沸腾的去离子水中,持续加热2 min,制成氢氧化铁胶体溶液,作为乳液的水相;
(3)在转速为300 rpm搅拌条件下,将PLLA的油相溶液逐滴加入到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液5 h,挥发除去有机溶剂,得到表面含铁元素的PLLA微球;收集固化的PLLA微球,用去离子水洗涤3遍后,冷冻干燥,标记为Fe(OH)3-PLLA微球。
图7为制备的Fe(OH)3-PLLA微球的整体形貌图,图7显示成功制备微Fe(OH)3-PLLA微球。
制得的Fe(OH)3-PLLA微球表面含有铁元素成分,且具有良好的细胞相容性,对小鼠骨髓间充质干细胞不具有毒害作用。
实施例4
(1)称取0.5 g PCL(Mw=80 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PCL的油相溶液;
(2)取60 ml质量分数为3%的FeCl3溶液加入到240 ml 沸腾的去离子水中,持续加热2 min,制成氢氧化铁胶体溶液,作为乳液的水相;
(3)在转速为300 rpm搅拌条件下,将PCL的油相溶液逐滴加入到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液5 h,挥发除去有机溶剂,得到表面含铁元素的PCL微球;收集固化的PCL微球,用去离子水洗涤3遍后,冷冻干燥,标记为Fe(OH)3-PCL微球。
图8为制备的Fe(OH)3-PCL微球的整体形貌图,图8显示成功制备出Fe(OH)3-PCL微球。
制得的Fe(OH)3-PCL微球表面含有铁元素成分,且具有良好的细胞相容性,对小鼠骨髓间充质干细胞不具有毒害作用。
实施例5
(1)称取0.25g PLGA(LA/GA =90/10, Mw=30 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PLGA的油相溶液;
(2)取5 ml质量分数为10%的FeCl3溶液加入到15 ml 沸腾的去离子水中,持续加热0.5 min,制成氢氧化铁胶体溶液,作为乳液的水相;
(3)在转速为300 rpm搅拌条件下,将PLGA的油相溶液逐滴加入到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液24 h,挥发除去有机溶剂,得到表面含铁元素成分的PLGA微球;收集固化的PLGA微球,用去离子水洗涤3遍后,冷冻干燥,标记为Fe(OH)3-PLGA微球。
制得的Fe(OH)3-PLGA微球表面含有铁元素成分,且具有良好的细胞相容性,对小鼠骨髓间充质干细胞不具有毒害作用。
实施例6
(1)称取1g PLGA(LA/GA =50/50, Mw=70 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PLGA的油相溶液;
(2)取5 ml质量分数为10%的FeCl3溶液加入到250 ml 沸腾的去离子水中,持续加热0.5 min,制成氢氧化铁胶体溶液,作为乳液的水相;
(3)在转速为500 rpm搅拌条件下,将PLGA的油相溶液逐滴加入到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液2 h,挥发除去有机溶剂,得到表面含铁元素成分的PLGA微球;收集固化的PLGA微球,用去离子水洗涤3遍后,冷冻干燥,标记为Fe(OH)3-PLGA微球。
制得的Fe(OH)3-PLGA微球表面含有铁元素成分,且具有良好的细胞相容性,对小鼠骨髓间充质干细胞不具有毒害作用。
实施例7
(1)称取1g PLLA(Mw=30 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PLLA的油相溶液;
(2)取100 ml质量分数为1%的FeCl3溶液加入到400 ml 沸腾的去离子水中,持续加热3 min,制成氢氧化铁胶体溶液,作为乳液的水相;
(3)在转速为500 rpm搅拌条件下,将PLLA的油相溶液逐滴加入到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液5 h,挥发除去有机溶剂,得到表面含铁元素的PLLA微球;收集固化的PLLA微球,用去离子水洗涤3遍后,冷冻干燥,标记为Fe(OH)3-PLLA微球。
制得的Fe(OH)3-PLLA微球表面含有铁元素成分,且具有良好的细胞相容性,对小鼠骨髓间充质干细胞不具有毒害作用。
实施例8
(1)称取0.2 g PLLA(Mw=100 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PLLA的油相溶液;
(2)取60 ml质量分数为3%的FeCl3溶液加入到240 ml 沸腾的去离子水中,持续加热2 min,制成氢氧化铁胶体溶液,作为乳液的水相;
(3)在转速为200 rpm搅拌条件下,将PLLA的油相溶液逐滴加入到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液5 h,挥发除去有机溶剂,得到表面含铁元素的PLLA微球;收集固化的PLLA微球,用去离子水洗涤3遍后,冷冻干燥,标记为Fe(OH)3-PLLA微球。
制得的Fe(OH)3-PLLA微球表面含有铁元素成分,且具有良好的细胞相容性,对小鼠骨髓间充质干细胞不具有毒害作用。
实施例9
(1)称取1 g PCL(Mw=50 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PCL的油相溶液;
(2)取60 ml质量分数为3%的FeCl3溶液加入到240 ml 沸腾的去离子水中,持续加热2 min,制成氢氧化铁胶体溶液,作为乳液的水相;
(3)在转速为300 rpm搅拌条件下,将PCL的油相溶液逐滴加入到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液5 h,挥发除去有机溶剂,得到表面含铁元素的PCL微球;收集固化的PCL微球,用去离子水洗涤3遍后,冷冻干燥,标记为Fe(OH)3-PCL微球。
制得的Fe(OH)3-PCL微球表面含有铁元素成分,且具有良好的细胞相容性,对小鼠骨髓间充质干细胞不具有毒害作用。
实施例10
(1)称取0.2 g PCL(Mw=150 kDa)加入到5 ml 二氯甲烷中,在300 rpm转速搅拌30 min,得到PCL的油相溶液;
(2)取60 ml质量分数为3%的FeCl3溶液加入到240 ml 沸腾的去离子水中,持续加热2 min,制成氢氧化铁胶体溶液,作为乳液的水相;
(3)在转速为300 rpm搅拌条件下,将PCL的油相溶液逐滴加入到氢氧化铁胶体溶液中,得到水包油的单乳液;
(4)持续搅拌单乳液5 h,挥发除去有机溶剂,得到表面含铁元素的PCL微球;收集固化的PCL微球,用去离子水洗涤3遍后,冷冻干燥,标记为Fe(OH)3-PCL微球。
制得的Fe(OH)3-PCL微球表面含有铁元素成分,且具有良好的细胞相容性,对小鼠骨髓间充质干细胞不具有毒害作用。
- 还没有人留言评论。精彩留言会获得点赞!