用于多模态成像研究的结直肠癌肝转移动物模型构建方法与流程
本发明肝转移瘤构建领域,尤其涉及一种用于多模态成像研究的结直肠癌肝转移动物模型构建方法。
背景技术:
目前,用于结直肠癌肝转移的动物模型主要有种植性结肠癌肝转移模型,转基因动物肿瘤模型和诱发性肿瘤模型,种植性结肠癌肝转移动物模型又分为原位种植性和异位种植性结肠癌肝转移模型,异位种植性模型又分为门静脉异位种植法、肝脏异位种植法、尾静脉异位种植法。
原位种植性模型是指将肿瘤细胞悬浮液或肿瘤组织块接种到盲肠或者结肠部位,该方法的优点是能够模拟结直肠癌在人体内的扩散过程,更接近结直肠癌肝转移的发生及发展过程。而局限性在于“原发性”肿瘤生长和转移需要的时间过长,原位注射手术难度较大,肝转移发生率相对较低,接种部位肿瘤组织生长过大,肠梗阻致死率高,因此限制了这种模型的应用。
门静脉注射法是通过直接把肿瘤细胞悬液直接注射到门静脉形成结直肠癌肝转移模型,实验动物发生肝转移的比例更高。门静脉异位接种模型的优势在于(1)经门静脉接种肿瘤细胞株的动物模型可以模拟肿瘤通过血管扩散的过程,该模型更准确地模拟了肿瘤的自发转移过程,并能在理论上限制腹腔内其他部位的肿瘤生长速度;(2)可重复性高,几乎在所有动物实验中都能产生肝转移,且与原位移植模型比较,可以在更短的时间内发生肝转移。该模型缺点是:(1)未能模拟肿瘤转移的全过程,减少了原发瘤最初侵袭周围组织和穿入血管等步骤;(2)实验动物生存时间相对较短;(3)不能注入过多的肿瘤细胞,否则容易出现肝血管栓塞而导致裸鼠死亡。
结肠癌肝脏异位种植模型是将结直肠癌细胞或组织块直接种植于肝脏而形成转移瘤。该方法成瘤率高且具有可重复性,并且并发症概率在可接受的范围内,但是大部分裸鼠仅在注射部位成瘤,而周围很少有转移的卫星结节,不符合临床肝转移瘤多发转移的特征,不能够准确反映人体内的真实情况,因此对于治疗性干预会出现不同的反应。
尾静脉注射法直接取一定体积的结直肠癌细胞悬浮液经裸鼠尾静脉注入,一段时间后,观察成瘤情况和肝转移情况。研究表明,尾静脉注射结直肠癌细胞悬液不能产生肝转移,一般不采用这种方法造模。
转基因动物肿瘤模型是应用分子生物学手段,对实验动物基因进行改造或修饰,从而培育出相应肿瘤的动物模型。在转基因动物肿瘤模型中,肿瘤的发生、发展在理论上与原发肿瘤是一致的,且可对任何动物进行建模,但由于目前对癌基因及抑癌基因本身的研究还有待深入,建立的模型还不够理想,短期内很难普及,目前只能作为一种发展方向。
诱发性肿瘤模型是人为地运用各种致癌因素作用于实验动物的特定组织或器官,从而产生相应肿瘤的动物模型。目前,常用的结肠癌化学诱导剂有二甲肼(DMH)、乙基-亚硝基尿素(ENU)、氧化偶氮甲烷(AOM)、肼的衍生物、芳香族胺等,均可通过喂食、注射、肛门放置栓剂等途径给药,化学诱导的肿瘤属实验动物的原发肿瘤,其发病机制及肿瘤生长环境接近于人体原发肿瘤,建立方法相对简单,实验重复性好。但该方法诱导周期较长,肝转移成瘤率与移植法相比也有一定差距。
技术实现要素:
本发明的目的就在于为了解决上述问题而提供一种用于多模态成像研究的结直肠癌肝转移动物模型构建方法。
本发明通过以下技术方案来实现上述目的:
本发明包括以下步骤:
(1)选取BALB/C-nu-nu雌性裸鼠50只,每只原始体重在(17±3)g,将其分成实验组和对照组,实验组为40只BALB/C-nu-nu雌性裸鼠,对照组为10只BALB/C-nu-nu雌性裸鼠。
(2)模型制作之前一周为稳定期,禁止对裸鼠进行一切刺激性的操作,实验组实验前裸鼠禁食进水12小时,细胞室制作细胞悬液,浓度为2.5×107/ml。裸鼠用10%的水合氯醛腹腔注射麻醉,麻醉剂剂量0.004ml/g,麻醉后仰卧位固定于手术板上,左上腹纵形切口,进腹后游离脾脏并拉至切口外,用5号针从脾脏下极进针穿刺脾脏,从脾脏下极穿刺脾脏后针头向脾脏上极方向推进,进针长度约1cm,缓慢注入结肠癌细胞0.1ml不等,可见脾包膜鼓起变白,注射时间约3min,注射结束后待脾脏颜色转红,快速拔出针头后用75%的酒精按压止血,并用生理盐水冲洗,确保无明显出血及癌细胞溢出,尽量避免腹腔内的种植转移,最后把脾脏放回腹腔内,缝合伤口;
(3)对照组脾脏内注射无菌PBS,余操作同实验组。
(4)模型制作完毕后,继续在SPF环境中饲养,并定期测量裸鼠的体重及观察裸鼠的精神状况,饲养七周后,实验组中的裸鼠即成为结直肠癌肝转移动物模型。
本发明的有益效果在于:
本发明是一种用于多模态成像研究的结直肠癌肝转移动物模型构建方法,与现有技术相比,本发明具有以下优点:
1、本发明为肝转移瘤动物模型的构建提供了一种与现有技术不同构思的新方法。
2、实验表明(见实施例2、实施例3),所构建的裸鼠结直肠癌肝转移动物模型经脾种植经门静脉转移到肝脏,组织病理学与人结直肠癌肝转移瘤相似,为肝转移结节:具有典型肝转移瘤临床特征,如:黄疸、乏力、纳差等症状。
3、由于本发明所述方法构建的裸鼠结直肠癌肝转移动物模型很好的模拟了人肝转移瘤的发生、发展过程,因而可以用于研究人的肝转移瘤的发病机制。
4、将本发明所述方法构建的结直肠癌肝转移动物模型采用CT、磁共振、超声和PET成像等多种模态成像,可观察肝转移瘤的发生、发展过程,肝转移瘤不同发展阶段的多种模态成像成像特点:评估药物及其他治疗措施对脾原发灶及其转移灶的预防作用和疗效。
5、由于所用的人结直肠癌细胞(HT29)其浓度为2.5×107/ml,所用剂量为0.1ml,只需一次性将细胞悬液注入脾脏既可以得到肝转移模型,因而本发明所述方法操作简单,造模成功率高,具有一定的经济和实用价值,值得推广。
附图说明
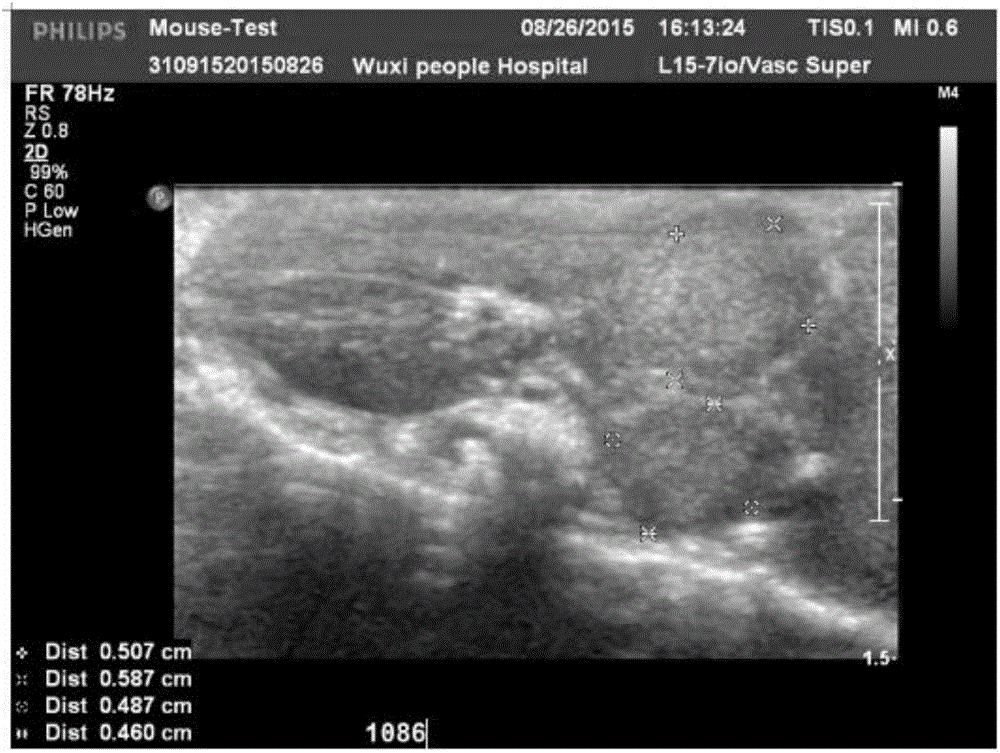
图1本发明所述方法的裸鼠结直肠癌肝转移动物模型的超声图像,图1A、图1B是肝脏超声扫查,肝内见强回声结节及肿块,大小不等,边界清楚,部分周边可见声晕;
图2本发明所述方法的裸鼠结直肠癌肝转移动物模型的CT图像,肝内血管和肝实质均明显强化,而肝内癌结节无强化,在此时间内扫描,可以将肝转移结节与肝内血管影进行鉴别。早期肝转移结节和脾原位结节的增强Micro-CT图像(红箭头所示肿瘤结节);
图3本发明所述方法的裸鼠结直肠癌肝转移动物模型的MRI图像,图3A是T2WI序列横断面,图3B是T2WI序列冠状位。肝脏可见多发异常信号,病灶边界尚清晰,T2WI序列呈略高信号,其内信号略不均匀;脾脏内亦可见高信号原位肿瘤;
图4本发明所述方法的裸鼠结直肠癌肝转移动物模型的PET图像,图4A是裸鼠18F-FDG PET图像可见肝脏多发高摄取区域,图4B18F-FB-NGA PET图像可见肝脏内充盈缺损;
图5是本发明所述方法构建的裸鼠结直肠癌肝转移动物模型经腹部纵行正中切口剖腹后,腹腔内的情况,肝脏内可见多个占位,脾脏内亦可见原位肿瘤;
图6是将本发明所述方法构建的裸鼠结直肠癌肝转移动物模型的肝转移瘤完整取下,经质量分数为10%的福尔马林固定,石蜡包埋,切片,HE染色(10×10)和大体病理图像。
具体实施方式
下面结合附图对本发明作进一步说明:
实验动物与材料
实验动物:BALB/C-nu-nu裸鼠,雌性,5周龄,饲养环境:SPF级动物实验室。
肿瘤细胞:HT-29细胞株。
实验所用的PBS及胰蛋白酶消化液均自行配置且经无菌处理。
本发明包括以下步骤:
(1)选取BALB/C-nu-nu雌性裸鼠50只,每只原始体重在(17±3)g,将其分成实验组和对照组,实验组为40只BALB/C-nu-nu雌性裸鼠,对照组为10只BALB/C-nu-nu雌性裸鼠。
(2)模型制作之前一周为稳定期,禁止对裸鼠进行一切刺激性的操作,实验组实验前裸鼠禁食进水12小时,细胞室制作细胞悬液,浓度为2.5×107/ml。裸鼠用10%的水合氯醛腹腔注射麻醉,麻醉剂剂量0.004ml/g,麻醉后仰卧位固定于手术板上,左上腹纵形切口,进腹后游离脾脏并拉至切口外,用5号针从脾脏下极进针穿刺脾脏,从脾脏下极穿刺脾脏后针头向脾脏上极方向推进,进针长度约1cm,缓慢注入结肠癌细胞0.1ml不等,可见脾包膜鼓起变白,注射时间约3min,注射结束后待脾脏颜色转红,快速拔出针头后用75%的酒精按压止血,并用生理盐水冲洗,确保无明显出血及癌细胞溢出,尽量避免腹腔内的种植转移,最后把脾脏放回腹腔内,缝合伤口;
(3)对照组脾脏内注射无菌PBS,余操作同实验组。
(4)模型制作完毕后,继续在SPF环境中饲养,并定期测量裸鼠的体重及观察裸鼠的精神状况,饲养七周后,实验组中的裸鼠即成为结直肠癌肝转移动物模型。
实施例1
实验动物与材料、设备
实验动物:实施例1构建的结直肠癌肝转移的动物模型。
无水乙醚:天津市富宇精细化工有限公司。
超声设备:型号:PHILIPS HD15,荷兰philips公司生产。
实验方法
对本发明构建的结直肠癌肝转移裸鼠模型进行肝脏超声扫查,操作如下:
(1)检查者带无菌手套,用无水乙醚对实验组裸鼠进行麻醉,麻醉好后用医用胶带将裸鼠固定于自制的检查板上。
用超声设备对裸鼠进行扫查,所用探头为L15-7io浅表探头,对肝脏异常回声记录,并测量大小后采集图像。
超声检查显示,肝内见强回声结节及肿块,大小不等,边界清楚,部分周边可见声晕。(见图1A-图1B)。
实施例2
实验动物与材料、设备
实验动物:实施例1构建的结直肠癌肝转移的动物模型。
异氟烷:上海雅培制药有限公司;氧气:无锡市蠡园医用氧气有限责任公司。小动物麻醉机:美国Stoelting Kopf/50262;Micro-CT:德国西门子公司。
实验方法
对本发明构建的结直肠癌肝转移裸鼠模型进行肝脏扫查,操作如下:
(1)显像前将裸鼠在小动物麻醉机上用混用3%(体积分数)异氟烷的氧气麻醉,显像过程中维持含1%(体积分数)异氟烷的氧气麻醉,俯卧位头先进的体位固定于扫描床上。
(2)采用的造影剂为Fenestra LC,造影剂用量为0.4ml/20g,每次扫描采取的增强方式:注入造影剂后1小时、3小时、4小时和24小时进行扫描。
(3)扫描结束后,将图像传至工作站,进行图像分析。
Micro CT显示注入造影后1小时—3小时,肝内血管和肝实质均明显强化,而肝内癌结节无强化,在此时间内扫描,可以将肝转移结节与肝内血管影进行鉴别。(见图2)
实施例3
实验动物与材料、设备
实验动物:实施例1构建的结直肠癌肝转移的动物模型。
异氟烷:上海雅培制药有限公司;氧气:无锡市蠡园医用氧气有限责任公司。
小动物麻醉机:美国Stoelting Kopf/50262;Micro-MRI:型号BRUKER 7.0T Biospec 70/20USR。
实验方法
对实施例1构建的结直肠癌肝转移裸鼠模型进行磁共振肝脏横断位及冠状位扫查,操作如下:
(1)显像前将裸鼠在小动物麻醉机上用混用3%(体积分数)异氟烷的氧气麻醉,显像过程中维持含1%(体积分数)异氟烷的氧气麻醉,俯卧位头先进的体位固定于扫描床上。
(2)用MR成像仪对裸鼠进行核磁共振扫描,扫描序列:T2WI横断面及冠状位。扫描结束后,将核磁共振扫描图像传至工作站进行测量。
核磁共振扫描显示,肝脏可见多发异常信号,病灶边界尚清晰,T2WI序列呈略高混杂信号。(见图3A、图3B)
实施例4
实验动物与材料、设备
实验动物:实施例1构建的结直肠癌肝转移的动物模型。
异氟烷:上海雅培制药有限公司;氧气:无锡市蠡园医用氧气有限责任公司。
小动物麻醉机:美国Stoelting Kopf/50262;Micro-PET:德国西门子/Inveon Dedicate。
实验方法
对实施例1构建的结直肠癌肝转移裸鼠模型进行PET显像,操作如下:
(1)显像前将裸鼠在小动物麻醉机上用混用3%(体积分数)异氟烷的氧气麻醉,显像过程中维持含1%(体积分数)异氟烷的氧气麻醉。
(2)麻醉好的裸鼠模型通过尾静脉注射100μci的同位素0.2ml,俯卧位头先进的体位固定于扫描床上,于注射药物的一小时后行扫描(18F-FDG),20分钟(18F-FB-NGA)。PET显像结果通过Siemens Invenon系统采集,显像时间为十分钟,所得数据用ASIPro VM软件分析处理扫描结束后,将PET扫描图像传至工作站进行测量。
核磁共振扫描显示,18F-FDG PET图像可见肝脏多发高摄取区域(见图4A),18F-FB-NGA PET图像可见肝脏内充盈缺损。(见图4B)
实施例5
实例4结束后,裸鼠脱臼法处死。术者带无菌手套,持手术剪,镊子,经模型鼠腹部正中切口剖腹,暴露出的肝脏见图5。
完整取下肝脏,质量分数为10%的福尔马林固定,石蜡包埋,切片,HE染色,镜下观察,如图6所示:癌组织形态不一,多呈椭圆形,胞浆丰富,核大、深染、畸形,核分裂象多见,呈弥漫性、浸润性生长,癌细胞间有结缔组织浸润。对照组模型按照实例2、实例3、实例4、实例5和实例6的方法进行操作,各种影像检查及解剖后组织观察均未见肿瘤形成。
以上显示和描述了本发明的基本原理和主要特征及本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!