壬二酸在制备抗急性髓系白血病和化疗增敏药物中的应用的制作方法
本发明属于抗肿瘤药物领域,具体涉及壬二酸在制备抗急性髓系白血病和化疗增敏药物中的应用。
背景技术:
急性髓系白血病(acute myeloid leukemia,AML)是血液系统最常见的恶性肿瘤,属于一类造血系统组织的克隆性恶性疾病。急性髓系白血病的诱导方案始终以蒽环类抗生素联合标准剂量阿糖胞苷(Arac)为基础,化疗后可出现骨髓抑制、胃肠道毒性、心脏毒性等毒副反应。此外,还存在化疗耐药,我们前期研究工作发现在AML复发患者总体抗氧化能力(T-AOC)降低,体内ROS水平显著增加,并且8-OHdG这一公认的氧化DNA损伤标志物也显著增加[1]。此外,随着ROS水平增加,促进NK、T细胞的凋亡,白血病细胞通过逃逸细胞介导的免疫从而大量增殖[2]。如何提高疗效,减轻化疗毒副作用,保证患者生活质量,提高生存率是需要解决的问题。
壬二酸(Azelaic Acid,AZA)是9碳直链饱和二元酸,别名杜鹃花酸,分子式C9H16O4和(CH2)5(CH2COOH)2。壬二酸是一种无毒无害的物质[3],AZA在临床上主要用于皮肤痤疮的治疗;已被证明AZA能抗人皮肤恶性黑色素瘤[4]、人脉络膜黑色素瘤[5],目前认为其抗癌作用的机理是清除氧自由基和抑制多种氧化还原酶,并且AZA是硫氧还蛋白Trx蛋白的抑制剂[6]。但其在急性髓系白血病中的作用尚未见报道。
参考文献
[1]Zhou,F.L.,W.G.Zhang,Y.C.Wei,et al.,Involvement of oxidative stress in the relapse of acute myeloid leukemia.J Biol Chem.2010;285(20):15010-5.10.1074/jbc.M110.103713.
[2]Zhou,F.L.,Q.Shen F.X.Claret,Novel roles of reactive oxygen species in the pathogenesis of acute myeloid leukemia.J Leukoc Biol.2013;94(3):423-9.10.1189/jlb.0113006.
[3]Breathnach AS:Azelaic acid:potential as a general antitumoural agent.Medical hypotheses 1999,52(3):221-226.
[4]Zaffaroni N,Villa R,Silvestro L,Sanfilippo O,Silvestrini R:Cytotoxic activity of azelaic acid against human melanoma primary cultures and established cell lines.Anticancer research 1990,10(6):1599-1602
[5]Breathnach AS,Robins EJ,Patzold HC,Bhasin YP,Ethridge LB,Garner A,Nazzaro-Porro M:Effect of dicarboxylic acids(C6 and C9)on human choroidal melanoma in cell culture.Investigative ophthalmology&visual science 1989,30(3):491-498.
[6]Y UT,Furuke K,Masutani H,Nakamura H,Yodoi J:Cell cycle inhibition of HTLV-I transformed T cell lines by retinoic acid:the possible therapeutic use of thioredoxin reductase inhibitors.Oncology research 1995,7(3-4):183-189.
技术实现要素:
本发明要解决的问题是提供壬二酸的新用途,即在制药中的新应用。
本发明的目的是提供壬二酸在制备抗急性髓系白血病和化疗增敏药物中的应用。
进一步地,本发明提供一种以壬二酸为活性成分的抗急性髓系白血病药物,需要的时候,还可以加入一种或多种药学上可接受的辅料,所述辅料包括药学领域常规的稀释剂、赋形剂、填充剂、粘合剂、湿润剂、吸收促进剂、表面活性剂、润滑剂、稳定剂等,必要时还可以加入香味剂、甜味剂及色素等。
所述的药物可以为本领域的常用药物剂型,例如片剂、胶囊剂、颗粒剂、口服液、缓释制剂、纳米制剂、注射剂等等。
进一步地,本发明提供一种抗肿瘤药物组合物,该组合物含有药学上有效量的壬二酸和药学上有效量的抗急性髓系白血病药物及药学上可接受的载体。
所述药学上有效量的抗急性髓系白血病药物是阿糖胞苷(Ara-c)。
本发明检测了壬二酸对多株AML细胞株(U937,THP-1,KG-1,NB4,and HL-60)的杀伤作用,发现AZA能呈剂量和时间依赖性抑制这些细胞的活力;其次,采用软琼脂糖克隆形成实验,发现AZA能抑制这些AML细胞的克隆增殖;利用Annexin-V/PI染色,通过流式细胞仪检测,发现AZA能诱导AML细胞的凋亡。由于阿糖胞苷(Ara-C)是治疗AML的经典化疗药物,本发明也探索了AZA对Ara-C的疗效的影响,通过Alamar Blue实验,发现AZA能够促进Ara-C杀伤AML细胞的疗效;通过Western Blot实验,发现AZA能够诱导凋亡标志物(C-PARP),同时也能抑制Jab1,p-Akt,Trx的蛋白量。通过Alamar Blue实验,我们发现抑制AML细胞株内的Jab1水平后,细胞对AZA更加敏感,提示AZA可能通过Jab1机制杀伤AML细胞。
本发明提出一种治疗急性髓系白血病(AML)的新药物——壬二酸,该药物无毒副作用,价格为大多数患者所接受,与化疗药物阿糖胞苷(Arac)联用,一方面能促进阿糖胞苷(Arac)对AML细胞的杀伤作用,另一方面,能减少Arac剂量,减轻化疗毒副作用。
附图说明
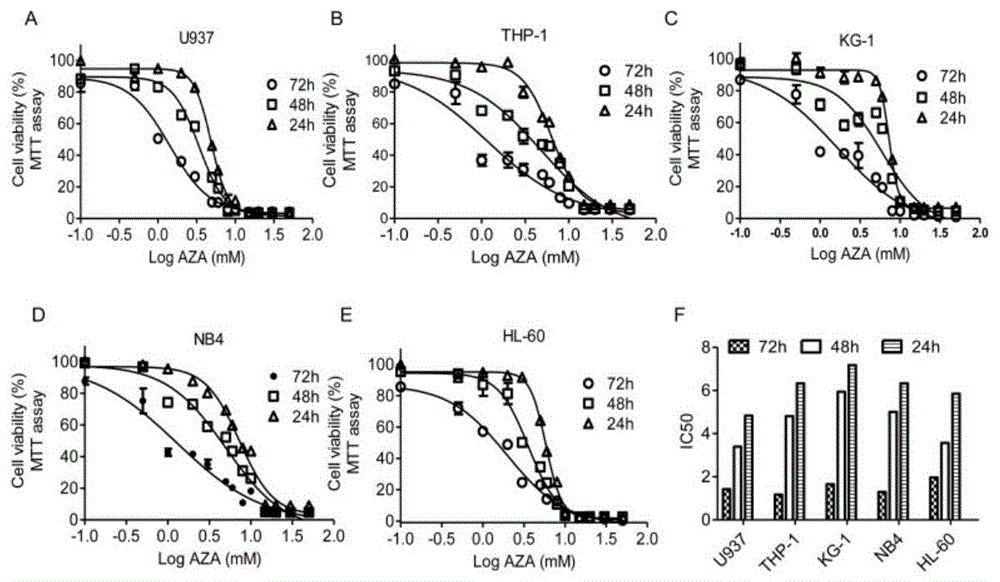
图1采用MTT的方法检测了壬二酸对多种AML细胞株(U937,THP-1,KG-1,NB4,and HL-60)的杀伤作用。
图2A软琼脂糖克隆形成实验观察AML细胞的克隆形成。
图2B利用Annexin-V/PI染色,流式细胞仪检测AZA对AML细胞凋亡的影响。
图3 AZA能够促进AraC对AML细胞的杀伤作用。
图4 AZA对C-PARP、Jab1,p-Akt,Trx蛋白表达量的影响。
图5抑制AML细胞株内的Jab1表达后影响AZA对AML细胞的杀伤作用。
具体实施方式
通过以下详细说明结合附图可以进一步理解本发明的特点和优点。所提供的实施例仅是对本发明方法的说明,而不以任何方式限制本发明揭示的其余内容。
一、细胞株:人急性髓系白血病M5细胞株(U937,THP-1,MOLM-13),M3细胞株(HL-60),M6细胞株(KG-1),以上细胞株均从ATCC(Manassas,VA)获得。
二、试剂:RPMI-1640培养液(Invitrogen,Carlsbad,CA),IMDM培养液(Invitrogen,Carlsbad,CA),10%胎牛血清(Invitrogen,Carlsbad,CA),L-谷氨酸(Invitrogen,Carlsbad,CA),PARP(BD Biosciences PharMingen,San Diego,CA,USA),Jab1抗体(Santa Cruz,CA,USA),p-Akt抗体(Santa Cruz,CA,USA),T-Akt抗体(Santa Cruz,CA,USA),β-actin抗体(Sigma-Aldrich,St.Louis,MO,USA),Annexin V/PI试剂盒(BD Biosciences PharMingen,San Diego,CA,USA),Alamar blue检测试剂(Invitrogen,Carlsbad,CA),ECL化学发光增强试剂(Bio-Rad,Hercules,CA),AZA(Sigma-Aldrich,Inc,St.Louis,MO),DMSO(Sigma-Aldrich,Inc,St.Louis,MO),MTT(Sigma-Aldrich,Inc,St.Louis,MO),Nucleofector Kit V(Amaxa Biosystems,Lonza,Allendale,NJ)
【实施例1】MMT法检测壬二酸对多种AML细胞株的杀伤作用
将U937、THP-1、MOLM-13、U937、THP-1、MOLM-13、KG-1细胞种植在96孔板上面,各100μL 6×104个/mL的细胞,分别加入0、1.25、2.5、5、10mM AZA各10μL,药物处理后24、48、72h后分别加入MTT,检测570nm处吸光度。
如图1所示,AZA能呈剂量和时间依赖性抑制这些细胞的活力。
【实施例2】软琼脂糖克隆形成实验
将AML细胞(U937、THP-1、MOLM-13、U937、THP-1、MOLM-13、KG-1)种植在六孔板上面,先将2ml包含0.7%琼脂的培养基倒入六孔板,待琼脂凝固,每孔加入1ml含有5000个细胞的0.35%琼脂的培养基,每次更换3ml指定AZA浓度的新鲜培养基,孵育14天后剩余细胞数>50的样本进行计数处理。
如图2A所示,AZA能抑制这些AML细胞的克隆增殖。
【实施例3】流式检测AZA对AML细胞细胞凋亡的影响
将1×105-1×107的细胞放入1.5ml EP管中3000r/min离心5min,弃上清,加入PBS 100μL悬浮细胞,加入Annexin-V/PI染色,4℃孵育45min,在AZA处理后24h,收集并再悬浮所有细胞在100ml缓冲液中,通过流式细胞仪检测,发现AZA能诱导AML细胞的凋亡,如图2B所示。
【实施例4】AZA能够促进AraC对AML细胞的杀伤作用
在96孔板中每孔接种1×104个AML细胞(U937、THP-1、MOLM-13、U937、THP-1、MOLM-13、KG-1),AML细胞使用Ara-c(5μM),AZA(5mM),或者两者联合处理((5μM Ara-c+5mM AZA),在处理24h后,将10μL Alamar Blue加入每一个孔中,等待孵育后不同时间点的测量。同时,使用不加细胞的Alamar Blue溶液作为对照。在波长560nm的光中测量其吸光度。如图3所示,AZA能够促进AraC对AML细胞的杀伤作用。
【实施例5】Western Blot实验检测AZA对C-PARP、Jab1,p-Akt,Trx的蛋白量的影响
细胞通过PBS清洗、收集之后,使用RIPA裂解,在离心后总蛋白储存在-80℃环境中,蛋白质浓度使用蛋白浓度试剂盒检测,等量蛋白进行十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(15%SDS-PAGE),转膜到PVDF膜(Millipore corp),5%脱脂牛奶浸没PVDF膜,室温摇床上封闭2h。按PARP,Jab1,p-Akt,T-Akt and β-actin抗体说明书4℃过夜孵育,将膜与辣根过氧化物酶标记抗体室温孵育1h,最后用SuperSignal West Pico Chemiluminescent HRP Substrate(Thermo)检测。
如图4所示,AZA能够诱导凋亡标志物(C-PARP),同时也能抑制Jab1,p-Akt,Trx的蛋白相对表达量。
【实施例6】Alamar Blue实验检测抑制AML细胞株内的Jab1表达后是否影响AZA对AML细胞的杀伤作用
用Nucleofector Kit V(Amaxa Biosystems,Lonza,Allendale,NJ)将siRNA对AML细胞进行转染,抑制AML细胞株内的Jab1水平后,通过Alamar Blue实验,如图5所示,发现AML细胞对AZA更加敏感,提示AZA可能通过Jab1机制杀伤AML细胞。
- 还没有人留言评论。精彩留言会获得点赞!