微针阵列及使用方法与流程
相关申请的交叉引用本申请要求提交于2015年1月21日的美国临时专利申请62/105,987的优先权,该临时专利申请的公开内容全文以引用方式并入本文。
背景技术:
:透皮和局部药物递送可用于治疗处理,但可使用这些途径有效递送的分子数可通过皮肤的阻隔性进行限制。穿过皮肤传输分子的主要屏蔽是角质层(皮肤的最外层)。已提出了多种不同的皮肤处理方法,以便提高诸如角质层的最外皮肤层的渗透性或孔隙率,从而增强穿过那些层或至那些层中的药物递送。角质层为由脂域分开的紧凑角化的细胞残余物的复杂结构。角质层是由失去其细胞核并且变为角质的角质细胞形成的,该角质细胞包含大多数上皮细胞。这些死细胞包括角质层,该角质层具有仅约10微米到30微米的厚度并且防止身体由外源性物质侵入并防止内源性流体和溶解分子向外迁移。各种皮肤处理方法包括使用微针、激光消融、射频消融、热消融、超声波导入、离子导入、或它们的组合。已公开了包括相对较小结构(有时称为微针或微钉)的阵列的装置以结合治疗剂和其它物质通过皮肤和其它表面的递送来使用。通常将装置压贴皮肤以努力刺穿角质层,使得治疗剂和其他物质可以顺序或同时穿过该层并进入下面的组织中。这些装置的微针会在接触角质层时将其刺穿,从而形成多个微观狭缝,微观狭缝用作通道,活性组分的分子可以通过通道被递送到主体内。为了递送活性组分,微针装置可以设置有贮存器,用于在将活性组分递送穿过角质层之前暂时地保持液态形式的活性组分。在一些构造中,微针可以为空心的,以提供直接从贮存器通过微针的液体流动路径,以使得能够穿过皮肤递送治疗物质。在替代构造中,可以将活性组分涂布在微针阵列上,并在已刺穿角质层之后将活性组分直接穿过皮肤递送。微针阵列可与能够使用若干次或作为一次性使用装置的注射及输注设备(即将空心微针施用至皮肤并且有利于通过空心微针输注物质的“施用装置”)结合使用。微针阵列通常仅用一次,用后即弃。技术实现要素:现在已发现,在包括多根空心微针的制品和抵靠其推压该制品的皮肤表面之间的相互作用可能对多根微针中的至少一根微针刺入皮肤中产生不期望的影响。现在还已发现,当制品包括微针阵列时,其中一个效应可能根据通过阵列中的微针中的一根或多根刺入皮肤中的深度而显著波动。本发明人认识到刺入深度的一致性可以通过将若干特征结构包括到制品的设计中进行控制。本发明的设计特征结构导致能够快速有效地并且一致地将针插入皮肤中的期望的深度并且将药物有效剂量迅速递送在多个皮肤位置中。此外,本发明设计的某些特征结构允许使用更简单、更稳定的工艺来制造该制品。本公开一般涉及制品,所述制品包括微针及其穿过皮肤表面递送物质或穿过皮肤表面除去生物流体的用途。特别地,本公开涉及一种制品,所述制品包括多根微针的阵列,所述微针被构造成在使用所述制品的过程中,通过促进微针与皮肤之间的接触并且通过降低皮肤与非微针表面之间接触的可能性,为多根微针中的每一根微针提供一致的刺入深度。本公开的某些方面提供一种制品。该制品可包括第一侧面、与第一侧面相背对的第二侧面以及至少三根空心微针。第一侧面可包括中心腔体部分和从第一侧面突出且与中心腔体部分不共面的平台部分。微针可从平台部分沿第一方向延伸。平台部分可基本上围绕中心腔体部分,并且可包括中心腔体部分近侧的内周边和中心腔体部分远侧的外周边。所述至少三根微针中的每一根包括主体,所述主体包括外表面;具有基部和第一形状的基部区段,该第一形状由外表面的第一节段限定;具有尖端和第二形状的尖端区段,该第二形状由外表面的第二节段限定,其中第二形状不同于第一形状;勾出基部区段和尖端区段轮廓的过渡平面;以及中心轴线。第一角度大于50°,并且小于或等于约85°,该第一角度由至少三根微针中的每一根的中心轴线以及从平台的外周边延伸并穿过至少一根微针的过渡平面的最短线限定。在任一实施方案中,第一角度可为约65°至约75°(包括端值在内)。在任一上述实施方案中,第一角度可为约70°。本公开的其他方面提供一种制品。该制品可包括第一侧面、与第一侧面相背对的第二侧面以及至少三根空心微针。第一侧面可包括中心腔体部分和从第一侧面突出且与中心腔体部分不共面的平台部分。微针可从平台部分沿第一方向延伸。平台部分可基本上围绕中心腔体部分,并且可包括中心腔体部分近侧的内周边和中心腔体部分远侧的外周边。所述至少三根微针中的每一根包括主体,所述主体包括外表面;具有基部和第一形状的基部区段,该第一形状由外表面的第一节段限定;具有尖端和第二形状的尖端区段,该第二形状由外表面的第二节段限定,其中第二形状不同于第一形状;勾出基部区段和尖端区段轮廓的过渡平面;以及中心轴线。所述至少三根微针中的每一根包括从基部至尖端所测量的高度。所述至少三根微针中的每一根的尖端区段可限定微针高度的至少约45%。在任一实施方案中,至少三根微针中的每一根的尖端区段可限定微针高度的至少约70-80%。短语“注射设备”是指能够在特定期间内递送或抽取流体的一体化装置,并且并不限于仅旨在用于注入的装置。因此,注射设备可用于例如将流体注射到真皮内或者从组织中抽取流体。术语“透皮”及其变型形式通常用于指对穿越皮肤的任何部分的活性成分的任何类型的递送。即,透皮通常可包括全身递送(即,在活性成分穿过真皮或基本上穿过真皮输送,使得活性成分递送到血流中的情况下)以及皮内递送(即,在活性成分部分地穿过真皮,例如穿过皮肤的外层(角质层)输送的情况下,在活性成分递送到皮肤中,例如用于治疗牛皮癣或用于局部麻醉剂递送的情况下)。即,本文使用的透皮递送包括递送这样的活性成分,该活性成分穿过皮肤的至少一部分(但不一定所有的皮肤层)输送,而不是仅局部施用于皮肤的外层。短语“空心微针”是指被设计用于刺穿角质层以有利于穿过皮肤递送药物的特定微观结构。以举例的方式,微针可包括能够刺穿角质层并且将液体药物制剂递送到角质层下面的皮肤或组织层的针或针状结构、以及其他结构。词语“优选的”和“优选地”指在某些情况下可提供某些有益效果的本发明实施方案。然而,在相同的情况下或其他情况下,其他实施方案也可能是优选的。此外,述及一个或多个优选的实施方案并非暗示其他实施方案不可用,也并非旨在将其他实施方案排除在本发明的范围之外。术语“包括”及其变型形式在说明书和权利要求中出现这些术语的地方不具有限制的含义。如本文所用,“一个”、“一种”、“所述(该)”、“至少一个(种)”以及“一个(种)或多个(种)”可互换使用。因此,例如,一根微针可以理解为“一根或多根”微针。术语“和/或”意指所列要素的一个或全部,或者所列要素的任何两个或多个的组合。另外,在本文中,通过端点表述的数值范围包括该范围内所含的所有数值(例如,1至5包括1、1.5、2、2.75、3、3.80、4、5等)。本发明的上述
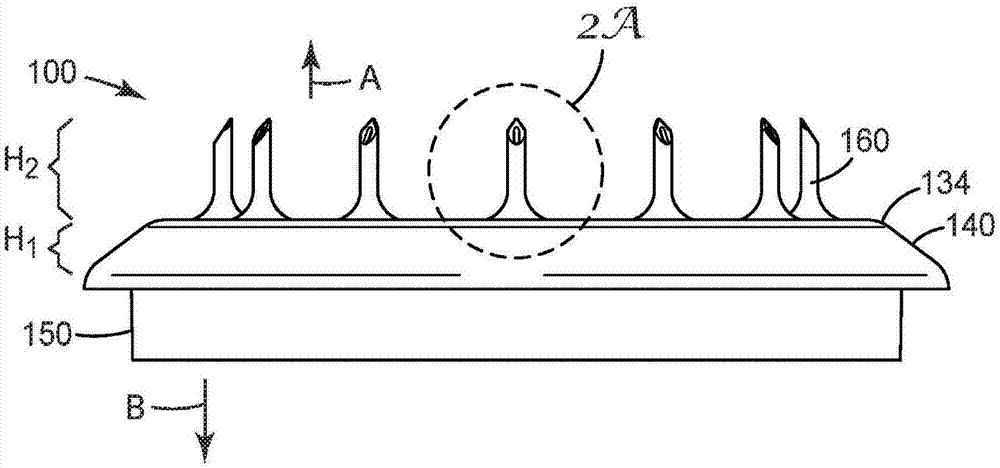
发明内容并非旨在描述本发明的每个公开的实施方案或每种实施方式。以下描述更具体地例示了示例性实施方案。在本申请全文的若干处,通过实施例列表提供了指导,这些实施例可以各种组合使用。在每种情况下,所引用的列表都只用作代表性的组,并且不应理解为排它性列表。下面将结合附图和描述介绍上述及其它实施方案的更多细节。通过具体实施方式、附图和权利要求书,其它特征、对象和优点将变得显而易见。附图说明将结合下列各图进一步解释本发明,其中各图中类似的结构部分采用类似的数字表示。图1是示出根据本公开的包括多根微针的制品的一个实施方案的透视图。图2是图1中的制品的侧视图。图2a是图2的制品的一部分的细部图。图3是图1的制品的第一侧面的平面图。图4是沿图3的制品的线4-4截取的剖视图。图4a是图4的空心微针中的一根的细剖视图。图5a是图1的制品的一部分的局部剖视示意性侧视图,示出了由微针的中心轴线与穿过微针中的过渡平面的线相交形成的角度θ1。图5b是图5a的制品的局部剖视示意性侧视图,示出了由微针的中心轴线与穿过微针中的过渡平面的线相交形成的角度θ2。图6是包括微针的制品的另一个实施方案的一部分的局部剖视示意性侧视图,示出了由微针的中心轴线与穿过微针中的过渡平面的线相交形成的角度θ3。图7是根据本公开的制品的平面图;示出了制品的第一侧面上限定的区域。图8是联接至制品的注射及输注施用装置的一部分的平面图,该制品包括根据本公开的多根微针;示出了与制品和注射及输注施用装置相关联的各种尺寸。具体实施方式在详细解释本公开的任何实施方案之前,应当理解,本发明在其应用中不仅限于下文描述内容中提及或下文附图中示出的构造细节和部件布置方式。本发明能够拥有其它实施方案,并且能够通过各种方式实践或进行。另外,应当理解,本文使用的措词和术语是出于描述目的而不应被视为限制性的。本文使用的“包括”、“包含”或“具有”及其变型形式意在涵盖其后列出的项目及其等同形式以及附加的项目。除非另外指明或限定,否则术语“安装”、“连接”、“支撑”和“联接”和它们的变型形式被广泛使用并涵盖直接和间接安装、连接、支撑和联接。应当理解,可采用其他的实施方案,并且可在不偏离本发明范围的情况下作出结构变化或逻辑变化。此外,例如“前”、“后”、“顶部”、“底部”等用语仅用于当元件彼此相关的时候描述元件,而决非意在陈述设备的具体取向,以指示或暗示设备的必要或所需取向,或指定在使用中将如何使用、安装、显示或定位本文所述发明。本公开一般涉及制品,所述制品包括微针及其穿过皮肤表面递送物质或穿过皮肤表面除去生物流体的用途。特别地,本公开涉及一种制品,所述制品包括多根微针的阵列,所述微针被构造成在使用所述制品的过程中,通过促进微针与皮肤之间的接触并且通过降低皮肤与非微针表面之间接触的可能性,为多根微针中的每一根微针提供一致的刺入深度。转向附图,图1-4示出了根据本公开的制品100的一个实施方案的各种视图。制品100包括第一侧面112和与第一侧面112相背对的第二侧面114。第一侧面112包括中心腔体部分120和平台部分130。平台部分130从第一侧面112突出且与中心腔体部分120不共面。在图1-4例示的实施方案中,中心腔体部分120和平台部分130均形成为单一主体110的一部分。然而,在任一实施方案中,预期中心腔体部分120和平台部分130可以是在制品中彼此邻近设置的独立部件(未示出)。中心腔体部分120与平台部分130不共面。尽管图1-4例示的实施方案示出了具有曲线表面的中心腔体部分120,该曲线表面远离由平台部分130形成的平面而倾斜,预期在任一实施方案中,中心腔体部分可包括一个或多个与平台部分不共面的斜面(未示出)。在任一实施方案中,中心腔体部分120可由实心结构组成,如图1-4所示。另选地,在任一实施方案中,中心腔体部分可包括、基本上由、或由开口(例如,通孔,未示出)组成。平台部分130基本上围绕中心腔体部分120。平台部分130包括中心腔体部分120近侧的内周边132和中心腔体部分远侧的外周边134。在任一实施方案中,内周边132和/或外周边134包括基本上倒圆的边缘,如图2中外周边的侧视图所示,以及如图4的内外周边的剖视图所示。另选地,在任一实施方案中,内周边132和/或外周边134包括基本上呈角的边缘(未示出)。制品100还包括从平台部分130沿第一方向延伸的多根空心微针160(参见箭头“a”,图2)。在任一实施方案中,多根空心微针160可构成一个阵列。阵列可包括圆形布置(即环形的或者漩涡状的阵列),如图3所示。预期具有其他直线或曲线几何形状(例如正方形、矩形、椭圆形、六边形;未示出)的其他阵列在根据本公开的制品中也是可用的。图2a示出了图2的制品100的其中一根微针160的细部图。在制品100的任一实施方案中,多根微针中的每一根微针160包括主体,该主体包括外表面163、基部区段166和尖端区段168。基部区段166包括基部162,其中微针160从平台部分130延伸。基部区段166具有由基部区段的外表面163限定的第一形状。在图2a的例示的实施方案中,第一形状为漏斗形状(即,具有曲率半径的大体上圆锥体形状),因此,微针的直径在基部162处比在尖端处宽。任选地,基部区段166具有凹形外表面。尖端区段168包括尖端164。尖端164是微针160的离基部162最远的部件。尖端区段168具有由微针160的外表面163限定的第二形状。第二形状可区别于第一形状。基部区段166和尖端区段168各自的形状在过渡平面167处是可以区分的。如本文所用的“过渡平面”是指这样的平面,其中由微针的外表面163与中心轴线的正切形成的角度在第一(尖端近侧)角度≤10°至第二(尖端远侧)角度大于约10°的范围内变化。在图3a的例示的实施方案中,微针160的外表面163基本上平行于中心轴线(未示出)。然而,在过渡平面167处,尖端区段168(即,第二形状)的基本上直的外表面变成基部区段166(即,第一形状)的扩张曲率半径,并且由外表面和中心轴线(未示出)的正切(未示出)的相交形成的角变成大于约10°。图2a中基本上圆柱形的尖端区段168是通过斜面165截顶的,该斜面形成了足够尖能刺穿角质层的尖端164。多根微针中的每一根微针160还包括空心通道169。空心通道169任选地从第一侧面112一直延伸穿过制品至第二侧面114,如图4所示。在任一实施方案中,空心通道可提供尽端的贮存器(例如,微针主体中的尽端贮存器,未示出),例如,在其中载有活性成分用于注射/递送到皮肤中。在任一实施方案中,延伸穿过制品100的空心通道169可以流体方式连接至设置在制品的第二侧面上的贮存器108,并且活性成分可从制品100的贮存器108并通过微针160的空心通道169注入患者体内。在任一实施方案中,第一侧面112任选地包括从平台部分130的外周边134的至少一部分侧向延伸的不含微针的周边部分140。在任一实施方案中,周边部分140基本上围绕平台部分130。周边部分140在与第一方向相反的第二方向(参见箭头“b”,图2)上远离平台部分130倾斜。在图1-4例示的实施方案中,中心腔体部分120、平台部分130和周边部分140均形成为单一主体110的部分。然而,在任一实施方案中,预期周边部分140和平台部分130可以是在制品中彼此邻近设置的独立部件(未示出)。图4a示出了设置在图4的制品单一主体110的第一侧面112上的节段微针160的其中一个的细部图。微针160包括第一开口187,该第一开口187靠近尖端164通向空心通道169,该空心通道169一直延伸穿过主体110至主体110的第二侧面112的第二开口189。任选地,在任一实施方案中,制品100还可包括凸块(例如,凸块106)。凸块106可用于制造目的,或者在使用过程中用于对准目的。在例示的实施方案中,凸块106从周边部分140侧向延伸;然而,其他可用的构形对于本领域的普通技术人员将显而易见。任选地,制品100还包括侧壁150,该侧壁150基本上沿与多根微针160相背对的方向(即图2中所示的第二方向“b”)延伸。例示的实施方案的侧壁150在制品100的第二侧面114上形成贮存器108。贮存器108任选地可以密封(未示出)并且可容纳通过经由多根微针160注射而待被递送的活性剂(例如,药物)。参见图2,制品可包括至少两个高度尺寸。第一高度尺寸h1是从平台部分130沿第二方向b延伸的倾斜的周边部分140的高度。第二高度尺寸h2是从平台部分130沿第一方向a延伸的每一根微针160的高度。重新参见图2a,多根微针中的每一根微针160均包括两个高度分量(分别是第一高度分量h2a和第二高度分量h2b),它们构成微针160的总体高度。第一高度分量代表微针160的基部区段166的高度,第二高度分量代表微针的尖端区段168的高度。在任一实施方案中,根据本公开的多根微针中的每一根微针的第一高度分量为约50μm至小于500μm。优选地,根据本公开的多根微针中的每一根微针的第一高度分量为约150μm至约350μm。更优选地,根据本公开的多根微针中的每一根微针的第一高度分量为约200μm至约300μm。甚至更优选地,根据本公开的多根微针中的每一根微针的第一高度分量为约250μm至约270μm。在任一实施方案中,根据本公开的多根微针中的每一根微针的第二高度分量为约300μm至约1940μm。在任一实施方案中,根据本公开的多根微针中的每一根微针的第二高度分量为约540μm至约1740μm。当第一高度分量为约250μm至约270μm时,优选地,根据本公开的多根微针中的每一根微针的第二高度分量为约540μm至约1240μm。当第一高度分量为约250μm至约270μm时,更优选地,根据本公开的多根微针中的每一根微针的第二高度分量为约640μm至约840μm。当第一高度分量为约250μm至约270μm时,甚至更优选地,根据本公开的多根微针中的每一根微针的第二高度分量为约700μm至约800μm。为了使活性化合物一致且有效地递送至皮肤中的适当位置,本发明人已发现根据本公开的包括至少三根微针的制品的构造应当有利于所有至少三根微针的刺入,直到每一根微针的至少尖端部分完全插入到皮肤中。在一个方面,在任一实施方案中,在根据本公开的制品中,多根微针中的每一根微针的第一高度分量和第二高度分量之间可以存在预定义的成比例关系。在任一实施方案中,尖端区段(如从多根微针中的至少一根微针的过渡平面到尖端所测量的)限定至少一根微针的高度的至少约45%。在任一实施方案中,尖端区段(如从多根微针中的每一根微针的过渡平面到尖端所测量的)限定微针的高度的至少约45%。在任一实施方案中,尖端区段(如从多根微针中的至少一根微针的过渡平面到尖端所测量的)限定至少一根微针的高度的约50%-95%。在任一实施方案中,尖端区段(如从多根微针中的每一根微针的过渡平面到尖端所测量的)限定微针的高度的约50%-95%。在任一实施方案中,尖端区段(如从多根微针中的至少一根微针的过渡平面到尖端所测量的)限定至少一根微针的高度的约60%-85%。在任一实施方案中,尖端区段(如从多根微针中的每一根微针的过渡平面到尖端所测量的)限定微针的高度的约60%-85%。在任一实施方案中,尖端区段(如从多根微针中的至少一根微针的过渡平面到尖端所测量的)限定至少一根微针的高度的至多约70%-80%(包括端值在内)。在任一实施方案中,尖端区段(如从多根微针中的每一根微针的过渡平面到尖端所测量的)限定微针的高度的至多约70%-80%(包括端值在内)。在任一实施方案中,本公开的制品中的多根微针中的每一根微针160包括如图5a、图5b和图6所示的中心轴线180。中心轴线180还代表微针160的从基部162朝向尖端164延伸穿过微针的纵向轴线。在一个方面,多根微针中的每一根微针160可在微针160的结构特征(即,微针过渡平面167)与平台部分130的一个或多个周边(即,内周边132和外周边134)之间具有空间关系,如图5a-b所示。在另一方面,在任一实施方案中,在多根微针的每一根微针与平台的外周边之间可存在空间关系,根据本公开在该平台上微针在制品中突起。图5a示出了根据本公开的包括多根微针的制品的节段的示意图。该制品包括第一侧面112,该第一侧面具有中心腔体部分120、平台部分130、倾斜的周边部分140以及设置在如上所述的平台部分130与周边部分140之间的外周边134。从平台部分130延伸出的是微针160。微针160包括具有第一形状的基部区段166以及具有第二形状的尖端区段168,这些区段由过渡平面167分开。图5a还示出了微针160的中心轴线180,以及从外周边134延伸穿过过渡平面167的最近点185至外周边134、至中心轴线180的最短线184。最短线184与中心轴线180相交形成角θ1。在本公开的制品的任一实施方案中,角θ1大于50°至约85°。在任一实施方案中,角θ1为约65°至约75°。在任一实施方案中,角θ1为小于约68°至约72°。在任一实施方案中,角θ1为约70°。本领域的普通技术人员将理解,当角θ1减小时,微针与外周边之间的平台部分的可能面积量也将减小。下文将讨论这种关系的重要性。另选地或除此之外,在多根微针中的每一根微针与平台的内周边之间可存在空间关系,微针在该平台上突起。图5b示出了图5a中所示的制品的节段的类似示意图。该制品包括第一侧面112,该第一侧面具有中心腔体部分120、平台部分130、倾斜的周边部分140以及设置在如上所述的平台部分130和周边部分140之间的内周边132。从平台部分130延伸出的是微针160。微针160包括具有第一形状的基部区段166以及具有第二形状的尖端区段168,这些区段通过过渡平面167分开。图5b还示出了微针160的中心轴线180,以及从内周边132延伸穿过过渡平面167的最近点183至内周边132、至中心轴线180的第一最短线182。第一最短线182与中心轴线180相交形成角θ2。在本公开的制品的任一实施方案中,角θ2大于50°至约85°。在任一实施方案中,角θ2为约65°至约75°。在任一实施方案中,角θ2为约68°至约72°。在任一实施方案中,角θ2为约70°。本领域的普通技术人员将理解,当角θ2减小时,微针和内周边之间的平台部分的可能面积量也将减小。下文将讨论这种关系的重要性。无论由多根微针中的每一根微针的基部区段和尖端区段限定的第一形状和第二形状如何,上文讨论的空间关系均可被应用。图6示出了制品的节段的示意图,所述制品包括与图5a所示的微针类似的多根微针,不同的是基部区段166具有限定截棱锥或截头圆锥体形状而非漏斗形状的第一形状。该制品包括第一侧面112,该第一侧面具有中心腔体部分120、平台部分130、倾斜的周边部分140以及设置在如上所述的平台部分130和周边部分140之间的外周边134。从平台部分130延伸出的是微针160。微针160包括具有第一形状的基部区段166以及具有第二形状的尖端区段168,这些区段由过渡平面167分开。图6还示出了微针160的中心轴线180,以及从外周边134延伸穿过过渡平面167的最近点185至外周边134、至中心轴线180的第二最短线184。第二最短线184与中心轴线180相交形成角θ3。在本公开的制品的任一实施方案中,角θ3大于50°至约85°。在任一实施方案中,角θ3为约65°至约75°。在任一实施方案中,角θ3为约68°至约72°。在任一实施方案中,角θ3为约70°。本领域的普通技术人员将理解,当角θ3减小时,微针与外周边之间的平台部分的可能面积量也将减小。下文将讨论这种关系的重要性。在根据本公开的制品的任一实施方案中,当沿着中心轴线测量时,多根微针中的至少一根微针的过渡平面设置成远离平台部分的约60μm至约490μm。在根据本公开的制品的任一实施方案中,当沿着中心轴线测量时,多根微针中的至少一根微针的过渡平面设置成远离平台部分的约200μm至约300μm。在根据本公开的制品的任一实施方案中,当沿着中心轴线测量时,多根微针中的至少一根微针的过渡平面设置成远离平台部分的约260μm。在根据本公开的制品的任一实施方案中,多根微针中的至少一根微针(从基部至尖端所测量)的高度为约600μm至约2000μm。在根据本公开的制品的任一实施方案中,多根微针中的至少一根微针(从基部至尖端所测量)的高度为约800μm至约1500μm。在根据本公开的制品的任一实施方案中,多根微针中的至少一根微针(从基部至尖端所测量)的高度为约900μm至约1100μm。在根据本公开的制品的任一实施方案中,多根微针中的至少一根微针(从基部至尖端所测量)的高度为约1000μm。在某些优选实施方案中,根据本公开的制品包括多根微针,其中每一根微针的第一高度分量为约200μm至约300μm,每一根微针的第二高度分量为约640μm至约840μm,角θ1为约65-75度,并且角θ2为约65-75度。在这些实施方案中,制品包括或操作地联接至药物贮存器并且制品为设备(例如组件)的一部分,其中制品操作地联接至至少一个储能装置,该至少一个储能装置能够以约4m/s至约12m/s的速度(在冲击之前)推进制品的微针并且能够将流体从贮存器推压至并通过空心微针。在任一实施方案中,第一储能部件(例如第一弹簧)可以用于产生使微针沿预定义的方向(例如朝向皮肤冲击部位)从第一位置(例如壳体内)移动至第二位置(例如与皮肤表面接触)的力,并且第二储能部件(例如第二弹簧)可用于将流体从贮存器推压至(并通过)空心微针。在某些特别优选的实施方案中,根据本公开的制品包括多根微针,其中每一根微针的第一高度分量为约250μm至约270μm,每一根微针的第二高度分量为约700μm至约800μm,角θ1为约68-72度,并且角θ2为约68-72度。在这些实施方案中,制品包括或操作地联接至药物贮存器并且制品为设备(例如组件)的一部分,其中制品操作地联接至储能装置(例如注射及输注施用装置),该储能装置能够以约4m/s至约12m/s的速度(在冲击之前)或约6m/s至约9m/s的速度(在冲击之前)推进制品的微针。有利地,这些优选实施方案的制品和组件能够实现每一根微针至皮肤组织中的预定义深度(例如,约400微米至约800微米)的高度可再现的刺入深度和在相对较短的时间段(例如约1.5分钟至约4分钟)内递送高度可再现的预定义体积(例如,约0.2ml至约3ml)的药物。根据本公开,微针的阵列包括从平面(即,平台部分130,如图1-4所示)延伸的多个空间上隔开的微针。阵列中针的构造(例如相对于制品的边缘和相对于最近的相邻微针)改善了刺入并且相应地改善了微阵列中每一根针对药物的递送。在另一方面,在任一实施方案中,根据本公开在由制品的第一侧面限定的第一投影面积和由制品的平台部分限定的第二区域之间可存在空间关系。如本文所用,术语“投影面积”是指制品的投射到制品的一侧的面积,因此,当制品的这一侧被推向表面时,能够与表面(例如,皮肤表面)接触。图7示出了包括根据本公开的多根微针160的制品100的顶视图(例如,示出了第一侧面112)。在图7例示的实施方案中,制品100包括形成具有圆形(环形的或者漩涡状的)形状的阵列的多根微针160。第一侧面112包括中心腔体部分120;平台部分130,多根微针160围绕中心腔体部分从该平台部分130延伸出,以及围绕平台部分130的周边部分140。第一侧面112限定第一区域a1(即,投影面积),该第一区域包括中心腔体部分120和周边部分140(两个部分均用第一类阴影示出)、由微针160的基部限定的区域(无阴影),以及平台部分130(用第二类阴影示出)。平台部分130限定第一区域a1内的第二区域a2。第二区域包括阴影平台区域以及由微针的基部限定的区域。在任一实施方案中,第二区域a2小于第一区域a1的约40%。在任一实施方案中,第二区域a2小于第一区域a1的约35%。在任一实施方案中,第二区域a2小于第一区域a1的约30%。在任一实施方案中,第二区域a2为第一区域a1的约25%至约40%。在任一实施方案中,本公开的制品可包括用于容纳药物的贮存器。贮存器可与每一根空心微针流体连通(或选择性流体连通)。在任一实施方案中,根据本公开的制品可操作地联接至本文所述的其它部件(例如,贮存器、储能部件)以形成注射及输注设备。注射及输注设备可用于将注射药物递送到受试者的皮肤中。此类注射及输注设备在本领域中是已知的并且包括例如国际专利公布wo2014/193725中所述的那些,该国际专利公布全文以引用方式并入本文。注射及输注设备可以被致动以使用存储的能量(例如来自弹簧)产生原动力,该原动力以预先确定的速度抵靠皮肤推进微针阵列制品。在任一实施方案中,注射及输注设备可被构造成以约2m/s至约20m/s的速度(在冲击皮肤前)推进微针阵列制品。在任一实施方案中,注射及输注设备可被构造成以约4m/s至约12m/s的速度(在冲击前)推进微针阵列制品。在任一实施方案中,注射及输注设备可被构造成以约6m/s至约9m/s的速度(在冲击前)推进微针阵列制品。在任一实施方案中,注射及输注设备可被构造成以约7m/s至约8m/s的速度(在冲击前)推进微针阵列制品。在任一实施方案中,包括根据本公开的微针制品的设备可用于用来将微针插入皮肤组织中的预定义深度的方法中。在任一实施方案中,阵列中每一根微针的刺入深度可以为约400μm至约850μm。在任一实施方案中,阵列中每一根微针的平均刺入深度可以为约580μm至750μm。在任一实施方案中,包括根据本公开的微针制品的设备可用于用来在预先确定的时间量内将预定义体积(例如,约0.2ml至约3ml)的药物递送至皮肤组织中的方法中。在任一实施方案中,预先确定的时间量可为约1-5分钟至约4分钟。有利地,这些递送(即输注)时间相对较短。这些输注时间可通过以预先确定的速率递送药物来实现。药物输注速率可以为约0.5ml/分钟至约1.3ml/分钟。根据本公开制造的微针制品(例如,包括具有空心微针的制品)可具有诸如以下专利和专利申请中所述的那些的各种构造和特征结构,所述专利或专利申请的公开内容全文以引用方式并入本文。微针阵列制品的一个实施方案包括在以下专利中公开的结构:美国专利申请公布第2005/0261631号(clarke等人),其描述了具有截锥形形状和受控纵横比的微针。微针制品的另一个实施方案包括在以下专利中公开的结构:美国专利第6,091,975号(daddona等人),其描述了用于刺穿皮肤的刀片状微突起。微针制品的另一个实施方案包括在以下专利中公开的结构:美国专利第6,312,612号(sherman等人),其描述了具有空心中心通道的锥形结构。微针阵列制品的另一个实施方案包括在以下专利中公开的结构:美国专利第6,379,324号(gartstein等人),其描述了在微针的尖端的顶表面处具有至少一个纵向刀片的空心微针。微针阵列制品的另一个实施方案包括在以下专利中公开的结构:美国专利申请公布第us2012/0123387号(gonzalez等人)和第us2011/0213335号(burton等人),这两者描述了空心微针。微针阵列制品的另一个实施方案包括在以下专利中公开的结构:美国专利第6,558,361(yeshurun)和第7,648,484(yeshurun等人),这两者描述了空心微针阵列及其制造方法。可在本公开的微针制品中采用的微针的特征结构的各种实施方案在以下专利中有所描述:pct公布wo2012/074576(duan等人),其描述了液晶聚合物(lcp)微针;和pct公布wo2012/122162(zhang等人),其描述了可在本公开的微针中采用的各种不同类型和组成的微针。包括具有根据本公开的特征结构的微针的制品可例如通过本领域已知的注塑方法制得。在一些实施方案中,微针材料可为(或包括)金属或聚合物材料优选地医疗级聚合物材料。示例性类型的医疗级聚合物材料包括聚碳酸酯、液晶聚合物(lcp)、聚醚醚酮(peek)、环烯烃共聚物(coc)、聚对苯二甲酸丁二醇酯(pbt)。优选类型的医疗级聚合物材料包括聚碳酸酯和lcp。本公开的微针制品可以任何合适的方式制成,诸如通过注塑、压缩模制、金属注塑、压印或挤出而制成。在任一实施方案中,空心微针阵列可通过下述方式而制成:注塑聚合物(诸如医疗级聚碳酸酯或lcp),之后进行激光钻孔,以形成微针的通道。用于将聚合物材料模制到本公开的实心微针制品中的模制方法的非限制性示例可见于美国专利no.8,088,321(ferguson等人)以及美国专利申请公布no.2012/0258284(rendon)和2012/0041337(ferguson等人),上述专利中每一者全文以引用方式并入本文中。公开了包括空心微针的制品的形成的公布的非限制性示例是pct公布wo2014/105458,该公布全文以引用方式并入本文。在一些实施方案中,微针材料可为(或包括)可生物降解的聚合物材料,优选地医疗级可生物降解的聚合物材料。示例性类型的医疗级可生物降解的材料包括聚乳酸(pla)、聚乙醇酸(pga)、pga和pla共聚物、聚酯-酰胺聚合物(pea)。在一些实施方案中,微针可由本文所称的可溶解、可降解或可崩解材料制备成“可溶解微针”。可溶解、可降解或可崩解材料为在使用期间溶解、降解或崩解的任何固体材料。具体地讲,“可溶解微针”在角质层下面的组织中充分溶解、降解或崩解,以允许治疗剂释放到组织中。治疗剂可涂布在可溶解微针上或掺入可溶解微针中。在一些实施方案中,可溶解材料选自碳水化合物或糖。在一些实施方案中,可溶解材料为聚乙烯吡咯烷酮(pvp)。在一些实施方案中,可溶解材料选自由以下项组成的组:透明质酸、羧甲基纤维素、羟丙基甲基纤维素、甲基纤维素、聚乙烯醇、蔗糖、葡萄糖、葡聚糖、海藻糖、麦芽糖糊精、以及它们的组合。在任一实施方案中,微针可由任何上述材料中的两种或更多种的组合制成(或包括任何上述材料中的两种或更多种的组合)。例如,微针的尖端可为可溶解材料,而微针的其余部分为医疗级聚合物材料。本公开的含微针的制品中的单根微针或多根微针可具有能够刺穿角质层的各种形状。在一些实施方案中,多根微针中的一根或多根可具有这样的区段(例如,基部区段、尖端区段或它们的组合),该区段具有四方锥体形状、三角锥体形状、阶梯锥体形状、圆锥体形状、微刀片形状、或皮下注射针的形状。在任一实施方案中,多根微针中的一根或多根的区段(例如,基部区段、尖端区段或它们的组合)可具有四方锥体形状。在任一实施方案中,多根微针中的一根或多根的区段(例如,基部区段、尖端区段或它们的组合)可具有三角锥体形状。在任一实施方案中,多根微针中的一根或多根的区段(例如,基部区段、尖端区段或它们的组合)可具有阶梯锥体形状。在任一实施方案中,多根微针中的一根或多根的区段(例如,基部区段、尖端区段或它们的组合)可具有圆锥体形状。在任一实施方案中,多根微针中的一根或多根的区段(例如,基部区段、尖端区段或它们的组合)可具有微刀片形状。在任一实施方案中,多根微针中的一根或多根的区段(例如,基部区段、尖端区段或它们的组合)可具有皮下注射针的形状。在任一实施方案中,微针阵列制品可包括具有上述微针形状中的任何两个或更多个的组合的微针阵列。微针阵列制品中的任一根微针的形状可为对称或非对称的。微针阵列制品中的任一根微针的形状可为截顶的(例如,多根微针可具有截棱锥形状或截头圆锥体形状)。在一个优选的实施方案中,微针阵列制品中的多根微针中的每一根微针具有四方锥体形状。在任一实施方案中,微针制品中的多根微针中的每一根微针为实心微针(即,微针不包括通孔)。在任一实施方案中,实心微针阵列制品中的多根实心微针中的每一根微针可具有这样的区段(例如,基部区段、尖端区段或它们的组合),该区段具有四方锥体形状、三角锥体形状、阶梯锥体形状、圆锥体形状或微刀片形状。在一个优选的实施方案中,实心微针阵列制品中的多根实心微针中的每一根微针具有这样的区段(例如,基部区段、尖端区段或它们的组合),该区段具有四方锥体形状或具有曲率半径的圆锥体形状。在一些实施方案中,微针阵列中的多根微针中的每一根微针为空心微针(即,所述微针包含贯通微针的空心膛孔)。空心膛孔可从微针的基部到微针的尖端或膛孔可从微针的基部到与微针的尖端错开的位置。在任一实施方案中,空心微针阵列中的多根空心微针中的一根或多根可具有圆锥体形状、圆柱形状、四方锥体形状、三角锥体形状、或皮下注射针的形状。在任一实施方案中,空心微针阵列制品中的多根空心微针中的一根或多根微针可具有圆锥体形状;任选地,具有曲率半径。在任一实施方案中,空心微针阵列制品中的多根空心微针中的一根或多根微针可具有圆柱形状。在任一实施方案中,空心微针阵列制品中的多根空心微针中的一根或多根微针可具有这样的区段(例如,基部区段、尖端区段或它们的组合),该区段具有四方锥体形状。在任一实施方案中,空心微针阵列制品中的多根空心微针中的一根或多根微针可具有这样的区段(例如,基部区段、尖端区段或它们的组合),该区段具有三角锥体形状。在任一实施方案中,空心微针阵列制品中的多根空心微针中的一根或多根微针可具有这样的区段(例如,基部区段、尖端区段或它们的组合),该区段具有皮下注射针的形状。在一个优选的实施方案中,空心微针阵列制品中的多根空心微针中的每一根微针具有这样的区段(例如,基部区段、尖端区段或它们的组合),该区段具有常规的皮下注射针的形状。在任一实施方案中,包括根据本公开的空心微针的制品可包括多根微针。多根微针任选地可形成阵列。在任一实施方案中,制品可包括本公开的空心微针中的约3至约30(包括端值)根的阵列。在一个优选实施方案中,制品可包括本公开的空心微针中的约8至约20(包括端值)根的阵列。在一个更优选实施方案中,制品可包括本公开的空心微针中的12、16或18根的阵列。在包括根据本公开的多根空心微针的制品的任一个实施方案中,每根微针的总体高度为约600μm至约2000μm。在包括根据本公开的多根空心微针的制品的任一个实施方案中,每根微针的总体高度为约700μm至约1500μm。在包括根据本公开的多根空心微针的制品的任一个实施方案中,每根微针的总体高度为约900μm至约1100μm。在包括根据本公开的多根空心微针的制品的任一个实施方案中,延伸穿过微针中的每一根的空心通道具有约10μm至约200μm的靠近微针尖端的直径。在包括根据本公开的多根空心微针的制品的任一个实施方案中,延伸穿过微针中的每一根的空心通道具有约10μm至约120μm的靠近微针尖端的直径。在包括根据本公开的多根空心微针的制品的任一个实施方案中,延伸穿过微针中的每一根的空心通道具有约25μm至约75μm的靠近微针尖端的直径。在包括根据本公开的多根空心微针的制品的任一个实施方案中,延伸穿过微针中的每一根的空心通道具有约75μm2至约32,000μm2的横截面积。在包括根据本公开的多根空心微针的制品的任一个实施方案中,延伸穿过微针中的每一根的空心通道具有约75μm2至约18,000μm2的横截面积。在包括根据本公开的多根空心微针的制品的任一个实施方案中,延伸穿过微针中的每一根的空心通道具有约700μm2至约3,000μm2的横截面积。本公开的微针阵列制品可通过注塑聚合物诸如医疗级聚碳酸酯或lcp来制造。通常,这些方法使用模具形成具有微针的基底,该微针从该基底延伸。在任一实施方案中,根据本公开的制品中的至少一根空心微针可具有尖端区段,该尖端区段具有有利于或不妨碍微针刺穿皮肤表面的能力的任何形状或结构。此外,尖端区段可包括开口(例如,凹入部、尽端腔体或一直延伸穿过微针的通孔),所述开口有利于活性化合物的递送(以及,任选地储存在其中)。在任一实施方案中,多根微针的至少一根空心微针包括基部、具有中心轴线和主体直径的细长主体以及具有两个斜面的尖端区段。尖端区段包括尖端、相对于中心轴线呈对角地取向并且延伸穿过主体直径的至少75%的第一斜面、基本上垂直于中心轴线取向且与第一斜面相交的第二斜面、由第一斜面的第一边缘和第二斜面的第二边缘限定的斜开口。具有两个斜面的微针尖端在pct公布wo2015/009524中有所描述,该公布全文以引用方式并入本文。在任一实施方案中,根据本公开的制品中的至少一根空心微针可具有尖端区段,该尖端区段包括由合并形成开口的两个通道形成的开口。因此,在这些实施方案中,至少一根微针包括基部、具有中心轴线的细长主体、具有斜面和该斜面中的斜开口的尖端区段、从斜开口轴向延伸穿过细长主体的至少一部分的第一通道,以及从第一通道径向延伸到斜开口的第二通道。第一通道具有基本上与中心轴线对齐的第一壁。第二通道具有被取向成基本上与中心轴线正交的第二壁。第一通道和第二通道合并以形成斜开口。微针尖端在pct公布wo2015/009523中有所描述,该微针尖端包括由合并形成开口的两个通道形成的开口,该公布全文以引用方式并入本文。在任一实施方案中,本公开的制品可与注射及输注设备(例如,一次性使用施用装置或可重复使用的施用装置)一起使用,该注射及输注设备被构造成将制品的多根微针抵靠皮肤表面推压。在任一实施方案中,可通过单个致动或通过双致动进行注射及输注设备的致动。美国专利申请公布2012/0123387(gonzalez等人)公开了单个致动注射及输注设备的非限制性示例,该公布全文以引用方式并入本文。例如,pct公布wo2014/099404中描述了具有双致动或双自动致动的微针制品的用途,该公布全文以引用方式并入本文。在任一实施方案中,本公开的制品可与包括粘合剂组件的注射及输注设备一起使用,诸如例如pct公布wo2014/099404中描述的包括粘合剂组件的注射及输注设备。在任一实施方案中,粘合剂组件可包括皮肤触压粘合剂层,诸如例如包括pct公布wo2014/099404中描述的皮肤触压粘合剂层的注射及输注设备。在任一实施方案中,皮肤触压粘合剂层可包括环形构造,该环形构造在使用过程中围绕本公开的微针制品,并且任选地,当活性化合物(例如为药物组合物一部分的活性化合物)从(或通过)微针递送到患者体内时,将制品固定至皮肤表面。图8示出了注射及输注设备的一个实施方案的面向皮肤表面的一部分的平面图,该注射及输注设备被构造成用于与包括根据本公开的多根空心微针的制品一起使用。注射及输注设备400包括基本上围绕制品100的皮肤触压粘合剂层490。该制品包括第一侧面112,该第一侧面112包括中心腔体部分120,该中心腔体部分120由与该中心腔体部分120不共面的平台部分130围绕(即,平台在中心腔体之上凸起)。空间上隔开的微针160的环形的或者漩涡状的阵列从平台部分130的第一侧面延伸。第一侧面112还包括围绕平台部分130且与平台部分不共面的任选的周边部分140(即,平台在周边部分上方凸起)。制品100使用各种附接装置(例如,粘合剂、夹具、摩擦配合件等等,未示出)附接(例如,可拆卸地附接)至注射及输注设备400。图8还示出了与制品100和注射及输注设备相关联的各种空间尺寸。在例示的实施方案中,平台部分130是围绕中心腔体部分的环状(即,环形的或者漩涡状的)平台。尺寸d1表示中心腔体部分120的直径,如平台部分130的内周边132所限定的。尺寸d2表示平台部分130的外径,如平台部分的外周边134所限定的。尺寸d3表示围绕平台部分130的环形周边部分140的外径。尺寸d4表示平台部分的宽度,如沿从圆形制品的中心延伸的半径(未示出)所测量的。此外,d5表示最短的距离,如沿从圆形制品的中心延伸的半径(未示出)所测量的,该距离在微针160的尖端和注射及输注设备400的皮肤触压粘合剂层490之间。在一个优选的实施方案中,皮肤触压粘合剂层的形状和尺寸被设计成使得阵列中每个微针尖端与皮肤触压粘合剂层490之间的最短距离大约相等(例如,小于约10%的波动)。示例性实施方案实施方案a是一种制品,其包括:第一侧面,该第一侧面包括中心腔体部分和从第一侧面突出且与中心腔体部分不共面的平台部分;与第一侧面相背对的第二侧面;以及从平台部分沿第一方向延伸的至少三根空心微针;其中平台部分基本上围绕中心腔体部分;其中平台部分包括中心腔体部分近侧的内周边和中心腔体部分远侧的外周边;其中至少三根空心微针中的每一根包括主体,所述主体包括:外表面;具有基部和第一形状的基部区段,该第一形状由该外表面的第一节段限定;具有尖端和第二形状的尖端区段,所述第二形状由所述外表面的第二节段限定,其中所述第二形状不同于所述第一形状;勾出所述基部区段和所述尖端区段轮廓的过渡平面;以及中心轴线;其中第一角度大于50°,并且小于或等于约85°,该第一角度由至少三根空心微针中的每一根的中心轴线以及从平台的外周边延伸并穿过微针的过渡平面的最短线限定。实施方案b是根据实施方案a所述的制品,其中第一角度为约65°至约75°。实施方案c是根据实施方案b所述的制品,其中第一角度为约68°至约72°。实施方案d是根据实施方案c所述的制品,其中第一角度为约70°。实施方案e是根据前述实施方案中任一项所述的制品,其中第二角度大于50°,并且小于或等于约85°,该第二角度由中心轴线以及从内周边延伸并穿过过渡平面的最短线限定。实施方案f是根据实施方案e所述的制品,其中第二角度为约65°至约75°。实施方案g是根据实施方案f所述的制品,其中第二角度为约68°至约72°。实施方案h是根据实施方案g所述的制品,其中第二角度为约70°。实施方案i是根据前述实施方案中任一项所述的制品,其中当沿着中心轴线测量时,过渡平面设置成远离平台部分的约60μm至约490μm。实施方案j是根据实施方案i所述的制品,其中当沿着中心轴线测量时,过渡平面设置成远离平台部分的约150μm至约350μm。实施方案k是根据实施方案j所述的制品,其中当沿着中心轴线测量时,过渡平面设置成远离平台部分的约200μm至约300μm。实施方案l是根据实施方案k所述的制品,其中当沿着中心轴线测量时,过渡平面设置成远离平台部分的约250μm至约270μm。实施方案m是一种制品,其包括:第一侧面,该第一侧面包括中心腔体部分和从第一侧面突出且与中心腔体部分不共面的平台部分;与第一侧面相背对的第二侧面;以及从平台部分沿第一方向延伸的至少三根空心微针;其中平台部分基本上围绕中心腔体部分;其中平台部分包括中心腔体部分近侧的内周边和中心腔体部分远侧的外周边;其中所述至少三根空心微针中的每一根包括主体,所述主体包括:外表面;具有基部和第一形状的基部区段,该第一形状由外表面的第一节段限定;具有尖端和第二形状的尖端区段,所述第二形状由所述外表面的第二节段限定,其中所述第二形状不同于所述第一形状;勾出所述基部区段和所述尖端区段轮廓的过渡平面;以及中心轴线;其中至少三根空心微针中的每一根包括从基部至尖端所测量的高度;其中至少三根空心微针中的每一根的尖端区段限定至少三根空心微针中的至少一根的高度的至少约45%。实施方案n是根据实施方案m所述的制品,其中至少三根空心微针中的每一根的尖端区段限定至少三根空心微针中的至少一根的高度的约60%至约85%。实施方案o是根据实施方案n所述的制品,其中至少三根空心微针中的每一根的尖端区段限定至少三根空心微针中的至少一根的高度的约70%至约80%。实施方案p是根据实施方案m至o中任一项所述的制品,其中基部区段为圆锥体形并且尖端区段为基本上圆柱形。实施方案q是根据实施方案m至实施方案p中任一项所述的制品,其中高度包括与基部区段相关联的第一高度分量,以及与尖端区段相关联的第二高度分量;其中第二高度分量为约540μm至约1240μm。实施方案r是根据实施方案q所述的制品,其中第二高度分量为约540μm至约940μm。实施方案s是根据实施方案r所述的制品,其中第二高度分量为约640μm至约840μm。实施方案t是根据实施方案s所述的制品,其中第二高度分量为约700μm至约800μm。实施方案u是根据实施方案q至t中任一项所述的制品,其中第一高度分量为约250μm至约270μm。实施方案v是根据前述实施方案中任一项所述的制品,其中第一侧面还包括从平台部分的外周边的至少一部分侧向延伸的不含微针的周边部分,其中周边部分在与第一方向相反的第二方向上远离平台部分倾斜。实施方案w是根据前述实施方案中任一项所述的制品,其中制品还包括从所述平台部分延伸或者,从所述周边部分(如果存在)延伸的侧壁部分,其中所述侧壁部分基本上沿与所述第一方向相反的方向延伸。实施方案x是根据前述实施方案中任一项所述的制品,其中中心腔体为闭合的腔体。实施方案y是根据实施方案a至w中任一项所述的制品,其中中心腔体是从第一侧面延伸穿过第二侧面的通孔。实施方案z是根据前述实施方案中任一项所述的制品,其中平台是环形的或者漩涡状的。实施方案aa是根据前述实施方案中任一项所述的制品,其中微针阵列是环形的或者漩涡状的。实施方案ab是根据前述实施方案中任一项所述的制品,其中单一主体包括平台部分、周边部分以及中心腔体部分。实施方案ac是根据前述实施方案中任一项所述的制品,其中多根微针中的至少一根微针包括:基部;具有中心轴线和主体直径的细长主体;尖端部分,该尖端部分包括尖端、相对于中心轴线呈对角地取向并且延伸穿过主体直径的至少75%的第一斜面、基本上垂直于中心轴线取向且与第一斜面相交的第二斜面、由第一斜面的第一边缘和第二斜面的第二边缘限定的斜开口;以及空心通道,该空心通道从斜开口轴向延伸到主体中。实施方案ad是根据前述实施方案中任一项所述的制品,其中多根微针中的至少一根微针包括:基部;具有中心轴线的细长主体;尖端部分,该尖端部分包括尖端、斜面以及斜面中的斜开口;第一通道,该第一通道从斜开口轴向延伸穿过细长主体的至少一部分,其中第一通道具有与中心轴线基本上对齐的第一壁;以及第二通道,所述第二通道从所述第一通道径向延伸到所述斜开口,其中所述第二通道具有被取向成基本上与所述中心轴线正交的第二壁;其中所述第一通道和所述第二通道合并以形成所述斜开口。实施方案ae是根据前述实施方案中任一项所述的制品,其中至少一根微针包括从靠近尖端的第一开口穿过制品延伸到制品的第二侧面中的第二开口的空心通道。实施方案af是根据前述实施方案中任一项所述的制品,该制品用于将流体注射到身体中。实施方案ag是根据实施方案a至ae中任一项所述的制品,该制品用于从体内抽取流体。实施方案ah是一种注射及输注设备,包括:根据前述实施方案中任一项所述的空心微针阵列制品;空心微针阵列制品保持件;第一储能部件,该第一储能部件被构造成用于使空心微针阵列制品从第一位置移动至第二位置;以及含有流体的贮存器,该贮存器与空心微针流体连通;其中设备被构造成用于以预先确定的速度沿预先确定的方向推进制品。实施方案ai是根据实施方案ah所述的注射及输注设备,其中贮存器被构造成用于保持约0.2ml至约5.0ml的流体体积。实施方案aj是根据实施方案ai所述的注射及输注设备,其中贮存器被构造成用于保持约0.2ml至约3.0ml的流体体积。实施方案ak是根据实施方案aj所述的注射及输注设备,其中贮存器被构造成用于保持约0.2ml至约2.0ml的流体体积。实施方案al是根据实施方案ak所述的注射及输注设备,其中贮存器被构造成用于保持约0.5ml至约2.0ml的流体体积。实施方案am是根据实施方案ah至al中任一项所述的注射及输注设备,其中预先确定的速度为约2m/s至约20m/s。实施方案an是根据实施方案am所述的注射及输注设备,其中预先确定的速度为约4m/s至约12m/s。实施方案ao是根据实施方案an所述的注射及输注设备,其中预先确定的速度为约6m/s至约9m/s。实施方案ap是根据实施方案ao所述的注射及输注设备,其中预先确定的速度为约7m/s至约8m/s。实施方案aq是根据实施方案ah至ap中任一项所述的注射及输注设备,还包括致动器,该致动器致动空心微针阵列制品从第一位置移动至第二位置。实施方案ar是根据实施方案ah至aq中任一项所述的设备,还包括第二储能部件,该第二储能部件被构造成用于提供使流体从贮存器移动至并通过空心微针的力。实施方案as是一种方法,其包括:提供根据实施方案aq或实施方案ar所述的注射及输注设备;致动致动器以将空心微针插入穿过皮肤表面。实施方案at是根据从属于实施方案ar的实施方案as所述的方法,还包括释放第二储能部件的储能的至少一部分以使流体从贮存器移动通过空心微针并且进入皮肤表面下面的组织中。实施方案au是根据实施方案as或实施方案at所述的方法,其中将空心微针插入穿过皮肤表面包括将空心微针插入至皮肤表面下面的约580μm至750μm的深度。实施例实施例1:微针制品的加工成形。微针制品使用标准注塑过程由聚合物材料制备而成。模制的微针制品使用模具组件制备而成,该模具组件由三个模段制得,其中每个模段由钢加工而成。第一模段包括限定模制阵列中针尖端的斜面形状的突起。第一模段中的每个突起具有限定微针尖端的尖端区段的特征结构的另外的圆柱形伸出部,该圆柱形伸出部包括靠近微针尖端的斜面上的开口和延伸穿过每根微针的主体的空心通道的一部分。第二模段用作模板来限定模制制品中微针的图案、模制制品中微针的外部形状和尺寸、和制品的第一侧面(包括中心腔体部分、平台部分、和周边部分,如上所述)。第三模段含有从平坦表面显现的圆柱形突起,其中每个突起限定微针空心通道的第二(基部近侧的)部分和位于模制制品中的每根微针基部处的开口。突起从中显现的平坦表面用于限定模制制品的基部区段的第二主表面。通过将第一模段的突起插入第二模段中的对应开口内,将第一模段和第二模段组装以形成紧密配合。所组装的第一模段和第二模段形成第一模具半部。将第三模段用作第二模具半部。在20或40吨的注塑机中将第一模具半部和第二模具半部安装在模具基部中。如本领域通用那样,模具组件的分模线具有用于在注射聚合物材料期间一般空气排出的主通风口和副通风口二者。将vectramt1300液晶聚合物(lcp)球剂(肯塔基州佛罗伦萨的泰科纳工程聚合物公司(ticonaengineeringpolymers,florence,ky))装载到螺杆内并加热直至熔融。将第一模具半部和第二模具半部加热至约140-248°f(60-120℃)的温度范围(下文中称为“注射时的模具温度”)。模制周期通过闭合第一模具半部与第二模具半部开始。用大约20至40吨的力将模具夹紧在一起。在夹紧位置中,第二模具半部中的突起尖端处的表面与第一模具半部的突起的尖端处的表面对齐并接触。以约7英寸/秒(17.8厘米/秒)的固定速度(下文中称为“注射速度”)将材料的总量的第一部分(大约50-99%的部件尺寸体积)注入模室中。在注射第一部分的材料后,通过施加约3,000-13,500psi(20,684-93,079千帕)范围内的固定压力(下文中称为“充填压力”)来迫使剩余的熔融材料进入凹模插入物中,使方法从注射驱动切换到压力驱动模式。充填压力施加2-6秒的固定时间(下文中称为“保持时间”)。随后释放充填压力并且使模室冷却至设定成低于lcp的软化温度的排出温度。打开模室并排出微针制品。实施例2:用于测试微针制品的注射施用装置。使用了与国际专利申请公布w02014/193725(参见图1-26)中所述的设备类似的完全组装的浅外形微针制品注射及输注设备。所有的注射及输注设备被制造成同一规格。每个注射及输注设备的外部壳体的总体长度为约122.8mm,在设备的圆形节段(含有微针阵列保持件的设备节段)中具有约40.5mm的宽度。注射及输注设备的容纳在细长节段(含有注射组件)中的宽度为约22.8mm。通向致动器腔体的外部开口具有约18mm的直径测量值。每个注射及输注设备中的玻璃料筒含有2ml的0.005%亚甲基蓝的5%右旋糖水溶液。每个料筒的长度为约46mm并且具有约9.7mm的内径尺寸。用于移动微针阵列保持件并将微针插入皮肤中的第一储能装置为在待命(预致动)状态下具有12.5n力的卷簧。用于引发梭动件的移动的第二储能装置为在待命(预致动)状态下具有16.5n力的卷簧。用于输注亚甲基蓝染料的第三储能装置为在待命(预致动)状态下具有15n力的卷簧。使用本文所述的注射和注入设备,在皮肤表面处的微针的速度为约7.4±1.4m/s。微针制品注射及输注设备中使用的空心微针制品(如图1所示)以直径为大约1.25cm(图8的尺寸d3)的圆形从vectramt1300液晶聚合物(lcp)中(如实施例1所述的那样)模制而成。圆形平台部分从制品的外侧边缘突出约1.0mm(图2的高度h1)并且周边部分相对于平台部分的平面以36.9度斜面远离平台部分倾斜。制品的闭合圆形腔体在制品的中心,其具有约6.8mm的直径(由平台的内周边所形成的圆形区域限定的直径量度d1(图8)),在腔体中心处具有约500微米的深度,以及约11mm的曲率半径。由平台的外周边形成的圆形区域的直径为约10.3mm(图8中的尺寸d2)。平台的宽度为约1.75mm(图11中的尺寸d4)。制品的特征为从制品的圆形平台部分延伸的12根空心微针的阵列。微针被均匀地间隔开,其中相邻微针之间的距离为约2.2mm(如从尖端至尖端所测量的)。每根微针被取向成使得尖端处的开口沿径向向量面朝制品的外周边。每根微针在基部处的外径为约0.45mm。每根微针的扩张基部区段具有约1mm的曲率半径。每根微针的尖端区段呈具有约25度斜面和具有70度夹角的倒角尖端的常规皮下注射针的形状。尖端附近的开口为长圆形形状(如图2a所示),并且尺寸为约200微米×80微米。每根微针具有约1000微米的总高度,如从平台表面处的微针的基部至微针的尖端所测量的那样。尖端区段的长度(如从尖端至从基本上圆柱形的尖端区段勾出扩张基部区段轮廓的过渡平面所测量的)为约739微米。尖端区段的中点处的外径为约254微米。从每根微针的尖端至尖端附近的开口的中心的距离为约270微米。穿过每根微针的尖端区段的空心通道的平均直径为约80微米。角θ(θ1,如图5a所示)为70.0度。实施例3:使用微针制品注射物质。使用约克郡(yorkshire)杂交家猪(明尼苏达州吉本市的midwestresearchswine(midwestresearchswine,gibbon,mn))在活的有机体内进行研究。选择后腿区域作为用于微针插入的施用部位。首先用电推剪修剪施用部位,并且随后用剃刀和剃须膏进行剃刮。用肥皂水和buf-puf剥落海绵(明尼苏达州圣保罗的3m公司(3mcompany,st.paul,mn))擦洗剃刮区域并且随后用去离子水冲洗。将动物以侧卧位放置在加热的桌子(38℃)上。用异氟烷气体将动物麻醉,并在整个实验期间使其维持在麻醉状态下。随后用70%异丙醇的水溶液擦拭施用部位。使用实施例2的注射设备。从设备的皮肤触压粘合剂部分中移除剥离衬件并将设备粘附至猪的皮肤。将设备致动以使得阵列保持元件依序剥离、将微针制品的微针插入猪皮肤内并且将亚甲基蓝溶液注射到猪中。在完成注射之后,使设备在皮肤上再保持一分钟。记录将整个样品注射到动物中所需的时间。将设备从皮肤移除并检查皮肤表面以确定皮肤表面上是否存在任何亚甲蓝溶液。皮肤上存在亚甲蓝溶液表明未将全部亚甲蓝注射到动物内。将亚甲基蓝溶液的其余部分保留在料筒中。结果示于表1中。总共进行十次重复。注射时间在94至237秒范围内,其中平均注射时间为157秒。在九次测试中,将所有亚甲基蓝溶液注射到动物中。在一次测试中,将98.9%的亚甲基蓝溶液注射到动物中。表1:注射时间(实施例3)。测试编号注射时间(秒)注射的亚甲基蓝的百分比1183100218510032371004185100520710061111007148100811910099998.91094100实施例4:微针制品的使用。进行研究以确定制品的微针在施用于约克郡(yorkshire)杂交家猪(midwestresearchswine)的皮肤表面时(在活的有机体内)的刺入深度(dop)。使用如实施例2中所述的空心微针制品。使用三步方法涂布制品上的微针。前两个步骤涉及将底漆涂层施用于微针并且第三步骤涉及将薄的若丹明b涂层施用于微针。在步骤1中,用包含0.5mg/ml聚乙烯醇(80%水解)(密苏里州圣路易斯的西格玛奥德里奇公司(sigma-aldrich,inc.,st.louis,mo))和35μg/ml的80(西格玛奥德里奇公司(sigma-aldrich))90%(w/v)乙醇的35微升溶液灌涂制品。随后将带涂层的制品在35℃下干燥20分钟。在步骤2中,用35微升的33.3mg/ml硫酸钾铝(新泽西州利文斯顿的百腾制造公司(pentamanufacturing,livingston,nj))水溶液灌涂步骤1的制品。随后将带涂层的制品在35℃下干燥30分钟。在步骤3中,用40微升的0.08%(w/v)若丹明b(西格玛奥德里奇公司(sigma-aldrich))水溶液灌涂步骤2的底漆制品。将带涂层的制品在35℃下干燥30分钟。该三步方法提供了制品,其中微针用薄型的不透明若丹明b涂层完全覆盖。选择后腿区域作为用于微针插入的施用部位。首先用电推剪修剪施用部位,并且随后用剃刀和剃须膏进行剃刮。用肥皂水和buf-puf剥落海绵(3m公司(3mcompany))擦洗剃刮区域并且随后用去离子水冲洗。将动物以侧卧位放置在加热的桌子(38℃)上。用异氟烷气体将动物麻醉,并在整个实验期间使其维持在麻醉状态下。随后用70%异丙醇的水溶液擦拭施用部位。使用具有若丹明b涂覆制品的实施例2中所述的注射设备。唯一不同的是使用空料筒,而不是填充有亚甲基蓝的料筒。从设备的皮肤触压粘合剂部分中移除剥离衬件并将设备粘附至猪的皮肤。将设备致动以使得阵列保持元件剥离并将微针制品的微针插入猪的皮肤内。使注射设备在皮肤上再保持5分钟。从动物上移除注射设备。通过测量从微针尖端到在施用至皮肤中后从微针擦拭掉或溶解掉的若丹明b涂层的位置的距离来间接地确定微针至猪皮肤中的刺入深度(dop)。使用放大率为100x的nikonlv-100显微镜(纽约州梅尔维尔市的尼康仪器公司(nikoninstruments,melville,ny))和imageplus数字图像分析软件(马里兰州贝塞斯达市的mediacybernetics公司(mediacybernetics,bethesda,md))进行测量。总共测试了五个微针制品。通过对来自每个制品的全部微针(n=60)进行取样来确定平均微针dop。结果示于表2中。表2:将微针制品施用于后腿区域时的刺入深度(dop)(实施例4)平均dop665微米标准偏差80微米%rsd12%本文引用的所有专利、专利申请和公布的全部公开内容以及可供使用的电子版材料均以引用方式并入。在本申请的公开内容和以引用的方式并入本文的任何文献的公开内容之间存在任何不一致的情况下,应以本申请的公开内容为准。上述具体实施方式和实施例仅为清楚理解本发明而给出。而不应被理解为不必要的限制。本发明不限于示出的和描述的具体细节,对本领域的技术人员而言显而易见的变型形式将包括在由权利要求书所限定的本发明中。所有的标题是为了阅读者方便,而不应该用于限制该标题后面的正文的含义,除非如此规定。在不脱离本发明的实质和范围的前提下,可进行各种修改。这些以及其它实施方案均在以下权利要求书的范围内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1