一种由川芎嗪制备的含药血清及其制备方法和应用与流程
本发明属于生物药物领域,具体涉及一种由川芎嗪制备的含药血清及其制备方法和在治疗骨肉瘤上的应用。
背景技术:
骨肉瘤是小儿骨肿瘤中最为常见的骨肉瘤类型。骨肉瘤来源于间充质细胞,其优先定位于具有高生长潜力的大骨骼,如股骨或胫骨,且原发性骨肉瘤易扩散至肺部成为患者的主要死亡原因。十九世纪七十年代以前,对于未转移的肢体骨肉瘤基本采取截肢手术进行治疗,且五年内的生存率仍然难以达到20%。骨肉瘤的约占人类恶性实体肿瘤总发病率的0.2%,在原发性的恶性骨肿瘤中,骨肉瘤的发病率占恶性肿瘤首位。骨肉瘤的发病率男性明显多于女性,且多发于15-25岁之间。然而多数骨肉瘤恶性程度高,预后差。近20年来,尽管国内外很多研究机构都进行了大量的相关研究,但骨肉瘤的治疗依然停滞不前。近年来,许多学者在中药提取物对骨肉瘤细胞系体外培养生长的抑制作用以及对细胞周期、细胞凋亡、迁移能力的影响等方面作了很多的探索并有了新进展,为新的植物型药物的发现和研制提供了线索,也为本发明提供了新的思路。
中医治疗肿瘤的重要方法之一是活血化瘀法。以中医理论对骨肉瘤进行分析,认为“气滞血瘀,痰湿凝聚”是其病机关键。川芎能够活血行气,是搜风定痛、调经活血的常用药物,而川芎嗪(TMP)是其有效成分之一。川芎嗪具有扩张血管、抗血小板凝集、改善血液流变性、抗脂质氧化及清除氧自由基等功效。有报道称川芎嗪具有抑制前列腺癌、宫颈癌、乳腺癌、白血病等多种恶性肿瘤的作用,因此川芎嗪的抗肿瘤作用越来越多的受到学者们的重视。目前已有实验证实川芎嗪具有抑制实体瘤生长转移、降低肿瘤组织微血管密度,体外抑制血管内皮细胞增殖以及抑制血管内皮生长因子(VEGF)诱导的血管内皮细胞增殖的作用。
近年来,中药血清药理学的相关研究在中药或中药复方研究中有了新的进展,它主要是通过模拟中药或中药复方在体内消化、吸收、转化、代谢的一些过程,然后通过采集服用(或注射)中药的动物的血液并分离血清,进行体外培养实验研究的一种新的方法。中药服用或注射的方法及简称如下:静脉注射(iv)、腹腔注射(ip)、口服(po)、皮下注射(ih)、灌胃(ig)、肌注(im)、静滴(iv)等。这种实验方法的提出,既可以在一定程度上排除中药或中药复方直接进行体外实验被产生的难以确定的因素干扰,也可以使实验结果的可信度大大提高。这种实验方法的提出,既可以在一定程度上排除中药或中药复方直接进行体外实验产生的难以确定的因素干扰,也可以使实验结果的可信度大大提高,更重要的是中药血清使疗效更加显著。吴风青对结肠癌患者给予用奥沙利铂(OXA)、亚叶酸钙(CF)和氟尿嘧啶(5-Fu)组成的folfox6方案化疗4疗程,根治术前用川芎嗪100mg静点15天,术后取结肠癌标本用免疫组化法分别染色多药耐药相关蛋白P-糖蛋白(Pgp),检测其表达,经研究发现川芎嗪对结肠癌多药耐药性基因表达有抑制作用。万慧芳等人使用不同浓度川芎嗪分别作用于LoVo结肠癌细胞48h,并观察川芎嗪对细胞凋亡率、PUMA、Bax、及Bcl-2基因表达的影响,发现其具有抑制人结肠癌LoVo细胞增殖及促凋亡作用。丰俊东等按大鼠体重比腹腔注射(ip注射)一定剂量川芎嗪之后经处理得到川芎嗪含药血清,使用其培养HepG2人肝癌细胞一段时间后检测得知TMP含药血清对人肝癌细胞Hep G2增殖有一定的抑制作用。黄永明等人通过研究发现单纯六味地黄汤含药血清对CIK细胞基本无诱导作用,联合细胞因子有促进CIK细胞的体外扩增作用,对KH-0S成骨肉瘤细胞株有较强的杀伤活性,且与浓度相关。目前常见的骨肉瘤细胞系有Saos-2、MG-63、M663、U2-OS、143B,HOS、SOSP-9607,F5M2、F4、MNNG/HOS、SW1353、UMR106等。但暂未发现使用川芎嗪制备的含药血清对MG-63人成骨肉瘤细胞做相关研究的报道。
技术实现要素:
发明目的:针对现有技术存在的问题,本发明提供一种由川芎嗪制备的含药血清;该含药血清可有效抑制骨肉瘤细胞的增殖、促进其凋亡、抑制其转移。
本发明还提供一种由川芎嗪制备的含药血清的制备方法及其应用。
技术方案:为了实现上述目的,如本发明所述的一种由川芎嗪制备的含药血清,所述含药血清为将盐酸川芎嗪注射液对大鼠进行注射后,采血得到。
其中,所述盐酸川芎嗪注射液按大鼠体重比(70-140)mg/kg进行注射。
所述所大鼠为清洁级SD雄性大鼠,大鼠购自扬州大学比较医学中心,体重为250~400g。
本发明所述的由川芎嗪制备的含药血清的制备方法,包括如下步骤:
(1)给大鼠按体重比注射盐酸川芎嗪注射液(70-140)mg/kg;
(2)末次注射后0.5-2h对大鼠进行麻醉,无菌条件下经腹主动脉采血;
(3)将血液静置4-8h,离心,取上清,灭活后过滤除菌,得到含药血清,分装,冻存备用。
作为优选,步骤(1)所述注射为每日注射1-2次,连续5-7d,末次禁食12-14h注射。
作为优选,步骤(3)所述离心为3000-5000rpm,4-6℃离心10-15min。
作为优选,步骤(3)所述灭活为56-60℃灭活25-30min。
作为优选,步骤(3)所述过滤除菌为通过滤膜过滤除菌,优选为0.22μm的滤膜。
本发明所述的由川芎嗪制备的含药血清在制备治疗骨肉瘤的药物中应用。
进一步地,所述由川芎嗪制备的含药血清在制备治疗MG-63人成骨肉瘤细胞的药物中应用。
有益效果:与现有技术相比,本发明具有如下优点:
1、本发明由川芎嗪制备的含药血清根据川芎嗪活血行气,搜风定痛、调经活血的功能,可有效抑制骨肉瘤细胞的增殖、促进其凋亡、抑制其转移。
2、本发明以MG-63人成骨肉瘤细胞作为模型,使用川芎嗪注射大鼠后处理得到的含药血清培养MG-63人成骨肉瘤细胞,对于抑制骨肉瘤细胞的增殖、促进其凋亡、抑制其转移的效果明显要优于川芎提取物以及现有治疗骨肉瘤的药物;其中给大鼠按体重比注射盐酸川芎嗪(70-140)mg/kg制备的含药血清,取浓度为10%(与DMEM培养基体积比)的含药血清抑制MG-63人成骨肉瘤细胞存活率可以达到23.79%以下,促进MG-63人成骨肉瘤细胞存活率凋亡率达到40.78%以上;而盐酸川芎嗪和现有治疗骨肉瘤的药物抑制细胞存活率最好的效果仅为73.12%、42.54%和42.16%,盐酸川芎嗪和现有治疗骨肉瘤的药物促进凋亡率最好的效果为15.74%、19.15%和18.24%;同时该含药血清可以有效的抑制MG-63人成骨肉瘤细胞的迁移能力,从而验证其具有抑制骨肉瘤的良好效果;本发明川芎嗪制备的含药血清制备的药物在治疗骨肉瘤时也具有显著的效果。
3、本发明的制备方法安全可控,并且便于操作、保管、贮存和运输。
附图说明
图1为将实施例4给大鼠按体重比注射盐酸川芎嗪140mg/kg制备的含药血清以及对照组孵育MG-63人成骨肉瘤细胞,Transwell细胞迁移检测细胞迁移能力的示意图;
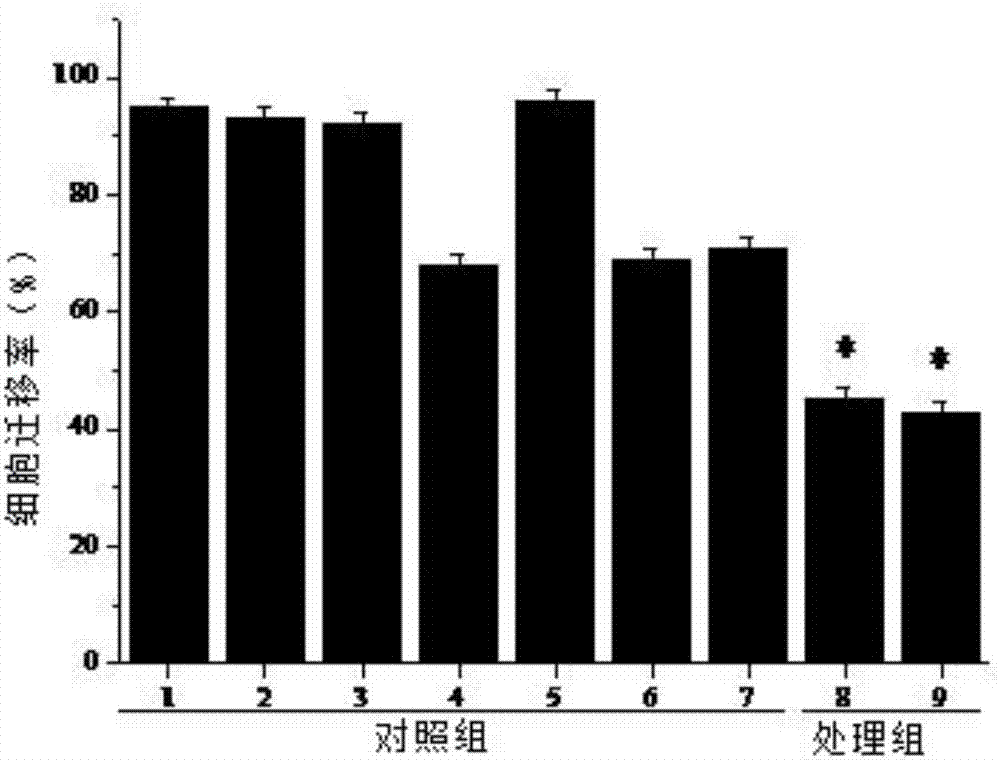
图2为将实施例5给大鼠按体重比注射盐酸川芎嗪105mg/kg制备的含药血清以及对照组孵育MG-63人成骨肉瘤细胞,Transwell细胞迁移检测细胞迁移能力的示意图;
图3为将实施例6给大鼠按体重比注射盐酸川芎嗪70mg/kg制备的含药血清以及对照组孵育MG-63人成骨肉瘤细胞,Transwell细胞迁移检测细胞迁移能力的示意图。
具体实施方式
以下结合实施例和附图对本发明作进一步说明。
实施例1
由川芎嗪制备的含药血清
(1)给400g清洁级SD雄性大鼠按体重比注射盐酸川芎嗪140mg/kg,每日1次,持续7d,末次禁食12h注射;盐酸川芎嗪注射液购买于山东潍坊制药有限公司;
(2)末次灌胃后2h对大鼠使用质量分数为3.5%的水合氯醛(3.5g水合氯醛,用蒸馏水溶解,再用蒸馏水稀释到100mL,按小鼠体重比注射0.9mL/100g,即100g的小鼠需要注射0.9mL上述水合氯醛)对大鼠进行麻醉,无菌条件下经腹主动脉采血;
(3)将血液静置8h,5000rpm,4℃离心10min,取上清,60℃灭活25min后通过0.22μm滤膜过滤除菌,得含药血清,分装,冻存于-80℃冰箱备用。
实施例2
由川芎嗪制备的含药血清
(1)给300g清洁级SD雄性大鼠按体重比注射盐酸川芎嗪105mg/kg,每日2次,持续5d,末次禁食12h注射;
(2)末次灌胃后1h对大鼠使用质量分数为3.5%的水合氯醛(0.9mL/100g)对大鼠进行麻醉,无菌条件下经腹主动脉采血;
(3)将血液静置8h,5000rpm,4℃离心10min,取上清,60℃灭活25min后通过0.22μm滤膜过滤除菌,得含药血清,分装,冻存于-80℃冰箱备用。
实施例3
由川芎嗪制备的含药血清
(1)给250g清洁级SD雄性大鼠按体重比注射盐酸川芎嗪70mg/kg,每日1次,持续7d,末次禁食14h注射;
(2)末次灌胃后1h对大鼠使用质量分数为3.5%的水合氯醛(0.9mL/100g)对大鼠进行麻醉,无菌条件下经腹主动脉采血;
(3)将血液静置4h,3000rpm,4℃离心15min,取上清,56℃灭活30min后通过0.22μm滤膜过滤除菌,得含药血清,分装,冻存于-80℃冰箱备用。
实施例4
将实施例1给大鼠按体重比注射盐酸川芎嗪140mg/kg后处理得到的含药血清孵育MG-63人成骨肉瘤细胞;
将MG-63人成骨肉瘤细胞解冻复苏后加入含有(体积比)10%胎牛血清(FBS)的DMEM培养基制成细胞悬液,分种于培养瓶中并置于5%CO2(细胞培养的常规环境,CO2体积分数为5%),饱和湿度95%,37℃培养箱中培养。正常培养时约每天更换1次培养液,等到细胞生长融合度达到70%-80%时进行传代培养;传代培养时首先弃去培养瓶中的旧培养液,加入37℃磷酸缓冲盐溶液(PBS)液洗瓶2次,在25cm2培养瓶中加入2mL浓度为0.25%的胰蛋白酶(即2.5g/L的胰蛋白酶溶液)进行消化。然后在倒置显微镜下仔细随时观察,当发现细胞质回缩、细胞间隙变大时终止消化。接下来弃去胰酶溶液,加入含(体积比)10%胎牛血清的DMEM培养基,之后用吸管轻柔吹打使贴壁细胞悬浮。紧接着将含悬浮细胞的培养液转移至10mL离心管中,1500rpm离心5min,弃上清液。将细胞重新悬浮于5mL含(体积比)10%胎牛血清的完全培养基中。细胞计数结束,选择合适浓度将细胞分装到新的无菌培养瓶进行培养。最后6h后可见细胞贴壁,以后每2-3天换液次,待细胞长滿瓶底70%-80%后再次消化传代。
取4-6代的生长良好,融合度约为60%-70%的细胞进行细胞实验。呈亚融合状态的细胞,轻柔吹打配成单细胞悬液并接种于96孔培养板,24孔培养板以及Tranwell铺板,细胞贴壁生长24h后用各个分组对MG-63人成骨肉瘤细胞进行孵育24h处理,具体分组情况如下:
对照组(共设7组,组1-组7):
1、空白对照组:用无血清DMEM培养液孵育细胞24h;
2、胎牛血清对照组:DMEM培养液中仅加入血清(所述血清为标准胎牛血清,购自杭州四季青生物科技有限公司),血清浓度(体积比)为10%,该DMEM培养液孵育细胞24h;
3、空白血清对照组:DMEM培养液中仅加入血清(血清采集方法与实施例1相同,不同在于没有注射),血清浓度(体积比)为10%,该DMEM培养液孵育细胞24h;
4、川芎嗪对照组:用盐酸川芎嗪与没有注射的大鼠得到的血清进行混合(血清采集方法与实施例1相同,不同在于没有注射,盐酸川芎嗪与实施例1的大鼠体重的重量比为140mg/kg),然后加入到DMEM培养液中,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
5、生理盐水对照组:给大鼠按体重比注射生理盐水140mg/kg得到的血清(血清采集方法与实施例1相同,不同之处盐酸川芎嗪换成生理盐水)加入到DMEM培养液中加入,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
6、现有药物对照组Ⅰ:用现有治疗骨肉瘤药物顺铂注射液与没有注射的大鼠得到的血清进行混合(血清采集方法与实施例1相同,不同在于没有注射,顺铂注射液与实施例1的大鼠体重的重量比为140mg/kg),然后加入到DMEM培养液中,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
7、现有药物对照组Ⅱ:给大鼠按体重比注射顺铂注射液140mg/kg得到的血清(血清采集方法与实施例1相同,不同之处盐酸川芎嗪换成顺铂注射液)加入到DMEM培养液中加入,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
处理组(共设2组,组8和组9):
按实施例1给大鼠按体重比注射盐酸川芎嗪140mg/kg制得的含药血清加入到DMEM培养液中,配制出含药血清浓度(体积比)为10%和15%两种DMEM培养液,分别用浓度10%和15%含药血清DMEM培养液孵育细胞24h。
实施例5
将实施例2给大鼠按体重比注射盐酸川芎嗪105mg/kg后处理得到的含药血清孵育MG-63人成骨肉瘤细胞,具体的细胞培养方法与实施例4相同。
对照组(共设7组,组1-组7):
1、空白对照组:用无血清DMEM培养液孵育细胞24h;
2、胎牛血清对照组:DMEM培养液中仅加入血清(所述血清为标准胎牛血清,购自杭州四季青生物科技有限公司),血清浓度(体积比)为10%,该DMEM培养液孵育细胞24h;
3、空白血清对照组:DMEM培养液中仅加入血清(血清采集方法与实施例2相同,不同在于没有注射),血清浓度(体积比)为10%,该DMEM培养液孵育细胞24h;
4、川芎嗪对照组:用盐酸川芎嗪与没有注射的大鼠得到的血清进行混合(血清采集方法与实施例2相同,不同在于没有注射,盐酸川芎嗪与实施例2的大鼠体重的重量比为105mg/kg),然后加入到DMEM培养液中,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
5、生理盐水对照组:给大鼠按体重比注射生理盐水105mg/kg得到的血清(血清采集方法与实施例2相同,不同之处盐酸川芎嗪换成生理盐水)加入到DMEM培养液中加入,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
6、现有药物对照组Ⅰ:用现有治疗骨肉瘤药物顺铂注射液与没有注射的大鼠得到的血清进行混合(血清采集方法与实施例2相同,不同在于没有注射,顺铂注射液与实施例2的大鼠体重的重量比为105mg/kg),然后加入到DMEM培养液中,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
7、现有药物对照组Ⅱ:给大鼠按体重比注射顺铂注射液105mg/kg得到的血清(血清采集方法与实施例1相同,不同之处盐酸川芎嗪换成顺铂注射液)加入到DMEM培养液中加入,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
处理组(共设2组,组8和组9):
按实施例2给大鼠按体重比注射盐酸川芎嗪105mg/kg制得的含药血清加入到DMEM培养液中,配制出含药血清浓度(体积比)为10%和15%两种DMEM培养液,分别用10%和15%含药血清DMEM培养液孵育细胞24h。
实施例6
将实施例3给大鼠按体重比注射盐酸川芎嗪70mg/kg后处理得到的含药血清孵育MG-63人成骨肉瘤细胞,具体的细胞培养方法与实施例4相同。
对照组(共设7组,组1-组7):
1、空白对照组:用无血清DMEM培养液孵育细胞24h;
2、胎牛血清对照组:DMEM培养液中仅加入血清(所述血清为标准胎牛血清,购自杭州四季青生物科技有限公司),血清浓度(体积比)为10%,该DMEM培养液孵育细胞24h;
3、空白血清对照组:DMEM培养液中仅加入血清(血清采集方法与实施例3相同,不同在于没有灌胃),血清浓度(体积比)为10%,该DMEM培养液孵育细胞24h;
4、川芎嗪对照组:用盐酸川芎嗪与没有注射的大鼠得到的血清进行混合(血清采集方法与实施例3相同,不同在于没有注射,盐酸川芎嗪与实施例3的大鼠体重的重量比为70mg/kg),然后加入到DMEM培养液中,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
5、生理盐水对照组:给大鼠按体重比注射生理盐水70mg/kg得到的血清(血清采集方法与实施例3相同,不同之处盐酸川芎嗪换成生理盐水)加入到DMEM培养液中加入,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
6、现有药物对照组Ⅰ:用现有治疗骨肉瘤药物顺铂注射液与没有注射的大鼠得到的血清进行混合(血清采集方法与实施例3相同,不同在于没有注射,顺铂注射液与实施例3的大鼠体重的重量比为70mg/kg),然后加入到DMEM培养液中,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
7、现有药物对照组Ⅱ:给大鼠按体重比注射顺铂注射液70mg/kg得到的血清(血清采集方法与实施例1相同,不同之处盐酸川芎嗪换成顺铂注射液)加入到DMEM培养液中加入,血清浓度(体积比)为10%,用该DMEM培养液孵育细胞24h;
处理组(共设2组,组8和组9):
按实施例3给大鼠按体重比注射盐酸川芎嗪70mg/kg制得的含药血清加入到DMEM培养液中,配制出含药血清浓度(体积比)为10%和15%两种DMEM培养液,分别用10%和15%含药血清DMEM培养液孵育细胞24h。
试验例1MTT方法检测药物对Huh7肝癌细胞增殖活性的作用
MTT全称3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide,汉语化学名为3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐,是一种黄色的染料。处于增殖期的活细胞细胞线粒体中含有的琥珀脱氢酶,可使外源性的MTT还原成难溶的针状Formazan结晶,呈蓝紫色,并沉淀在活细胞中,细胞活力与Formazan的形成量成正比,DMSO能使Formazan结晶溶解,使用酶标仪于波长570nm处测定吸收值,以此间接反映细胞增殖的情况。在一定细胞数范围内,MTT结晶形成的量与细胞数成正比。
分别取实施例4,5,6各分组孵育后制备的96孔板的细胞,每孔定量加100μL含(体积比)15%胎牛血清(FBS)完全培养基;置于5%CO2,饱和湿度95%,37℃培养箱中进行培养24~72h;培养终止前4h加入10μL/孔(浓度为5mg/mL)的MTT;继续培养4h后,小心吸弃上清培养液后加100μL/孔二甲基亚砜(DMSO)终止反应,于振荡器上震荡10min左右,使结晶物充分溶解;酶标仪570nm检测OD值,实验至少重复三次。记录结果,计算存活率。
细胞存活率(%)=处理组平均OD值/对照组平均OD值×100%。
结果如1至3所示。
表1 140mg/kg的盐酸川芎嗪注射液注射大鼠时MTT法检测MG-63人成骨肉瘤细胞存活率
*表示与对照组比较差异显著
表2 105mg/kg的盐酸川芎嗪注射液注射大鼠时MTT法检测MG-63人成骨肉瘤细胞存活率
*表示与对照组比较差异显著
表3 70mg/kg的盐酸川芎嗪注射液注射大鼠时MTT法检测MG-63人成骨肉瘤细胞存活率
*表示与对照组比较差异显著
由表1-3可知,给大鼠按体重比分别注射盐酸川芎嗪140、105、70mg/kg制备得到的含药血清,当使用浓度(体积比)为10%和15%的含药血清时MG-63人成骨肉瘤细胞存活率可以达到23.79%和22.96%以下,与川芎嗪对照组的细胞存活率以及现有药物对照组的细胞存活率相比具有明显的优势,都具有很好的抑制MG-63人成骨肉瘤细胞存活效果,说明本发明实施例制备的含药血清具有良好的抑制MG-63人成骨肉瘤细胞的存活的作用。
由表2可知,给大鼠按体重比注射盐酸川芎嗪105mg/kg制得的含药血清效果最好,浓度为10%和15%含药血清组的细胞存活率分别是21.12%,21.23%;15%含药血清组时细胞存活率为21.23%,与10%含药血清组无统计学差异,因此,通过给大鼠按体重比注射盐酸川芎嗪105mg/kg制得的含药血清,使用浓度10%的含药血清就可以取得良好的抑制MG-63人成骨肉瘤细胞存活效果。
试验例2流式细胞术检测细胞凋亡
磷脂酞丝氨酸(PS)只分布在细胞膜脂质双层的内侧,而在细胞凋亡早期,细胞膜中的磷脂酰丝氨酸由脂膜内侧翻向外侧。在鞘液的约束和包围下,待测样本的细胞排成单列由流动室喷嘴高速喷出,而形成细胞液柱。液柱在通过检测区时,在入射激光束的照射下可产生侧向散射光(SSC)和前向散射光(FSC),它们分别反映细胞颗粒度和大小,根据这些特性将细胞分类。样本经一种或几种特殊荧光标记后,可在激光束的激发下产生特定荧光,该特定荧光可被光学系统检测并分析,由此得到相应的各种细胞特性。AnnexinV是一种分子量35~36kDa的Ca2+依赖性磷脂结合蛋白,与磷脂酰丝氨酸有高度亲和力,故可通过细胞外侧暴露的磷脂酰丝氨酸与凋亡早期细胞的胞膜结合。将AnnexinV进行FITC标记,以标记了AnnexinV作为荧光探针,利用流式细胞仪可检测细胞凋亡的发生。
分别取实施例4,5,6各分组孵育后制备的24孔板的细胞,弃去培养上清后加入每孔加入0.5mL浓度为0.25%的胰蛋白酶(即2.5g/L的胰蛋白酶溶液),在倒置显微镜下观察,待细胞开始变圆,加少量含血清培养液,终止消化,吹打悬浮细胞后移至离心管中,1000rpm下离心10min,弃上清,用预冷的PBS洗涤2次,用250μL结合缓冲液重悬细胞。调节其浓度为1×106/mL,取100μL细胞悬液于5mL流式管中,加入5μL AnnexinVFITC和10μL 20μg/mL的PI溶液,混匀后室温避光孵育15min,在反应管中加入400μL PBS,上流式细胞仪分析。实验结果经计算机软件ModFit LT3.0分析软件分析细胞周期细胞数,每组实验至少重复3次;结果见表4-6所示。
表4 140mg/kg的盐酸川芎嗪注射液注射大鼠时MG-63人成骨肉瘤细胞凋亡率的变化
*表示与对照组比较差异显著
表5 105mg/kg的盐酸川芎嗪注射液注射大鼠时MG-63人成骨肉瘤细胞凋亡率的变化
*表示与对照组比较差异显著
表6 70mg/kg的盐酸川芎嗪注射液注射大鼠时MG-63人成骨肉瘤细胞凋亡率的变化
*表示与对照组比较差异显著
由表4至6可知,给大鼠按体重比分别注射盐酸川芎嗪140、105、70mg/kg制备得到的含药血清,当使用浓度(体积比)10%和15%的含药血清时MG-63人成骨肉瘤细胞凋亡率可以达到40.78%和41.25%以上,与川芎嗪对照组的细胞凋亡率以及现有药物对照组的细胞凋亡率相比具有明显的优势,都可以使MG-63人成骨肉瘤细胞的凋亡率大大增加,说明本发明实施例制备的含药血清具有良好的促进MG-63人成骨肉瘤细胞的凋亡的作用。
由表5可知,给大鼠按体重比注射盐酸川芎嗪105mg/kg制得的含药血清效果最好,浓度为10%和15%含药血清组的细胞凋亡率分别是42.97%,43.15%效果最好;15%含药血清组时细胞凋亡率与10%含药血清组无统计学差异,因此,通过给大鼠按体重比注射盐酸川芎嗪105mg/kg制得的含药血清,使用其浓度为10%的含药血清就可以取得良好的促使MG-63人成骨肉瘤细胞凋亡效果。
试验例3 Transwell侵袭实验检测川芎嗪制备含药血清对细胞侵袭能力的影响。
细胞迁移实验是将Transwell小室放入培养板中,小室内称为上室,培养板内称下室,上下层培养液以聚碳酸酯膜相隔,将研究的肿瘤细胞种在上室内,下室加入含FBS或某些特定的趋化因子的培养液,由于聚碳酸酯膜具有通透性,肿瘤细胞会向营养成分高的下室迁移,计数进入下室的细胞数量就能反应细胞的迁移能力。
分别取实施例4,5,6的经过各个分组孵育的Transwell铺板细胞,细胞的终浓度大小约为5×105个/mL;24孔板的下室内加入500μL的含浓度(体积比)20%FBS的DMEM,在Transwell小室内加入100μL的细胞悬液,常规培养24h;细胞培养完成后,轻提Transwell小室,倾倒室内的培养基,用适量的PBS将细胞洗涤2遍,之后每孔加入1mL 4%的多聚甲醛(4%的多聚甲醛为4g多聚甲醛融于100mLPBS中制得;PBS缓冲液的配制:NaCl 8g,KCl 0.2g,Na2HPO4 1.44g,KH2PO4 0.24,加入800mL去离子水,充分搅拌,用HCl调节pH值至7.4,补充去离子水定容至1000mL,高压蒸汽灭菌,保存于4℃。)固定细胞15min,PBS再清洗3次,每次5min,再使用0.1%的结晶紫染色细胞30min,用PBS洗涤3次,每次5min,使用超纯水轻轻冲洗湿润小室表面的细胞,最后用湿润棉签轻轻擦去未迁移过膜的细胞,风机风干;倒置Transwell小室,显微镜进行观察和拍照。于显微镜下随机选取5个视野观察细胞,并计数迁移细胞数。
图1为实施例1给大鼠按体重比注射盐酸川芎嗪140mg/kg制备的含药血清孵育MG-63人成骨肉瘤细胞细胞,Transwell细胞迁移检测细胞迁移能力,具体分组参照实施例4,其中1空白对照组;2胎牛血清对照组;3空白血清对照组;4川芎嗪对照组;5生理盐水对照组;6现有药物对照组Ⅰ;7现有药物对照组Ⅱ;8浓度(体积比)10%含药血清组;9浓度(体积比)15%含药血清组。图中*为P<0.05,差异显著。
图2为实施例2给大鼠按体重比注射盐酸川芎嗪105mg/kg制备的含药血清孵育MG-63人成骨肉瘤细胞细胞,Transwell细胞迁移检测细胞迁移能力,具体分组参照实施例5,其中1空白对照组;2胎牛血清对照组;3空白血清对照组;4川芎嗪对照组;5生理盐水对照组;6现有药物对照组Ⅰ;7现有药物对照组Ⅱ;8浓度(体积比)10%含药血清组;9浓度(体积比)15%含药血清组。图中*为P<0.05,差异显著。
图3为实施例3给大鼠按体重比注射盐酸川芎嗪70mg/kg制备的含药血清孵育MG-63人成骨肉瘤细胞细胞,Transwell细胞迁移检测细胞迁移能力,具体分组参照实施例6,其中1空白对照组;2胎牛血清对照组;3空白血清对照组;4川芎嗪对照组;5生理盐水对照组;6现有药物对照组Ⅰ;7现有药物对照组Ⅱ;8浓度(体积比)10%含药血清组;9浓度(体积比)15%含药血清组。图中*为P<0.05,差异显著。
从图1至3可以看出,给大鼠按体重比分别注射盐酸川芎嗪140、105、70mg/kg后经腹主动脉取血离心后,将其配制成与DMEM培养液体积比10%、15%的含药血清对MG-63人成骨肉瘤细胞行孵育,结果表明含药血清孵育的MG-63人成骨肉瘤细胞相对于对照组4川芎嗪对照组、6现有药物对照组Ⅰ和7现有药物对照组Ⅱ迁移能力显著降低,说明本发明实施例制备的含药血清具有良好的抑制MG-63人成骨肉瘤细胞迁移的作用。
- 还没有人留言评论。精彩留言会获得点赞!