魔芋葡甘聚糖‑明胶基胶囊的制备方法与流程
本发明涉及一种胶囊的制备方法,具体涉及一种魔芋葡甘聚糖-明胶基胶囊的制备方法。
背景技术:
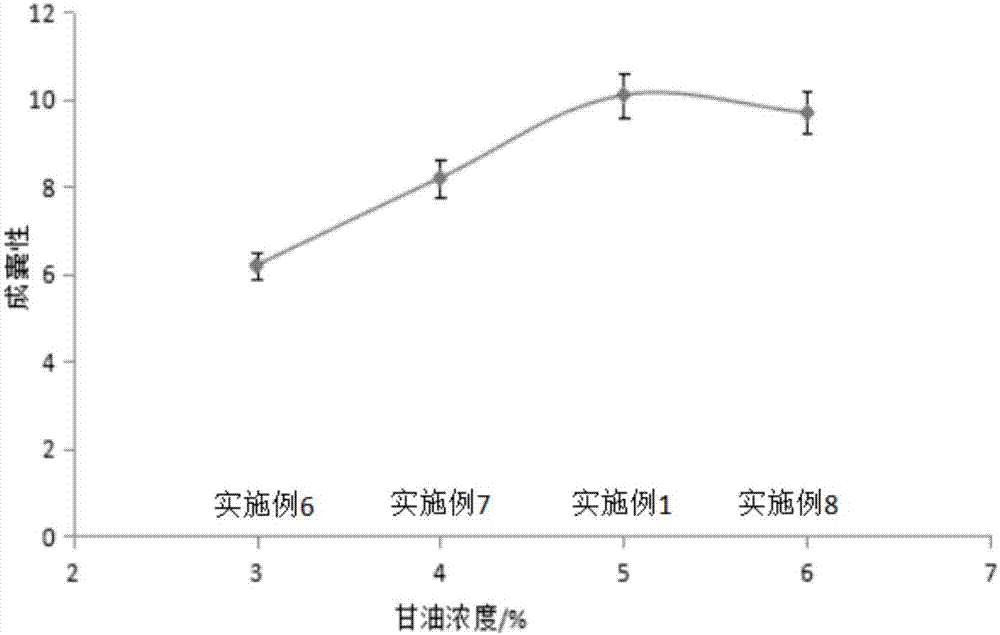
:胶囊剂系指药物装于空胶囊中制成的制剂。中国药典将胶囊定义为两类:硬胶囊和软胶囊。硬胶囊的外形为椭圆形,是由囊体和帽构成,两者有各自的凹槽和模形,两者能紧密的套合成为一体。将胶囊剂与片剂和其他类型的剂型相比,胶囊剂的特点是可以掩盖药物的不良气味,吸收好、药物的稳定性好,经过180多年的发展,在口服固体制剂中,胶囊剂已成为了主要剂型,胶囊剂与其他剂型相比具有很多优点,所以在药品市场上胶囊剂所占数目逐步扩大。此外胶囊装的药物,一般都是对食道和胃肠道粘膜有刺激性、有反应的粉末或颗粒,或味道不好、易于挥发、在口腔中易与唾液产生反应,以及易进入气管的药。当这些药装入胶囊,既保护了药物药性完好无损,也保护了消化器官和呼吸道。另外,有些药物需要在肠内释放溶解,胶囊可以保护药物不被胃酸破坏。但是胶囊剂可能会造成药物流失、药物浪费。胶囊剂具有下列特点:(1)适当遮盖药物难闻的苦味及臭味(2)药物的生物利用度高(3)增加药物稳定性(4)能弥补其他固体剂型的不足(5)可控制药物的释放时间和释放药物具体位置。但是,有些液体溶液不适用胶囊剂,因会将胶囊溶化;刺激性较强的药物,均不宜制成胶囊剂,因胶囊剂在溶化时,会导致局部浓度过高而刺激粘膜。风化药物可使胶囊软化,潮解药物可使胶囊过分干燥失水而变脆,都不可以做成胶囊剂。明胶是由动物皮肤、骨、肌膜等结缔组织中的胶原进行降解而成为白色或淡黄色、半透明、微带亮度的薄片或粉粒;故又叫做动物明胶。工业明胶是淡黄色透明或半透明等薄片或粉粒。无味,无臭。在冷水中吸水膨胀。在热水中容易溶解,在甘油和醋酸中也易溶解,但在乙醇和乙醚中不溶。是一种大分子的亲水胶体,明胶的主要组成为氨基酸组成相同而分子量分布很宽的多肽分子混合物,分子量一般在几万至十几万,明胶既具有酸性,又具有碱性,是一种两性物质,明胶的胶团是带电的,在电场作用下,它将向两极中的某一极移动。明胶分子结构上有大量的羟基,另外还有许多羧基和氨基,这使得明胶具有极强的亲水性。凝胶性是明胶最重要的功能性质,它是指明胶分子在一定条件下由无规则卷曲态逐渐恢复成有序三螺旋结构,此过程主要分三个阶段:第一,当温度降至凝固点约(35℃)以下时,明胶溶液中无规则卷曲的多肽链复旋成左手螺旋,相邻的左手螺旋链段间作用产生氢键交联,重新形成类胶原螺旋体的核心区域,此过程称为“复性”;第二,类胶原螺旋体聚合形成微凝胶;第三,聚集体进一步形成具有一定刚性的网络凝胶。明胶的凝胶性受明胶的氨基酸组成、平均分子量及分子量分布、胶液浓度和ph、凝胶温度和凝冻时间等多种因素影响。明胶不溶于有机溶剂,特别不易在冷水中溶解,可吸水膨胀至自身的5-10倍,明胶易在温水中溶解,温度降低而成凝胶,溶点在24-28℃之间,所以溶解度与凝固温度相差比较小,容易受水分、温度、湿度的影响而产生变化。明胶含有内氨酸、甘氨酸、脯氨酸及羟脯氨酸等人体所需的18种氨基酸。明胶的制备方法是以动物的皮、骨作为原料,通过分类、洗浸、脱脂、中和、水解、过滤、浓缩、凝胶、烘干、粉碎等十几道工序制成,制成一种无味、半透明、坚硬颗粒或粉末。生产工艺有酸法(a型)、碱法(b型),非常少数采用酶法制备明胶。明胶是肽分子聚合物质,是胶原蛋白多级的水解产物,在食品、医药等工业领域起到非常广泛应用。食用明胶是一种食品添加剂,具有非常高的价值,它可以直接制成浓汤、水晶冻、色拉、蛋黄汁、糖霜、奶油糖、饮料、啤酒等;照相明胶用于制造胶卷、胶片等感光材料;明胶在医药领域可制成空心胶囊、明胶海绵等。伴随着医药行业的发展,明胶胶囊在中国从无到有,在现代工艺生产中是具有广泛应用的,在中国胶囊制作领域有着飞快发展,已经有了很大的提高,对医药领域起到重要作用。明胶空心胶囊明胶为原材,添加适量的增塑剂、水、崩解剂等,经过吸水溶胀、溶解胶液、蘸胶成型、烘干、拔壳、切割及整理和套合等工序制备。明胶具有水溶性,而且具有亲和力,明胶经过烘干失水后能够成膜且质地坚硬,开始明胶胶囊就是因为这个原理制作出明胶胶囊的。明胶胶囊制剂在体内温度的作用下吸水溶解并且发生破裂或崩解,因为这样的性质在人的胃中溶解被消化的。明胶空心胶囊剂在医药类制剂中所占的百分比正在逐年上升,因此呈现在我们面前的是一个日益增长的庞大的明胶胶囊市场。近几年来,明胶胶囊在市场占有一定地位,我国医药行业的产值也己经达到了上万亿元,其中在所有医药制剂的产值中,国内明胶空心胶囊剂占到了总产值的20%左右,每年有1000亿粒左右的明胶空也胶囊使用量,在全球明胶空心胶囊行业中占到了30%左右。这使明胶空心胶囊的产量明显供过于求,生产能力过剩,使明胶空心胶囊行业的激烈异常激烈,这样的现象产生具有两面性,优点是可以推动整个行业发展,促进行业研制新型明胶基胶囊壳,而缺点是商家看到利益而引发的不良后果,2012年曝光的毒胶囊事件,原因也是因为明胶的价格高,制备工艺复杂,所以明胶空心胶囊也是存在问题的,是将来医药行业需要解决的。魔芋葡甘聚糖是一种优良的天然高分子化合物,同时具有特别的理化性质,x-射线衍射表明,魔芋葡甘聚糖的粒子近似于无定型结构,极易溶于水,且吸水后体积急剧膨胀魔芋葡甘聚糖可与水分子通过氢键、分子偶极、瞬间偶极、诱导偶极等作用力聚集,形成庞大而较难自由运动的大分子在溶解过程中,水分子的扩散迁移速度远远大于魔芋葡甘聚糖大分子的扩散迁移速度,使得魔芋胶颗粒发生溶胀或膨胀,其吸水量可达到相当于自身体积的80~100倍。魔芋在碱性条件下容易发生沉淀例如,naoh的添加可促进凝胶的形成这可能是由于乙酰基的脱除导致魔芋葡甘聚糖分子的自身聚集、分子链的缠绕,从而形成局部和连续的凝胶网络结构,魔芋葡甘聚糖在naoh溶液中形成的溶胶,其溶胶凝胶转化温度高于水溶胶,在魔芋葡甘聚糖凝胶形成过程中,凝固剂添加越多,凝胶化速度越快;但凝固剂过多,则凝胶气泡难以排除,由于魔芋葡甘聚糖凝胶在碱性条件下加热,其分子链上的乙酰基脱除,形成的凝胶十分稳定,即使在100℃下反复加热,其凝胶强度也基本不变,这种独特的性质在高分子多糖领域是非常罕见的另外,魔芋葡甘聚糖凝胶通过透析除碱后,仍能保持较好的凝胶结构。根据魔芋葡甘聚糖特殊的吸水性、成膜性、凝胶性。将利用魔芋葡甘聚糖与其他高分子材料通过共混可以得到性能良好的复合膜材料,会具有良好的生物降解性。魔芋葡甘聚糖在水中分散呈胶体状,被广泛用作食品添加剂,主要由甘露聚糖和葡萄糖以β-1,4键键合的高分子量非离子型甘露聚糖,有少量以β-1,4键的之键结构,沿葡甘露聚糖主链上平均每隔9~19个单糖单位有一个乙酰基,它有助于葡甘露聚糖的溶解。平均分子量20万~200万在水中的粘度非常大,溶解度很小,导致其在食品、饮料中的添加量很小通常小于2%,功能十分有限。因此对大分子进行适当水解降低表观粘度,以提高在水中的溶解度,实现对魔芋葡甘聚糖的可控降解,若能适度地改变其分子量,则可使魔芋葡甘聚糖化学-生物法改性,以进一步扩大其应用领域。因此利用酶解反应具有高效性、专一性、反应条件温和、得到产物纯度较高以及对环境的影响较小等优点,选择β-甘露聚糖酶作为魔芋葡甘聚糖水解反应的催化剂,通过控制水条件,使魔芋葡甘聚糖发生有限水解,从而达到适度降低其分子量。魔芋葡甘聚糖具有生物相容性、生物降解性、保水性、成膜性、可塑性、增稠性和成胶等特性,已被广泛应用于食品、医药、化工、石油、化妆品等诸多领域,用作食品添加剂、乳化剂和保水剂,还可制成保健食品等。魔芋成为植物的药用时间久远,是一种复合性多糖,吸水后可作为为流质性膳食纤维,虽然不被人体吸收,但可促进肠胃蠕动,促进人体对蛋白质等营养物质的消化和吸收,惯性便秘,防治肠癌、食道癌。对糖尿病、高血压、冠心病、动脉硬化的效果显著。此外,魔芋葡甘聚糖还可增加高密度脂蛋白,对人体伴有的脂代谢紊乱有明显疗效。它脂肪含量少,可制成清淡、低热食品,是一种理想的天然减肥保健和抗癌食品。魔芋胶溶液具有良好的流变性,因此用作食品加工领域的添加剂和增稠剂。此外,与玉米淀粉、黄原胶、卡拉胶等多糖形成复合体系,能够起到协同作用,出现凝胶性能提高的现象,可以使整个体系粘度增加。魔芋葡甘聚糖是天然、优质、无毒无害、可溶性的大分子多糖,这样优越的性质可以在药物领域发挥这越来越大的作用。魔芋葡甘聚糖的优越,已经在各行各业中有着广阔的应用。本发明以魔芋葡甘聚糖和明胶混合制备胶囊壳,利用魔芋葡甘聚糖的特性,实现与明胶共混,在可以制备出符合国家药典标准的胶囊壳下,为了推广魔芋最为当今发展较快的新型材料,未来市场上魔芋将占据一定地位,在市场上,我们服用的各种胶囊制剂等是使用可食用明胶制作而成的,我们在日常生活中可以广泛接触到明胶,它具有口感好、蛋白质高、脂肪低等优势。在植物空囊研发出来之前,药辅企业大多采用食用明胶为原材料来制作生产明胶空胶囊。考虑使用者的健康,研制出更绿色更环保的替代品,是全社会所需要的创新精神,而魔芋独特的结构赋予了它优良的功能特性,研究表明,魔芋葡甘聚糖及其改性产物还具有很多的功能特性,说明魔芋葡甘聚糖是一种安全、健康的膳食纤维。为所有这些优点使得魔芋凝胶成为胶囊制备的不可替代的候选,为了商家利益考虑,引进新型替代品或者复合制剂制备胶囊壳,采用产量大的原料制备空心胶囊,实现科技创新,也符合国家发展的趋势。技术实现要素:本发明的一个目的是解决至少上述问题和/或缺陷,并提供至少后面将说明的优点。为了实现根据本发明的这些目的和其它优点,提供了一种魔芋葡甘聚糖-明胶基胶囊的制备方法,包括以下步骤:步骤一、按重量份,取0.5~1.5份甘露酶加入2500~3500份水中,搅拌均匀,然后缓慢向烧杯中加入300~500份魔芋精粉;室温降解8~12min;再向烧杯中加入300~500份魔芋精粉,降解8~12min;再向烧杯中加入300~500魔芋精粉,降解8~12min;再向烧杯中加入300~500份魔芋精粉,降解8~12min;调节ph,然后灭活10~30min;冷却至室温,即得魔芋葡甘聚糖降解液;步骤二、取魔芋葡甘聚糖降解液,加入甘油,在60~80℃下,搅拌均匀,然后加入明胶,在50rpm下搅拌,直至降解液中的明胶完全溶解,得到混合溶胶;所述魔芋葡甘聚糖降解液中的魔芋葡甘聚糖与明胶的重量比为1~1.5:1;所述甘油的加入量占混合溶胶质量的4~6%;步骤三、将混合溶胶脱气后,静置蘸胶、冷冻、拔壳、切割、干燥,即得到魔芋葡甘聚糖-明胶基胶囊。优选的是,所述调节ph至9~11,所述灭活采用在80℃恒温水浴锅中进行。优选的是,所述魔芋葡甘聚糖降解液中的魔芋葡甘聚糖与明胶的重量比为1:1;所述甘油的加入量占混合溶胶质量的5%。优选的是,所述静置蘸胶的温度为27~28℃;所述冷冻的温度为-15~-20℃,冷冻时间为3~10min。优选的是,所述灭活采用的方法为:将调节ph后的混合液输入高压脉冲电场处理室中,利用高压脉冲电场进行处理,所述高压脉冲处理室中两极板的间距为3~5cm;高压脉冲处理参数为:脉冲幅度为12~18kv,脉冲频率为200~300hz,脉冲宽度为12~15us;脉冲数15~20个。优选的是,所述高压脉冲处理室外围设置有冷水循环系统,其中循环冷水温度为1~3℃,水循环速度为1~3m/s。优选的是,所述步骤三中,混合溶胶脱气的方法为:采用超声脱气器,控制混合溶胶的流速为0.1~0.3m3/h,超声功率为200~300w,超声频率为25~30khz,进行脱气。优选的是,所述明胶替换为重量比为1:1~3的明胶和改性淀粉。优选的是,所述改性淀粉的制备方法为:按重量份,在超临界反应装置中加入10~20份羟丙基淀粉、3~5份没食子酸、5~10份乙醇、50~80份水,调节ph至5,搅拌均匀,然后将体系密封,通入二氧化碳至30~40mpa、温度40~45℃下的条件下反应30~60min,然后卸去二氧化碳压力,加入1~3份环氧氯丙烷、2~5份壳聚糖和1~3份菊粉,然后再次注入二氧化碳至压力为45~60mpa,搅拌30~60min,卸压,然后用乙醇沉淀,冷冻干燥,得到改性淀粉;通过羟丙基淀粉分子链上的活性羟基反应生成的共聚物用于制备植物空心胶囊,可有效集成这两种天然原材料的优良性能,显著提高了胶囊的品质及成胶囊工艺(浸蘸法)可操作性,并大幅度降低植物胶囊制备成本,可解决目前植物胶囊制造中普遍存在的生产成本过高、操作复杂、质标不稳定及品质不可控等问题。优选的是,所述步骤二的过程替换为:将魔芋葡甘聚糖降解液、甘油和明胶置于带搅拌的密封容器中,向其中通入氮气使氮气饱和,然后将该密封容器置于1.5mev、30ma的电子加速器中进行辐照搅拌处理,制得混合溶胶;所述辐照采用的辐照剂量率为200~500kgy/h,辐照剂量为500~2000kgy,搅拌速度为50r/min。。本发明至少包括以下有益效果:本发明制备的魔芋葡甘聚糖-明胶基胶囊胶囊壳厚度均匀、易拔壳无破裂、无插劈、气泡少、无瘪头、无薄头,对胶囊壳的强度和弹性检测,脆碎度比单一明胶胶囊壳低,表示具有更强的弹性。对溶出度检测,可以测定魔芋葡甘聚糖-明胶胶囊的释药效果,试验得到4-5min左右开始释药,60min左右,溶出率为95.5%。本发明的其它优点、目标和特征将部分通过下面的说明体现,部分还将通过对本发明的研究和实践而为本领域的技术人员所理解。附图说明:图1为本发明实施例1~5中得到的胶囊的成囊性结果图;图2为本发明实施例1,6~8中得到的胶囊的成囊性结果图;图3为本发明实施例1,9~12中得到的胶囊的成囊性结果图;图4为本发明实施例1,13~16中得到的胶囊的成囊性结果图;图5为本发明中5-氨基水杨酸浓度与峰面积标准曲线图;图6为采用本发明的胶囊壳在不同时间的5-氨基水杨酸溶出度曲线图。具体实施方式:下面结合附图对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。应当理解,本文所使用的诸如“具有”、“包含”以及“包括”术语并不配出一个或多个其它元件或其组合的存在或添加。实施例1:一种魔芋葡甘聚糖-明胶基胶囊的制备方法,包括以下步骤:步骤一、按重量份,取0.025g甘露酶加入80ml蒸馏水中,搅拌均匀,然后缓慢向烧杯中加入10g魔芋精粉;室温降解10min;再向烧杯中加入10g魔芋精粉,降解10min;再向烧杯中加入10g魔芋精粉,降解10min;再向烧杯中加入10g魔芋精粉,降解10min;调节ph至10,然后置于80℃恒温水浴锅中灭活20min;冷却至室温,即得魔芋葡甘聚糖降解液;降解液含量为40/120=34%;步骤二、取魔芋葡甘聚糖降解液(魔芋葡甘聚糖的含量为4g),加入甘油,在70℃下,150rpm搅拌均匀,然后加入明胶4g,在50rpm下搅拌,直至降解液中的明胶完全溶解,得到混合溶胶;所述甘油的加入量占混合溶胶质量的5%;步骤三、将混合溶胶脱气后,在27℃下静置蘸胶、-18℃冷冻5min、拔壳、切割、干燥,即得到魔芋葡甘聚糖-明胶基胶囊。实施例2:加入明胶的量为8g,其余工艺过程和参数与实施例1中的完全相同。实施例3:加入魔芋葡甘聚糖降解液的量为(魔芋葡甘聚糖的含量为8g),其余工艺过程和参数与实施例1中的完全相同。实施例4:加入魔芋葡甘聚糖降解液的量为(魔芋葡甘聚糖的含量为6g),其余工艺过程和参数与实施例1中的完全相同。实施例5:加入魔芋葡甘聚糖降解液的量为(魔芋葡甘聚糖的含量为12g),其余工艺过程和参数与实施例1中的完全相同。实施例6:所述甘油的加入量占混合溶胶质量的3%;其余工艺过程和参数与实施例1中的完全相同。实施例7:所述甘油的加入量占混合溶胶质量的4%;其余工艺过程和参数与实施例1中的完全相同。实施例8:所述甘油的加入量占混合溶胶质量的6%;其余工艺过程和参数与实施例1中的完全相同。实施例9:步骤一中,调节ph至8,其余工艺过程和参数与实施例1中的完全相同。实施例10:步骤一中,调节ph至9,其余工艺过程和参数与实施例1中的完全相同。实施例11:步骤一中,调节ph至11,其余工艺过程和参数与实施例1中的完全相同。实施例12:步骤一中,调节ph至12,其余工艺过程和参数与实施例1中的完全相同。实施例13:在26℃下静置蘸胶,其余工艺过程和参数与实施例1中的完全相同。实施例14:在28℃下静置蘸胶,其余工艺过程和参数与实施例1中的完全相同。实施例15:在29℃下静置蘸胶,其余工艺过程和参数与实施例1中的完全相同。实施例16:在30℃下静置蘸胶,其余工艺过程和参数与实施例1中的完全相同。实施例17:所述灭活替换为以下方法:将调节ph后的混合液输入高压脉冲电场处理室中,利用高压脉冲电场进行处理,所述高压脉冲处理室中两极板的间距为3cm;高压脉冲处理参数为:脉冲幅度为12kv,脉冲频率为200hz,脉冲宽度为12us;脉冲数15个;所述高压脉冲处理室外围设置有冷水循环系统,其中循环冷水温度为1℃,水循环速度为1m/s。其余工艺过程和参数与实施例1中的完全相同。实施例18:所述灭活替换为以下方法:将调节ph后的混合液输入高压脉冲电场处理室中,利用高压脉冲电场进行处理,所述高压脉冲处理室中两极板的间距为4cm;高压脉冲处理参数为:脉冲幅度为15kv,脉冲频率为250hz,脉冲宽度为15us;脉冲数18个;所述高压脉冲处理室外围设置有冷水循环系统,其中循环冷水温度为2℃,水循环速度为2m/s。其余工艺过程和参数与实施例1中的完全相同。实施例19:所述步骤三中,混合溶胶脱气的方法为:采用超声脱气器,控制混合溶胶的流速为0.2m3/h,超声功率为250w,超声频率为25khz,进行脱气。其余工艺过程和参数与实施例1中的完全相同。实施例20:所述步骤三中,混合溶胶脱气的方法为:采用超声脱气器,控制混合溶胶的流速为0.2m3/h,超声功率为250w,超声频率为25khz,进行脱气。其余工艺过程和参数与实施例1中的完全相同。实施例21:所述明胶替换为重量比为1:1的明胶和改性淀粉;所述改性淀粉的制备方法为:按重量份,在超临界反应装置中加入10份羟丙基淀粉、3份没食子酸、5份乙醇、50份水,调节ph至5,搅拌均匀,然后将体系密封,通入二氧化碳至30mpa、温度40℃下的条件下反应30min,然后卸去二氧化碳压力,加入1份环氧氯丙烷、2份壳聚糖和1份菊粉,然后再次注入二氧化碳至压力为45mpa,搅拌30min,卸压,然后用乙醇沉淀,冷冻干燥,得到改性淀粉。其余工艺过程和参数与实施例1中的完全相同。实施例22:所述明胶替换为重量比为1:2的明胶和改性淀粉;所述改性淀粉的制备方法为:按重量份,在超临界反应装置中加入15份羟丙基淀粉、4份没食子酸、8份乙醇、80份水,调节ph至5,搅拌均匀,然后将体系密封,通入二氧化碳至35mpa、温度40℃下的条件下反应45min,然后卸去二氧化碳压力,加入2份环氧氯丙烷、4份壳聚糖和2份菊粉,然后再次注入二氧化碳至压力为60mpa,搅拌45min,卸压,然后用乙醇沉淀,冷冻干燥,得到改性淀粉。其余工艺过程和参数与实施例1中的完全相同。实施例23:所述步骤二的过程替换为:将魔芋葡甘聚糖降解液、甘油和明胶置于带搅拌的密封容器中,向其中通入氮气使氮气饱和,然后将该密封容器置于1.5mev、30ma的电子加速器中进行辐照搅拌处理,制得混合溶胶;所述辐照采用的辐照剂量率为200kgy/h,辐照剂量为600kgy,搅拌速度为50r/min。其余工艺过程和参数与实施例1中的完全相同。实施例24:所述步骤二的过程替换为:将魔芋葡甘聚糖降解液、甘油和明胶置于带搅拌的密封容器中,向其中通入氮气使氮气饱和,然后将该密封容器置于1.5mev、30ma的电子加速器中进行辐照搅拌处理,制得混合溶胶;所述辐照采用的辐照剂量率为500kgy/h,辐照剂量为2000kgy,搅拌速度为50r/min。其余工艺过程和参数与实施例1中的完全相同。对上述实施例1~24中得到胶囊壳进行成囊性检测:根据药典和中国医药包装协会标准中对胶囊的要求,确定了六项鉴定指标分别为胶囊壁厚、拔壳难易程度、色泽、插劈、气泡、痘头薄头综合为成囊性,进行胶囊壳的评定,分数分为1-12,分数越高,表明胶囊的成囊性越好;其中,实施例1~5的胶囊的成囊性结果如图1所示,实施例1在魔芋葡甘聚糖与明胶的比值为1:1左右时,成囊性效果最好。进行6次对5组胶囊壳分别进行打分,且求平均值为7.9、10.2、9.7、8.2、8.1,最终汇总结论壁厚比较均匀、拔壳比较容易、色泽均匀、无插劈,明胶与降解魔芋的混合,在一定的浓度范围内时,粘性增加,而有利于成壳,明胶浓度过大时,粘度过大,难蘸胶,难成壳;降解魔芋浓度低,会使蘸胶后难拔壳,降解魔芋浓度过大时,胶液粘度低、壁过厚,成囊效果不好。其中,实施例1,6~8的胶囊的成囊性结果如图2所示,实施例1甘油浓度在5%左右时为最佳浓度,进行6次对4组胶囊壳分别进行打分,且求平均值为6.2、8.2、10.2、9.7,甘油浓度是影响胶囊壳壁厚、拔壳浓度的最重要的因素,因为甘油是一种亲水性的增塑剂,低浓度增塑剂的加入改善了高聚物分子链间及分子内形成的氨键作用,软化胶囊壳的刚性结构。然而甘油的浓度较高,能够增大分子之间的距离,扩大了分子之间的间隙,导致胶囊壳的致密性下降,从而使制得的胶囊壳的弹性降低,本发明测得当甘油浓度低于5%时,随着甘油浓度的增加胶囊壳成囊性增加,制得胶囊壳弹性好、壁厚度良好;当甘油浓度大于5%时,随着甘油浓度增加,胶囊壳的成囊性降低,胶囊壳变软、弹性不好,存在胶囊壳头变瘪。甘油浓度为5%时,成囊性为10.2,之后随着增加浓度成囊性变化平缓。其中,实施例1,9~12的胶囊的成囊性结果如图3所示,实施例1中ph值为10为最佳ph值。进行6次对5组胶囊壳分别进行打分,且求平均值,为8.1、9.8、10.2、9.9、8.3,ph对壁的厚度、拔壳程度影响较大因为魔芋葡甘聚糖溶胶在酸性条件下可保持良好的性能,而碱性条件下容易发生沉淀,naoh的添加可促进凝胶的形成这可能是由于乙酰基的脱除导致魔芋葡甘聚糖分子的自身聚集、分子链的缠绕,从而形成局部和连续的凝胶网络结构,所以凝胶在碱性条件下加热,其分子链上的乙酰基脱除,形成的凝胶十分稳定。ph值在9时开始随着ph值增加成囊性增加平缓,在ph值为10时,成囊性最高为10.2。其中,实施例1,13~16的胶囊的成囊性结果如图4所示,实施例1蘸胶温度为27℃时,胶囊壳成囊性最佳。进行6次对5组胶囊壳分别进行打分,且求平均值为7.9、10.2、9.7、8.2、8.1,蘸胶温度是影响胶囊壳壁厚度、拔壳程度的重要影响因素。在溶胶后,胶液温度可达到45℃左右,但胶液温度下降比较快,所以在最适温度蘸胶比较困难,而胶液温度过高,流动性强,难蘸胶导致胶囊壳壁过薄、难拔壳易破;胶液温度过低,流动性差,粘度过大,蘸取的胶液不能成型,导致胶囊壳壁过厚,当胶液温度在27℃左右蘸取胶液时,壁厚度最佳、拔壳程度最佳、胶囊壳成囊性最佳,温度小于27℃时,蘸胶后成囊性效果较差,当蘸胶时,胶液温度一定时,根据蘸胶环境温度的不同,蘸胶效果也不同,而蘸胶胶液温度的在一定范围内变化极小,而在27℃左右一定范围外,蘸胶效果极差,所以在制备试验的过程中,必须将温度控制好,否则蘸胶失败。其中,实施例17~24的胶囊的成囊性结果如表1所示;表1实施例1718192021222324成囊性10.810.911.211.311.811.911.511.6对上述实施例1~24中得到胶囊壳脆碎度检测,取各实施例制备的胶囊壳50粒,放置在平皿中,放入装有饱和硝酸镁溶液的干燥器中,置于25℃保持恒温24h,将其取出,马上逐粒放入直立在木板上的内径为24mm,高为200mm的玻璃管内,将直径为22mm的圆柱形砝码从玻璃管口自由落下,观察胶囊有无破裂,计算脆碎个数;结果如表2所示;表2实施例12345678脆碎个数13323432实施例910111213141516脆碎个数32233233实施例1718192021222324脆碎个数11000011对实施例1得到胶囊壳溶出度含量测定:首先进行人工胃液配制:ph=1.5盐酸溶液:吸取2.5ml浓盐酸于1000ml试剂瓶中,加入1000ml蒸馏水,摇匀,用配制的0.5mol/l的hcl、0.5mol/l的naoh调至ph为1.5,用ph计测定ph,即得。设定摇床的温度为37℃,转速为100rpm;取六个100ml锥形瓶,分别编号为1~6,向每个锥形瓶中加入ph1.5的模拟胃液45ml,再将锥形瓶放入摇床中预热,准备实施例1制备的六个空心胶囊壳(每个胶囊壳的厚度及重量要尽量相近),向每个胶囊壳加入20mg于分析天平上精密称取的5-氨基水杨酸(加量续精确);装填药品用减量法(先将样品放于称量瓶中,置于天平盘上,称取样品和称量瓶的重量,然后取出所需的试样量,再称得剩余样品和称量瓶的重量,两次称量之差,即为所需试样的重量);待锥形瓶的温度近37℃,向每个锥形瓶中加入对应的5-氨基水杨酸胶囊;待胶囊壳裂解完全后,取出锥形瓶,静置,使囊材降解物沉淀;5-氨基水杨酸标准品的制备:分析天平上精密称定100mg5-氨基水杨酸,加入到100ml容量瓶中,并用ph1.5的模拟胃液定容至刻度,即得标准品;取六个50ml容量瓶,分别编号,用移液枪分别向六个容量瓶移取5-氨基水杨酸标准品0.5ml,1.0ml,1.5ml,2.0ml,2.5ml,3.0ml并用ph1.5的模拟胃液定容至刻度,摇匀。标准曲线的绘制:用模拟胃液做空白,于303nm处分别测定六个标准品的吸光度,以5-氨基水杨酸的浓度为横坐标,吸光度为纵坐标,绘制标准曲线;溶出度测定:用移液枪分别吸取5-氨基水杨酸胶囊溶出液5ml,微膜过滤,取续滤液1ml于50ml容量瓶中,并用ph1.5的模拟胃液定容至刻度,摇匀;用蒸模拟胃液做空白,于303nm处分别测定六个5-氨基水杨酸胶囊溶出液的吸光度,记录;利用标准曲线,找出对应横坐标上的的浓度;5-氨基水杨酸浓度与峰面积标准曲线如图5,标准曲线y=0.1281x+0.0086,r2=0.9977,线性范围0.5mg/ml-3mg/ml。结果表明5-氨基水杨酸0.5mg/ml-3mg/ml范围内浓度与吸光率成线性关系。计算出胶囊壳平均溶出量为87.43%。累积溶出度测定:取6个100ml锥形瓶,分别编号,向每个锥形瓶中加入ph1.5的模拟胃液50ml,再将锥形瓶放入摇床中预热;准备实施例1制备的6个空心胶囊壳,向每个胶囊壳加入20mg于分析天平上精密称取的5-氨基水杨酸;待锥形瓶的温度近37℃,向每个锥形瓶中加入对应的5-氨基水杨酸胶囊,待分别溶出5min、10min、25min、30min、45min、60min后,用移液枪分别吸取6个5-氨基水杨酸胶囊溶出液5ml于50ml容量瓶中,并用ph1.5的模拟胃液定容至刻度,摇匀;用蒸馏水做空白,于303nm处分别测定6个5-氨基水杨酸胶囊溶出液的吸光度,记录;通过标准曲线,找出对应横坐标上的的浓度。溶出度计算公式如下:熔出度=c×d/w×100%其中,d:稀释体积,吸取1ml溶出液于50ml容量瓶中;w:装药量。从图6可以分析5-氨基水杨酸在4min-5min时开始释放,10min左右胶囊壳开始加快释放药物,25min后释药速率平缓。在60min时溶出度为95.5%。采用同样的操作方法,将上述采用的实施例1的胶囊壳替换为实施例17~18中的胶囊壳;其胶囊壳平均溶出量结果和60min溶出度如表3所示;表3尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节和这里示出与描述的图例。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1