用于治疗心律失常的无引线起搏装置的制作方法
本申请要求2017年3月20日提交的美国临时专利申请no.62/473,663的权益和优先权,其公开内容通过引用并入本文。
本公开涉及医疗装置以及用于制造和/或使用医疗装置的方法。更具体而言,本公开涉及无引线心脏装置和方法,比如无引线起搏装置和方法,以及用于这种无引线装置的输送装置和方法。
背景技术:
已经开发了各种各样的医疗装置来用于医疗用途,例如心脏用途。这些装置中的一些包括导管、引线、起搏器和类似者,以及用于输送这种装置的输送装置和/或系统。这些装置可以通过各种不同的制造方法中的任何一种制造,并且可以根据多种方法中的任何一种使用。在公知的医疗装置、输送系统和方法中,每个都具有某些优点和缺点。一直需要提供替代的医疗装置和输送装置以及用于制造和使用医疗装置和输送装置的替代方法。
技术实现要素:
本公开提供用于医疗装置(包括心脏感测和起搏装置以及输送装置)的设计、材料、制造方法和用途的替代方案。
在第一示例中,一种用于向患者心脏输送起搏脉冲的无引线起搏装置可以包括:电源,其用于提供电源电压;壳体,其至少部分地支撑所述电源,所述壳体具有第一端部、第二端部以及在所述第一端部与所述第二端部之间延伸的一侧;多个电极,其在所述壳体上;固定构件,其从所述壳体沿径向延伸;远侧延伸部,其连接到所述壳体并向所述壳体的远侧端部的远侧延伸;以及引导线管腔,其从处于所述壳体的所述一侧中并且处于所述固定构件的近侧的一定位置处的引导线端口延伸到所述远侧延伸部的远侧端部。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述壳体可以包括支撑所述电源的本体部分和连接到所述本体部分的头部,其中所述引导线端口可以位于所述头部中。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述头部可以从所述本体部分的远侧端部向远侧延伸。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述引导线端口可以位于所述本体部分的远侧端部的远侧。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述头部包括模制部分,并且可以模制在所述远侧延伸部的近侧端部上。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,多个电极中的一个电极可以由所述壳体的头部支撑,并通过所述模制部分暴露。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,通过所述模制部分暴露的电极可以暴露在所述头部的第一侧,并且所述引导线端口可以位于所述头部的与所述头部的第一侧大致相对的第二侧。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述无引线起搏装置可以进一步包括沿着所述远侧延伸部彼此纵向地间隔开的多个电极以及延伸穿过所述远侧延伸部的多根线,其中每根线沿着所述远侧延伸部将电极连接到所述电源。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述无引线起搏装置可以进一步包括细长近侧构件,其从所述壳体的近侧端部向近侧延伸。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述细长近侧构件的至少一部分可以是柔性的。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述细长近侧构件的至少一部分可以是刚性的。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述细长近侧构件可以进一步包括细长延伸部,其从所述壳体的近侧端部向近侧延伸,所述细长延伸部可以具有第一外径;以及附属部,其位于所述细长延伸部的近侧端部处,所述附属部可以具有大于所述第一外径的第二外径。
在另一示例中,一种用于将无引线起搏装置定位在患者的冠状窦中的定位系统,所述定位系统可以包括无引线起搏装置,其具有:电源;壳体,其支撑所述电源;电极,其由所述壳体支撑并与所述电源连通;固定构件,其从所述壳体沿径向延伸;远侧延伸部,其向所述壳体的远侧端部的远侧延伸;引导线管腔,其从处于所述壳体的一侧并且处于所述固定构件的近侧的引导线端口延伸穿过所述远侧延伸部到所述远侧延伸部的远侧端部;以及近侧构件,其向所述壳体的近侧延伸;并且所述定位系统可以进一步包括:引导线,其构造成延伸穿过所述引导线管腔;定位装置,其构造成接合所述近侧构件;以及输送导管,其用于接收所述无引线起搏装置,并将所述无引线起搏装置定位在冠状窦处。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述输送导管可以具有弯折部,所述弯折部邻近所述输送导管的远侧末端,以便从患者的右心房进入冠状窦。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述输送导管的远侧末端部分可以包括用于扩张冠状窦的扩张器。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述定位装置可以与所述近侧构件互锁以促进所述无引线起搏装置在目标位置处的定位。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述定位系统可以进一步包括取回装置,其具有细长本体和构造成与所述近侧构件接合的接合远侧端部。
在另一示例中,一种将无引线起搏装置定位在冠状窦中的方法可以包括:使引导线前进到冠状窦中;将输送导管的远侧末端定位邻近冠状窦的口;使无引线起搏装置前进通过所述输送导管的远侧末端,并将所述无引线起搏装置的壳体定位在完全处于冠状窦内的位置处,并将所述无引线起搏装置的向所述壳体的远侧端部的远侧延伸的远侧延伸部定位在从冠状窦延伸的血管内;以及在所述壳体完全定位在冠状窦内并且所述远侧延伸部定位在从冠状窦延伸的血管中的同时,将所述无引线起搏装置的向所述壳体的近侧延伸的近侧构件定位在右心房内的一定位置处。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述方法可以进一步包括通过使所述输送导管的远侧末端前进通过冠状窦的口来扩张冠状窦。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述方法可以进一步包括通过接合右心房中近侧构件来从冠状窦取回所述无引线起搏装置。
在另一示例中,一种无引线起搏装置可以包括:壳体,其构造成定位在冠状窦内;远侧延伸部,其向所述壳体的远侧端部的远侧延伸,所述远侧延伸部构造成定位在从冠状窦延伸的血管内;电极,其由所述壳体支撑;远侧电极,其由所述远侧延伸部支撑;以及处理模块,其位于所述壳体的内部空间内,并电联接到由所述壳体支撑的电极以及由所述远侧延伸部支撑的远侧电极,其中所述处理模块可以构造成基于使用由所述壳体支撑的电极感测到的近场信号来确定是否发生了心房事件,并且基于使用所述远侧电极感测到的近场信号来确定是否发生了心室事件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述处理模块可以构造成基于对是否发生了心房事件的确定以及对是否发生了心室事件的确定来生成心脏刺激脉冲。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所生成的心脏刺激脉冲可以通过由所述壳体支撑的电极来生成。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所生成的心脏刺激脉冲可以通过所述远侧电极来生成。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述处理模块可以构造成基于使用由所述壳体支撑的电极感测到的远场信号来确定是否发生了心室事件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述处理模块可以基于使用由所述壳体支撑的电极感测到的近场感测信号来确定在患者心脏的右心房中是否发生了心房事件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述处理模块可以基于使用由所述壳体支撑的电极感测到的近场感测信号来确定在患者心脏的左心房中是否发生了心房事件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,由所述壳体支撑的电极可以是第一电极,并且所述无引线起搏装置可以进一步包括由所述壳体支撑的第二电极。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述处理模块可以构造成基于使用所述第二电极感测到的近场信号来确定是否发生了心房事件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述处理模块可以构造成基于使用所述第一电极感测到的近场信号来确定在患者心脏的右心房中是否发生了心房事件,并且基于使用所述第二电极感测到的近场感测信号来确定在患者心脏的左心房中是否发生了心房事件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述第一电极可以是双极电极,并且所述第二电极可以是双极电极。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述远侧延伸部可以支撑多个电极。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,由所述远侧延伸部支撑的多个电极可以包括处于所述远侧延伸部的远侧端部处的第一环电极以及向所述第一环电极的近侧间隔开的第二环电极。
在另一示例中,一种无引线起搏装置可以包括:壳体,其构造成定位在冠状窦内;远侧延伸部,其连接到所述壳体的远侧端部并且向所述壳体的远侧延伸;管腔,其延伸穿过所述远侧延伸部到远侧引导线端口;第一电极,其由所述壳体的近侧端部支撑;第二电极,其由所述壳体的远侧端部支撑;近侧引导线端口,其形成所述管腔的近侧端部,并且在第一电极与第二电极之间的一定位置处延伸穿过所述壳体的一侧;第三电极,其由所述远侧延伸部支撑;以及处理模块,其位于所述壳体的内部空间内,并且电联接到所述第一电极、第二电极和第三电极;其中所述处理模块可以构造成基于使用所述第一电极和第二电极中的一者或两者感测到的近场信号来确定是否发生了心房事件,并且基于使用第三电极感测到的近场信号来确定是否发生了心室事件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述处理模块可以构造成基于对是否发生了心房事件的确定以及对是否发生了心室事件的确定来生成心脏刺激脉冲。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述处理模块可以构造成基于使用所述第一电极和第二电极中的一者或两者感测到的远场信号来确定是否发生了心室事件。
在再一示例中,一种使用无引线起搏装置的方法可以包括:使用无引线起搏装置的位于患者心脏的冠状窦中的壳体所支撑的电极来感测患者心脏的心房的近场信号;使用无引线起搏装置的位于从冠状窦延伸的血管中的远侧延伸部所支撑的远侧电极来感测患者心脏的心室的近场信号;基于通过由所述壳体支撑的电极感测到的近场信号来识别心房心脏事件;以及基于由所述远侧电极感测到的近场信号来识别心室心脏事件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述方法可以进一步包括基于识别到的心房心脏事件和识别到的心室心脏事件中的一者或两者来生成心脏刺激脉冲。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述方法可以进一步包括使用由所述无引线起搏装置的位于患者心脏的冠状窦中的壳体所支撑的电极来感测患者心脏的心室的远场信号,以及基于由所述壳体支撑的电极感测到的远场信号来识别心室心脏事件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,其中由所述壳体支撑的电极是第一电极,所述方法可以进一步包括使用所述无引线起搏装置的位于患者心脏的冠状窦中的壳体所支撑的第二电极来感测患者心脏的心房的近场信号,以及基于由所述第一电极和第二电极中的一者或两者感测到的近场信号来识别在患者心脏的右心房或左心房中是否发生了心房心脏事件。
在另一示例中,一种用于向患者心脏输送起搏脉冲的无引线起搏装置可以包括:电源,其用于提供电源电压;壳体,其至少部分地支撑所述电源,其中所述壳体具有第一端部、第二端部以及在所述第一端部与所述第二端部之间延伸的一侧;一组电极,其由所述壳体支撑,并且与所述电源连通,并且其中所述壳体可以构造成设置在患者心脏的冠状窦内,并且可以在所述壳体设置在冠状窦内的同时促进血液流动经过所述壳体。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述无引线起搏装置可以进一步包括固定构件,其构造成使所述壳体的至少一部分与冠状窦的壁间隔开。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述一组电极可以包括阴极电极,并且所述固定构件可以构造成与冠状窦的壁交互,以偏压所述阴极电极抵靠在患者心脏的心肌上。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述固定构件可以包括相对于所述壳体的所述一侧沿径向延伸的一个或更多个锚定件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述一个或更多个锚定件可以围绕所述壳体的圆周对称地定位。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述一个或更多个锚定件可以围绕所述壳体的圆周不对称地定位,以偏压所述壳体的一部分抵靠在冠状窦的形成患者心脏的腔室壁的内壁上。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述固定构件可以包括沿着所述壳体定位的第一固定构件以及沿着所述壳体定位并且与所述第一固定构件沿轴向间隔开的第二固定构件。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述固定构件可以由生物可吸收材料制成。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述壳体可以包括沿着所述壳体的长度延伸的纵向地延伸的流动特征,并且所述流动特征可以构造成在冠状窦的壁与所述壳体的所述一侧之间建立空间,以允许血液在所述壳体位于冠状窦内的同时沿着所述壳体的所述长度流动。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述流动特征可以是沿着所述壳体的长度延伸的凹槽。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述流动特征可以是沿着所述壳体的长度延伸的平坦表面,使得所述壳体的截面的圆周包括倒圆部分和平坦部分。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述壳体可以沿着所述壳体的长度有角,以形成所述壳体的凹入侧和所述壳体的与所述壳体的凹入侧相对的凸出侧,并且当所述壳体位于冠状窦中时,所述壳体的凹入侧可以邻近冠状窦的形成患者心脏的腔室壁的壁。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述一组电极可以包括阳极电极和阴极电极。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述无引线起搏装置可以进一步包括在所述壳体的第一侧具有近侧引导线端口的引导线管腔,并且所述阴极电极可以暴露于冠状窦的处于所述壳体的与所述壳体的第一侧相对的第二侧的壁。
在另一示例中,一种用于向患者心脏输送起搏脉冲的无引线起搏装置可以包括:电源,其用于提供电源电压;壳体,其至少部分地支撑所述电源,所述壳体具有第一端部、第二端部以及在所述第一端部与所述第二端部之间延伸的一侧;一组电极,其由所述壳体支撑,并且与所述电源连通;多个锚定件,其围绕所述壳体沿周向延伸并且从所述壳体沿径向向外延伸,并且所述锚定件可以构造成在所述壳体定位在冠状窦内的同时与患者心脏的冠状窦的壁接合。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述多个锚定件可以沿着所述壳体的圆周对称地定位。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述多个锚定件可以沿着所述壳体的圆周不对称地定位。
在另一示例中,一种将无引线起搏装置定位在患者心脏的冠状窦中的方法可以包括:使引导线前进到患者的冠状窦中;使无引线起搏装置在已前进的引导线上前进,所述无引线起搏装置包括:电源,其用于提供电源电压;壳体,其至少部分地支撑所述电源,所述壳体具有第一端部、第二端部以及在所述第一端部与所述第二端部之间延伸的一侧;电极,其由所述壳体支撑并与所述电源连通;和流动特征,其构造成在所述无引线起搏装置位于冠状窦中时允许血液流动经过所述无引线起搏装置,并且所述方法可以进一步包括调节所述无引线起搏装置在冠状窦中的定向,以将所述无引线起搏装置的流动特征定位成邻近冠状窦的与冠状窦的形成患者心脏的腔室壁的壁间隔开的壁。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,当所述电极可以处于所述壳体的第一侧并且所述流动特征至少处于所述壳体的与所述壳体的第一侧相对的第二侧时,将所述无引线起搏装置的流动特征定位成邻近冠状窦的与冠状窦的形成患者心脏的腔室壁的壁相对的壁,会使电极定位在患者心脏中的心肌的目标区域处。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述流动特征可以包括围绕所述壳体的圆周不对称地间隔开的多个锚定件,并且所述锚定件中的一个或更多个可以接合冠状窦的与冠状窦的形成患者心脏的腔室壁的壁相对的壁,以在无引线起搏装置定位在冠状窦中时建立用于血液的流动路径。
在另一示例中,一种用于向患者心脏输送起搏脉冲的无引线起搏装置可以包括:电源,其用于提供电源电压;壳体,其至少部分地支撑所述电源,所述壳体具有第一端部、第二端部以及在所述第一端部与所述第二端部之间延伸的一侧;一组电极,其由所述壳体支撑,并且与所述电源连通,并且其中所述壳体可以有角以在所述壳体定位在患者心脏的冠状窦内时遵循患者心脏的轮廓。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,有角壳体可以将所述一组电极中的一个电极定置成抵靠在冠状窦的形成患者心脏的腔室壁的内壁上。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述无引线起搏装置可以进一步包括延伸穿过所述壳体的所述一侧并且形成延伸穿过所述壳体的引导线管腔的近侧端部的引导线端口,所述电极可以位于所述壳体的第一侧,并且所述引导线端口可以位于所述壳体的与所述壳体的第一侧相对的第二侧。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,有角壳体可以具有凹入侧和凸出侧,并且电极可以位于所述壳体的凹入侧。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,有角壳体可以具有平滑曲线部分,其曲率半径构造成遵循冠状窦的形成患者心脏的腔室壁的内壁的轮廓。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述壳体的平滑曲线部分可以跨越所述壳体的第一部分,并且所述壳体的第二部分可以向所述壳体的第一部分的远侧端部的远侧延伸。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述壳体可以具有第一部分和从第一部分的远侧端部向远侧延伸的第二部分,并且所述壳体的第一部分和第二部分形成所述壳体的凹入侧和所述壳体的凸出侧。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述壳体的第一部分可以具有第一线性纵向轴线,并且所述壳体的第二部分可以具有第二线性纵向轴线,其相对于第一线性纵向轴线形成小于180度的角度。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述一组电极中的一个电极可以位于所述壳体的第二部分的凹入侧,所述壳体的凹入侧具有织构化表面,并且所述壳体的凸出侧可以具有光滑表面。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述无引线起搏装置可以进一步包括相对于所述壳体的一侧沿径向延伸的多个锚定件,并且所述锚定件可以接合冠状窦的外壁,以将所述一组电极中的一个电极定置成抵靠在冠状窦的形成患者心脏的腔室壁的内壁上。
在另一示例中,一种用于将无引线起搏装置定位在患者的冠状窦中的定位系统可以包括无引线起搏装置,其具有:有角壳体;在远侧具有弯折部的输送导管;并且所述无引线起搏装置的有角壳体可以有角以便于经过在所述输送导管的远侧端部处的所述弯折部。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述无引线起搏装置进一步包括向有角壳体的远侧延伸的远侧延伸部。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,有角壳体可以具有第一部分和向第一部分的远侧端部的远侧延伸的第二部分。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,有角壳体可以具有平滑曲线部分,其具有遵循输送导管中的弯折部的曲率半径,并且所述平滑曲线部分可以跨越有角壳体的第一部分和第二部分。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述有角壳体的第一部分可以具有第一线性纵向轴线,并且所述有角壳体的第二部分可以具有第二线性纵向轴线,其相对于第一线性纵向轴线形成小于180度的角度。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述定位系统可以进一步包括引导线,其中所述有角壳体可以包括引导线端口,其延伸穿过所述有角壳体的一侧到从所述引导线端口向远侧延伸的引导线管腔,并且所述有角壳体可以构造成通过所述引导线端口接收引导线,并沿所述引导线随行到冠状窦。
在再一示例中,一种将无引线起搏装置定位在冠状窦中的方法可以包括:使引导线前进到冠状窦中;使无引线起搏装置在所述引导线上前进并进入冠状窦中,其中所述无引线起搏装置包括有角壳体;以及使所述无引线起搏装置与冠状窦的壁接触来定向有角壳体,使得有角壳体的凹入部分面向冠状窦的形成患者心脏的腔室壁的内壁。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,所述方法可以进一步包括使在远侧端部处具有弯折部的输送导管的远侧端部前进通过患者的下腔静脉到患者心脏的右心房,并且其中有角壳体可以有助于使所述无引线起搏装置前进经过输送导管的弯折部并进入冠状窦中。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,使无引线起搏装置与冠状窦的壁接触可以使无引线起搏装置的电极定置成抵靠在冠状窦的内壁上。
对于上述示例中的任一个而言替代地或附加地,在另一示例中,电极可以位于有角壳体的第一侧,并且有角壳体可以包括处于所述有角壳体的与所述有角壳体的第一侧相对的第二侧的引导线端口,并且使所述无引线起搏装置在穿过引导线端口的引导线上前进可以引导电极趋向冠状窦的内壁。
以上对一些实施例的概述并不旨在描述本公开的每个所公开的实施例或每个实施方式。下面的附图和具体实施方式更具体地例示这些实施例中的一些。
附图说明
结合附图考虑以下详细描述可以更全面地理解本公开,附图中:
图1是植入心脏内的示例无引线起搏装置的示意图;
图2是示例可植入无引线起搏装置的侧视图;
图3是示例可植入无引线起搏装置的示意性框图;
图4是示例可植入无引线起搏装置的远侧部分的剖视侧视图;
图5是用于与心脏中的示例可植入无引线起搏装置一起使用的示例取回装置的示意图;
图6a-6c是用于可植入无引线起搏装置的示例近侧构件的构造的侧视图;
图7是心脏中的示例可植入无引线起搏装置的示意图;
图8a和8b是心脏中的示例可植入无引线起搏装置的示意图;
图9是心脏中的示例可植入无引线起搏装置的示意图;
图10是心脏中的示例可植入无引线起搏装置的示意图;
图11是示例可植入无引线起搏装置的一侧;
图12是示例可植入无引线起搏装置的一侧;
图13a和13b是示意图,示出了示例可植入无引线起搏装置沿着引导线被推动并离开引导导管的远侧端部;
图14a和14b是用于与可植入无引线起搏装置的近侧构件接合和/或分离的示例互锁机构的示意图;
图15a-15c是用于与可植入无引线起搏装置的近侧构件接合和/或分离的示例互锁机构的示意图;
图16-21是一系列的示意图,其示出了示例可植入无引线起搏装置向患者心脏中的输送以及从患者心脏的取回。
虽然本公开服从各种修改和替代形式,但是其特定情况已经通过示例方式在附图中示出并且将被详细描述。然而,应该理解的是,意图不是将本公开的多个方面限制于所描述的特定实施例。相反,意图是覆盖落于本公开的精神和范围内的所有变型、等同方案和替代方案。
具体实施方式
对于以下定义的术语,这些定义将适用,除非在权利要求书中或在本说明书中的其它地方给出了不同的定义。
所有数值在本文中都被假定为被术语“大约”修饰,不管是否被明确地指出。术语“大约”通常是指一定范围的数字,其将被本领域的技术人员认为等同于所举值(即,具有相同的功能或结果)。在许多情况下,术语“大约”可以包括被四舍五入到最接近有效数字的数字。
通过端点对数值范围的列举包括处于该范围内的所有数字(例如,1-5包括1、1.5、2、2.75、3、3.80、4和5)。
如在本说明书和所附权利要求书中使用的,单数形式“一”、“一个”和“该”包括复数的对象,除非内容另有明确规定。如在本说明书和所附权利要求书中使用的,术语“或”在其意义上通常被采用来包括“和/或”,除非内容另有明确规定。
应指出的是,说明书中对“一实施例”、“一些实施例”、“其它实施例”等的提及表示所描述的实施例可以包括一个或更多个特定的特征、结构和/或特性。然而,这种记载并不一定意味着所有的实施例均包括所述特定的特征、结构和/或特性。附加地,当关联于一个实施例描述特定特征、结构和/或特性时,应该明白的是,这种特征、结构和/或特性也可以关联于其它实施例使用,不管是否有明确的描述,除非另有明确的相反说明。
以下详细描述应该参考附图来阅读,其中不同附图中的相似结构被相同地编号。附图(其并不一定按比例进行绘制)示出了说明性实施例而且并不旨在限制本公开的范围。
以下描述应该参考附图来阅读,其中不同附图中的相似元件被相同地编号。描述和附图(其并不一定按比例进行绘制)示出了例示性实施例而且并不旨在限制本公开的范围。
心脏起搏器提供电刺激到心脏组织,以使心脏收缩并且因此泵送血液穿过血管系统。常规起搏器通常包括电引线,其从皮下地或肌下地植入的脉冲发生器延伸到邻近心脏腔室的内或外壁定位的电极。作为常规起搏器的替代方案,自足式或无引线心脏起搏器已经被提出。无引线心脏起搏器是小型封装体,其通常固定到心脏腔室之中或周围的心内植入部位。小型封装体通常包括双极起搏/感测电极、电源(例如电池)和关联的电子电路(用于控制起搏/感测电极),并且因此提供电刺激到心脏组织和/或感测生理状况。在一些情况下,无引线心脏起搏器可以包括从小型封装体延伸的近侧和/或远侧延伸部,其中延伸部可以包括一个或更多个起搏/感测电极。封装体可以使用输送装置输送到心脏,所述输送装置可以推进穿过股静脉,进入下腔静脉中,进入右心房中,并进入冠状窦和延伸穿过和/或到达冠状窦的血管中。相应地,可能希望的是提供心脏起搏装置和输送装置,其便于推进穿过脉管系统。
本文中描述的无引线起搏装置可以检测和治疗心律失常,并且更具体而言,将电刺激治疗输送到患者心脏的右心房、左心房、右心房和/或左心室。例如,一个或更多个装置可以被植入患者心脏之上或之内,并且一个或更多个装置可以构造成根据一个或更多个治疗程序将电刺激治疗输送到患者心脏的一个或更多个腔室和/或治疗一个或更多个类型的检测到的心律失常。一些示例电刺激治疗包括心动过缓治疗、心脏再同步治疗(crt)、抗心动过速起搏(atp)治疗、除颤和/或心脏复律治疗及类似治疗。一些示例心律失常包括心房颤动或心房扑动、心室颤动和心动过速。
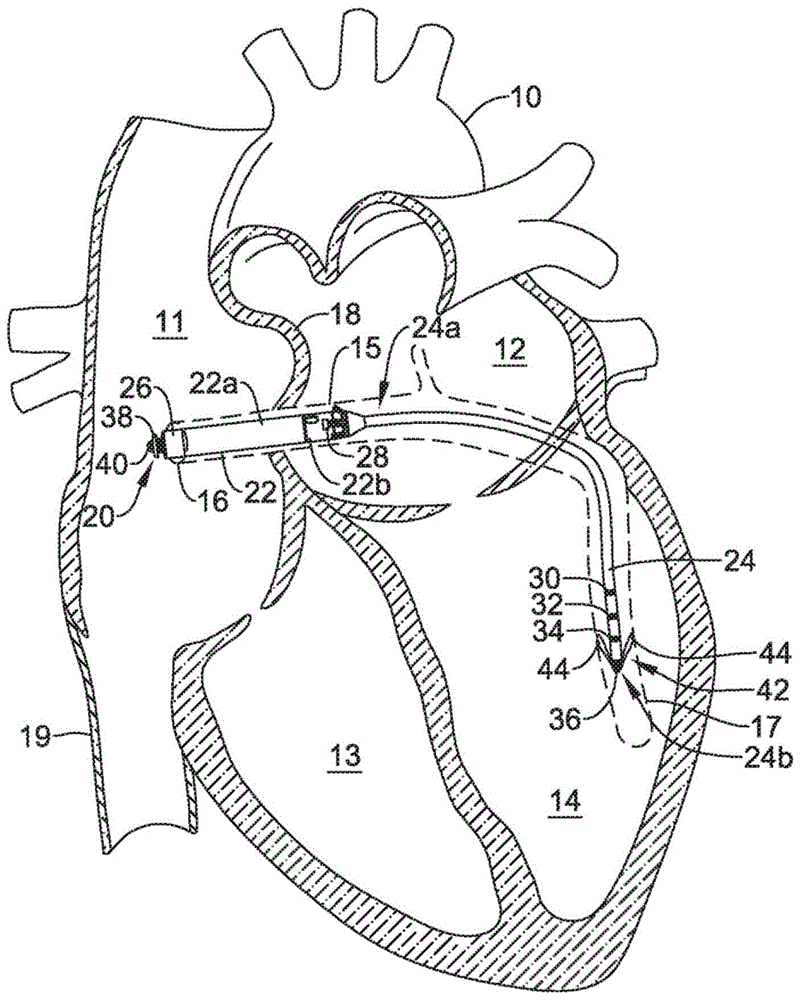
图1是一示例性系统的概念图,该系统用于向患者心脏输送电刺激治疗,包括将电刺激治疗输送到患者心脏的右心房、左心房、右心房和/或左心室。图1示出了植入心脏10之中和周围的示例性无引线起搏装置20。图1的心脏10被示出为显示右心房11、左心房12、右心室13、左心室14、冠状窦15、冠状窦口16、心大静脉17和隔膜18。
在图1的示例中,无引线起搏装置20包括具有近侧端部和远侧端部的壳体22以及向壳体22的远侧端部的远侧延伸的远侧延伸部24。然而,在一些情况下,可以不包括远侧延伸部24和/或可以包括一个或更多个其它远侧和/或近侧延伸部。壳体22可以是单个部分,或可以具有第一部分22a(例如,罐或本体)、第二部分22b(例如,头部或模制部分)、和/或一个或更多个其它部分。可想到的是,壳体22不必沿着其整个长度具有相同的截面形状。当被植入时,壳体22可以完全地或部分地设置在患者心脏10的冠状窦15内,而远侧延伸部24可以完全地或部分地设置在从冠状窦15延伸的血管内(例如,心大静脉17、前室间静脉和/或其它横向下行血管)。
壳体22可以具有适于植入患者心脏10内的目标位置处的任何尺寸。在一个示例中,壳体22可以具有足以装配在冠状窦15内的截面直径或面积。冠状窦15的尺寸在人类中可以在约0.12英寸(3mm)至约0.6英寸(15mm)之间变化。在不同实施例中,壳体22的直径可以定范围在约0.1英寸(2.54mm)至约0.4英寸(10mm)之间。这些尺寸可以允许壳体22植入不同尺寸的冠状窦内,同时仍允许足够的血液流动穿过冠状窦15。
壳体22可以在其外部表面上具有一个或更多个纹理。在一些情况下,壳体22的纹理可以包括便于壳体22稳定在患者体内的一定位置处的第一纹理以及便于血液通行经过壳体22的第二纹理。在壳体22可以构造成放置在患者的冠状窦15内的一个示例中,壳体22的旨在邻近和/或触及可兴奋心肌组织的第一侧(例如,如以下论述的凹入侧和/或另一侧)可以具有纹理化表面(例如,具有粗糙纹理)以便于将壳体22稳定在壳体22的预期位置处,并且壳体22的旨在邻近和/或触及脂肪或心包组织的第二侧(例如,如以下论述的凸出侧或另一侧)可以相对于壳体22的纹理化的第一侧具有光滑表面,以便于血液和/或其它流体通过冠状窦15内的壳体22。可以通过喷砂、喷珠、喷碳酸氢钠、电抛光、沉积和/或一种或更多种其它纹理化技术对纹理化表面进行纹理化。光滑表面可以从抛光、施加保护层或涂层和/或一种或更多种其它光滑处理技术而光滑。
在一些实施例中,无引线起搏装置20可以附加地包括一个或更多个电极。在一个示例中,壳体22可以支撑第一电极26和第二电极28,而远侧延伸部24可以支撑远侧电极。在一些情况下,远侧电极可以包括多个电极(例如,第一近侧环电极30、第二近侧环电极32、第三近侧环电极34、远侧环电极36、和/或一个或更多个其它电极)。虽然所描述的电极可以作为环电极示出,但是根据应用可以采用其它电极类型。
尽管由壳体22支撑的电极26、28被示出为分别设置在壳体22的第一部分22a和第二部分22b上,但是在一些情况下,设置在壳体22上的电极的数量和位置可以根据应用而变化。例如,在无引线起搏装置20包括两个壳体部分的情况下,无引线起搏装置20可以具有仅设置在第一壳体部分22a或第二壳体部分22b之一上的电极。可能希望的是在壳体22上将电极配置壳体22的各种纵向长度处,以便于在电极和冠状窦15的壁之间建立良好的接触。在一些情况下,无引线起搏装置20可以不具有设置在壳体22上的任何电极。
在壳体22上的电极26、28的一个示例配置中,位于壳体22的第一部分22a上的第一电极26可以是阳极电极,并且位于壳体22的第二部分22b上的第二电极28可以是阴极电极。然而,由于电极可以是双极电极,因此示例配置中的第一电极26可以改变为阴极电极,并且示例配置中的第二电极28可以改变为阳极电极。配对的双极电极的极性可以切换,而不管电极的位置如何。
当被提供时,无引线起搏装置20的电极可以用于向心脏10输送电刺激,和/或感测一个或更多个生理信号。在一些情况下,无引线起搏装置20可以使用电极(例如,电极26-36或其它电极)中的一个或更多个来与一个或更多个其它装置(比如但不限于一个或更多个其它无引线心脏起搏器和/或可植入心律转复除颤器)通信。在一些情况下,无引线起搏装置20可以使用传导通信技术进行通信,并且可以通过电极(例如,电极26-36或其它电极)中的一个或更多个来输送和/或接收通信信号。
在一些情况下,壳体22可以包括近侧构件38(例如,对接毂或其它构件),其大体上从壳体22的近侧端部延伸。在图1所示的示例中,近侧构件38可以从壳体22的第一部分22a延伸。在植入期间,近侧构件38可以可释放地联接到定位装置(图1中未示出)。当被联接时,定位装置的移动可以转移到壳体22,从而允许使用者(比如医生)将壳体22操纵到心脏10内的适当位置,例如进入或靠近冠状窦15。
在一些情况下,无引线起搏装置20可以从引导导管(图1中未示出)被输送,并且引导导管的环绕壳体22的部分可以符合壳体22,以在引导导管和壳体22之间建立可靠连接。当就位时,引导导管可以缩回,或者管心针或其它推动装置可以将壳体22推出引导导管。在这些情况下,近侧构件38可以进一步包括系绳锚定件40。在输送期间,系绳可以联接到系绳锚定件40,以允许使用者将壳体22拉回到引导导管内以便进一步定位。在一些情况下,系绳可以是绳子,并且绳子可以通过环抱系绳锚定件40而联接到系绳锚定件40。为了从壳体22释放系绳,使用者可以简单地切断系绳,或拉动系绳的一端直到系绳自身从系绳锚定件40解开。
尽管远侧延伸部24在图1中示出,但是在一些情况下,无引线起搏装置20可以不包括远侧延伸部24。在无引线起搏装置20包括从壳体22的远侧端部(例如,壳体22的第二部分22b,如图1中所示)延伸的远侧延伸部24的情况下。当被包括时,远侧延伸部24可以延伸到冠状窦15中并且固定在冠状窦15内。在一些情况下,远侧延伸部24可以延伸穿过冠状窦15并进入心大静脉17(如图1中所示)或从冠状窦延伸的一个或更多个其它血管中。
远侧延伸部24可以包括近侧端部24a和远侧端部24b。远侧延伸部24的远侧端部24b可以包括一个或更多个固定构件42。固定构件42可以帮助将远侧延伸部24的远侧端部24b固定在冠状窦15或心大静脉17内。固定构件42可以包括一个或更多个锚定件44(例如,叉齿、螺旋线圈、爪或其它锚定件),其由硅、生物相容性聚合物、生物相容性金属、另一生物相容性材料、形状记忆材料(例如,镍钛诺或其它形状记忆材料)和/或生物可吸收材料制成。可以采用生物可吸收材料来促进从患者移除无引线起搏装置20,因为内皮生长原本可能发生在锚定件44上。锚定件44可以从远侧延伸部24径向向外延伸并且压靠心大静脉17的壁。锚定件44和心大静脉17的壁之间的力可以将远侧延伸部24的远侧端部24b保持就位。
固定构件42的锚定件44(例如,以及因而的固定构件42)可以有角以允许轻松插入通过身体血管(例如,静脉、冠状窦等),同时便于抵靠身体血管的瓣膜固定在目标部位和/或植入位置处。在一些情况下,固定构件42的锚定件44可以向近侧有角,以便于向远侧插入到身体血管中和/或穿过身体血管,并且可以在近侧方向上从远侧延伸部24的纵向轴线径向向外延伸,以接合身体血管中的瓣膜并将远侧延伸部24固定在植入位置处(例如,用以防止或限制近侧移动)。
尽管在图中远侧延伸部24上示出了一个固定构件42,但是远侧延伸部24可以支撑一个或更多个附加固定构件,其与图中示出的固定构件42沿轴向间隔开。在其它情况下,远侧延伸部24可以不包括固定构件42。
在一些情况下,固定构件42可以包括一个或更多个电极或线环,并且可以用作天线以与一个或更多个其它装置通信和/或接收来自所述一个或更多个其它装置的电能。例如,无引线起搏装置20可以通过固定构件42的电极和/或线环使用感应和/或传导通信技术接收能量传递和/或进行通信。
如以上提及的,远侧延伸部24可以包括一个或更多个电极(例如,电极30-36)。在这些情况中的一些中,电极30-36可以设置为靠近远侧延伸部24的远侧端部24b并且远离壳体22,然而在其它情况下,远侧延伸部24上的电极中的一个或更多个可以跨越远侧延伸部24的一定长度(例如,整个长度)。
在一些情况下,远侧延伸部24上的电极可以用于向心脏10输送电刺激。例如,无引线起搏装置20可以通过电极中的一个或更多个的组(例如,来自电极30-36或其它电极的组)将电刺激输送到心脏10的左心室14。在一些情况下,无引线起搏装置20可以使用电极30-36中的两个或更多个同时地或有延迟地(例如经由多电极起搏)将电刺激输送到心脏10的左心室14。在一些附加或替代情况下,无引线起搏装置20可以使用电极30-36中的一个或更多个来与一个或更多个其它装置通信(例如,电极30-36可以用作天线)。例如,无引线起搏装置20可以通过电极30-36中的一个或更多个使用感应或传导通信技术来接收能量传递和/或进行通信。
无引线起搏装置20上的电极26-36和/或其它电极可以有能力感测电信号、提供电刺激信号、或感测电信号且提供电刺激信号。信号处理、通信和/或治疗脉冲生成可以发生在无引线起搏装置的任何部分处(适当的处理模块可以位于此处)。在一个示例中,用于无引线起搏装置20的电极(例如,电极26-36和/或其它电极)的信号处理、通信和治疗脉冲生成可以发生在壳体22内的或由壳体22支撑的模块中,但这不是必需的。
无引线起搏装置20的电极26-36和/或其它电极可以构造成执行心脏激活事件的近场和/或远场感测。心脏激活事件的“近场”感测是指感测起源于对应电极所在之处的局部腔室(例如,电极正在感测之处的同一腔室)的心脏激活事件。心脏激活事件的“远场”感测是指感测起源于除对应电极所在之处的局部腔室之外的腔室的心脏激活事件。例如,如果无引线起搏装置20的电极位于冠状窦15中,且电极邻近冠状窦15的形成右心房11的壁的壁附近,则电极正在近场感测右心房激活事件,并且正在远场感测左心房激活事件、左心室激活事件和右心室激活事件。
在图1的示例中,其中无引线起搏装置20植入冠状窦15以及从冠状窦15延伸的血管(例如,心大静脉17)中,第一电极26(例如,壳体22上的位于近侧的电极)可以位于冠状窦15中邻近右心房11,第二电极28(例如,壳体22上的位于远侧的电极)可以位于冠状窦15中邻近左心房12,并且由远侧延伸部24支撑的电极30-36可以位于心大静脉17中邻近左心室14。在这种植入构造中,第一电极26可以感测在右心房11中的心房激活事件(p波)的近场信号并向右心房11的心脏组织提供起搏脉冲,第二电极可以感测在左心房12中的心房激活事件(p波)的近场信号并向左心房12的心脏组织提供起搏脉冲,并且由远侧延伸部24支撑的电极30-36可以感测源自心房并通过房室结和希浦(his-purkinje)路径传导在左心室14中的心室激活事件(r波)的近场信号,并向左心室14的心脏组织提供起搏脉冲。
附加地或替代地,无引线起搏装置20的电极26-36或其它电极可以通过远场感测来感测信号。例如,可以由壳体22支撑的电极26、28可以感测远场心室激活活动(r波),并且由远侧延伸部24支撑的电极30-36可以感测远场心房激活活动(p波)。然而,这种感测到的信号可能被衰减和延迟和/或幅度和持续时间可能不足以可靠地感测心房和心室激活活动,并且在考虑通过远场感测感测到的信号时可能需要考虑通过近场感测感测到的信号。
在一些情况下,无引线起搏装置20可以作为单个装置植入(例如,没有一个或更多个其它无引线起搏装置或者一个或更多个可植入心律转复除颤器),其可以根据需要向右心房11、左心房12、右心室13和/或左心室14提供电刺激。例如,无引线起搏装置20可以构造成根据治疗程序输送电刺激以治疗心房颤动或心房扑动。然而,在其它情况下,无引线起搏装置20可以与在心脏10之中和/或周围的一个或更多个不同位置处植入的一个或更多个其它可植入心律转复除颤器和/或一个或更多个其它无引线起搏装置一起植入。
在使用无引线起搏装置20的一个示例中,无引线起搏装置20可以是用于向心脏10输送心脏再同步治疗(crt)的单个或多个装置系统的一部分。在这些示例中,无引线起搏装置20可以感测右心房11和左心房12之一者或两者中的心电信号。一旦无引线起搏装置20感测到传播通过右心房11和/或左心房12的心电信号,则无引线起搏装置20可以在一延迟周期(例如,av延迟)之后将起搏脉冲输送到左心室14。延迟周期的长度可以被确定或被选择成使得无引线起搏装置20可以在传播的心电信号到达右心室13并使右心室13收缩时向左心室14输送起搏脉冲。以这种方式,无引线起搏装置20可以进行操作以提供右心室13和左心室14的同步收缩。在一些附加情况中,无引线起搏装置20可以基于感测到的心率来调节延迟周期。例如,当无引线起搏装置20感测到心率增加时,无引线起搏装置20可以缩短延迟周期的长度。相反地,当无引线起搏装置20感测到心率降低时,无引线起搏装置20可以延长延迟周期。
如所论述的,无引线起搏装置20可以经由冠状窦15将起搏脉冲输送到右心房11和/或左心房12。在这些实施例中,无引线起搏装置20可以在无引线起搏装置20将起搏脉冲输送到右心房11和/或左心房12之时或稍后开始计算延迟周期。与前述实施例一样,这可以引起右心室13和左心室14的同步收缩。在无引线起搏装置20是在右心室13内具有附加无引线起搏装置的系统的一部分的情况下,无引线起搏装置20可以在无引线起搏装置20向右心房11和/或左心房12输送起搏脉冲之后将触发信号传送到附加无引线起搏装置。在接收到触发之后,附加无引线起搏装置可以在其自身的延迟周期之后将起搏脉冲输送到右心室13。在这些示例的至少一些中,附加无引线起搏装置的延迟周期与无引线起搏装置20的延迟周期可以是一致的,使得附加无引线起搏装置和无引线起搏装置20两者同步地将起搏脉冲输送到右心室13和左心室14。然而,在其它实施例中,附加无引线起搏装置的延迟周期与无引线起搏装置20的延迟周期可以是不同的,例如通过右心室13和左心室14的传导不同时,以便使右心室13和左心室14同步收缩。
图2是示例性无引线起搏装置20的示意图。示例性无引线起搏装置20可以包括具有第一壳体部分22a和第二壳体部分22b的壳体22,有时具有向壳体22的远侧延伸的远侧延伸部24。壳体22可以是一体式壳体或可以包括两个或更多个壳体部分(例如,第一部分22a、第二部分22b和/或一个或更多个其它壳体部分),在其中容纳无引线起搏装置20的一个或更多个部件。壳体22通常可以包括生物相容性材料,比如生物相容性金属和/或聚合物,并且在被植入患者的身体内时,可以将无引线起搏装置20的部件密闭地密封隔绝于患者身体的流体和组织。无引线起搏装置20可以附加地具有一个或更多个电极,比如电极26、28和/或其它电极,其在所示的示例中被壳体22支撑(例如,驻留在壳体22上,从壳体22延伸,和/或除此之外以一定方式被壳体22支撑)。在一些情况下可想到的是壳体22可以具有不同数量的电极,或完全没有电极。
在壳体22包括两个或更多个部分的情况下,第一部分22a可以是本体,并且第二部分22b可以是头部。第一部分22a(例如,本体)可以由适于封装无引线起搏装置20的电子部件的生物相容性金属材料或其它材料制成。第二部分22b(例如,头部)可以由生物相容性聚合物或其它材料制成。在一些情况下,第二部分可以由聚合物制成,并且通过包覆模制工艺模制在壳体22的第一部分22a的远侧端部上。当第二部分22b由模制技术形成时,远侧延伸部24可以通过在远侧延伸部24的近侧端部上模制第二部分22b而连接到壳体22。
在一些情况下并且如以上论述的,壳体22可以包括近侧构件38(例如,对接毂),其从壳体22的第一部分22a的近侧端部延伸。在一些情况下,近侧构件38可以具有延伸部46,其具有第一外径并从壳体22突出,其中延伸部46的近侧端部可以连接到或形成具有第二直径的附属部48。在图2中示出的示例中,附属部48的第二外径可以大于延伸部46的第一外径,但其它合适的构造也是可想到的。
在植入期间,定位装置可以可释放地联接到近侧构件38。当联接好时,定位装置的移动可以转移到壳体22,从而允许使用者在植入期间定位无引线起搏装置20。在一些情况下,代替或加上延伸部46和附属部48,近侧构件38可以包括互锁机构的一半,并且定位装置可以具有互锁机构的第二半,其可以可释放地联接到近侧构件38的互锁机构。
在一些情况下,壳体22可以包括固定构件50。固定构件可以构造成在无引线起搏装置20被植入心脏10的冠状窦15内时,将无引线起搏装置20保持在冠状窦15内。固定构件50可以包括一个或更多个锚定件52(例如,叉齿、螺旋线圈、爪或其它锚定件),其由硅、生物相容性聚合物、生物相容性金属、另一生物相容性材料、形状记忆材料(例如,镍钛诺或其它形状记忆材料)和/或生物可吸收材料制成。可以采用生物可吸收材料来促进从患者移除无引线起搏装置20,因为生长原本可能发生在锚定件52上。锚定件52可以从远侧延伸部24径向向外延伸并且压靠冠状窦15的壁。锚定件52与冠状窦15的壁之间的力可以将壳体22保持就位在冠状窦15内。
固定构件50的锚定件52(例如,以及因而的固定构件50)可以有角以允许轻松插入通过身体血管(例如,静脉、冠状窦等),同时便于抵靠身体血管的瓣膜固定在目标部位和/或植入位置处。在一些情况下,固定构件50的锚定件52可以向近侧有角,以便于向远侧插入到身体血管中和/或穿过身体血管,并且可以在近侧方向上从壳体22的纵向轴线径向向外延伸,以接合身体血管中的瓣膜并将壳体22固定在植入位置处(例如,用以防止或限制近侧移动)。
在至少一些示例中,固定构件50可以进一步相对于冠状窦15的管腔将壳体22保持期望配置中,例如漂浮在冠状窦15的管腔的中部(例如,当锚定件52围绕壳体22相等地沿周向间隔开时),或者压靠在冠状窦15的形成心脏10的腔室壁的壁上(例如,当锚定件52围绕壳体22沿周向间隔开,但不是相等地)。
尽管在图中在壳体22上示出了一个固定构件50,但是壳体22可以支撑一个或更多个附加固定构件,其与图中示出的固定构件50沿轴向间隔开。在其它情况下,壳体22可以不包括固定构件50。
在一些情况下,固定构件50(和/或固定构件42)可以包括一个或更多个电极或线环,并且可以用作天线以与一个或更多个其它装置通信和/或接收来自所述一个或更多个其它装置的电能。例如,无引线起搏装置20可以通过固定构件50的电极和/或线环使用感应和/或传导通信技术接收能量传递和/或进行通信。
壳体22的第二部分22b可以包括一个或更多个凹部53。在一个示例中,壳体22的第二部分22b可以包括凹部53,其与固定构件50的每个锚定件52对齐,使得锚定件52可以在无引线起搏装置向目标位置(例如,冠状窦15)输送期间,响应于被施加的力(例如,来自引导导管、导入器护套等)而铰动并至少部分地定位在对应凹部53内。
在至少一些情况下,壳体22可以具有延伸穿过壳体22的一侧的引导线端口54,其中所述一侧从壳体22的第一端部延伸到第二端部。在一些情况下,引导线端口54可以设置在壳体22的第二部分22b之中或附近,并且可以构造成接收引导线。在无引线起搏装置20包括远侧延伸部24的情况下,远侧延伸部24可以包括延伸到远侧延伸部24的远侧端部24b的远侧末端外的对应引导线端口。在这种情况下,引导线可以沿心大静脉17(或与冠状窦15连通的其它血管)放置。可以通过将远侧延伸部24穿到引导线的近侧端部上,然后使无引线起搏装置20在引导线上前进直到就位,来使无引线起搏装置20在引导线上随行。在无引线起搏装置20不包括远侧延伸部24的实施例中,壳体22可以包括第二引导线端口。
远侧延伸部24可以是薄的、细长的和柔性的构件,特别是相对于壳体22。例如,远侧延伸部24可以是在壳体22的长度的两倍到十倍之间。附加地并且如以上论述的,远侧延伸部24可以具有一个或更多个固定构件42。在一些情况下,固定构件42可以设置在远侧延伸部24的远侧端部24b之处或附近。在一些情况下,远侧延伸部24可以包括一个或更多个电极(例如,电极30-36)。
电极30-36和/或其它电极可以设置成接近远侧延伸部24的远侧端部24b,或者可以沿着远侧延伸部24的长度散开(例如,彼此纵向间隔开),如图2中所示。远侧延伸部24上的电极的其它配置和/或构造也是可想到的并且可以被采用。在电极的一个示例配置中(例如,采用电极30-36),电极中的每个可以是环电极,并且电极36(例如,远侧环电极)可以设置在远侧延伸部24上靠近远侧延伸部24的远侧末端,电极34(例如,第三近侧环电极)可以在电极36的近侧间隔四十(40)毫米,电极32(例如,第二近侧环电极)可以在电极34的近侧间隔十(10)毫米,并且电极30(例如,第一近侧环电极)可以在电极32的近侧间隔十(10)毫米。电极30-36的这种构造可以在远侧延伸部24插入心大静脉17或其它血管中时与左心房12对齐,以允许无引线起搏装置20感测和/或起搏患者心脏10的左心房12。在一些情况下,远侧延伸部24可以被偏压以形成一定形状,比如螺旋线圈或者一个或更多个环。
图3是可以容纳在无引线起搏装置20的壳体22内的一个或更多个电子模块的示意性框图。在一些情况下,无引线起搏装置20可以包括能量存储模块56(例如,用于供应/提供电源电压的电源)、处理模块58、通信模块60、脉冲发生器模块62、电感测模块64和/或机械感测模块66。图3还示出了导体68-72,其可以从模块56、58、60、62、64中的一个或更多个延伸,和/或延伸到一个或更多个电极(例如,电极26-36或其它电极)。尽管图3中仅示出了三个导体,但是不同的导体可以从壳体22中的模块延伸到无引线起搏装置20的电极中的每个。相应地,在至少一些情况下,无引线起搏装置20的所有电子元件和能量存储模块可以容纳在壳体22内,而仅有一个或更多个导体延伸到电极。在一个示例中,导体68可以延伸到由壳体22支撑的第一电极26,导体70可以延伸到由壳体22支撑的第二电极28,并且导体72可以代表延伸到远端延伸部上的电极30-36的导体,其中单个导体可以延伸到各个电极30-36并且延伸到远侧环电极36的导体可以沿着和/或绕着远侧延伸部24的管腔76盘绕直到导体到达远侧环电极36。附加地或替代地,根据需要,其它导体可以绕着管腔76盘绕。延伸到电极的每个导体可以与其它导体电隔离,并且在一些情况下,每个导体可以通过其自己的管腔延伸到相关的电极,但这不是必需的。
在图3中示出的示例中,通信模块60可以电联接到电极26-36,并且可以构造成向患者的组织输送通信信号比如电通信脉冲,以与其它装置比如传感器、编程器、其它医疗装置和/或类似者通信。如本文所使用的电通信脉冲可以是任何调制信号,其通过自身或结合一个或更多个其它调制信号将信息传送到另一装置。在一些实施例中,电通信脉冲可以局限于亚阈值信号,其不会导致心脏的捕获但仍传送信息。电通信脉冲可以被输送到位于患者身体之内或之外的另一装置。通信模块60可以附加地构造成感测由可以位于患者身体之内或之外的其它装置输送的电通信脉冲。
通信模块60可以进行通信以帮助实现一个或更多个期望的功能。一些示例功能包括输送感测数据、使用通信数据来确定比如心律失常等事件的发生、协调电刺激治疗的输送和/或其它功能。在一些情况下,无引线起搏装置20可以使用电通信脉冲来传达原始信息、处理过的信息、消息和/或命令、和/或其它数据。原始信息可以包括比如感测到的电信号(例如,感测到的ecg)、从联接的传感器收集到的信号等信息。在一些实施例中,处理过的信息可以包括已使用一种或更多种信号处理技术过滤了的信号。处理过的信息还可以包括由无引线起搏装置20和/或另一装置确定的参数和/或事件,比如所确定的心率、所确定心跳的定时、其它所确定事件的定时、阈值跨越的确定、所监测时间周期的到期、活性水平参数、血氧参数、血压参数、心音参数等。消息和/或命令可以包括指示另一装置采取行动的指令等、发送装置的即将发生的动作的通知、从接收装置进行读取的请求、向接收装置写入数据的请求、信息消息和/或其它消息命令。
脉冲发生器模块62可以构造成生成电刺激脉冲,并经由电极26-36中的一个更多个将电刺激脉冲输送到患者的组织,以便实现一种或更多种电刺激治疗。如本文所使用的电刺激脉冲旨在包括任何电信号,其可以被输送到患者的组织,以达治疗任何类型的疾病或异常的目的。例如,当用于治疗心脏疾病时,脉冲发生器模块62可以生成电刺激起搏脉冲,用于捕获患者的心脏,即响应于所输送的电刺激脉冲使心脏收缩。在另一实施例中,电刺激脉冲可以是用于为心脏除去颤动的除颤/心脏复律脉冲。在又另一实施例中,电刺激脉冲可以是抗心动过速起搏(atp)脉冲。这些仅仅是一些示例。当用于治疗其它病痛时,脉冲发生器模块62可以生成适于神经刺激治疗或类似者的电刺激脉冲。脉冲发生器模块62可以包括一个或更多个电容器元件和/或其它电荷存储装置,以协助生成并输送适当的电刺激脉冲。在所示实施例中,脉冲发生器模块62可以使用存储在能量存储模块56中的能量来生成电刺激脉冲。
在至少一些实施例中,通信模块60(亦或无引线起搏装置20)可以进一步包括切换电路,用以选择性地连接电极26-36中的一个或更多个到通信模块60,以便选择通信模块60输送电通信脉冲给哪个电极26-36。可想到的是,通信模块60可以经由传导信号、射频(rf)信号、光信号、声信号、电感耦合和/或任何其它合适的通信方法与其它装置通信。
脉冲发生器模块62可以包括修改电刺激脉冲的能力,比如通过调节电刺激脉冲的脉冲宽度和/或幅度。当起搏心脏时,这可以帮助定制电刺激脉冲以捕获特定患者的心脏,有时会减少电池使用量。对于神经刺激治疗,调节脉冲宽度和/或幅度可以帮助针对特定应用定制治疗和/或帮助使治疗对于特定患者更有效。
电感测模块64可以电连接到一个或更多个电极26-36,并且电感测模块64可以构造成接收通过电极26-36传导的心电信号。在一些实施例中,当无引线起搏装置20已植入冠状窦15和/或从其延伸的血管中时,心电信号可以代表来自无引线起搏装置20的电极所在之处或周围的腔室的局部信息(例如,近场信息)。例如,如果无引线起搏装置20的电极位于心脏的心室之处或周围,则由电极感测到的心电信号可以是近场信号并且可以代表心室心电信号。
机械感测模块66可以包括或电连接到各种传感器,比如加速度计、血压传感器、心音传感器、血氧传感器和/或测量心脏和/或患者的一个或更多个生理参数的其它传感器。机械感测模块66在存在时可以收集来自传感器的指示各种生理参数的信号。电感测模块64和机械感测模块66两者可以连接到处理模块58,并且可以将代表感测到的心电信号和/或生理信号的信号提供给处理模块58。尽管相对于图2描述为分离的感测模块,但是在一些实施例中,电感测模块64和机械感测模块66可以组合到单个模块中。
处理模块58可以构造成控制无引线起搏装置20的操作。例如,处理模块58可以构造成接收来自电感测模块64的近场和/或远场心电信号和/或来自机械感测模块66的生理信号。基于接收到的近场和/或远场信号,处理模块58可以确定例如心律失常的发生和类型(例如,在发生心房和/或心室事件时)。在一个示例中,处理模块58可以识别p波、r波、t波和/或其它所关注的心脏事件,以及每个波/事件的相对定时。
在如图1中所见的已植入无引线起搏装置20的一个示例中,处理模块58可以基于使用由壳体22支撑的电极26、28中的一个或更多个感测到的近场信号来确定是否发生了心房事件,基于使用由远侧延伸部24支撑的电极30-36中的一个或更多个感测到的近场信号确定是否发生了心室事件,和/或基于使用双极或其它构造中的空间上相对的电极(例如,壳体22上的电极26、28中的一个或更多个以及远侧延伸部24上的电极30-36中的一个或更多个)感测到的近场信号来确定是否发生了心房事件或心室事件。附加地或替代地,处理模块58可以基于使用电极26、28中的一个或更多个感测到的远场信号来确定是否发生了心室事件,基于使用电极30-36中的一个或更多个感测到的远场信号来确定是否发生了心房事件,和/或基于使用双极或其它构造中的空间上相对的电极(例如,壳体22上的电极26、28中的一个或更多个以及远侧延伸部24上的电极30-36中的一个或更多个)感测到的远场信号来确定是否发生了心房事件或心室事件。此外,取决于哪个电极感测到了信号,处理模块58可以基于感测到的信号的类型(例如,远场或近场)、感测信号的电极在心脏10内的位置、以及感测到的信号相对于一个或更多个其它感测到的信号的定时中的一个或更多个,来确定所确定的心脏激活事件发生在哪个腔室。例如,处理模块可以表明基于在右心房11处从第一电极26感测到的近场信号确定的心脏事件表明心脏事件是右心房心脏激活事件。
处理模块58可以进一步接收来自通信模块60的信息。在一些实施例中,处理模块58可以附加地使用这种接收到的信息来确定心律失常的发生和类型。然而,在其它实施例中,无引线起搏装置20可以使用接收到的信息,而不是从电感测模块64和/或机械感测模块66接收的信号。例如,接收到的信息比从电感测模块64和/或机械感测模块66接收的信号更准确时,或者电感测模块64和/或机械感测模块66已被禁用或从无引线起搏装置20被省略时。
基于所确定的心律失常(例如,所确定的心房和/或心室心脏事件),处理模块58可以根据一种或更多种电刺激治疗来控制脉冲发生器模块62以生成电刺激脉冲,从而治疗所确定的心律失常。例如,处理模块58可以控制脉冲发生器模块62以生成具有变化参数和处于不同序列的起搏脉冲,以实现一种或更多种电刺激治疗。例如,在控制脉冲发生器模块62以输送心动过缓起搏治疗时,处理模块58可以控制脉冲发生器模块62以输送设计成以规则间隔捕获患者心脏的起搏脉冲,以帮助防止患者心脏下降到低于预定阈值。在一些情况下,起搏的速率可以随着患者的活性水平的增加而增加(例如,速率自适应起搏)。对于atp治疗,处理模块58可以控制脉冲发生器模块62以快于患者固有心率的速率输送起搏脉冲,以试图迫使心脏响应于所输送的起搏脉冲而不是响应于固有心电信号发生跳动。一旦心脏跟随起搏脉冲,则处理模块58可以控制脉冲发生器模块62以将所输送的起搏脉冲的速率向下降低到更安全的水平。在crt中,处理模块58可以控制脉冲发生器模块62以与另一装置协调地输送起搏脉冲,以使心脏更有效地收缩。在脉冲发生器模块62能够生成用于除颤/心脏复律治疗的除颤和/或心脏复律脉冲的情况下,处理模块58可以控制脉冲发生器模块62以生成这种除颤和/或心脏复律脉冲。在一些情况下,处理模块58可以控制脉冲发生器模块62以生成电刺激脉冲,以提供与上述那些示例不同的电刺激治疗。
除了控制脉冲发生器模块62以生成不同类型的电刺激脉冲且处于不同的序列,在一些实施例中,处理模块58还可以控制脉冲发生器模块62以生成具有变化的脉冲参数的各种电刺激脉冲。例如,每个电刺激脉冲可以具有一定的脉冲宽度和脉冲幅度,并且可以从一个或更多个电极被引导。处理模块58可以控制脉冲发生器模块62来以特定脉冲宽度、特定脉冲幅度和特定电极(例如,无引线起搏装置20的电极26-36或其它电极中的一个或更多个)生成各种电刺激脉冲。作为一个示例,如果电刺激脉冲没有有效地捕获心脏,则处理模块58可以使脉冲发生器模块62调节电刺激脉冲的脉冲宽度和/或脉冲幅度。对各种电刺激脉冲的特定参数的这种控制可以帮助无引线起搏装置20实现更有效地输送电刺激治疗。
在一些实施例中,处理模块58可以进一步控制通信模块60来向其它装置发送信息。例如,处理模块58可以控制通信模块60以生成一个或更多个电通信脉冲来与装置系统的其它装置通信。例如,处理模块58可以控制通信模块60来以特定序列生成电通信脉冲,其中特定序列传达不同的信息。通信模块60还可以接收用于处理模块58的潜在动作的通信信号。
在再一些情况下,处理模块58可以控制切换电路,通过其使通信模块60和脉冲发生器模块62输送电通信脉冲和/或电刺激脉冲到患者的组织。如上所述,通信模块60和脉冲发生器模块62两者可以包括电路,用于将一个或更多个电极26-36连接到通信模块60和/或脉冲发生器模块62,使得那些模块可以经由壳体22所支撑的电极26、28中的一个或更多个和/或远侧延伸部24所支撑的电极30、32、34、36中的一个或更多个将电通信脉冲和电刺激脉冲输送到患者的组织。通过其使通信模块60和/或脉冲发生器模块62输送电通信脉冲和电刺激脉冲的一个或更多个电极的特定组合可以影响通信脉冲的接收性和/或电刺激脉冲的有效性。尽管描述的是通信模块60和脉冲发生器模块62中的每个可以包括切换电路,但是在一些实施例中,无引线起搏装置20可以具有连接到无引线起搏装置20的通信模块60、脉冲发生器模块62和电极26-36的单个切换模块。在这类情况下,处理模块58可以控制切换模块来视情况连接无引线起搏装置20的模块60/62和电极26-36,以经由壳体22所支撑的电极26、28中的一个或更多个和/或远侧延伸部24所支撑的电极30、32、34、36中的一个或更多个生成电通信脉冲和电刺激脉冲给患者的组织。
在一些情况下,处理模块58可以包括预编程芯片,比如超大规模集成(vlsi)芯片或专用集成电路(asic)。在这类实施例中,芯片可以预编程有控制逻辑,以便控制无引线起搏装置20的操作。通过使用预编程芯片,处理模块58可以使用比其它可编程电路更少的电力,同时能够维持基本功能,从而潜在地增加无引线起搏装置20的电池寿命。在其它情况下,处理模块58可以包括可编程微处理器或类似者。这种可编程微处理器可以允许使用者在制造之后调节无引线起搏装置20的控制逻辑,从而允许无引线起搏装置20比使用预编程芯片时更大的灵活性。
在附加情况中,处理模块58可以包括存储器电路,并且处理模块58可以在存储器电路上存储信息和从存储器电路读取信息。在其它情况下,无引线起搏装置20可以包括分离的存储器电路(未示出),其与处理模块58通信,使得处理模块58可以从该分离的存储器电路读取信息并向该分离的存储器电路写入信息。存储器电路(无论是处理模块58的一部分还是与处理模块58分离)可以是易失性存储器、非易失性存储器、或易失性存储器和非易失性存储器的组合。
能量存储模块56可以提供电源给无引线起搏装置20以用于其操作。在一些实施例中,能量存储模块56可以是不可再充电的锂基电池。在其它实施例中,不可再充电的电池可以由其它合适的材料制成。在一些实施例中,能量存储模块56可以包括可再充电的电池。在又一些其它实施例中,能量存储模块56可以包括其它类型的能量存储装置,比如超级电容器。
图4示出了壳体22的第二部分22b和远侧延伸部24的近侧部分24a的局部示意性剖视图。如图4中所见,壳体22的第二部分22b的一侧中的引导线端口54处于穿过壳体22的第二部分22b形成的引导线管腔74的近侧端部处。引导线管腔74可以延伸穿过壳体22的第二部分22b到远侧延伸部24的管腔76的近侧端部,其中管腔76终止于远侧端口(图4中未示出)。引导线端口54、引导线管腔74和延伸穿过远侧延伸部24的管腔76可以形成用于接收引导线的通道,以便于无引线起搏装置20沿引导线随行到目标位置。在一些情况下,无引线起搏装置20可以使用快速交换技术在引导线上随行,其中线被反装通过远侧延伸部24中的远侧端口,其与管腔76连通并穿过管腔76、引导线管腔74和引导线端口54。可以采用其它引导线随行技术。
延伸穿过壳体的第二部分22b的引导线管腔74可以以任何方式形成。在一个示例中并且当第二部分22b可以通过包覆模制工艺形成时,芯体材料可以插入到包覆模具中,模制材料(例如,聚氨酯树脂、硅和/或适于包覆模制工艺的其它生物相容性模制材料)可以被施加,并且芯体材料可以在包覆模制材料固化后从包覆模制材料被移除以形成引导线端口54和引导线管腔74。引导线端口54在壳体22的第二部分22b中的这种定位可以便于壳体22的第一部分22a的部件被密闭地密封在第一部分22a内。
引导线端口54可以沿着壳体22的任何部分形成。如图4中所示,引导线端口54可以位于壳体22的第二部分22b的近侧端部与定位在壳体22的第二部分22b内的第二电极28之间。在一些情况下,引导线端口54可以形成在壳体22的与第二电极28的暴露部分29相对的一侧,如图4中所示。第二电极28的暴露部分29可以是电极的整个部分或者可以是电极的一部分,其通过壳体22的第二部分22b的材料暴露,而电极的另一部分可以被第二部分22b的材料覆盖。在一个示例中,第二电极28可以是环电极,并且第二电极28的一个或更多个部分可以通过壳体的材料暴露,以形成第二电极28的暴露部分29。
引导线端口54和第二电极28的暴露部分29相对于彼此的这种构造可以便于第二电极28的暴露部分29与患者身体内的目标位置之间的接触。例如,引导线将希望尽可能地遵循最大曲率半径,并且由于患者的冠状窦15围绕心脏10延伸,插入冠状窦中的引导线可以沿着冠状窦的外壁(例如,与冠状窦的形成心脏10的腔室壁的壁相对的壁)自然地随行,因为引导线能够遵循比其原本将能够遵循的曲率半径更大的曲率半径。因此,在该示例中,当引导线端口54位于壳体22的第二部分22b的与电极28的暴露部分29相对的一侧时,引导线端口54可以邻近冠状窦15的与冠状窦15的形成心脏10的腔室壁间隔开的壁,并且作为结果,电极28的暴露部分29可以定位在冠状窦15的形成心脏10的腔室壁的壁附近。
图5示出了植入在图1的心脏10内的无引线起搏装置20的特写图。无引线起搏装置20可以构造成使得壳体22的大部分或全部(如图5中所示)设置在冠状窦15内。在一些情况下,壳体22可以具有从壳体22向近侧延伸的近侧构件38,并且无引线起搏装置20可以构造成使得在无引线起搏装置20被植入时,近侧构件38可以向近侧延伸穿过冠状窦口16并进入右心房11中。在图5的示例中,其中近侧构件38延伸穿过冠状窦口16到右心房11,近侧构件38可以比设置在其它位置(例如,冠状窦15内或其它位置)时更容易接近,从而在有必要移除无引线起搏装置20时,允许通过延伸穿过插入右心房11中的导管80(例如,引导导管或输送导管)的取回装置78(例如,勒除器或其它装置,其具有用于延伸穿过脉管系统的细长本体以及构造成与无引线起搏装置20的近侧构件38接合的接合远侧端部)更容易地取回无引线起搏装置20。
图6a-6c示出了近侧构件38的各种示例性构造。近侧构件38可以包括从壳体22的近侧端部延伸的柔性或刚性的延伸部46以及在延伸部46的近侧端部处的附属部48。尽管壳体22和延伸部46的构造可以变化,但是在图6a-6c中,壳体22和延伸部46可以在延伸部46的近侧端部处具有不同类型的附属部48的情况下大致类似。图6a示出了平坦附属部48,其大致垂直于延伸部46。图6b示出了箭头形附属部48,其在它从近侧端部向远侧延伸时沿径向向外延伸。图6c示出了圆形或球形附属部48。尽管在图6a-6c中示出了平坦形、箭头形和球形附属部48,但是可以采用附属部48的足以通过取回装置78抓取或接合的其它构造。
如以上讨论的,无引线起搏装置20可以构造成植入患者的冠状窦15内,并因此被定尺寸为装配在冠状窦内。然而,当放置在冠状窦15中时,无引线起搏装置20可以闭塞或部分地闭塞冠状窦15,并且防止或限制流动穿过冠状窦15的血液。尽管流动穿过冠状窦15的血液最终可以找到去往心脏10的其它通路,但是有可能通过构造无引线起搏装置20以在被插入冠状窦15中时建立流体通路,来植入无引线起搏装置20,同时允许血液流动经过已植入的无引线起搏装置20。
图7示出了无引线起搏装置20的一个示例构造,其构造成在无引线起搏装置20植入冠状窦15内的同时允许血液流动经过无引线起搏装置20。如以上讨论的,无引线起搏装置20可以包括具有一个或更多个锚定件52的一个或更多个固定构件50。如图7中所示,固定构件50的锚定件52可以从无引线起搏装置20的壳体22径向向外延伸。作用在冠状窦15的壁上的固定构件50可以使冠状窦15的壁扩张,并在冠状窦15的壁与无引线起搏装置的壳体22的一侧之间建立空间86。由于建立了空间86,因此血液可以有能力在无引线起搏装置20植入冠状窦15中的同时经过无引线起搏装置20并流动到心脏10中。尽管图7中示出了四(4)个锚定件,但是可以采用任何其它数量的锚定件,其适于建立供流体在壳体22的一侧与冠状窦的壁之间流动的空间86。
在一些情况下,固定构件50的锚定件52可以沿着壳体22的圆周不对称地定位或定置,如在图7中的一个示例中所示的。在一些情况下,锚定件52的定位可以围绕壳体22的圆周不对称地定位或定置,使得第二电极28的暴露部分可以与冠状窦15的第二壁部84(例如,内壁部)接触,所述第二壁部还形成心脏的腔室(例如,如图7中所示的左心房12或其它腔室)的壁。在这种情况下,锚定件52可以至少抵靠冠状窦15的第一壁部82(例如,外壁部)扩张,所述第一壁部与冠状窦15的形成心脏10的腔室壁的第二壁部84大致相对。这种抵靠第一壁部82的扩张可以引导第二电极28的暴露部分29抵靠第二壁部84,以促进心脏的壁(例如,第二壁部84)与第二电极28之间的良好电接触。附加地,引导线端口54(图7中未示出)可以位于壳体的与第二电极28的暴露部分29相对的一侧且邻近锚定件52,以进一步促进锚定件52作用在第一壁部82上以及第二电极28的暴露部分29与第二壁部84之间的良好电接触。虽然图7示出了第二电极28的位置,但是可以采用类似的构造来确保无引线起搏装置20的其它电极(例如,电极26、30、32、34和36和/或其它电极)与心脏10的壁之间的良好电接触。
在一些情况下,第二壁部84可以邻近于和/或可以包括可兴奋心肌组织,而第一壁部82可以邻近于和/或可以包括脂肪或心包组织(例如,不是可兴奋心肌组织的组织)。可兴奋心肌组织可以是心脏10的组织,其响应于电刺激以达促进心脏10的操作的目的(例如,促进响应于电刺激对心脏10的捕获)。图8a-8b示出了无引线起搏装置20的另一示例构造,其构造成在无引线起搏装置20植入冠状窦15内的同时允许血液流动经过无引线起搏装置20。如图8a-8b中所示,无引线起搏装置20可以包括处于壳体22中的凹部88。凹部88可以具有任何尺寸,并且可以处于壳体22上的任何位置,其适于在无引线起搏装置20植入冠状窦内时,促进血液流动经过无引线起搏装置20。尽管在图8a-8b中示出了单个凹部88,但是壳体22中可以存在多于一个的凹部88。在一些情况下,凹部88可以是细长凹槽(图8a)和/或细长平坦表面(图8b),其延伸达壳体22的一定长度或一定长度的一部分。可想到凹部88的其它构造,并且可以采用适于允许血液通过无引线起搏装置(在植入冠状窦15中时)的任何凹部。例如,凹部88可以是引导线管腔,其中引导线管腔可以构造成在引导线不处于引导线管腔内时允许血液流动穿过其中。
当在壳体22中具有凹部88的无引线起搏装置20植入冠状窦15内时,空间86可以建立在壳体22与冠状窦15的第一壁部82之间,以促进血液流动经过已植入的无引线起搏装置20并进入心脏10的右心房11中。附加地,引导线端口54(图8a-8b中未示出)可以位于壳体22的与第二电极28的暴露部分29相对的一侧且邻近凹部88,以促进第二壁部84与第一电极26和/或第二电极28的暴露部分29之间的良好电接触。在凹部88可以是引导线管腔的情况下,凹部88的引导线管腔的近侧开口可以位于壳体22的近侧端部处,并且凹部88的引导线管腔的远侧开口可以邻近于引导线端口54并在引导线端口54的近侧,以允许引导线延伸穿过凹部88并进入引导线端口中。虽然图8a-8b示出了第二电极28的位置,但是可以采用类似的构造来确保无引线起搏装置20的其它电极(例如,电极26、30、32、34和36和/或其它电极)与心脏10的壁之间的良好电接触。此外,凹部88可以被采用为锚定件52或其它固定构件50的替代方案或与之组合,以保持第一电极26和/或第二电极28的暴露部分29与心脏10的第二壁部84之间的良好电接触,并且在壳体22与冠状窦15的第一壁部82之间建立空间,以允许血液流动经过已植入的无引线起搏装置20。
图9-12示出了无引线起搏装置20的弯曲的或有角的壳体22。在一些情况下,在壳体22中进行弯曲或设置一定角度可以便于将无引线起搏装置20输送到心脏10并将无引线起搏装置20植入心脏10中。附加地或替代地,壳体22或壳体22的至少一部分可以是柔性的或可弯折的。在一个示例中,当壳体22有角或弯曲时,壳体22和其中的部件可以在一个或更多个位置处是柔性的,以便于矫直壳体22(例如,在输送通过直通道期间和/或在一个或更多个其它时间),并且允许壳体22恢复弯曲或有角构造(例如,在输送期间当壳体22穿过弯曲通道时、被植入时和/或一个或更多个其它时间)。壳体22可以构造成被动地(例如,响应于附近的解剖结构)或主动地(例如,响应于控制)在直的与弯曲的或有角的构造之间移动。
图9是右心房11、左心房12和冠状窦15的示意性局部剖视图,其中无引线起搏装置20插入冠状窦15中。无引线起搏装置20的壳体22可以沿着其长度有角(例如,壳体22可以具有平滑曲线或具有相对于彼此形成小于180度的角度的两个或更多个部分),并且构造成紧密遵循心脏10的曲线。此外,当第二电极28的暴露部分29处于壳体22的凹入侧时,第二电极28的暴露部分29可以在无引线起搏装置20插入到冠状窦15中并且具有角构造的壳体22接触冠状窦15时,对着和/或面向第二壁部84定向。
图10是具有导管80的心脏的示意性局部剖视图,其中导管80在远侧端部处(例如,在远侧末端之处或附近)具有弯折部81,以便于进入始自右心房11的通道(例如,冠状窦15、右心耳、或与右心房11连通的其它通道)。在一些情况下,一旦无引线起搏装置20通过下腔静脉19到达右心房11中,可能需要相对急剧转弯进入冠状窦15或其它通道中。因此,在一些情况下,导管80的远侧端部处的弯折部81(例如,曲线或转弯)可以定位用于引导装置从下腔静脉19进入右心房11中,然后进入冠状窦15中。替代地或附加地,导管80的远侧端部处的弯折部81(例如,曲线或转弯)可以定位用于引导装置从上腔静脉进入右心房11中,然后进入冠状窦15中。弯折部81的角度可以取决于被采用来实现进入冠状窦15的进场路径和/或取决于一个或更多个其它考虑因素。此外,无引线起搏装置20的壳体22中的曲线或角度可以便于遵循导管80中的弯折部81并转弯进入冠状窦15中,如图10中所示。
图11和12示出了无引线起搏装置20的具有弯曲或有角构造的壳体22的示例构造。图11示出了具有平滑曲线的壳体22。平滑曲线可以仅沿着壳体22的第一部分22a、仅沿着壳体的第二部分22b、或者沿着壳体22的第一部分22a和第二部分22b两者的至少一部分延伸。第二电极28的暴露部分29可以位于壳体22的凹入侧之上或附近,并且引导线端口54可以位于壳体22的凸出侧之上或附近,以便于第二电极28的暴露部分29与冠状窦15的第二壁部84之间的良好接触,例如类似于图9中所示。附加地或替代地,第一电极26可以暴露于或位于壳体22的凹入侧上,以便于第一电极26与冠状窦的第二壁部84之间的良好接触,例如类似于图9中所示。
图12示出了壳体22,其具有第一有角部分92和第二有角部分94,这可以导致壳体22具有凹入侧和凸出侧。在一些情况下,第一有角部分92可以具有第一纵向轴线l1,并且第二有角部分94可以具有第二纵向轴线l2,其中第一纵向轴线l1和第二纵向轴线l2以角度a相交,该角度可以相对于第一线性纵向轴线l1小于180度。第一有角部分92和第二有角部分94可以沿着壳体22的长度形成在任何位置处。例如,第二有角部分94可以从第一有角部分92沿着第一壳体部分22a(如图12中所示)、沿着第二壳体部分22b、或者在第二壳体部分22b的近侧端部和第一壳体部分22a的远侧端部处延伸。类似于如以上相对于具有平滑曲线的壳体所论述的,第二电极28的暴露部分29可以位于壳体22的凹入侧之上或附近,并且引导线端口54可以位于壳体22的凸出侧之上或附近,以便于第二电极28的暴露部分29与冠状窦15的第二壁部84之间的良好接触,类似于图9中所示。附加地或替代地,第一电极26可以暴露于或位于壳体22的凹入侧上,以便于第一电极26与冠状窦的第二壁部84之间的良好接触。
在一些实施例中,无引线起搏装置20可以用引导导管(比如图13a的导管80)输送到植入部位(例如,冠状窦15和/或与之连接的血管)。导管80可以大体上定尺寸为能够在导管80的管腔内接收无引线起搏装置20、引导线96和定位装置98。当设置在导管80内时,无引线起搏装置20可以通过互锁机构100连接到定位装置98。互锁机构100可以与壳体22的近侧构件38可释放地联接。
为了将无引线起搏装置20输送到植入部位,无引线起搏装置20可以穿到引导线96上,该引导线96可能已经在冠状窦15内定位和/或沿心大静脉17(或从冠状窦15延伸的其它血管)定位。在一些情况下,引导线96可以穿过引导线端口54并且离开远侧延伸部24的远侧端部,如图13a中所示。包括无引线起搏装置20在内的导管80然后可以在引导线96上前进。一旦就位,比如在心脏10的冠状窦15中,导管80可以例如沿箭头102的方向缩回,从而暴露无引线起搏装置20,如图13b中所示。无引线起搏装置20可以通过定位装置98保持就位。在其它情况下,代替或加上缩回导管80,定位装置98可以用于将无引线起搏装置20推出导管80的端部。
在一些情况下,定位装置98可以是半柔性的,但保持足够的刚度以在被操纵时向无引线起搏装置20施加力。例如,一旦导管80就位,并且导管80然后被缩回,使用者可以通过近侧构件38操控定位装置98以在无引线起搏装置20上施加力。以这种方式,使用者可以将无引线起搏装置20操纵到期望的位置。一旦就位,使用者可以分离互锁机构100与近侧构件38,并且可以缩回引导线96和导管80,包括定位装置98。一旦分离,使用者然后可以从身体缩回导管80,包括定位装置98。
图14a和14b示出示例性定位装置98和互锁机构100。在图14a和14b中所示的示例中,定位装置98可以包括护套104。在一些情况下,护套104可以包括一个或更多个结构特征,其施加足够水平的刚度以允许使用者在定位装置98经由近侧构件38联接到壳体22时推动、拉动和以其它方式移动定位装置98和壳体22。例如,在一些实施例中,护套104可以是编织护套,或者可以具有联接到护套104的编织覆盖物或内支撑构件。在其它实施例中,定位装置98可以包括联接到护套104的盘绕线。
在所示示例中,互锁机构100可以包括构件106,其可以在一端终止于叉状部108。在一些情况下,构件106可以一直沿护套104延伸,并且可以被使用者操控以使叉状部108在打开位置(参见图14a)与闭合位置(参见图14b)之间转换。
图14a示出了处于打开构造并且靠近近侧构件38设置的叉状部108。当联接互锁装置100时,使用者可以将叉状部108定位在靠近或围绕近侧构件38的位置。一旦就位,使用者可以操控互锁构件106,以将叉状部108从打开位置转换到闭合位置。图14b示出了处于围绕近侧构件38的闭合位置的叉状部108。
在图14a和14b中所示的示例中,护套104可以有能力相对于互锁构件106移动。例如,在打开位置,护套104可以不设置成围绕叉状部108,如图14a中所示。叉状部108可以被偏压,使得当叉状部108在护套104外时,叉状部108可以扩张到比护套104的直径更大的程度。为了将叉状部108转换到闭合位置,使用者可以简单地使护套104相对于互锁构件106滑动,比如趋向叉状部108。当护套104滑动趋向叉状部108时,叉状部108的至少一部分可以被护套104压缩。对叉状部108的这种压缩可以使叉状部108转换到闭合位置,如图14b中所示。
图15a-15c示出了定位装置98和互锁机构100的另一实施例。图15a示出了设置在近侧构件38附近的互锁机构100和定位装置98。在这些实施例中,定位装置98可以包括护套104,如相对于图14a-14b所描述的。互锁机构100可以包括胀大构件110和囊体112。在一些情况下,囊体112可以具有大体环形形状,或具有孔或凹部的任何其它合适形状。为了联接到近侧构件38,使用者可以将处于未胀大状态的囊体112围绕近侧构件38定位,如图15b中所示。一旦囊体112围绕近侧构件38定位,使用者可以通过注射胀大介质穿过胀大构件110并进入囊体112中来使囊体112胀大。当囊体112胀大时,它围绕近侧构件38扩张,从而将近侧构件38固定到囊体112并因此固定到定位装置98,如图15c中所示。当联接好时,使用者可以操纵定位装置98从而操纵附接到近侧构件38的壳体22到期望位置。
图16-21示出了引导线96和导管80在无引线起搏装置20植入心脏10内时的示例用途。尽管所示的方法包括通过下腔静脉获得对患者心脏10的进入,但是对心脏10的进入可以另外或替代地通过上腔静脉和/或其它入路来获得。
在一些实施例中,将无引线起搏装置20植入心脏10内可以通过将引导线(比如引导线96)定位心脏10内开始。引导线96可以通过患者皮肤中的延伸到已经被导入器或其它装置扩张的动脉或静脉(例如,股静脉或其它血管)中的开口实现对心脏10的进入,所述导入器或其它装置具有扩张特征并且使引导线96前进到达和/或穿过下腔静脉或其它身体血管。
在一些情况下,引导线96可以具有设置在引导线96的一端上的一个或更多个不透射线的标记。当引导线96对于心脏10被操纵就位时,这种不透射线的标记可以允许通过一个或更多个医学成像系统更容易地观察引导线96。在一些实施例中,不透射线的标记可以彼此间隔达已知距离。在这类实施例中,通过计算心脏10内的两个特征之间的不透射线的标记的数量,可以确定两个特征之间的距离。在一些实施例中,无引线起搏装置20可以以各种尺寸制造,或者无引线起搏装置20的各个部分,比如壳体22和远侧延伸部24,可以以各种尺寸和长度制造。通过确定患者心脏10的不同特征之间的距离,例如冠状窦口16与右心房11中的隔膜18之间的距离,如图16中所示,可以为特定患者选择合适尺寸的壳体22或远侧延伸部24。
在测量心脏10的各个特征之间的距离之后,或者在不需要这种测量的实施例中,然后可以将引导线96定位在冠状窦15内,如图17中所示。在一些情况下,引导线96可以被操纵一路穿过冠状窦15并进入心大静脉17或从冠状窦15延伸的其它血管中。一旦引导线96就位,可选地容纳有无引线起搏装置20的导管80可以在引导线96上被操纵到心脏10内的位置。图18示出了前进到冠状窦15并定位在冠状窦15内的导管80。在一些情况下,导管80可以在导管80的远侧端部之处或附近(例如,在远侧末端之处或附近)具有扩张器特征。扩张器特征可以构造成接合冠状窦15的口16,并且扩张和/或插进冠状窦15,使得无引线起搏装置20可以被接收在其中。在一个示例中,导管80的扩张器特征可以呈圆锥形渐缩末端的结构,使得导管80向冠状窦15中的前进使冠状窦15的内径扩大。在另一示例中,扩张器特征可以是倒圆的,或者可以具有比圆锥形渐缩部更急变的渐缩部。可想到其它扩张器特征构造,并且可以采用适于扩张冠状窦15的任何构造。因此,如果冠状窦15有必要被扩大以接收无引线起搏装置20,则导管80的远侧端部或远侧末端可以前进通过冠状窦15的口16,以使冠状窦15扩张足以接收无引线起搏装置20的量。
图19示出了引导导管80和无引线起搏装置20定位在冠状窦15内,并且近侧构件38向近侧延伸离开冠状窦15进入右心房11中,其中定位装置98和互锁机构100连接到近侧构件38。可以在互锁机构100连接到近侧构件38的同时通过以定位装置98在引导线96上且穿过导管80推动无引线起搏装置20,来使无引线起搏装置20前进到该位置。替代地,可以仅采用导管80或引导线96中的一个来定位无引线起搏装置20。此外,可想到的是,可以既不以导管80也不以引导线96来定位无引线起搏装置20。在一些情况下,互锁机构100可以连接到或可以接合近侧构件38,直到经由与定位装置98的近侧端部的交互将它确实地或有意地释放或断开。
在一些情况下,可以在冠状窦15内调节无引线起搏装置20。在一个示例中,可以经由与定位装置98的近侧端部的交互来调节无引线起搏装置20在冠状窦15内的定向,以将流动特征(例如,固定构件50和/或凹部88)定位邻近冠状窦15的壁(例如,第一壁部82),其与冠状窦15的形成患者心脏10的腔室壁的壁(例如,第二壁部84)间隔开。这种调节可以便于将一个或更多个电极放置成与冠状窦15的形成患者心脏10的腔室壁的壁良好接触(例如,在患者心脏10中的心肌的目标部位之处或附近)。
一旦无引线起搏装置20就位,定位装置98、导管80和引导线96就可以缩回。图20示出了无引线起搏装置20在定位装置98、导管80和引导线96已经缩回之后可以如何定位的示例。尽管无引线起搏装置20的壳体22被示出为在冠状窦15中沿着右心房11和左心房12延伸,但是无引线起搏装置20的壳体22可以在冠状窦15内完全沿着右心房11或完全沿着左心房12定位。在一些情况下,无引线起搏装置20的壳体22可以沿着右心房11和左心房12两者定置,使得第一电极26与右心房11的组织接触并且第二电极28在与左心房12的组织接触。在这种情况下,无引线起搏装置20可以被编程为以相应的电极26、28或其它电极来感测和/或起搏右心房11和左心房12中的一个或更多个,因为电极是双极的。
在一些情况下,可以从冠状窦15移除已植入的无引线起搏装置20和/或可以调节已植入的无引线起搏装置20的定位。图21示出了取回装置78插入冠状窦15中并且与无引线起搏装置20的近侧构件38接合。一旦取回装置78已经接合无引线起搏装置20的近侧构件38,取回装置78和无引线起搏装置20可以从冠状窦15和患者心脏10完全取出,和/或重新定位在冠状窦15和/或与冠状窦15连通的血管内。在一些情况下,护套(未示出)可以插入冠状窦15中并且定位在无引线起搏装置20的至少一部分上,以使锚定件50朝向无引线起搏装置的纵向轴线铰动,并且促进无引线起搏装置20在冠状窦15内向近侧移动和/或离开冠状窦15。
本领域技术人员将意识到的是,本公开可以被体现为除了本文中描述和想到的特定实施例之外的多种形式。例如,如本文中所描述的,各种实施例包括被描述为执行各种功能的一个或更多个模块。然而,其它实施例可以包括附加模块,其将所描述的功能分离到比本文中描述的模块更多的模块上。附加地,其它实施例可以将所描述的功能整合到更少的模块中。
尽管可能已经相对于少于所有的实施例描述了各种特征,但是本公开可想到那些特征可以被包括在任一实施例上。此外,尽管本文中描述的实施例可能省略了各种所描述特征的一些组合,但是本公开可想到包括每个所描述特征的任何组合的实施例。因此,可以在形式和详情上发生偏差,而不背离如在所附权利要求书中描述的本公开的范围和精神。
- 还没有人留言评论。精彩留言会获得点赞!