一种新型抗抑郁缓控释给药系统的制作方法
本发明涉及一种抗抑郁药物的用于治疗抑郁症的控释给药系统,属于药剂
技术领域。
背景技术:
用药目的在于通过一定的给药途径给予治疗剂量的药物以达到所需的血液浓度,并维持所需的血药浓度。为了获得期望的治疗效果,可以使用不同的剂型。一次给药过程包括常规胶囊或片剂单次给药,在药物在体内吸收分布使血药浓度迅速上升,随即快速消除。普通剂型单次给药血药浓度难以长时间维持稳定的血药浓度。
目前常规剂型采用间隔重复给药来维持稳定血药浓度。达到稳定血药浓度所需时间取决于给药剂量和给药间隔;但是多次给药存在一定问题,例如:给药间隔时间与药物半衰期不匹配,会导致血药浓度波动较大。同事,在初始给药,需要一定的药物吸收时间血药浓度才能达到治疗剂量,难以快速缓解某些疾病症状。如果患者不按时服用药物,难以维持一定时间内的稳态血药浓度,也可能出现血药浓度较大波动,升至超过阈值产生毒性或严重不良反应,低于有效剂量无法产生药效。
因此控释药物制剂存在迫切需要。目前片剂,胶囊剂,酏剂和混悬剂是常规的药物剂型。这些常规剂型给药后血药浓度呈峰谷型,且不能维持一段时间稳态血药浓度。同时,这些剂型药物半衰期3~5h,每天需服用2~3次。因此需要控释剂型,定时、缓慢地向外释放药物,使血药浓度恒定,无"峰谷"现象,从而更好地发挥疗效。
目前现有的控释剂型,缓慢地向外释放药物,用于达到某些治疗效果。例如,在美国专利no.4327725;no.4612008;no.4765989和no.4783337公开。这些专利中公开了一种以恒定速率向外释放药物,维持稳定血药浓度的剂型,不会产生较大的血药浓度波动,减少药物毒副作用。
上述剂型在某些疾病治疗中可产生良好的疗效,但是37℃的体温下药物溶,这可能导致药物过早释放。给药后,药物制剂吸收流体后产生对流和流体静压力,药物溶解度增加,导致药物的过早释放。
针对上述问题,目前需要一种够定时、定量、匀速地向外释放药物的一种新型制剂。
技术实现要素:
针对上述问题,本发明拟提供一种能控制药物释放速率的剂型。本发明剂型可提供一种定时、定量、匀速地向外释放药物的一种剂型,减少药物过早释放现象,从而延长药物作用时间。同时,每天口服用一次,减少给药次数,增加患者顺应性。而且,可以减少胃肠道不良反应,避免药物毒性作用。采用药物及其药学上可接受的盐,可与聚合物作为载体形成药物组合物。
抗抑郁药主要用于治疗抑郁症和各种抑郁状态。常见的第一代抗抑郁药物有两种,即单胺氧化酶抑制剂(maoi)和三环类抗抑郁药(tca)。
单胺氧化酶类,如异丙肼是上世纪50年代问世的第一个抗抑郁药物。属于这一类的还有异卡波肼、苯乙肼、反苯环丙胺等。这些药物曾一度广为应用,不久因陆续出现与某些食物和药物相互作用,引起高血压危象、急性黄色肝萎缩等严重不良反应而被淘汰。
80年代后期出现了新一代半日受氧化酶抑制剂,即可逆性单胺氧化酶一个亚型(mao-a)抑郁剂,它的特点是:1对mao-a选择性高,对另一种同功酶mao-b选择性小,故仍可降解食物中的酷胺,从而减少高血压危象风险。2对mao-a抑制作用具有可逆性,仅8-10小时即可恢复酶的活性,而老的半日胺氧化酶抑制剂抑制时间长达2周之久,因而也降低了与食物相互作用的危险。主要产品有吗氯贝胺,剂量150-450mg/d,分次服。据称疗效与三环类抗抑郁药相当。
虽比老的半日胺氧化酶抑制剂安全,但仍应注意体位性低血压及潜在的食物、药物间相互作用,一般也不作为首选药。
三环类是继单胺氧化酶抑制剂之后的另一类抗抑郁药,以丙咪嗪为代表。三环类抗抑郁药共有产品10余种,我国除丙咪嗪外还有阿米替林、多虑平和氯丙咪嗪。马普替林虽为四环结构,但药理作用与三环类抗抑郁药一致。三环类抗抑郁药的适应证为各种类型抑郁症,有效率约70%-80%,起效时间1-2周,剂量范围50-250mg/d,缓慢加量,分次服。因镇静作用较强,晚间剂量宜大些。治疗范围血药浓度丙咪嗪和阿米替林为50-250ng/ml。
三环类抗抑郁药临床应用时间最长,药理作用研究得也最多最充分,简言之,其主要药理作用为:1阻滞单胺递质(主要为肾上腺素和5-ht)再摄取,使突触间隙单受含量升高而产生抗抑郁作用。2阻断多种递质受体,它与治疗作用无关,却是诸多不良反应的主要原因,如阻滞乙酰胆碱m受体,可能出现口干、视力模糊、窦性心动过速、便秘、尿潴留、青光眼加剧、记忆功能障碍;阻滞肾上腺素a1受体,可能出现加强哌唑嗪的降压作用、体位性低血压、头昏、反射性心动过速;阻滞组胺h1受体,可出现加强中枢抑制剂作用、镇静、嗜睡、增加体重、降低血压;阻滞多巴胺d2受体,可出现锥体外系症状、内分泌改变。
抗抑郁药物副作用较重者,宜减量、停药或换用其他药。一般不主张两种以上抗抑郁药联用,由于本病有较高复发率,症状缓解后尚应维持治疗4-6个月,以利巩固疗效,防止复发。
新型药物可选择性5-ht再摄取抑制药(ssri)是新型抗抑郁药物。本类药物从20世纪70年代开始研制,已开发有数十种,临床常用的有氟西汀、帕罗西汀、舍曲林、氟伏沙明、西酞普兰等。本类药物镇静作用小,也不损伤精神运动功能,对心血管和自主神经系统功能影响很小。本类药物还具有抗抑郁和抗焦虑双重作用,多用于脑内5-ht减少所致的抑郁症。
抗抑郁药是反映消除病理情绪低落、提高情绪。用以治疗抑郁症性疾病的精神药物。它不同于精神振奋剂,只能消除病理性抑郁情绪,并不提高正常人的情绪。已用于临床的有三类。
(一)三环类抗抑郁药(tricyclicantidepressants,tca):常用药物有丙咪嗪(imipramine)、阿米替林(amitriptyline)、多虑平(doxepine),氯丙咪嗪(chlorimipramine)等,治疗剂量为50~200mg/d。主要适用于内因性抑郁症及其它疾病中出现的抑郁症状。还可用于治疗症及惊恐发作。严重心、肝、肾疾患和青光眼患者禁用,老年、孕妇、前列腺肥大及癫痫患者慎用。
tca抗抑郁作用机理尚未tca阻断胺泵、减少突触前膜对生物胺的回收,特别是减少去甲腺素(ne)和5—羟色胺(5—ht)的回收,使突触后受体部位有效神经递质的浓度增高,起到抗抑郁作用。
tca的镇静作用出现最早,继之为饮食和行为方面的进步,一般在2~4周后才出现情绪改善。应用时,采取剂时递增法,于取得治疗效应后,继续应用治疗剂量治疗4~6周,然后递减至半量维持治疗6个月。
tca的副作用,以外周性抗胆碱能副作用为常见,如口干、便秘、视物模糊、排尿困难和体位性低血压,老年患者中可导致尿潴留,肠麻痹等。对血压的影响和对心脏的毒性较大,可引起心肌损害,应密切观察心律及心电图变化。还有诱发躁狂、双手细震颤及抗胆碱能性谵妄状态等副作用。
(二)单胺氧化酶抑制剂(monoamineoxidaseinhibitor,maoi)是最早出现的抗抑郁药,主要通过抑郁制单胺氧化酶(mao),减少中枢神经系统内单胺类递质的破坏,增加突触间隙内的浓度,起到提高情绪的作用。由于maoi的副作用较多,抗抑郁效果不及tca,近20年来已逐渐被tca取代。
常用药物有苯乙肼(肼类),从15mg每日2次开始,逐渐加量,最高日量为75mg;超苯环丙胺日用剂量为10~30mg。治疗期间应注意观察其抗胆碱能副作用和对肝脏的损害,有心血管、肝、肾疾病者忌用。服药期内不宜吃含酷胺较高的食物(如乳酪、鸡肝、啤酒等),否则易产生高血压危象。maoi和许多药物或食物产生交互作用应引起医务人员警惕和提醒患者注意。一般不与tca合用,如需改用tca时,应先停用maoi2周后,再开始服用tca。
(三)四环类抗抑郁药(tetracyclica)代表药物是麦普替林(maprotiline)疗效与tca相似,但具有奏效快、副作用少、抗抑郁作用谱广等优点。因其对心脏毒性较小,病人对该药的耐受性较好,更适用于老年或已有心血管疾病的抑郁症患者。用药方法同tca,最高日量为200mg。
抗抑郁药由于其病症和用药特点,临床上有联合用药,缓控释制剂对患者更加安全有效。
本发明中包含三环类抗抑郁药、单胺氧化酶抑制剂和四环类抗抑郁药,以及药学上可接受的复合物成分。
附图说明
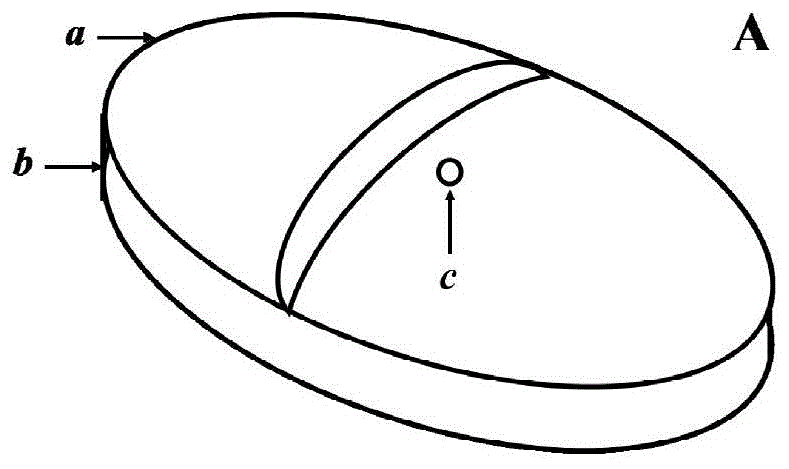
图1为本发明剂型的平面图。
图2为图1的剖面图。
图3为图1的外层示意图。
具体实施方式
在附图和说明书中,相关附图中的相同部分由相同数字标识。在说明书和附图的描述中较早出现的术语及其实施例在本公开的其他地方进一步描述。
这些附图是本发明提供剂型的实施例,但不局限于这些实施例。在图1中,本剂型a包括主体部分a,壁b是主体部分a包裹层,在图1中未标出。剂型a包括至少一个通道c,剂型a的内部与外部连接。图1展示了控释渗透剂,该渗透剂型通过渗透作用缓慢递送药物。本发明渗透控释剂型,可实现血液或组织中维持基本恒定的药物水平。渗透控释剂表示药物递送作用的持续时间超过常规药物递送所持续时间。
图2是图1的剖面图。如图2所示,剂型a包括主体部分a,壁b形成隔室d。在附图中,内部隔室d通过出口通道c与剂型a的外部相连。
剂型a中壁b包含全部或至少一部分药物组合物,该组合物可通过外部流体(如水性和生物流体)渗透到使用环境。壁b材料无毒,对隔室d中存在的药物和其他成分无渗透。壁b包括惰性的组合物,保持剂型a的药物物理和化学完整性。短语“保持其物理和化学完整性”是指壁b不会与剂型a中释放药物发生化学反应;壁b具有一个或多个出口c通道水溶性物质浸出或掺入壁b,促使药物渗出,不会对动物,人类或任何其他包含剂型成分产生不利影响的材料。壁b的材料包括纤维素酯聚合物,纤维素醚聚合物和纤维素酯醚聚合物。这些纤维素聚合物在脱水葡萄糖单元上的取代度ds范围,3≥ds>0。取代度是指存在于包含纤维素聚合物的脱水葡萄糖单元上的被取代基取代的羟基的平均数。代表性材料包括选自纤维素酰化物,纤维素二酰化物,纤维素三酰化物,乙酸纤维素,纤维素二乙酸酯,纤维素三乙酸酯,单、二和三纤维素链烷酸酯,单、二和三纤维素芳酸酯的成分。示例性的聚合物包括ds为1的的乙酰基含量为21%的乙酸纤维素;ds为1~2且乙酰基含量为21~35%的乙酸纤维素;ds为2~3且乙酰基含量为35~44.8%的乙酸纤维素等。更具体的纤维素聚合物包括具有1.8的ds,39.2~45%的丙基含量和2.8~5.4%的羟基含量的丙酸纤维素;ds为1.8,乙酰基含量为13~15%,丁酰基含量为34~39%的乙酸丁酸纤维素;乙酰基含量2~29%,丁酰基含量17~53%,羟基含量0.5~4.7%和ds为2.9~3的乙酸丁酸纤维素酯纤维素三酰化物,例如三戊酸纤维素,三月桂酸纤维素,三棕榈酸纤维素,三琥珀酸纤维素和三辛酸纤维素;ds为2.2~2.6的纤维素二酰化物,例如二琥珀酸纤维素。
另外的聚合物包括乙氧基含量为40%~55%的各种醚化程度的乙基纤维素,乙醛二甲基乙酸纤维素,乙酸纤维素氨基甲酸乙酯,乙酸纤维素氨基甲酸甲酯,乙酸纤维素二乙基氨基乙酸酯,半渗透性聚酰胺;半透性聚氨酯;半渗透性磺化聚苯乙烯;通过共阴离子聚阴离子和聚阳离子形成的半渗透性交联选择性聚合物,半渗透性轻度交联的聚苯乙烯衍生物,半渗透性交联的聚苯乙烯磺酸钠;半透性交联的聚(乙烯基苄基三甲基氯化铵)。
隔室d包括标识为药物层f的药物组合物e,该药物组合物包含用点标识的药物g。
该剂型包含的药物具有治疗抑郁症作用。该药物在体外可阻止神经对血清素、肾上腺素和多巴胺的吸收,且不抑制单胺氧化酶。该药物可拮抗利血平诱导的体温过低,增强左旋多巴的作用,减少组胺诱导的促肾上腺皮质激素释放,诱导急性和慢性给药后的环腺苷单磷酸,起到治疗抑郁症的作用。剂型a中药物f的治疗量为0.5mg至750mg,单个剂型包含2、5、10、25、40、50、75、100、150、250、300、500和600mg的药物f,用于以单剂量或多于一个剂量的方式给药延长时间在24小时内。具有治疗作用药物已在前面做了详细阐述。
药物组合物e包含药物f,包含药物的载体材料,所述组合物载体材料选自0%~25%wt羟丙基烷基纤维素的成分组成,其中烷基由1~7个碳组成,包括甲基纤维素成分的分子量为9000至1250000的乙基,异丙基,丁基,戊基和己基,以线g表示,以羟丙基甲基纤维素,羟丙基乙基纤维素,羟丙基异丙基纤维素,羟丙基丁基纤维素和羟丙基己基纤维素为例;选自0%~20%wt的羟烷基纤维素的成分,其中烷基为1~6个碳,包括甲基,乙基,丙基,丁基,戊基和己基,其中纤维素成分具有7500至750000的分子量,并且示例为斜线h代表的羟甲基纤维素,羟乙基纤维素,羟丙基纤维素,羟异丙基纤维素和羟丁基纤维素;选自0~35%wt的分子量为3500至750000的乙烯基聚合物的成分,该乙烯基聚合物由聚正乙烯基酰胺,聚正乙烯基乙酰胺,聚正乙烯基乙基乙酰胺,聚-n-乙烯基甲基丙酰胺,聚正乙烯基乙基丙酰胺,聚正乙烯基甲基异丁酰胺,聚正乙烯基-2-吡咯烷酮,聚正乙烯基哌啶酮也称为聚乙烯吡咯烷酮和聚正乙烯基吡咯烷酮,聚正乙烯基己内酰胺,聚-n-乙烯基-5-甲基-2-吡咯烷酮和聚-n-乙烯基-3-甲基-2-吡咯烷酮,以及具有选自乙酸乙烯酯,乙烯醇,乙烯基的聚n-乙烯基吡咯烷酮共聚物;小圆圈i表示的氯化物,氟乙烯,丁酸乙烯酯,月桂酸乙烯酯和硬脂酸乙烯酯;包括0~35%wt的具有结构式(c6h12o5)n«h2o的麦芽糖糊精聚合物,其中n为3至7500,麦芽糖糊精聚合物为500至1250000数均分子量,以小圆形i表示;选自0~40%wt聚乙烯氧化物,具有分子量在100000~600000,由半方形q表示。组合物e包含0~4.5%wt润滑剂,包括硬脂酸镁,硬脂酸钙或硬脂酸等。组合物e中所有成分的总重量以100%wt计(重量百分比)。
隔室d包括位移组合物或推动层j;推动层j由具有重复分子单元(-o-ch2ch2-)n的聚合物组成,其中n是由聚(环氧烷)表示的50000至300000的正整数,以波浪线k表示;具有(c6h12o5)nh2o结构的麦芽糖糊精聚合物0,其中n为50至62000,且分子量为9000至10000000,由三角形l表示;其中包含分子量为10000至5000000的羧甲基纤维素聚合物,包括碱性羧甲基纤维素,羧甲基纤维素钠和羧甲基纤维素钾,羧甲基纤维素铵,羧甲基-2-羟乙基纤维素钠,羧甲基-甲基纤维素钠,碱性羧甲基-羟丙基甲基纤维素,碱式羧甲基-2-羟乙基甲基纤维素碱羧甲基-2-羟丁基甲基纤维素,碱羧甲基-2-羟乙基-乙基纤维素和碱性羧甲基-2-羟丙基纤维素,其中碱是钠和钾,如图2中所示以椭圆形m表示。推动层j中的聚合物吸收了生物流体在内的外部水性流体,将药物从剂型中推入,保持本体结构,不与药物发生作用。推动层j包含4~35%wt的促渗剂,并由垂直线n表示。渗透剂包括具有吸收特性的盐,氧化物,酯,碳水化合物和酸,包括硫酸镁,氯化镁,氯化钠,氯化锂,氯化钾,硫酸钾,硫酸钠,硫酸钠,亚硫酸盐,硫酸锂,氯化铵,乳酸钾,甘露醇,尿素,琥珀酸镁,酒石酸,棉子糖,山梨糖醇,蔗糖,果糖和葡萄糖的成分。推动层j包括0.5~30%wt纤维素聚合物的o由字母v表示。o代表的纤维素聚合物,包括分子量为9000至225000的羟丙基纤维素,羟丙基甲基纤维素,羟丙基乙基纤维素,羟丙基异丙基纤维素,羟丙基丁基纤维素,羟丙基戊基纤维素和羟丙基己基纤维素中的成分。推动层包含0~5%wt的润滑剂,如硬脂酸以及硬脂酸镁,油酸钙,油酸和辛酸等。
从图3中可以看出,剂型a表面有一层外涂层p。外涂层p包含10mg~500mg的药物g,药物g由点表示。外涂层p提供快速释放药物的形式。药物16与包含载体甲基纤维素,羟丙基纤维素,羟丙基甲基纤维素以及羟丙基纤维素和羟丙基甲基纤维素的混合物的水溶性组合物混合。涂层p包含聚乙二醇或乙酰化甘油三酸酯,在生物流体的情况下溶解,快速释放药物。涂层p缩短了药物起效时间。
本发明所述的剂型a,可以制成口服剂型,另外还可以制成舌下和颊下给药途径给药,舌下和颊下途径可用于更快的治疗,当治疗需要较小剂量的药物时也可使用。口、舌下通路可作为药物首次肝代谢的旁路。可以通过舌下或颊下途径给药,避免胃肠道首过效应。
剂型a为渗透控释剂时,包括含有一个或多个通道c。表述“至少一个通道”包括可通过其泵送药物的多孔元件,中空纤维,毛细管,多孔覆盖物,多孔插入物,微孔构件,多孔组合物等。该表述还包括在使用的流体环境中从壁b腐蚀或浸出的材料,以产生至少一个通道的剂型a。适用于形成至少一个或多个通道的代表性材料包括:易腐蚀的聚(乙醇酸)或聚(乳酸)酸在壁中的成分;凝胶状的细丝;聚乙烯醇;可浸出的材料,例如流体可去除的成孔多糖,盐或氧化物等。可以通过从壁中浸出如山梨糖醇,蔗糖,乳糖,果糖等的材料来形成一个或多个通道,以提供渗透尺寸的孔通道。通道可以具有任何形状,例如圆形,三角形,正方形,椭圆形等,从剂型a中定量释放药物。剂型a可以在剂型的一个或多个表面上以间隔开的关系构造一个或多个通道。
渗透控释剂a的壁b可以采用空气悬浮技术,将在空气和壁形成组合物流中将压缩的药物-推芯层压板悬浮和翻滚,直到将壁施加到药物推压隔室上。空气悬浮适用于独立形成壁。渗透剂也可以在空气悬浮包衣机中对壁进行组合物包衣,可使用二氯甲烷:甲醇助溶剂80:20(w:w),乙醇-水或丙酮-水助溶剂95:5(w:w),使用2.5至4%的固体。空气悬浮涂布机,使用80:20(w:w)的二氯甲烷-甲醇助溶剂,也可用于壁包衣涂布。其他壁形成技术,例如锅包衣系统,其中通过将组合物连续喷雾在推药室上来沉积壁形成组合物,同时在旋转锅中翻滚。最后,将壁包衣的隔室在强制空气中于30°c至50°c下干燥一周去除残留溶剂。通常,通过这些技术形成的壁的厚度为0.05mm~0.8mm.
剂型a采用标准的制造工艺来制备。例如,在一种制造中,将药物和辅料混合并压制成固体层;可以将药物和其他成分与溶剂混合,并混合成通过常规方法(例如球磨,压延,搅拌或辊磨)形成的固体或半固体,然后压制成预选的形状。该层具有与剂型中区域内部尺寸匹配,并且还具有与第二层相对应的尺寸以用于与其形成接触装置。接下来,药物层和推动层的层合可以通过常规的压层技术来压片。最后,两层隔室形成构件被涂覆有外壁包裹。通过激光制作通道,浸出或机械钻孔以接触药物层的,当使用激光形成通道时,该剂量形式由激光设备自动光学定向,以在预选的表面上形成通道。
在另一种制备方法中,渗透泵控释剂通过湿法制粒制备。在制粒过程中,将处方量的药物与辅料混合后,以异丙醇-二氯乙烷80:20(v:v)也可以使用100%的变性酒精制软材,过40目筛制粒;然后,含药片芯中的其他辅料等量递加方式缓慢加入上述湿颗粒中,加入上述粘合剂制软材,过20目筛网制粒;将所制颗粒在30℃至50℃下干燥18至24小时。将干燥的颗粒筛分,然后用20目筛网筛分。接下来,使润滑剂通过80目筛网并将其添加到干筛网颗粒混合物中。将颗粒放入研磨罐中,并在罐磨机中混合1至15分钟。推动层通过相同的湿法制粒技术制成。将组合物在压层压机中压制成各自的层。将颗粒放入研磨罐中,并在罐磨机中混合1至15分钟。推动层通过相同的湿法制粒技术制成。
流化床制粒法可用于剂型a制粒。将粉末状成分在制粒机中干混后,将粘合剂(例如,聚乙烯(吡咯烷酮)水溶液,变性酒精或95:5乙醇/水)喷在粉末上;成分可以溶解或悬浮在制粒流体中;然后将包衣的粉末在制粒机中干燥。该过程将其中存在的所有成分制粒,同时添加粘合剂。将颗粒干燥后,将润滑剂例如硬脂酸或硬脂酸镁添加到制粒机中,增加颗粒流动性。
通过将药物与形成组合物的成分混合并将组合物压制成具有与隔室的内部尺寸相对应的尺寸的固体薄片,可以在另一种制造方式中制造本发明的剂型。在另一种制造方法中,通过常规方法如球磨,压延,搅拌或辊磨将药物和其他形成药物组合物的成分以及溶剂混合成固体或半固体,然后压制成预选的层形成形状。接下来,让包含渗透聚合物,渗透剂的组合物层与包含药物的层接触。包含药物的第一层,包含渗透聚合物和渗透剂组合物的使用常规的层压技术形成第二层。可以通过将压制的双层形状模压,喷涂或浸入壁形成材料中来施加壁。可以用于施加壁的另一种当前优选的技术是空气悬浮涂层过程。该方法包括使上述两层在气流中悬浮和翻滚,直到形成壁的组合物围绕这两层为止。
适用于制造壁,多层芯和薄片的示例性溶剂包括惰性无机和有机溶剂。溶剂包括水性溶剂,醇,酮,酯,醚,脂族烃,卤代溶剂,脂环族,芳族化合物,杂环溶剂及其混合物的成分。典型的溶剂包括丙酮,双丙酮,乙醇,甲醇,乙醇,异丙醇,丁醇,乙酸甲酯,乙酸乙酯,乙酸异丙酯,乙酸正丁酯,甲基异丁基酮,甲基丙基酮,正己烷,正庚烯乙二醇单乙醚,乙二醇单乙酸乙酯,二氯甲烷,二氯乙烷,二氯丙烯,四氯化碳,氯仿,硝基乙烷,硝基丙烷,四氯乙烷,乙醚。
(1)一种药物组合物,其包含0.5mg至750mg的药物g,其中所述的药物与聚(环氧烷)聚合物共混。
(2)一种药物组合物,其包含0.5mg至750mg的药物g,其中所述的药物与纤维素聚合物共混。
(3)一种药物组合物,其包含0.5mg至750mg的药物g,其中所述的药物与麦芽糖糊精聚合物共混。
(4)动物胃肠道给药方法,其中所述方法包括:(ⅰ)包含抗抑郁药物药物通过给药,续释放药物和控释剂型;(ⅱ)在延长的时间段内给予治疗剂量的药物以产生抗抑郁作用。
(5)在使用环境中给药的剂型,其中该剂型包含抗抑郁药物持续释放剂型和控释剂型,其中所述剂型包括用于储存药物的装置和用于在延长的时间段内释放药物的装置。
(6)通过口服给药递送药物至使用环境的剂型,其中该剂型包含:(ⅰ)壁,该壁至少包含部分可渗透流体通过的组合物;(ⅱ)隔室;(ⅲ)隔室中的药物组合物,其包含药物f;(ⅳ)隔室中的推动层,包含促渗剂;(ⅴ)剂型中的出口通道,从剂型中递送药物。
(7)根据(6)所述的用于将药物通过口服递送至使用环境的剂型,其中所述药物为抗抑郁药物。
以下实施例仅是对本发明的说明,并不限制本发明范围;因为根据本公开,这些实施例及其他等同物如附图和所附权利要求对于本领域技术人员而言将显而易见。
实施例1
如下制备适于输送治疗范围内的药物剂型:首先,将587.5g聚合度约3200羧甲基纤维素钠,300g粉状氯化钠,50g分子量约60000的羟丙基纤维素和平均分子量50的甲氧基含量29%wt,平均羟丙基含量为10%wt和平均分子量约为11300g的羟丙基甲基纤维素混合并通过420μm筛来制备置换层或推动层。10g红色三氧化二铁通过250μm筛。将所得的粉末在搅拌机中混合成均匀的共混物,加入无水乙醇将所得混合物湿法制粒,过约840μm筛分筛,形成涂覆的推动层颗粒,将其在室温条件下干燥过夜;然后将干燥的颗粒再次通过840μm筛分筛;将2.5g硬脂酸镁(已预先通过具有180μm开口的筛孔进行筛分)与涂覆的颗粒混匀;
如下制备包含药物的组合物:首先,将840g麦普替林,100g分子量约60000g的羟丙基纤维素和50g聚乙烯吡咯烷酮混合制备药物组合物;分子量约为40000g的聚合物通过420μm筛,并在混合器中混合制成均匀的共混物。然后,在搅拌下加入无水乙醇湿法制粒,过约840μm筛分筛湿颗粒,制成包衣文拉法辛药物,过夜风干。然后将干燥的颗粒再次通过840μm筛分筛;将10g硬脂酸镁(已预先通过具有180μm开口的筛孔进行筛分)与干燥颗粒混匀;
然后,将推动层组合物和药物组合物如下压成双层片芯:首先,将87mg药物组合物置于9/32英寸的圆模腔中,并用标准的凹入圆形工具轻轻捣固以形成略有凝聚力的层;然后,将70mg的推动组合物添加至模具中,并将所得填充物压缩,从而形成两层芯。
接下来将双层芯放置在包衣锅中,并用壁形成溶液包被。通过将380g乙酰含量为39.8%wt的乙酸纤维素溶解在7220g丙酮中来制备壁形成溶液。在单独的混合容器中,将20g分子量为每摩尔约3350g的聚乙二醇溶解在约380g纯水中。将两种溶液混合以形成壁包衣溶液,将其喷涂到芯上,直到约20mg的壁组合物沉积在双层芯的表面上。
通过在该剂型的药物组合物侧面以该剂型的表面为中心钻出一个出口,从而在整个壁上形成一个输出口。将所得剂型置于37℃的模拟生理液中,并且该剂型在15h的延长时间内匀速释放73mg麦普替林。
实施例2
除了药物组合物包含890g麦普替林,100g羟丙基纤维素和10g硬脂酸镁之外,按照实施例1的程序进行所述的制造程序。所得剂型在16小时的延长时间内在模拟肠液中匀速释放了77mg麦普替林。
实施例3
药物组合物由650.0g麦普替林,240.0g平均分子量约为1800g/摩尔和平均聚合度为11.1麦芽糖糊精组成外,其余全部按所述实施例1的步骤进行,80.0g羟丙基纤维素,20.0g聚乙烯吡咯烷酮和10.0g硬脂酸镁。所得剂型在人工肠液中测试,15h内匀速释放了57mg麦普替林。
实施例4
药物组合物由840.0g的麦普替林,150.0g的平均分子量为每摩尔约100,000g的聚环氧乙烷和10.0g的镁组成外,重复上述实施例1的步骤,硬脂酸重约为25mg。所得剂型在模拟的肠液中测试,20小时内匀速释放了73mg麦普替林。
实施例5
如实施例1中合成组合物,除了以流化床制粒法制备推动层之外,还可以将羧甲基纤维素钠,氯化钠,羟丙基纤维素和氧化铁红先过具有420μm筛网混合,将得到的粉末装入流化床中,并将由浓度为5%的羟丙基甲基纤维素在水中的粘合剂溶液喷雾到其上,从而形成用于推动层的颗粒。
实施例6
由740.0g平均分子量5百万的聚环氧乙烷组成,200.0g氯化钠,50.0g平均分子量约11300的羟丙基甲基纤维素,5.0g的红色三氧化二铁和5.0g的硬脂酸镁组成,其他组成和方法与实施例1相同。
本发明的另外的实施方案涉及用于递送本发明的涵盖结构式的药物用于其预期治疗的方法。一个实施方案涉及一种通过在延长的时间内以给予有效治疗剂量的持续释放和控释剂型,该剂型包含0.5mg至750mg药物。本发明的另一个实施方案涉及将本发明公开所含结构式的药物递送至胃肠道的方法,其中该方法包括以下步骤:(ⅰ)口服进入胃肠道,剂型包括:(1)一种无毒的壁组合物,其包括通过壁吸收外部水性流体到剂型中的装置;(2)内部隔室;(3)在隔室中包含结构式的药物的组合物,其包含单位剂量的所述药物;(4)在隔室中加入推动层,以将药物从隔室中推出;(5)在壁上至少有一个用于从剂型中输送药物的出口装置;(ⅱ)使流体通过壁吸收到隔室中,从而使组合物形成可递送的剂型,并随之使推动组合物膨胀并通过剂型的出口装置推动药物组合物;(ⅲ)在延长的时间内将有效治疗量的药物以控制的速率递送至患者体内。该方法还包括从即时释放的外部剂量的药物中分配一定剂量的所述药物给患者,以提供快速药物作用。
由于前述说明书包括本发明的优选实施例,因此应理解,在不脱离本发明范围的情况下,可以根据所公开的发明原理对本发明进行变化和修改。
- 还没有人留言评论。精彩留言会获得点赞!