用于使防腐剂溶液灭菌的系统、方法和装置与流程
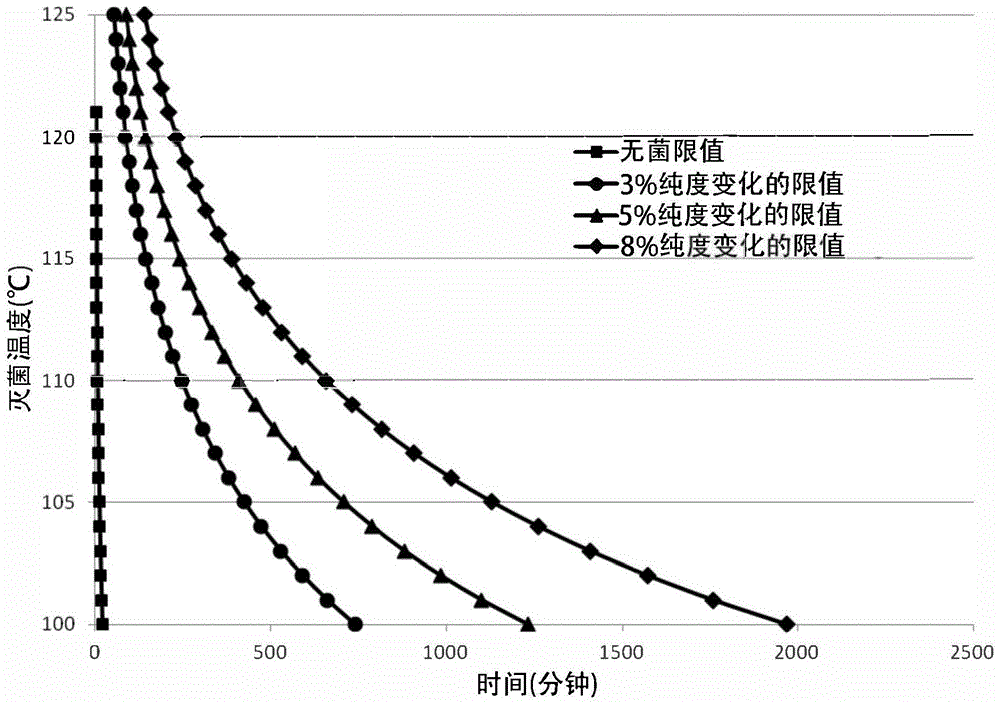
本申请是申请日为2016年6月30日,申请号为:2016105130566,名称为“用于使防腐剂溶液灭菌的系统、方法和装置”的发明专利申请的分案申请。发明领域本发明的各方面涉及灭菌领域,并且特别涉及局部用防腐剂溶液的灭菌。发明背景在美国,关于局部用防腐剂溶液的灭菌要求目前没有规定。因此,目前在美国销售的防腐剂溶液一般不经过灭菌过程。然而在其他司法管辖区,如欧盟(eu)国家,需要一定程度的灭菌。已知的由carefusioncorp.制造的在70%v/v的异丙醇水溶液(即醇溶液)中含有2%w/v的葡萄糖酸氯己定(chlorhexidinegluconate)的防腐剂溶液用于欧盟国家时则使用已知的灭菌方法进行灭菌。业内认为由于预期的降解,高温灭菌是不合适的。参见例如kellym.pyrek,“sterilityofantisepticproducts:fdainvestigates,deliberatesonpotentialrecommendations,”infectioncontroltoday(july2013):24-26;和block,seymours.disinfection,sterilization,andpreservation.philadelphia:lippincottwilliams&wilkens,322–323.2001。已知的灭菌方法包括使含有葡萄糖酸氯己定醇溶液的玻璃安瓿在76-80℃下的对流烘箱中热处理24-31小时。目前认为,相对低的温度和相对长的处理时间对于使防腐剂醇溶液充分灭菌且不使抗微生物剂分子过度降解是必要的,由此避免降低作为防腐剂包含在其中的葡萄糖酸氯己定的浓度和纯度。申请人共同待决的美国申请号14/150,488描述了用于使醇溶液灭菌的可替代性方法,其在此明确地通过引用整体并入本文中。然而,尚无已知的使水性防腐剂溶液灭菌的方法,该方法在不过度使抗微生物剂分子降解的情况下提供无菌溶液。因此,本领域中对于使水性防腐剂溶液灭菌的方法存在未满足的需求。发明概述本发明的各方面通过提供用于使抗微生物剂溶液有效灭菌,同时保持作为水性防腐剂的抗微生物效力和符合法规要求的活性药物部分的纯度的系统、方法和装置来克服以上指出的问题以及其他问题。一种用于使水性防腐剂溶液灭菌的方法,该方法包括:提供含有水性防腐剂溶液的容器,该水性防腐剂溶液包含双(二氢吡啶基)癸烷衍生物或双胍;将水性防腐剂溶液加热至预定温度;使水性防腐剂溶液在预定温度下保持预定时间;和当预定时间结束时,终止水性防腐剂溶液的加热。选择所述预定温度和所述预定时间,以使得在终止加热后,该水性防腐剂溶液是无菌的。在另一示例方面中,选择灭菌温度和灭菌时间,以使得在终止加热之后,防腐剂溶液具有至少约90%的灭菌后纯度,并且从初始纯度到灭菌后纯度的纯度百分点变化为至多约8%。在另一个示例方面中,防腐剂溶液包含水和约2.0%w/v的葡萄糖酸氯己定。在另一个方面中,灭菌温度为约100℃并且灭菌时间为约20分钟至约33小时。在在另一个示例方面中,灭菌温度为约110℃并且灭菌时间为约6分钟至约11小时。在另一个方面中,灭菌温度为约115℃并且灭菌时间为约3.5分钟至约6小时。在在另一个方面中,灭菌温度为约125℃并且灭菌时间为约1分钟至约2小时。在另一示例方面中,选择所选择的灭菌温度和所选择的灭菌时间,从而使得在终止加热之后,防腐剂溶液具有至少约93%的灭菌后纯度,并且从初始纯度到灭菌后纯度的纯度百分点变化为至多约5%。在另一示例方面中,选择所选择的灭菌温度和所选择的灭菌时间,从而使得在终止加热之后,防腐剂溶液具有至少约95%的灭菌后纯度,并且从初始纯度到灭菌后纯度的纯度百分点变化为至多约3%。关于本发明的各方面的其他优点和新特征将部分地在以下说明中进行阐述,以及部分地在查阅以下内容或通过其实践进行了解之后对于本领域技术人员而言将变得更加显而易见。附图简要说明图1是根据本发明的某些方面的灭菌温度和灭菌时间数据的图。图2是各种葡萄糖酸氯己定制剂的阿伦尼乌斯绘图(arrheniusplot)的图。图3是具有各种异丙醇(ipa)浓度的缓冲和未缓冲的2%葡萄糖酸氯己定水性制剂的百分比总相关物质(%trs)降解速率的图。图4是2%葡萄糖酸氯己定水溶液的ph速率曲线图。发明详述本发明的各方面通过提供用于使水性防腐剂溶液灭菌同时保持抗微生物效力并同时符合法规要求的系统、方法和装置来克服以上指出的问题以及其他问题。可以参考一个或多个示例性实施方案来说明防腐剂涂敷器的各个方面。如本文所用,术语“示例性”的意思是“用作实例、例子或说明”,并且不应被解释为相对于本文所公开的灭菌方法的其他实施方案必然是优选或有利的。如本文所用,术语“约”优选意指为所提供的值的±5%,并且更优选为±1%。本发明的各方面包括使包含在容器中的水性防腐剂溶液灭菌的方法。该方法可以包括将包含在容器或安瓿内的水性防腐剂溶液加热到一定预定温度并使该温度保持一定量的预定时间,该时间足以使该溶液灭菌同时保持足以符合法规要求的防腐剂溶液纯度。抗微生物效力与防腐剂溶液的纯度直接相关。通常,当防腐剂分子的纯度太低时,该溶液在作为抗微生物剂溶液起作用时不是有效的。此外,防腐剂溶液内较高的杂质水平可对患者的健康产生有害影响。容器优选为由适合于容纳防腐剂溶液的材料形成的自包含结构。在一个方面中,容器可以由易碎材料制成,从而使得当施加足够的力时,该容器破裂。例如,该材料可以包含塑料或玻璃。术语“容器”和“安瓿”在本文中可互换使用。容器壁可以具有足以承受灭菌过程、运输和储存的厚度。当容器易碎时,材料和厚度也可以足以允许容器在施加局部压力后破裂。厚度范围可以根据容器的尺寸而变化。玻璃或塑料容器的示例厚度包括约0.15mm至约0.45mm。在另一示例方面中,容器可以包含能够承受灭菌过程的非易碎材料,如金属(钢、铝等)或如包含聚合物和/或箔材料或由聚合物和/或箔材料组成的袋。例如,该容器可以是具有聚合物和箔的复合材料的曲颈瓶状箔袋。该袋的示例厚度可以为约0.002英寸至0.010英寸。虽然本文特别关注防腐剂溶液,但是该容器可以可替代地含有药物、化学组合物、清洁剂、化妆品或类似物。例如,该容器可以填充有防腐剂组合物(例如,包含一种或多种防腐剂分子的组合物),优选抗微生物液体或凝胶组合物。例如,防腐剂溶液可以含有非活性成分/剂,其具有的功能包括保湿、皮肤光滑、可视化、溶解度、稳定性、粘度、润湿等。在本发明的一个方面,防腐剂溶液是水性的。即,溶液的溶剂主要是水。如本文所用,水性的是指至少约50%v/v的水,更优选至少约60%v/v的水,更优选至少约70%v/v的水,更优选至少约80%v/v的水,更优选至少约90%v/v的水,更优选至少约95%v/v,最多至100%v/v的水。当溶液是小于100%v/v的水时,剩余的体积可以包括一种或多种其他溶剂,例如醇溶剂。示例醇溶剂包括乙醇、异丙醇和正丙醇。例如,该溶液可以含有小于约50%v/v、更优选小于约40%v/v、更优选小于约30%v/v、更优选小于约20%v/v、更优选少于约10%v/v、低至0%v/v的醇。优选的醇可以是异丙醇。该容器可以含有待涂敷于期望的表面并对该期望的表面具有抗微生物作用的足够量、足够浓度和足够纯度的防腐剂溶液。在一个方面中,该期望的表面是患者的皮肤。应该理解的是,防腐剂溶液的量可以变化。在一个方面中,防腐剂溶液的量可以是0.01-100ml防腐剂。更优选地,所需要的防腐剂溶液的量可以为约0.5-60ml,还优选地可以为约0.5-30ml。实例包括0.67、1、1.5、3、10.5和26ml的防腐剂。在其中期望较大量的溶液例如26ml的情况下,可以在单个涂敷器中应用多个较小的容器(例如两个13ml的容器)。合适的防腐剂分子包括双(二氢吡啶基)癸烷衍生物(例如奥替尼啶(octenidine)盐)和/或双胍类(例如氯己定盐)。如本文所用,术语“衍生物”是指a)与第一化学物质结构上相关并且由其衍生的化学物质;b)由相似的第一化合物形成的化合物或者由另一第一化合物可想象到的化合物,如果第一化合物的一个原子被另一个原子或另一组原子代替;c)由母体化合物衍生或获得的并且含有母体化合物的必需元素的化合物;或d)可以在一个或多个步骤中由具有相似结构的第一化合物产生的化合物。除了氯己定/氯己定盐之外的双胍类/双胍衍生物的实例包括阿来西定(alexidine)、阿来西定盐,聚己酰胺、聚己酰胺盐、聚氨基丙基双胍、聚氨基丙基双胍盐,以及其他烷基双胍类。优选的防腐剂包括奥替尼啶盐,如奥替尼啶二盐酸盐(双(二氢吡啶基)癸烷衍生物和阳离子型表面活性剂);和氯己定盐,如葡萄糖酸氯己定(阳离子型双胍)。防腐剂的浓度可以根据所使用的具体防腐剂种类或所期望的抗微生物作用而变化。例如,当使用奥替尼啶或奥替尼啶盐时,浓度可以为约0.0001%w/v至约2.0%w/v,更优选约0.01%w/v至约1.0%w/v,还更优选约0.1%w/v至约0.6%w/v。当使用氯己定或氯己定盐时,浓度可以为约0.1%w/v至约5.0%w/v,更优选约0.5%w/v至约3.0%w/v,还更优选约1.0%w/v至约2.0%w/v。在一个方面中,当使用双胍(例如氯己定或氯己定盐)时,当涂敷于皮肤时(例如,在本文描述的灭菌方法之后),溶液的纯度可以是至少约90%纯,更优选至少约93%纯,还更优选至少约95%纯。如本文所用,纯度意指溶液中防腐剂分子相对于防腐剂分子的浓度加上由防腐剂分子衍生的或与防腐剂分子相关的物质的浓度的总浓度的百分比浓度。例如,95%纯的防腐剂溶液意指如果存在100个分子,其为防腐剂分子或由防腐剂分子衍生的或与防腐剂分子相关的分子,那么分子中的95个为防腐剂分子并且这些分子中的5个为由防腐剂分子衍生的或与防腐剂分子相关的分子。这些由防腐剂分子衍生的或与防腐剂分子相关的分子具有降低的抗微生物活性或没有抗微生物活性。因此,较低纯度的溶液将具有较低的抗微生物效力,因为较少的目标防腐剂分子被递送至患者的皮肤。此外,较低纯度的溶液将不符合法规要求。通过测量溶液中相较于防腐剂分子和由防腐剂分子衍生的或与防腐剂分子相关的分子的浓度的防腐剂分子的浓度,人们可确定溶液的纯度以及纯度是否足以符合法规要求。在一个优选的方面中,在该容器中提供的防腐剂溶液包含以下成分,基本上由以下成分组成或由以下成分组成:作为唯一溶剂的水和约2.0%w/v的防腐剂分子。在一个优选的方面中,防腐剂分子可以是葡萄糖酸氯己定。已经发现,当容器内的水性防腐剂溶液达到特定的温度并在该温度下保持特定量的时间时,该溶液被充分灭菌,同时保持足够的作为防腐剂的抗微生物效力,并且同时满足法规要求。在本发明的一个方面中,可以使防腐剂溶液达到约100℃至约140℃、更优选约110℃至约130℃、还更优选约115℃至约125℃的温度(本文中也称为“灭菌温度”)。如本文所用,术语“预定灭菌时间”意指溶液处于灭菌温度的时间长度。也就是说,“灭菌时间”不包括溶液达到灭菌温度所花费的时间(即不包括“倾斜升温(rampup)”时间),并且也不包括溶液返回至加热之前溶液所处的温度所花费的时间(即不包括“冷却”时间)。溶液的温度达到灭菌温度所花费的时间在本文中称为“倾斜升温”时间,返回到起始温度的时间在本文中称为“冷却”时间。如本文所用,术语“预定灭菌温度”意指溶液达到并在灭菌时间期间保持的温度或温度范围,与溶液的起始温度无关。只是为了说明的目的,对于起始温度为21℃的溶液而言,灭菌时间为60分钟和灭菌温度为110℃意指从溶液达到110℃的时刻开始至溶液在冷却过程开始期间降到低于110℃的时刻为止的时间段为60分钟。因此,溶液从21℃上升到110℃所花费的时间(即倾斜升温时间)以及溶液返回至21℃所花费的时间(即冷却时间)不包括在灭菌时间中。本文提供的预定灭菌时间和灭菌温度通常假设在倾斜升温和冷却过程中的热暴露不影响药物产品的灭菌,因为在小规模上,这些过程可被认为是瞬时的。然而,在商业规模上,加热产品所用的时间将影响灭菌过程的总致死率,使得稳态灭菌时间减少。当施加倾斜升温和冷却的影响至周期时,药物产品的灭菌可通过使用以下方程对于各个预定灭菌时间和灭菌温度计算的f值来描述(参见"laboratorymanualforfoodcannersandprocessors",vol.1,avipublishingco.,westport,ct,1968):其中:t是灭菌产品在特定时间t的温度。δt为t的后续测量之间的时间间隔。ts=目标灭菌温度z=温度系数,通常假设为等于10℃,但对于具体微生物是可计算的,因此是变量。只是为了说明的目的,灭菌温度为121℃以及预定灭菌时间为6分钟(即倾斜升温和冷却不影响药物产品的灭菌)对应于为了使药物产品灭菌在121℃下最小f值(f121)为15分钟。可使用该最小所需f值来定量其中倾斜升温和冷却确实影响药物产品的灭菌的过程。在这样的过程中,可计算倾斜升温和冷却对于最小所需f值的影响。如果在f121=15分钟限定的灭菌周期期间,未达到121℃的温度,按照作为实际周期期间热输入的总和计算f121,仍然能够满足周期参数。已经发现,可选择灭菌温度和灭菌时间的组合以提供经灭菌的水性防腐剂溶液,其在作为防腐剂使用时具有足以符合法规要求的纯度。例如,对于约100℃的灭菌温度,灭菌时间可以是至少约20分钟至约33小时。对于约110℃的灭菌温度,灭菌时间可以是至少约6分钟到至多约11小时。对于约115℃的灭菌温度,灭菌时间可以是至少约3.5分钟至约6小时。对于约125℃的灭菌温度,灭菌时间可以是至少约1分钟到至多约2小时。在本发明的一个方面中,以上示例灭菌温度和灭菌时间可以应用于包含约100%v/v的水和约2.0%w/v的葡萄糖酸氯己定的防腐剂溶液或上文描述的其他防腐剂溶液。已经发现,将容器中含有的防腐剂溶液加热至上述灭菌温度并使该温度保持上述灭菌时间,足以使溶液灭菌,同时保持足以符合法规要求的纯度。防腐剂分子的降解量可通过测量防腐剂溶液在倾斜升温时间之前(即,在使溶液升至灭菌温度的过程之前)的初始纯度和测量防腐剂溶液在冷却时间之后(即,在防腐剂溶液返回至在使溶液升至灭菌温度的过程之前溶液所处的温度之后)的灭菌后纯度来定量。因此,如本文所用,“初始纯度”是倾斜升温之前的纯度,并且“灭菌后纯度”是冷却之后溶液的纯度。在本发明的一个方面中,防腐剂溶液(例如葡萄糖酸氯己定)的初始纯度可以是至少约90%,优选至少约93%,并且更优选至少约95%。纯度的含义在上文提供。发现所得的灭菌后溶液具有足以提供作为防腐剂的期望的抗微生物效力并且符合法规要求的纯度。在一个示例方面中,已发现葡萄糖酸氯己定分子在加热处理时降解为以下分子中的一种或多种:n-[[6-[[[(4-氯苯基)脒基]脒基]氨基]己基]脒基]脲(n-[[6-[[[(4-chlorophenyl)carbamimidoyl]carbamimidoyl]-amino]hexyl]carbamimidoyl]urea),n-(4-氯苯基)胍,n-(4-氯苯基)脲,1-(6-氨基己基)-5-(4-氯苯基)双胍,n-(4-氯苯基)-n’-[[6-[[[(4-氯苯基)脒基]脒基]氨基]己基]脒基]脲,1-(4-氯苯基)-5-[6-[[(苯基脒基)脒基]氨基]己基]双胍,1-[6-(脒基氨基)己基]-5-(4-氯苯基)双胍和4-氯苯胺。因此,在一个示例方面中,溶液的纯度可通过比较葡萄糖酸氯己定的量与上面所列出的所有葡萄糖酸氯己定相关物质的量来确定。然而,应当注意的是,上面的列举不是穷尽的。本领域的普通技术人员将能够确定哪些分子是防腐剂分子在灭菌过程之后的降解物。如上文所述,防腐剂溶液在加热被终止之后并且当溶液已返回至使溶液升至灭菌温度的过程之前溶液所处的温度(例如环境温度)时的纯度在本文中称为灭菌后纯度。如上文所述,优选在防腐剂溶液已冷却时测量灭菌后纯度,因为在冷却期间可以发生降解。在本发明的一个方面中,通过选择灭菌温度和灭菌时间的适当组合,可以使灭菌后纯度保持为相对接近于初始纯度,同时仍是无菌的。特别地,选择灭菌温度和灭菌时间的组合,从而使得从初始纯度到灭菌后纯度的纯度百分点变化为至多约8%,更优选至多约5%,更优选至多约4%,并且最优选至多约3%。应当理解,百分点变化是指初始纯度和灭菌后纯度之间的绝对百分点差值。例如,95%的初始纯度到90%的灭菌后纯度的变化为5%的百分点变化。除了保持足够的纯度之外,已经发现,可选择灭菌温度和灭菌时间的适当组合,从而使得该溶液是无菌的。如本文中所用,无菌的意指按照以下文献中描述的程序测试的“7天无菌”:u.s.pharmacopeialconvention(usp)chapter55“biologicalindicators–resistanceperformancetests,”usp36;从2013年5月1日起正式实施。无菌的还意指在紧随灭菌之后完全没有微生物。在一个方面中,枯草芽孢杆菌(bacillussubtilis)可以用作测试微生物。因此,在一个方面中,无菌溶液通过上文所述的“7天无菌”测试显示没有枯草芽孢杆菌的生长。在另一个方面中,用枯草芽孢杆菌接种的溶液在紧随灭菌方法之后完全没有活的枯草芽孢杆菌。在本发明的另一方面中,发现本发明的方法在灭菌温度和灭菌时间的特定组合下具有至少约10-6的无菌保证水平(sal)。sal是在灭菌程序之后在物品上存在微生物的概率的量度。10-6的sal意指1/1,000,000的机会在经灭菌的产品中存在活微生物。因此,sal测量灭菌方法得到未经灭菌的产品的概率。测定sal的计算在下面的实施例中更详细地描述。例如,已发现,使水性防腐剂溶液暴露于105℃温度约11分钟、115℃温度约2.3分钟或者121℃约1.8分钟的方法均会具有至少10-6的sal(即1/1,000,000的机会在经灭菌的溶液中存在活微生物)。如上文所述,在灭菌时间结束之后,可以将溶液冷却。例如,在灭菌时间之后可以花费约10至约40分钟来冷却防腐剂溶液。可使用冷却装置来缩短该时间。该额外时间与特定的灭菌温度相关联。例如,与较低的灭菌(例如100℃)相比,较高的灭菌温度(例如125℃)在灭菌之后将花费更长时间以返回室温。因此,包括冷却的总处理时间可以包括额外的比灭菌时间更长的约10至约20分钟。可以使用能够加热防腐剂溶液至灭菌温度并使溶液在该灭菌温度下保持灭菌时间同时优选限制倾斜升温时间的任何机器在本发明的范围内。示例设备可以包括水浴、油浴、高压釜、对流烘箱、水喷淋式灭菌器(cascadingwatersterilizer)等。当使用水喷淋式灭菌器时,倾斜升温时间可以是约15分钟,而冷却时间可以是约25分钟。水喷淋式灭菌器提供恒定的水流,该水流将溶液加热至灭菌温度,在整个灭菌时间内保持灭菌温度并最终使溶液冷却。如以上所提供的,提供具有足以满足法规要求的纯度的灭菌溶液的灭菌时间和灭菌温度的示例组合如下所述:灭菌温度可以为约100℃并且灭菌时间可以是约20分钟至约33小时;灭菌温度可以为约110℃并且灭菌时间可以是至少约6分钟至约11小时;灭菌温度可以为约115℃并且灭菌时间可以是至少约3.5分钟到至多约6小时;灭菌温度可以为约125℃并且灭菌时间可以是至少约1分钟到至多约2小时。在进行上述灭菌过程之后的无菌水性溶液可以用于各种情形之中。例如,可以将其中溶液被灭菌的初始容器置于防腐剂涂敷器。例如,可以将初始容器中的无菌溶液置于多产品试剂盒或另一最终产品的子组件内。实施例在以下各实施例中测试容纳在玻璃安瓿中的100%v/v的水和2.0%w/v的葡萄糖酸氯己定的水性防腐剂溶液的样品。以下实验通过将所指示类型的浴(例如,水或油)加热至所指示的温度(例如,70℃-114℃)来进行。溶液具有所指示的初始纯度并且在表中指示的时间测试纯度。表中列出的纯度百分比值是葡萄糖酸氯己定在热处理并冷却至环境温度后的绝对纯度。每个温度重复测试两次。δ纯度百分比值是相对于基线纯度的百分点变化。例如,在表1中,将水浴加热至70℃并且测试具有98.95%纯度的溶液。在8小时时,葡萄糖酸氯己定溶液的纯度为98.92%,其相对于98.95%的初始纯度发生了0.03%百分点变化。实验#1表1-70℃,初始纯度98.95%,水浴表2-90℃,初始纯度98.95%,水浴表3-105℃,初始纯度98.95%,油浴表4-114℃,初始纯度98.95%,油浴实验#2表5-70℃,初始纯度99.24%,水浴表6-90℃,初始纯度99.24%,水浴表7-105℃,初始纯度99.24%,油浴表8-114℃,初始纯度99.24%,油浴然后使用本领域中的标准方法用上述数据来制备阿仑尼乌斯方程(arrheniusequation)。阿仑尼乌斯方程的使用是公知的和可接受的模拟温度对反应速率的依赖性的方法。使用阿仑尼乌斯方程,得到以下预测的纯度值:表9–使用阿仑尼乌斯方程预测的纯度下面示出所测量的各个灭菌温度和灭菌时间对于防腐剂的特性的影响。表10总结了在暴露于各个灭菌温度和灭菌时间之后葡萄糖酸氯己定的纯度%变化。纯度百分比变化通过比较溶液在倾斜升温时间之前(即在使溶液升至灭菌温度的过程之前)的纯度与溶液在冷却时间之后(即在溶液返回环境温度之后)的纯度而得到。“x”、“y”和“z”分别表示灭菌温度和灭菌时间将导致不大于3%、5%和8%的纯度变化。表10–加热和温度对化学稳定性的影响灭菌时间(小时)注释:x=溶液具有不大于3%的纯度变化y=溶液具有不大于5%的纯度变化z=溶液具有不大于8%的纯度变化可对其他阈值(例如,低于或高于8%的纯度变化,例如2%、4%和6%)进行相同的处理。除了上述测试外,进行进一步的测试以确定在一定温度下何时可达到10-6的无菌保证水平(sal)。按照usp55“biologicalindicators–resistanceperformancetests”程序测定sal。将大于或等于1,000,000但小于10,000,000个测试枯草芽孢杆菌芽孢插入到包含在100%v/v水中的2.0%w/v的葡萄糖酸氯己定的5ml水溶液样品中。在105℃、115℃和121℃持续不同时间来测试样品。结果如下:表11–105℃下的微生物测试tntc=数目太多而未能计数表12–115℃下的微生物测试tntc=数目太多而未能计数表13–121℃下的微生物测试tntc=数目太多而未能计数然后根据usp55程序使用以上数据计算“d值”。术语d值具有微生物学中使用的通常含义。具体地,其是指十倍减少时间并且是在一定温度下杀死90%的正在研究的生物体所需要的时间。因此,在菌落减少1d之后,仅剩下10%的原始生物体,即种群数量在计数方案中减少了一个小数位。d值可使用残存曲线法(survivorcurvemethod)来计算,该方法是本领域中已知的数据分析方法(基于iso11138-1:2006描述的方法)。将残存曲线法应用于上表11-13的数据,计算得到的d值以及置信上限和置信下限:表14–d值温度(℃)d值(min)1051.751150.381210.29d值可被用来计算无菌保证水平(sal)(参见usp55程序)。sal是在微生物学中使用的术语,用于描述单个单元在其经受灭菌过程之后为非无菌的概率。10-6sal意指有1/1000000的机会在经灭菌的物品中保留单个活微生物。使用置信上限d值来计算以下达到10-6sal的时间:表15–sal10-6时间因此,如表15所示,使防腐剂溶液暴露至105℃的温度约10.5分钟,115℃的温度约2.3分钟,或121℃下约1.8分钟,将各自具有10-6的sal(即1/1000000的机会在灭菌过程之后存在活微生物)。使用标准数学建模,对表11-13中示出的数据,具有下式的指数预测函数:y=2,122,036·e(-0.116x)(i)其中y是以分钟表示的时间,x是以摄氏度表示的温度。因此,式(i)表示在给定温度下达到至少10-6sal的最少时间。使用式(i),生成以下预测数据点:表16–预测性sal10-6时间图1示出拟合捕集以保持在灭菌过程之后的具体纯度变化的参数空间(时间和温度)的函数的灭菌时间和温度(曲线之间的区域)。图1中的数据点包括来自上面表9和表16的数据点。黑色方块表示100℃至125℃的数据点,其中相应的时间是无菌的。以下公式拟合于100℃至125℃的方块数据点:对于100≤t≤125,t=2.122×106×e-0.116t(ii)其中t是以摄氏度表示的温度,t是以分钟表示的时间。上面表9中示出的数据点也绘制在图1中。黑色菱形表示100℃至125℃的数据点,其中相应的时间具有至多8%的纯度百分比变化。黑色三角形表示100℃至125℃的数据点,其中相应的时间具有至多5%的纯度百分比变化。黑色圆圈表示100℃至125℃的数据点,其中相应的时间具有至多3%的纯度百分比变化。以下公式拟合于黑色菱形数据点(即具有至多8%的纯度变化的点):对于100≤t≤125,t=7.341×107×e-0.155t(iii)以下公式拟合于黑色三角形数据点(即具有至多5%的纯度变化的点):对于100≤t≤125,t=4.588×107×e-0.155t(iv)其中t是以摄氏度表示的温度,并且t是以分钟表示的时间。以下公式拟合于黑色圆圈数据点(即具有至多3%的纯度变化的点):对于100≤t≤125,t=2.753×107×e-0.155t(v)其中t是以摄氏度表示的温度,并且t是以分钟表示的时间。从图1中可看出,对于100℃至125℃之间的温度,由式(ii)和式(iii)定义的函数所界定的区域表示提供具有至多8%纯度变化的无菌溶液的温度和时间组合。这个区域因此可通过用式(iii)减去式(ii)来呈现:对于100≤t≤125,t=7.341×107×e-0.155t-2.122×106×e-0.116t其中t是以摄氏度表示的温度,并且t是以分钟表示的时间。从图1中可看出,对于100℃至125℃之间的温度,由式(ii)和式(iv)定义的函数所界定的区域表示提供具有至多5%纯度变化的无菌溶液的温度和时间组合。这个区域因此可通过以下关系呈现:对于100≤t≤125,t=4.588×107×e-0.155t-2.122×106×e-0.116t其中t是以摄氏度表示的温度,并且t是以分钟表示的时间。从图1中可看出,对于100℃至125℃之间的温度,由式(ii)和式(v)定义的函数所界定的区域表示提供具有至多3%纯度变化的无菌溶液的温度和时间组合。这个区域因此可通过以下关系呈现:对于100≤t≤125,t=2.753×107×e-0.155t-2.122×106×e-0.116t其中t是以摄氏度表示的温度,并且t是以分钟表示的时间。具体而言,上面的结果,即2%w/v的葡萄糖酸氯己定水溶液在灭菌之后保持足够纯,是令人惊讶的。进行了其他实验,其中将具有100%v/v的水和2%w/v的葡萄糖酸氯己定的水溶液在密封的安瓿中在121℃加热不同时间。与2%w/v的葡萄糖酸氯己定醇溶液(溶剂:70%v/v异丙醇,余量为水)进行比较。结果表明,在25℃下2%w/v的葡萄糖酸氯己定水溶液的降解速率显著低于2%w/v的葡萄糖酸氯己定醇溶液(13-18倍)。以前的研究已经表明,在25℃下具有100%v/v的水和20%w/v的葡萄糖酸氯己定的水溶液的降解速率与2%w/v的葡萄糖酸氯己定的醇溶液的降解速率几乎相同。因为20%w/v的葡萄糖酸氯己定水溶液具有与2%w/v的葡萄糖酸氯己定的醇溶液相同的降解速率,预期2%w/v的葡萄糖酸氯己定水溶液将会表现出相似的降解速率。为了预测葡萄糖酸氯己定降解程度的差异是否是溶液固有的并且是否在任何时间和温度下都会存在,通过监测总相关物质相对于时间和温度的增长对2%w/v的葡萄糖酸氯己定水溶液、具有20%w/v的葡萄糖酸氯己定的水溶液和2%w/v的葡萄糖酸氯己定的醇溶液建立了阿仑尼乌斯方程。测试两个不同制造商(在本文中称为制造商a和制造商b)的20%w/v的葡萄糖酸氯己定水溶液。为了测试的目的,供应的两个不同的20%w/v的葡萄糖酸氯己定水溶液用水稀释至2%w/v的葡萄糖酸氯己定(即,保持100%v/v的水)。两个2%w/v的葡萄糖酸氯己定水溶液的阿仑尼乌斯方程与20%w/v的葡萄糖酸氯己定水溶液和具有2%w/v的葡萄糖酸氯己定的醇溶液的阿仑尼乌斯方程进行比较。结果示于图2中。如图2所示,来自制造商a和制造商b的两个2%w/v的葡萄糖酸氯己定水溶液的降解速率都显著低于2%w/v的葡萄糖酸氯己定醇溶液和20%w/v的葡萄糖酸氯己定水溶液二者。与20%w/v的葡萄糖酸氯己定水溶液和2%w/v的葡萄糖酸氯己定醇溶液相比,对于2%w/v的葡萄糖酸氯己定水溶液在25℃下的降解速率的预测示于下表17中。表17–预测的25℃下的总相关物质的降解速率*根据相应的阿仑尼乌斯方程外推的值此外,如图2和表17所示,确定2%w/v的葡萄糖酸氯己定醇溶液的降解速率在所有温度下均与20%w/v的葡萄糖酸氯己定水溶液相当。鉴于进一步的测试表明降解速率的差异不是只与以下因素的一个直接相关:醇含量、ph值/表观ph值的差异以及稀释的量,上述降解结果是特别令人惊讶的。为了研究异丙醇对降解速率的影响,用非缓冲体系(水)或缓冲体系(50mm乙酸盐缓冲液,ph约5)制备具有增加的异丙醇浓度的制剂。使用缓冲体系,除了改变异丙醇浓度之外,还为了在使葡萄糖酸氯己定制剂降解时最小化溶液表观ph值差异的影响。结果示于图3中,其表明随着异丙醇浓度的增加,葡萄糖酸氯己定的降解速率(总相关物质(trs)的形成增多)也增加。为了测定ph对葡萄糖酸氯己定的降解速率的影响,使用50mm的乙酸盐缓冲液在不同ph下制备2%w/v的葡萄糖酸氯己定水性制剂(参见图4)。当水溶液的ph在约4.0-5.0的范围内时,葡萄糖酸氯己定的降解率不依赖于ph。当溶液的ph增加至高于ph5时,葡萄糖酸氯己定的降解速率也增加。稀释20%w/v的葡萄糖酸氯己定水溶液以得到2%w/v的葡萄糖酸氯己定水溶液不会显著影响溶液的ph(δph为约0.2个ph单位)。此外,当稀释葡萄糖酸氯己定时,2%w/v的葡萄糖酸氯己定水溶液的ph(ph6.4)高于20%w/v的葡萄糖酸氯己定水溶液的ph(ph6.2)。因此,基于图4示出的结果,其中随着ph的增加降解也增加,观察到的2%w/v的葡萄糖酸氯己定水溶液和20%w/v的葡萄糖酸氯己定水溶液之间的降解速率的差异不是ph现象。总之,不同的机制控制着观察到的在如上所述的各种葡萄糖酸氯己定制剂之间的降解速率的差异。因此,观察到的2%w/v的葡萄糖酸氯己定水溶液比2%w/v的葡萄糖酸氯己定的醇溶液和20%w/v的葡萄糖酸氯己定水溶液更低的降解速率是令人惊讶的。尽管本发明的各方面已经结合示例性实施方式进行了描述,但是本领域技术人员应该理解,可以在不脱离本发明的范围的情况下对如上所述的各方面做出变化和修改。在考虑本说明书或根据本文所公开的内容进行实践之后,其他各种变化对于本领域技术人员而言将是显而易见的。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1